文章信息
- 薛丹, 倪健, 张鹏, 杨春静, 赵阳, 夏振文, 尹兴斌, 李友林
- XUE Dan, NI Jian, ZHANG Peng, YANG Chun-jing, ZHAO Yang, XIA Zhen-wen, YIN Xing-bin, LI You-lin
- 多指标正交设计优选芪防鼻敏颗粒水提醇沉工艺
- Optimization of aqueous extraction-alcohol precipitation technology for Qifang Bimin granules with multi-index orthogonally designed experiments
- 天津中医药, 2016, 33(1): 39-42
- Tianjin Journal of Traditional Chinese Medicine, 2016, 33(1): 39-42
- DOI: 10.11656/j.issn.1672-1519.2016.01.10
-
文章历史
- 收稿日期: 2015-10-05
2. 中日友好医院国家中医药管理局重点研究室, 北京 100029
过敏性鼻炎(Allergic Rhinitis,AR)又叫变应性鼻炎,是最常见的过敏性疾病之一,在全球的发病率为10%~25%[1],在中医属于鼻鼽的范畴,以突然和反复发作的鼻痒、鼻塞、喷嚏、流清涕为特征[2, 3],大多数医家认为本病是肺脾肾三脏虚损,风寒异气之邪乘袭[4]。西医对过敏性鼻炎的治疗主要是对症治疗,常用药物为抗组胺药、减充血剂、抗胆碱药、糖皮质类固醇激素、肥大细胞膜稳定剂、白三烯受体拮抗剂等[5, 6, 7]。中医药辨证治疗过敏性鼻炎具有远期疗效稳定,复发率低等特点,标本兼治,从根本上治愈疾病[8]。
芪防鼻敏方是临床经验方,全方由黄芪、桂枝、白芍等12味药组成,具有健脾益肺,温阳固表,宣通鼻窍之效,用于肺脾两虚,胃阳不固,肺窍不利所致的鼻鼽,症见喷嚏、鼻塞、鼻痒、流清涕,畏寒恶风,动则喘乏,食少便溏;过敏性鼻炎见上述症状者。长期以汤药及配方颗粒形式用于治疗过敏性鼻炎,且具有较好的疗效。该方重用黄芪补脾益肺、实卫固表为君药;药理研究表明黄芪具有类激素样和免疫促进作用,提高机体免疫力,减少疾病复发[9];桂枝、白芍调和营卫,发表解肌为臣药。本研究结合颗粒剂性质稳定、生物利用度高、便于工业化生产和携带服用方便的优点,拟将其制成颗粒剂,为过敏性鼻炎患者提供一种新的中成药。根据处方中药物所含化学成分的理化性质及药理作用,采用正交实验法,以黄芪甲苷、芍药苷为指标,优选芪防鼻敏颗粒的水提醇沉工艺。
1 仪器与试药 1.1 仪器岛津LC-20AT高效液相色谱仪(日本岛津公司;Agilent1100 型高效液相色谱仪(美国Agilent 公司) ,2000ES蒸发光散射检测器( 奥泰公司); BT125D型电子分析天平(北京赛多利斯仪器系统有限公司);ZDHW型调温电热套(北京市中兴伟业仪器有限公司);KQ3200DE型数控超声波清洗器(江苏省昆山市超声仪器有限公司);DZ-28BC型真空干燥箱(天津市泰斯特仪器有限公司);HH-4型恒温水浴锅(国华电器有限公司)。
1.2 试药黄芪甲苷(中国药品生物制品检定研究院,批号:110781-201314);芍药苷(月旭材料科技(上海)有限公司,批号:23180-57-6);黄芪、白芍等饮片均购自北京同仁堂饮片有限责任公司,经检验符合《中华人民共和国药典》(2010版)标准,甲醇、乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
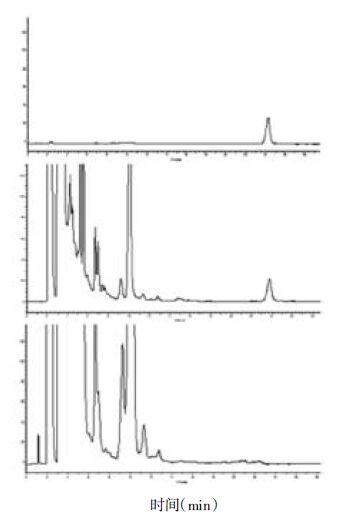
2 方法与结果 2.1 黄芪甲苷含量测定 2.1.1 色谱条件安捷伦Agilent Zorbax SB-C18色谱柱(4.6 mm×250 mm,5 μm),乙腈-水(30∶70)为流动相,流速1.0 mL/min,柱温25 ℃,蒸发光散射检测器(ELSD)参数:漂移管温度100 ℃,载气(压缩空气)流速2.7 L/min,进样量10 μL(图1)。
|
| A:芍药苷对照品;B:供试品;C:阴性样品 图1 黄芪甲苷液相色谱图 Fig.1 HPLC chromatograms of astragaloside IV |
精密称取黄芪甲苷对照品适量,加甲醇制成浓度为0.513 g/L的溶液,即得。
2.1.3 供试品溶液的制备取干膏适量,粉碎成细粉,精密称定,加水50 mL超声使溶解,用水饱和正丁醇振摇提取4次,每次50 mL,合并正丁醇液,用氨试液充分洗涤2次,每次50 mL,弃去氨试液,正丁醇液蒸干,残渣加甲醇溶解,转移至5 mL量瓶中,加甲醇至刻度,摇匀,用微孔滤膜(0.22 μm)滤过,取续滤液即得。
2.1.4 阴性样品溶液的制备按处方比例及制备工艺制备不含黄芪的干膏,按照2.1.3供试品制备方法制备样品即得阴性对照液。
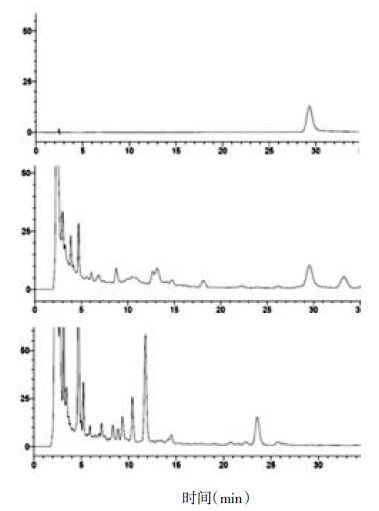
2.2 芍药苷含量测定 2.2.1 色谱条件Agilent Zorbax SB-C18色谱柱(4.6 mm×250 mm,5 μm),甲醇-0.1%磷酸溶液(21∶79)为流动相,流速1.0 mL/min,检测波长230 nm,柱温30 ℃,进样量5 μL(图2)。
|
| 图2 芍药苷液相色谱图 Fig.2 HPLC chromatograms of paeoniflorin |
精密称取芍药苷对照品适量,加甲醇制成浓度为0.042 96 mg/mL的溶液,即得。
2.2.3 供试品溶液的制备取干膏适量,粉碎成细粉,精密称定,置50 mL量瓶中,加甲醇35 mL,超声处理(功率150 W,频率40 KHz)30 min,放冷,加甲醇至刻度,摇匀,滤过,取续滤液过0.22 μm微孔滤膜滤过即得。
2.2.4 阴性样品溶液的制备按处方比例及制备工艺制备不含白芍的干膏,按照2.2.3供试品制备方法制备样品即得阴性对照液。
2.3 水提工艺优选 2.3.1 水提正交实验设计通过预实验研究参考相关文献[10, 11, 12, 13],选取加水倍量、提取时间、提取次数为影响因素,以黄芪甲苷提取率、芍药苷提取率、干膏得率为考察指标优选最佳水提工艺,因素水平见表1。
| 水平 | 因素 | ||
| 加水倍量(倍)A | 提取时间(小时)B | 提取次数(次)C | |
| 1 | 8 | 1 | 1 |
| 2 | 10 | 1.5 | 2 |
| 3 | 12 | 2 | 3 |
2.3.2 实验方法
按处方比例称取黄芪、白芍等药材共9份,按L9(34)正交表进行水煎煮提取,提取液滤过,浓缩,真空干燥(65 ℃,-0.08 MPa)至恒重,精密称定重量,计算干膏得率。按照2.1.3、2.2.3供试品制备方法制备供试品,分别测定其中黄芪甲苷、芍药苷的提取率。
2.3.3 水提正交实验结果采用多指标综合评分法[14],以各指标提取率最大值为参照,将数据归一化分析,根据处方配比,黄芪(X)的权重系数为7/9,白芍(Y)的权重系数为2/9,综合评分(M)=(7X/9×74.93+2Y/9×79.47)×100。正交实验结果见表2,方差分析结果见表3。
| 编号 | A加水倍量(倍) | B提取时间(h) | C提取次数(次) | D空白列 | 黄芪甲苷提取率(%) | 芍药苷提取率(%) | 综合评分(分) |
| 1 | 1(8) | 1(1) | 1 | 1 | 46.70 | 28.91 | 56.56 |
| 2 | 1 | 2(1.5) | 2 | 2 | 64.07 | 58.34 | 82.82 |
| 3 | 1 | 3(2) | 3 | 3 | 71.35 | 58.34 | 90.38 |
| 4 | 2(10) | 1 | 2 | 3 | 73.88 | 35.27 | 86.55 |
| 5 | 2 | 2 | 3 | 1 | 74.93 | 79.47 | 100.00 |
| 6 | 2 | 3 | 1 | 2 | 50.57 | 45.44 | 65.20 |
| 7 | 3(12) | 1 | 3 | 2 | 71.49 | 64.77 | 92.33 |
| 8 | 3 | 2 | 1 | 3 | 56.78 | 63.19 | 76.61 |
| 9 | 3 | 3 | 2 | 1 | 74.03 | 68.06 | 95.87 |
| I | 229.76 | 235.44 | 198.37 | 252.44 | |||
| II | 251.75 | 259.43 | 265.25 | 240.34 | |||
| III | 264.81 | 251.45 | 282.71 | 253.55 | |||
| R | 35.05 | 23.99 | 84.34 | 13.20 |
| 来源 | 自由度 | 离差平方和 | 方差 | P |
| A | 2 | 209.15 | 104.57 | >0.05 |
| B | 2 | 99.53 | 49.77 | >0.05 |
| C | 2 | 1321.16 | 660.58 | <0.05 |
| 误差D | 2 | 35.77 | 17.88 | |
| 注:P<0.05为差异显著,P<0.01为差异极显著。 |
以综合评分为标准,直观分析表明,各因素影响大小顺序为C>A>B>D,最佳提取组合为A3B2C3,即药材加12倍量水煎煮3次,每次1.5 h;方差分析表明,提取次数C具有显著性差异,其余影响因素均无显著性差异,故确定水提取工艺为A3B2C3,即12倍量水,提取3次,每次1.5 h。
2.3.4 验证实验为进一步考察最佳提取工艺的稳定性与可靠性,按处方比例称取药材3份,按最佳提取工艺进行验证实验,操作方法同前述,测定黄芪甲苷、芍药苷提取率,结果见表4。
| 编号 | 黄芪甲苷提取率(%) | 芍药苷提取率(%) | 综合评分(分) |
| 1 | 74.96 | 77.57 | 98.92 |
| 2 | 76.02 | 73.33 | 98.79 |
| 3 | 73.47 | 76.71 | 97.14 |
| 平均值 | 74.82 | 75.87 | 98.28 |
结果表明,验证实验结果与正交表中最优实验组结果相当,说明该提取工艺稳定可行。
2.4 醇沉工艺优选 2.4.1 相对密度对醇沉工艺的影响影响醇沉的主要因素有药液浓缩相对密度、醇浓度,查阅相关文献显示,黄芪、白芍等药的水提液醇沉浓度多为60%[15, 16]。以黄芪甲苷、芍药苷转移率为指标,考察相对密度对60%醇沉工艺的影响。按处方称取药材以最佳提取工艺提取,药液浓缩至相对密度分别为(60 ℃)1.05~1.10、1.10~1.15 、1.15~1.20左右,加入乙醇至60%,冷藏静置过夜,减压过滤,上清液浓缩得干浸膏,按照2.1.3、2.2.3供试品制备方法制备供试品,分别测定其中黄芪甲苷、芍药苷的转移率。
2.4.2 实验结果通过综合评分法直观分析醇沉最佳相对密度为1.15~1.20(60 ℃),在此条件下黄芪甲苷、芍药苷均有较高的转移率,故确定最佳醇沉工艺为提取液浓缩至相对密度1.15~1.20(60 ℃),醇沉浓度为60%,冷藏静置过夜。相对密度对醇沉工艺影响实验结果见表5。
| 编号 | 相对密度(60%) | 黄芪甲苷转移率(%) | 芍药苷转移率(%) | 综合评分(分) |
| 1 | 1.05~1.10 | 76.22 | 85.54 | 95.05 |
| 2 | 1.10~1.15 | 76.89 | 88.26 | 96.38 |
| 3 | 1.15~1.20 | 80.64 | 85.73 | 99.36 |
称取处方量药材,按照最优水提醇沉工艺验证3批,验证结果见表6,与醇沉实验最优实验比较,说明该醇沉工艺稳定可行。
| 编号 | 黄芪甲苷转移率(%) | 芍药苷转移率(%) | 综合评分(分) |
| 1 | 77.32 | 88.55 | 94.91 |
| 2 | 81.43 | 85.91 | 98.12 |
| 3 | 82.73 | 80.85 | 98.07 |
| 平均值 | 80.49 | 85.10 | 97.03 |
处方中药味较多,成分复杂,若以单一成分为评价指标优选最优提取条件,不能保证其整体质量,故本实验以君药黄芪的主要有效成分黄芪甲苷、臣药白芍主要有效成分芍药苷为综合评价指标,考察芪防鼻敏颗粒的最优水提醇沉工艺,使其更具有代表性、全面性。
3.2确定的水提醇沉条件与文献[15, 16, 17, 18]基本一致。
4 结论实验采用正交实验,以黄芪甲苷、芍药苷提取率综合评分为指标,优选出芪防鼻敏颗粒的最优水提醇沉工艺,验证实验表明,该工艺稳定可行,可用于指导制剂生产。
| [1] | 闭 旭. 变应性鼻炎的研究进展[J]. 中外医学研究, 2013,11(34):154-156. |
| [2] | 林秋良. 变应性鼻炎的发病因素、症状证候特征及饮食特征研究[D]. 北京:北京中医药大学,2006. |
| [3] | 谢 强,付文洋. 变应性鼻炎中医治疗研究现状[J]. 西部中医药,2015, 28(3):140-142. |
| [4] | 黄圣文. 过敏性鼻炎证治的古今文献研究[D]. 北京:北京中医药大学, 2006. |
| [5] | 吴继勇. 益气温阳方治疗变应性鼻炎的临床研究[D]. 南京:南京中医药大学, 2010. |
| [6] | 张靓冉,阮 标,余咏梅. 变应性鼻炎治疗的研究进展[J]. 中国现代医生,2015,53(18):155-160. |
| [7] | 韦木春. 过敏性鼻炎的治疗药物研究进展[J]. 中国医药指南,2013, 11(20):497-498. |
| [8] | 章文华,孟宪军. 过敏性鼻炎的中医辨证论治[J]. 光明中医,2009, 24(4):780-781. |
| [9] | 王兰娣, 黄 芸. 大剂量生黄芪治疗变应性鼻炎临床观察[J]. 光明中医, 2013, 28(1):193-194. |
| [10] | 陈永祥,孙耀志,高 松,等. 正交试验优选黄芪桂枝五物汤的水提取工艺[J]. 中国实验方剂学杂志,2012,18(2):56-58. |
| [11] | 钱 琳,邓 楠. 黄芪提取工艺研究[J]. 中国现代医学杂志,2009, 19(11):1605-1608. |
| [12] | 孙文格,赵午申,郑 倩,等. 正交设计法优选调胃颗粒的水煎煮提取工艺[J]. 中国医院药学杂志,2010,30(13):1158-1159. |
| [13] | 王 帆,桂双英,王举涛. 正交试验法优选复方白芍颗粒提取工艺[J]. 安徽中医学院学报,2012,31(6):71-73. |
| [14] | 陈 雯,杜守颖,陆 洋. 多指标正交试验优选仙灵骨葆胶囊中丹参、补骨脂提取工艺[J]. 中国中药杂志, 2009, 34(14):1792-1794. |
| [15] | 陈伟铭,窦建卫,王静怡,等. 正交试验优选养心开郁片醇沉工艺[J]. 陕西中医,2015,36(01):109-111. |
| [16] | 李霁明. 白芍单味颗粒剂水煎醇沉工艺研究[J]. 安徽医药,2011, 15(2):156-157. |
| [17] | 石 航,白 洁,冯 欣,等. 多指标优选芪归银方的水提醇沉工艺[J]. 中华中医药学刊, 2015,33(4):813-816. |
| [18] | 刘晓华,于小华. 正交设计法优选黄芪中黄芪甲苷的最佳水提取工艺[J]. 海峡药学,2010,22(8):22-23. |
2. China-Japan Friendship Hospital and Key Laboratory of the State Pharmaceutical Administration, Beijing 100029, China
 2016, Vol. 33
2016, Vol. 33