文章信息
- 柴士伟, 刘芳
- CHAI Shi-wei, LIU Fang
- 淫羊藿化学成分分离鉴定
- Isolation and identification of chemical constituents from Epimedium brevicornu Maxim.
- 天津中医药, 2016, 33(2): 114-117
- Tianjin Journal of Traditional Chinese Medicine, 2016, 33(2): 114-117
- DOI: 10.11656/j.issn.1672-1519.2016.02.14
-
文章历史
- 收稿日期: 2015-09-16
淫羊藿为小檗科淫羊藿属植物淫羊藿(Epimedium brevicornu Maxim.)、箭叶淫羊藿[Epime- dium sagittatum(Sieb. et Zucc.) Maxim]、柔毛淫羊藿(Epimedium pubescens Maxim.)或朝鲜淫羊藿(Epimedium koreanum Nakai)的干燥叶,具有补肾阳,强筋骨,祛风湿的功效。常用于肾阳虚衰,阳萎遗精,筋骨微软,风湿痹痛,麻木拘挛等[1, 2, 3, 4, 5]。文献报导其主要含有黄酮、菲、木脂素、酚苷以及紫罗酮类等化学成分[6, 7, 8, 9, 10, 11, 12]。本文采用有机溶剂萃取法,结合正相硅胶、Sephadex LH-20、反相ODS及制备高效液相等柱色谱法,从淫羊藿干燥叶体积分数95%乙醇提取物中分离鉴定了7个化合物,经波谱方法鉴定其结构分别为:2,3,4,6,7-五甲氧基-菲(1)、4,5,-二羟基-2,3,6 -三甲氧基-9,10-二氢菲(2)、5,7,4′-三甲氧基-4-苯基香豆素(3)、3,5,7,4′-四甲氧基黄酮(4)、4-羟基-3-异戊二烯基-苯甲酸(5)、4-羟基肉桂酸甲酯(6)、4-羟基-(2E)-2-壬烯酸(7),其中化合物1~7均为首次从淫羊藿属植物分离得到。
1 药材、仪器和试剂淫羊藿药材购买于河北省安国市药材市场,经天津中医药大学第一附属医院主任药师马瑛鉴定为小檗科淫羊藿属植物淫羊藿(Epimedium brevicornu Maxim.)的干燥叶,标本(20130125)存放于天津中医药大学第一附属医院饮片库房。
制备高效液相色谱仪为Agilent 1200 series(美国安捷伦公司);制备色谱柱:Agilent Eclipse XDB-C18柱(250 mm×21.2 mm,7μm);Agilent 6410三重四级杆质谱仪(美国安捷伦公司);BRUKER AVANCE Ⅲ 500超导核磁共振波谱仪(瑞士布鲁克公司,TMS为内标)。
柱层析硅胶(青岛海洋化工厂分厂);薄层层析板(天津思利达科技有限公司);反相ODS(50 μm,120 Å,日本YMC公司);Sephadex LH-20(美国GE公司);分析纯甲醇、乙醇、石油醚(60~90 ℃)、乙酸乙酯及色谱纯甲醇(天津市康科德科技有限公司)、分析纯二氯甲烷、氯仿、丙酮(天津市江天化工技术有限公司)。
2 提取与分离20 kg淫羊藿干燥叶粗粉用8倍量体积分数为95%乙醇回流提取3次,每次2 h,滤过,合并滤液,50 ℃下减压回收,真空干燥得干膏3 800 g。取3 000 g,加去离子水10 000 mL混悬,用等体积的乙酸乙酯萃取3次,合并乙酸乙酯层,减压浓缩得乙酸乙酯萃取物约1 000 g。对萃取物进行硅胶柱层析分离,二氯甲烷-丙酮(1:0→10:1→5:1,2:1→1:1→0:1)梯度洗脱,薄层(TLC)检识,合并相同流分,得8个流分(Fr.1-8)。
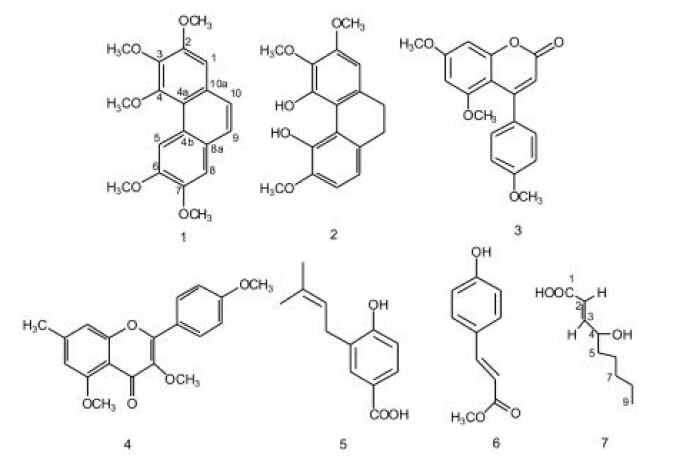
Fr.2(100 g)经硅胶柱色谱,石油醚-丙酮(100:0→0:100)梯度洗脱,TLC检识,合并相同流分,得到12个流分,其中Fr.1.12 (620 mg)经ODS开放柱色谱和制备高效液相色谱制备得到了化合物1(23 mg)。Fr.4(112 g)经硅胶柱色谱,石油醚-丙酮(100:0→0:100)梯度洗脱,得到8个流分,其中Fr.4.7(1 120 mg)经ODS开放柱色谱和制备高效液相色谱分离得到了化合物2(34 mg)和化合物4(90 mg)。Fr.4.8(935 mg)经ODS开放柱色谱和制备高效液相色谱分离得到了化合物3(10 mg)。Fr.6(160 g)经ODS开放柱色谱和制备高效液相色谱分离得到了化合物7(20 mg)。Fr.8(130 g)经硅胶柱色谱,二氯甲烷-甲醇(100:0→0:100)梯度洗脱,TLC检识,合并相同流分,得到15个流分,其中Fr.8.8 (510 mg)经sephadex LH-20(甲醇洗脱)及ODS开放柱色谱和制备高效液相色谱分离得到了化合物5(65 mg);Fr.8.15 (620 mg)经sephadex LH-20及ODS开放柱色谱和制备高效液相色谱分离得到了化合物6(35 mg)。化合物1~7的结构式见图1。
|
| 图1 化合物1~7结构 Fig.1 Structures of compounds 1~7 |
化合物1: 白色无定形粉末,易溶于甲醇。在正离子MS谱中,可观测到准分子离子峰m/z:329.1 [M+H]+,推测其分子量为328。在1H-NMR(500 MHz,CD3OD) 谱低场区,可以观测到5个芳香氢质子信号:δ 7.19(1H,s,H-1),7.30(1H,s,H-8),7.52(1H,d,J = 8.5 Hz,H-10),7.57(1H,d,J = 8.5 Hz,H-9),9.03 (1H,s,H-5);在中高场区可以观测到5个甲氧基质子信号δ 3.97(3H,s,7-OCH3),3.97(3H,s,3-OCH3),3.98(3H,s,2-OCH3),3.99(3H,s,4-OCH3),4.01(3H,s,6-OCH3)。在13C-NMR(125 MHz,CD3OD)谱上出现14个相应的芳香碳信号:δ 106.6(C-1),153.2(C-2),143.8 (C-3),152.7(C-4),108.9 (C-5),150.2(C-6),149.6 (C-7),109.7(C-8),127.3(C-9),126.0(C-10),119.7(C-4a),125.6(C-4b),128.9 (C-8a)和131.2(C-10a),以及5个甲氧基信号:δ 56.2(2-OCH3),61.7(3-OCH3),61.1(4-OCH3),56.4 (6-OCH3)和56.3 (7-OCH3)。1H、13C-NMR谱数据与文献对照[13],结果基本一致,鉴定化合物1为2,3,4,6,7-五甲氧基-菲。
化合物2:白色无定形粉末,易溶于甲醇。在正离子ESI-MS谱中,可以观测到准分子离子峰m/z:303.0 [M+H]+,推测其分子量为302。在1H-NMR (500 MHz,CD3OD)谱低场区,可以观测到3个芳香氢质子信号:δ 6.60(1H,s,H-1),6.80(1H,d,J = 8.0 Hz,H-8),6.84(1H,d,J = 8.0 Hz,H-7);在高场区可以观测到一组脂肪氢质子信号:δ 2.61(4H,br s,H-9,10)及3个甲氧基质子信号δ 3.82 (3H,s,3-OCH3),3.87 (3H,s,2-OCH3),3.88(3H,s,6-OCH3)。在13C-NMR (125 MHz,CD3OD) 谱上出现12个相应的芳香碳信号:δ 105.6 (C-1),153.4 (C-2),137.8 (C-3),148.3 (C-4),142.6 (C-5),149.0 (C-6),110.8 (C-7),120.2 (C-8),116.4 (C-4a),122.4 (C-4b),133.8 (C-8a) 和137.7 (C-10a),以及2个脂肪碳和3个甲氧基信号:δ 31.6 (C-9),32.7 (C-10),56.8 (2-OCH3),61.2 (3-OCH3)和56.5 (6-OCH3)。1H、13C-NMR谱数据与文献对照[14],结果基本一致,鉴定化合物2为4,5,-二羟基-2,3,6 -三甲氧基-9,10-二氢菲。
化合物3:白色无定形粉末,易溶于甲醇。在正离子ESI-MS谱中,可以观测到准分子离子峰m/z:312.9[M+H]+,推测其分子量为312。在1H-NMR(500 MHz,CD3OD)谱低场区,可以观测到一组AA′BB′芳香氢质子信号:δ 6.99(2H,d,J=8.5 Hz,H-3′,5′),7.81(2H,d,J=8.5 Hz,H-2′,6′),还可观测到3个孤立的芳香质子信号:δ 6.41(1H,s,H-6),6.51(1H,s,H-3),6.64(1H,s,H-8);在中高场区可以观测到3个甲氧基质子信号:δ 3.85(3H,s,5-OCH3),3.86(3H,s,4′-OCH3),3.90(3H,s,7-OCH3)。在13C-NMR(125 MHz,CD3OD)谱上出现1个内酯羰基信号:δ179.9(C-2);14个相应的芳香碳信号:δ107.1(C-3),163.4(C-4),162.0(C-5),97.4(C-6),166.4(C-7),94.2(C-8),109.1(C-4a),161.2(C-8a),124.3(C-1′),129.0(C-2′,6′),115.5(C-3′,5′)和164.1(C-4′);碳谱中还可观测到3个甲氧基信号:δ56.6(7-OCH3),56.5(4′-OCH3)和56.0(5-OCH3)。1H、13C-NMR谱数据与文献对照[15],结果基本一致,鉴定化合物3为5,7,4′-三甲氧基-4-苯基香豆素。
化合物4:黄色无定形粉末,易溶于甲醇。在正离子ESI-MS谱中,可以观测到准分子离子峰m/z:342.9[M+H]+,推测其分子量为342。在1H-NMR(500 MHz,CD3OD)谱低场区,可以观测到2个间位耦合芳香氢信号:δ6.45(1H,d,J=2.0 Hz)和δ 6.66(1H,d,J=2.0 Hz)分别为6位和8位氢信号;低场区还可观测到B环的一组AA′BB′芳香氢信号:δ 7.05(2H,d,J=9.0Hz,H-3′,5′),8.05(2H,d,J=9.0 Hz,H-2′,6′),提示B对位取代;此外,还可观测到4个甲氧基质子信号:δ 3.77(3H,s,3-OCH3),3.87(3H,s,4′-OCH3),3.90(3H,s,5-OCH3)和3.91(3H,s,7-OCH3)。在13C-NMR(125 MHz,CD3OD)谱上出现黄酮苷元相应的碳信号:δ 155.3(C-2),141.9(C-3),176.0(C-4),162.3(C-5),97.1(C-6),166.3(C-7),93.8(C-8),160.3(C-9),109.8(C-10),123.9(C-1′),131.1(C-2′,6′),115.1(C-3′,5′)和163.2(C-4′),以及4个甲氧基信号:δ 60.3(3-OCH3),56.6(5-OCH3),56.6(7-OCH3)和56.0(4′-OCH3)。1H、13C-NMR谱数据与文献对照[16],结果基本一致,鉴定化合物4为3,5,7,4′-四甲氧基黄酮。
化合物5:白色粉末,易溶于氯仿。在正离子ESI-MS谱中,可观测到准分子离子峰m/z:207.1[M+H]+,推测其分子量为206。在1H-NMR(500 MHz,CD3OD)谱低场区,可以观测到一组ABX芳香氢质子信号:δ 6.78(1H,d,J=8.0 Hz,H-5),7.70(1H,dd,J=2.0,8.0 Hz,H-6),7.74(1H,d,J=2.0Hz,H-2);还可以观测到1个烯氢信号:δ5.32(1H,t,J=7.5Hz,H-2′);在高场区可以观测到一组脂肪氢质子信号:δ 3.29(2H,m,H-1′)及2个甲基质子信号δ 1.72(3H,s,H-4′),1.75(3H,s,H-5′)。13C-NMR(125 MHz,CD3OD)谱上出现6个相应的芳香碳信号:δ122.5(C-1),132.5(C-2),129.4(C-3),166.1(C-4),115.3(C-5)和130.5(C-6);1个羰基碳信号δ170.5(C-7),及一组异戊二烯基信号δ29.0(C-1′),123.3(C-2′),133.7(C-3′),17.9(C-4′),26.0(C-5′)。1H、13C-NMR谱数据与文献对照[17],结果基本一致,鉴定化合物5为4-羟基-3-异戊二烯基-苯甲酸。
化合物6:白色无定形粉末,易溶于甲醇。在正离子ESI-MS谱中,可以观测到准分子离子峰m/z:179.1[M+H]+,推测其分子量为178。在1H-NMR(500 MHz,CD3OD)谱低场区,可以观测到一组AA′BB′芳香氢质子信号:δ 6.81(2H,d,J=9.0Hz,H-3′,5′),7.46(2H,d,J=9.0Hz,H-2′,6′),及一对反式烯氢信号:δ 6.32(1H,d,J=16.0 Hz,H-8),7.62(1H,d,J=16.0 Hz,H-7);氢谱中还可观测到1个甲氧基信号:δ 3.35(3H,s,9-OCH3)。在13C-NMR(125 MHz,CD3OD)谱上出现6个相应的芳香碳信号:δ127.3(C-1),131.2(C-2,6),116.9(C-3,5),161.3(C-4),一对烯碳信号:δ146.8(C-7),115.4(C-8),1个羰基碳信号δ168.7,以及1个甲氧基信号δ 49.9。1H、13C-NMR谱数据与文献对照[18],结果基本一致,鉴定化合物6为4-羟基肉桂酸甲酯。
化合物7:白色无定形粉末,易溶于甲醇。在正离子ESI-MS谱中,可以观测到准分子离子峰m/z:173.1[M+H]+,推测其分子量为172。在1H-NMR(500 MHz,CD3OD)谱低场区,可以观测到一组反式烯氢质子信号:δ 5.95(1H,dd,J=1.5,16.0 Hz,H-2),6.90(1H,dd,J=5.0,16.0 Hz,H-3);氢谱中还可观测到:δ 0.91(3H,t,J=7.0 Hz,H-9),1.33(4H,m,H-6,8),1.35(2H,m,H-7),1.54(2H,m,H-5),4.21(1H,dd,J=5.0,11.0Hz,H-4)。在13C-NMR(125 MHz,CD3OD)谱上出现2个相应的烯碳信号:δ121.1(C-2),152.7(C-3),71.7(C-4),37.6(C-5),26.2(C-6),23.9(C-7),32.9(C-8),14.4(C-9);碳谱中还有1个羰基碳信号δ170.2(C-1)。1H、13C-NMR谱数据与文献对照[19],结果基本一致,鉴定化合物7为4-羟基-(2E)-2-壬烯酸。
4 结论从淫羊藿叶体积分数为95%的乙醇提取物的乙酸乙酯萃取物中分离鉴定了7个化合物,分别为:2,3,4,6,7-五甲氧基-菲(1)、4,5,-二羟基-2,3,6-三甲氧基-9,10-二氢菲(2)、5,7,4′-三甲氧基-4-苯基香豆素(3)、3,5,7,4′-四甲氧基黄酮(4)、4-羟基-3-异戊二烯基-苯甲酸(5)、4-羟基肉桂酸甲酯(6)、4-羟基-(2E)-2-壬烯酸(7)。化合物1~7为首次从淫羊藿属分离得到化合物。
| [1] | 国家药典委员会. 中华人民共和国药典[S]. 北京:中国医药科技出版社, 2010. |
| [2] | 孟宁, 孔凯, 李师翁, 等. 淫羊藿属植物化学成分及药理活性研究进展[J]. 西北植物学报, 2010,30(5):1063-1073. |
| [3] | 谢娟平,孙文基. 淫羊藿属植物化学成分及药理研究进展[J]. 海峡药学, 2006,18(5):17-20. |
| [4] | 宋剑,王超,李知遥, 等. 淫羊藿总黄酮抗老年痴呆化学成分研究[J]. 中国现代中药, 2009,11(8):23-26. |
| [5] | 李牡丹,石旭,关萍. 淫羊藿的研究进展[J]. 山地农业生物学报, 2009,28(2):170-174. |
| [6] | 韩广轩, 王麦莉, 张军东, 等. 淫羊藿化学成分的研究进展[J]. 药学实践杂志, 2002,20(6):359-361. |
| [7] | 韩冰, 沈彤, 鞠建华, 等. 淫羊藿属植物化学成分研究概况[J]. 国外医药·植物药分册. 2003,18(4):151-153. |
| [8] | 袁航,曹树萍,陈抒云, 等. 淫羊藿的化学成分及质量控制研究进展[J]. 中草药, 2014,45(24):3630-3640. |
| [9] | 贾敏鸽,周金云,孙文基. 陕西产淫羊藿资源分布与化学成分研究概况[J]. 时珍国医国药,2006,17(10):2087-2091. |
| [10] | 郭丽娜,马莹慧,赵伟, 等. 淫羊藿属植物中化学成分分析研究进展[J]. 中国新药杂志,2013,22(8):919-922,936. |
| [11] | 李遇伯,孟繁浩,鹿秀梅, 等. 淫羊藿化学成分的研究[J]. 中国中药杂志, 2005,30(8):586-588. |
| [12] | 刘丽萍,徐晓芳,孙东东, 等. 淫羊藿水提部位化学成分的HPLC-ESI-Q-TOF-MS分析[J]. 中国实验方剂学杂志, 2014,20(19):112-116. |
| [13] | Leong YW, Kang CC, Harrison LJ, et al. Phenanthrenes, dihydrophenanthrenes and bibenzyls from the orchid bulbophyllum vaginatum[J]. Phytochemistry, 1997, 44(1):157-165. |
| [14] | Radwan MM, ElSohly MA, Slade D, et al. Non-cannabinoid constituents from a high potency Cannabis sativa variety[J]. Phytochemistry, 2008, 69:2627-2633. |
| [15] | Ito A, Chai HB, Shin YG, et al. Cytotoxic constituents of the roots of exostema acuminatum[J]. Tetrahedron, 2000, 56:6401-6405. |
| [16] | Sutthanut K, Sripanidkulchai B, Yenjai C, et al. Simultaneous identification and quantitation of 11 flavonoid constituents in kaempferia parviflora by gas chromatography[J]. Journal of Chromatography A, 2007, 1143:227-233. |
| [17] | Hayashi K, Komura S, Isaji N, et al. Isolation of antioxidative compounds from brazilian propolis:3,4-dihydroxy-5-prenylcinnamic acid, a novel potent antioxidant[J]. Chemical & Pharmaceutical Bulletin, 1999, 47(11):1521-1524. |
| [18] | Percec V, Peterca M, Sienkowska MJ, et al. Heiney. Synthesis and retrostructural analysis of libraries of AB3 and constitutional isomeric AB2 phenylpropyl ether-based supramolecular dendrimers[J]. Journal of the American Chemical Society, 2006,128(10):3324-3334. |
| [19] | McGrath CE, Tallman KA, Porter NA, et al. Structure-activity analysis of diffusible lipid electrophiles associated with phospholipid peroxidation:4-Hydroxynonenal and 4-Oxononenal Analogues[J]. Chemical Research in Toxicology, 2011, 24:357-370. |
 2016, Vol. 33
2016, Vol. 33