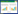文章信息
- 张铁军, 许浚, 韩彦琪, 张洪兵, 龚苏晓
- ZHANG Tie-jun, XU Jun, HAN Yan-qi, ZHANG Hong-bing, GONG Su-xiao
- 中药大品种质量标准提升研究的思路与实践
- Research ideas and application on the quality standard improvement of major traditional Chinese medicine varieties
- 天津中医药, 2017, 34(1): 4-12
- Tianjin Journal of traditional Chinese Medicine, 2017, 34(1): 4-12
- http://dx.doi.org/10.11656/j.issn.1672-1519.2017.01.03
-
文章历史
- 收稿日期: 2016-10-13
中医药是中华民族的宝贵遗产,是世界传统医药的瑰宝,为中华民族的生存繁衍作出了不可磨灭的贡献。但是,近些年来,由于各种原因,中医药的有效性受到各种质疑,“古方虽效,今用无功”、“品质退化”、“中医将毁于中药”等说法频繁见于各种报道;同时,随着化药的一致性评价、中药的工艺核查以及中药制药工业的技术升级等制药工业技术要求和政策环境的发展变化,使中药质量成为行业关注的焦点,同时,也对中药的标准化建设提出更高的要求。
近些年来,中药科技工作者为中药质量控制做了大量的工作,我国中药质量控制水平也有了长足的进步,但现行质量标准仍存在诸多问题:1)质量控制指标单一,质控指标与中药的安全性、有效性关联性不强,成分的专属性特异性不强,含量低。2)质控方法的科学性、专属性差。3)限度性标准及标准限度的确定与实际情况存在较大差异。这些现实情况使得现行质量控制方法和质量标准难以合理反映和评价中药的有效性和质量一致性。因此,迫切需要建立和完善中药质量控制的科学模式,对中药质量进行系统提升研究。
中药大品种通过质量标准提升研究,建立可溯源的、与临床疗效高度关联的全程质量控制体系和质量标准,为中药质量控制提供可参照的模式和研究范例。
笔者以疏风解毒胶囊和元胡止痛滴丸为例,论述中药大品种质量标准提升研究的思路、方法与实践。
1 质量控制指标(质量标志物)的筛选和确定中药成分复杂,各成分具有不同的生物活性,各成分之间在疾病生命系统中表现出复杂的关联规律,体现“多重药理功效”特点,这也是中药复方配伍原理和中药干预疾病的特色及优势的核心所在。因此,建立复方中药质量控制的科学模式,首先要通过中药化学物质组与其生物效应表达相关性研究,确定质量控制的核心指标,进而以质量要素完整性表达的技术方法建立系统、全面的质量控制体系。
1.1 化学物质组的辨识和表征 1.1.1 原型成分的辨识和表征复方中药化学成分极为复杂,化学成分是中药发挥疗效的物质基础。药效物质基础不清是质量标准提升的最大障碍,因此,首先应研究和辨识中药的化学成分构成,阐明中药的物质基础,进而为中药质量控制指标的确定以及质量要素的传递、溯源和质量控制提供明确的指标和依据。
本课题组[1-4]对疏风解毒胶囊的化学物质基础进行研究,通过高效液相色谱-四级杆-飞行时间串联质谱法(HPLC-Q-TOF-MS/MS)共识别了96个离子流色谱峰,分析确定了其中94个化合物:氨基酸7个,糖类1个,环烯醚萜类7个,苯乙醇苷类11个,二苯乙烯类1个,黄酮类24个,木脂素类6个,蒽醌类6个,三萜类18个,香豆素类1个,生物碱类5个,其他小分子化合物2个。对所有化合物分别进行了药材来源归属,结果分别来源于处方中的虎杖(12个)、连翘(18个)、板蓝根(14个)、柴胡(8个)、败酱草(14个)、马鞭草(11个)、芦根(5个)、甘草(21个)。
采用高效液相色谱-串联质谱(HPLC-MS/MS)方法,对元胡止痛滴丸所含生物碱和香豆素类成分进行表征和辨识,共鉴定出元胡止痛滴丸中51个化合物,包括28个生物碱类成分和23个香豆素类成分。包括原小檗碱类,原阿片碱类、阿朴啡类等。白芷主要的化学成分为香豆素类,主要为线性呋喃香豆素如欧前胡素、异欧前胡素等,此外还含有线性二氢香豆素、角型香豆素、角型二氢香豆素、简单香豆素等。
通过上述研究基本阐明了中药大品种疏风解毒胶囊和元胡止痛滴丸的化学物质组,并对各成分的药材来源进行归属,可作为质量溯源的依据。
1.1.2 入血成分及其代谢产物的辨识大多数中药临床口服用药,原型药效物质需吸收入血才能发挥作用,质量控制应关联药物的最终“效应成分”。因此,原型化学物质组阐明之后,应进一步分析入血成分及其代谢产物。并且,基于化合物-靶点-通路的药物成分“显效形式”,根据疾病的病理部位和药物干预方式,应进一步对入血成分的组织分布进行研究。
本课题组[5]采用血清药物化学的方法,运用UPLC-Q/TOF-MS结合代谢组学的方法,快速地分析和鉴定了口服给予元胡止痛方后大鼠血浆和脑组织中的吸收原型成分及其代谢产物。从口服给予元胡止痛滴丸后大鼠血浆中鉴定出40个与元胡止痛滴丸相关的外源性化学成分,包括26个原型成分和14个代谢产物。其中15个原型成分同样在给药组大鼠脑组织中被检测到,表明它们能够穿过血脑屏障渗透进入脑组织,是主要用来治疗头痛的最终效应成分。
通过上述研究基本阐明了元胡止痛滴丸的化学物质组、入血成分及其代谢产物以及透过血脑屏障成分。从药物体内过程角度进一步锁定质量控制指标。
1.2 化学成分生源途径及特有性分析中药化学成分复杂,一种中药含有多种化学成分,而不同药材可能含有相同的化学成分。如:小檗碱广泛存在于毛茛科、小檗科、芸香科等的药材中;黄酮类成分芦丁、酚酸类成分原儿茶酸等分布更为广泛。这类成分难以反映中药材中的特有性,作为质量控制指标依据不足。中药化学成分多为植物的次生代谢产物,次生代谢产物是植物在长期的进化中对环境的适应结果,其在植物中生成和分布通常有种属、器官组织和生长发育期的特异性。这些在植物体内含量不等的次生代谢物均有自己独特的合成途径。因此,在明确中药的化学物质组的前提下,通过对化学成分的生源途径及特有性进行分析,选择具有代表性、特异性的化学成分,进一步聚焦锁定质量控制指标,提高质量控制的针对性和指向性。
本课题组对元胡止痛滴丸中延胡索的化学成分的生源途径和特有性进行了分析。延胡索中的生物碱类化合物主要为3类,分别是原小檗碱型生物碱(叔胺类延胡索甲素、延胡索乙素等和季铵类小檗碱、巴马汀等)、原托品碱型生物碱(原阿片碱、α-别隐品碱等)和阿朴菲型生物碱(D-海罂粟碱等)。这3类生物碱具有共同的生源前体——酪氨酸,酪氨酸首先合成2种前体原料多巴胺和4-羟基苯乙醛,这2种前体原料在去甲乌药碱合成酶的作用下,缩合形成苄基异喹啉生物碱生物合成的第一个中间体去甲乌药碱。去甲乌药碱经过几次甲基化作用,接受来自腺苷甲硫氨酸的甲基,转化为另一个重要中间体(S)-网状番荔枝碱。(S)-网状番荔枝碱为四氢苯基异喹啉类生物碱合成途径的分支点。在特异性合酶的作用下(S)-网状番荔枝碱可进一步合成D-海罂粟碱、延胡索乙素、黄连碱、原阿片碱等生物碱[6-8],生源关系见图 1。
|
| 图 1 延胡索生物碱生源关系 Fig. 1 Biosynthesis relationship of alkaloids in Corydalis Rhizoma |
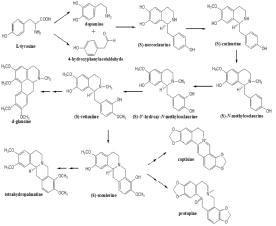
延胡索中的延胡索甲素、延胡索乙素、小檗碱、巴马汀、原阿片碱、α-别隐品碱等均属于异喹啉类生物碱。异喹啉生物碱在生源途径中是单一来源的生物碱,并且,在紫堇属植物中,苄基异喹啉类生物碱可能是原托品碱类、苯骈菲啶类、阿朴碱类、枯拉灵类等其它几种基核结构类型生物碱的前体物质,它们之间可能具有如图 2所示的生源关系[9-11]。
|
| 图 2 紫堇属植物生物碱的生源关系 Fig. 2 Biosynthesis relationship of alkaloids in plants from Corydalis DC. |
从成分的特异性分析:相对于原小檗碱型生物碱(叔胺类延胡索甲素、延胡索乙素等和季铵类小檗碱、巴马汀等)而言,原托品碱型生物碱(原阿片碱、α-别隐品碱等)和阿朴菲型生物碱(D-海罂粟碱等)处于生源途径的下游位置,因此,可认为该类成分的植物特异性较强,而原阿片碱、黄连碱更被视为罂粟科植物的特征性成分。从成分的量看,延胡索甲素、延胡索乙素等是延胡索的主要成分。
综合生源途径及成分的特异性分析,认为延胡索乙素、延胡索甲素、黄连碱、巴马汀、去氢延胡索甲素、D-四氢药根碱及原阿片碱可考虑作为延胡索的质量标志物。
1.3 药效物质基础的筛选和确认化学物质组不等同于药效物质基础,中药质量控制主要是通过药效物质基础(有效成分)的含量控制而达到对其有效性进行控制的目的。因此,在以上研究之后,还要进行药效物质基础的筛选和确认。
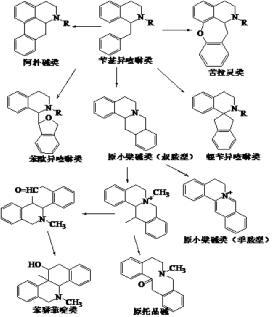
1.3.1 基于网络药理学方法药效物质基础的预测中药成分复杂,给药效物质基础研究带来诸多困难。近年来,网络药理学应用于中药作用机理研究和活性成分的预测,为中药的药效物质基础研究带来新的思路和方法。通过网络药理学研究,建立化合物-靶点-通路功效网络,预测药效物质基础及作用机理,提高研究效率。本课题组基于元胡止痛滴丸血清药物化学研究结果[5],并结合相关文献报道,选定延胡索中10个生物碱类入血原型成分,白芷中12个香豆素类入血原型成分和6个代谢物。采用网络药理学方法,利用反向对接技术对元胡止痛滴丸28个血中移行成分的作用靶点、通路进行虚拟预测,得到“化合物-靶点-通路”网络药理图(图 3)。结果表明,此28个化合物都能作用于与痛经相关的52个靶点及31条通路,其主要是通过激素调节、中枢镇痛、平滑肌解痉、抗炎和免疫相关通路来起到相应的治疗效果,体现了元胡止痛滴丸治疗痛经多成分多靶点的作用机制。
|
| 图 3 元胡止痛滴丸治疗痛经化合物-靶点-通路-功效网络图 Fig. 3 “Compound-Target-Pathway-Efficacy” network of Yuanhu Zhitong dropping pills (A: 254 nm下紫外谱图;B: 正模式质谱图;C: 负模式质谱图;D: NF-κB抑制率图) |
进一步选取元胡止痛滴丸中君药延胡索中的生物碱类代表性成分延胡索乙素、巴马汀、D-海罂粟碱和原阿片碱,及白芷中的两个香豆素类代表性成分欧前胡素和异欧前胡素,进行潜在靶点和作用通路的预测,通过分析实验数据发现,以延胡索乙素、巴马汀、海罂粟碱、原阿片碱为代表的生物碱类化合物可以单独作用于与中枢镇痛相关的9个蛋白靶点和9条信号通路,通过调节神经镇痛介质而发挥治疗痛经的作用。以欧前胡素和异欧前胡素为代表的香豆素类成分可单独作用于与性激素、炎症以及痉挛关系密切的9个蛋白靶点和2条信号通路,通过调节性激素的分泌与释放,抑制炎症因子的表达,缓解平滑肌痉挛而起到治疗原发性痛经的作用。同时,6个化合物还共同作用于涉及免疫反应、炎症表达、平滑肌痉挛以及性激素调节等相关的5个蛋白靶点和8条信号通路。
因此,提示延胡索乙素、巴马汀、D-海罂粟碱、原阿片碱、欧前胡素、异欧前胡素可能为元胡止痛滴丸主要药效物质基础,可作为质量标志物。
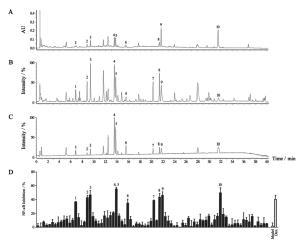
1.3.2 基于核心药效学指标的药效物质基础的确认采用核心药效学指标,进行组-效相关性的快速筛选也是中药复杂体系药效物质基础筛选确定的可行方法。疏风解毒胶囊为急性上呼吸道感染用药,抗炎作用为其主要药效学指标之一,本课题组[4]采用UPLC/Q-TOF-MS整合NF-κB双荧光素酶报告基因系统的筛选体系,快速准确地筛选鉴定疏风解毒胶囊中潜在的抗炎活性成分,明确其抗炎药效物质基础。通过活性筛选实验,在100余个流分中筛选确定了10个活性强的流分,并确定其结构。主要有苯乙醇苷类(连翘酯苷E、连翘酯苷A、异连翘酯苷A、毛蕊花糖苷)、环烯醚萜苷类(戟叶马鞭草苷、马鞭草苷)、木脂素类(连翘苷)、黄酮类(3-羟基光甘草酚、牡荆苷)和蒽醌类(大黄素)化合物。见图 4。
|
| 图 4 疏风解毒胶囊UPLC/Q-TOF及抗炎活性分析 Fig. 4 UPLC/Q-TOF for SJC and analysis on anti-inflammtory components |
进一步以原代小鼠腹腔巨噬细胞为研究对象,对筛选结果进行验证实验。建立了脂多糖(LPS)诱导的炎症模型,在体外细胞水平上评价马鞭草苷、连翘酯苷A、连翘苷、牡荆苷、大黄素五个单体化合物的抗炎效果。结果表明,五个化合物的干预能显著地抑制原代小鼠腹腔巨噬细胞中LPS诱导的肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)的表达水平,并且呈现一定的剂量依赖关系,验证了五个单体化合物的抗炎效果。
1.3.3 基于中药“药性”属性的药效物质基础的表征和确认药性中药的基本属性,反映了中药的本质特征,而性味配伍则是遣药制方的关键环节,是指导临床实践的重要基础理论。“药性”与“药效(功效)”均是中医药理论的核心概念,是从不同侧面、不同角度对中药的生物效应表达方式的客观描述。“药味(性)”和“药效”体现中药的“物质基础”作用人体疾病主体的不同层面、不同方式的生物效应表达形式,二者呈现复杂的离合关系。“性-效-物”的表征、相关性规律研究是阐释中药的药效物质基础、作用原理以及配伍规律、指导临床实践的重要依据和研究路径。因此,笔者提出将中药的“药性”纳入中药药效物质基础研究及质量评价指标筛选及确定依据。并提出研究表征方法和路径。
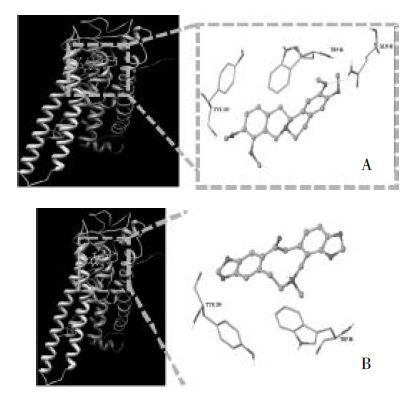
1.3.3.1 基于味觉、嗅觉受体分子对接的“性(味)”物质基础虚拟筛选和确定基于药物分子-味觉(嗅觉)受体结合理论,运用计算机虚拟筛选方法进行“性(味)”物质基础筛选。以延胡索和白芷代表性化合物为小分子配体库,进行hTAS2R10苦味受体对接筛选,其结果与阳性配体奎宁的对接结果比较发现,原小檗碱型的代表性化合物延胡索乙素与构建的苦味受体hTAS2R10的亲和力较强,而原托品碱类成分对接结果较差,故推测原小檗碱型化合物可能为延胡索药材中的苦味成分。对接结果见图 5。
|
| 图 5 hTAS2R10与延胡索乙素(A)和原阿片碱(B)结合模式图 Fig. 5 Docking results of hTAS2R10 with tetrahydropalmatine(A)and protopine(B) |
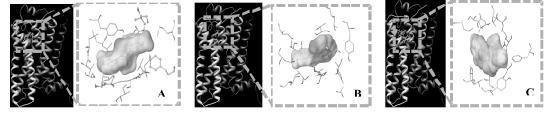
以延胡索和白芷代表性化合物为小分子配体库,进行OR7D4辛味受体对接筛选,其结果与阳性配体辣椒素对接打分比较发现,延胡索乙素、原阿片碱、欧前胡素与OR7D4的对接得分均高于辣椒素,初步推测其可能为辛味物质基础。对接结果见图 6。
|
| 图 6 OR7D4与欧前胡素(A)、延胡索乙素(B)和原阿片碱(C)结合模式图 Fig. 6 Docking results of OR7D4 with imperatorin(A),tetrahydropalmatine(B)and protopine(C) |
中药的“五味”具有功效的内涵,如辛“能散、能行”,甘“能补、能缓、能和”,酸“能收、能涩”,苦“能泄、能燥、能坚”,咸“能下、能软”。并与四气、升降浮沉、归经等药性理论存在复杂的内在联系。
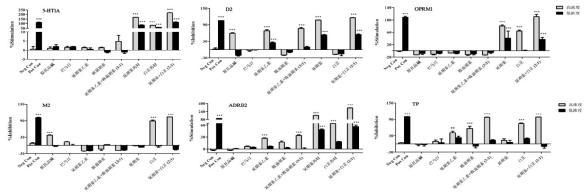
G蛋白偶联受体是一大类膜蛋白受体的统称。这类受体参与了很多细胞信号转导过程。与G蛋白偶联受体相关的疾病为数众多,并且大约40%的现代药物都以G蛋白偶联受体作为靶点。本课题组[13]应用胞内钙离子浓度变化荧光技术,对元胡止痛滴丸中延胡索、白芷药材及其主要成分进行G蛋白偶联受体结合实验,结果见图 7。
|
| 图 7 延胡索、白芷及其主要成分对6个GPCRs受体的激动和拮抗作用 Fig. 7 Activation and antagonism of Corydalis Rhizoma,Angelicae Radix,and representative six compounds on GPCRs |
结果表明:延胡索、白芷药材均可作用于多个相关功能受体,且2者配伍后效果优于单一给药;原小檗碱类延胡索乙素和原阿片碱类原阿片碱可作用于与辛、苦味相关的功能受体,故可能为辛、苦味物质基础;香豆素类欧前胡素可拮抗血栓素受体,体现了辛味药物活血化瘀的功效,其可能为辛味成分。延胡索和白芷配伍后可以通过激活5-羟色胺1A(5-HT1A)、M-阿片受体基因受体(OPRM1)、β2肾上腺素酯受体(ADRβ2)受体,抑制多巴胺Ⅱ型受体(D2)、M2和TP受体来调节一系列的下游生物信号转导效应,从而发挥多种生物活性,产生增效作用。延胡索乙素和欧前胡素配伍后可以通过激活ADRB2受体,抑制D2和TP受体来调节下游生物信号通路,从而发挥多种生物活性,产生增效作用。
通过以上研究,明确了中药大品种的化学物质组、药效物质基础及生源特异性成分,综合评价确定了质量控制指标。
2 样品测定和质量标准的确定质量控制指标确定以后,需建立质量控制方法,并应用建立的方法对研究对象进行测定,根据测定结果建立质量标准,按照建立的标准进行质量控制。一个“好的”质量标准,不但质量控制指标与其安全性、有效性的关联性强,而且还需要反映药材质量差异的真实情况,这样才能对中药的质量真伪、优劣和一致性进行合理有效的评价和控制。中药原料药材大多为来源于自然界的动植物有机体,与自然界存在千丝万缕的联系,并遵循生物遗传和变异的基本规律。在药材基原个体发育过程中,形成其质量的基本内容,因此,药材质量是由其种质的遗传物质基础及其个体发育过程中的生态(环境)历程所决定的。药材质量的表达具有多维性和多重性的特点,既反映在形态和化学物质组群等方面,又有药效和药性的两方面的基本内涵,并且,最终以方剂的形式在临床上得以体现。因此,实验样品的覆盖度和代表性对于质量标准的建立至关重要。
2.1 样品的覆盖度样品的覆盖度主要针对影响中药质量的基原种内变异、地理、生态差异和采收时间等要素。
2.1.1 基原中药基原以种界定分类学范围,但事实上种内变异广泛存在,按照经典分类学定义,“种是生命系统线上的基本间断”,而种内是连续的、多种式样的变异过程。实验研究取样一般在个体水平,但个体与种之间尚可能存在居群、变型、变种、亚种等分类阶元,种内变异可能表现在形态性状上,也可能表现在次生代谢产物上,由此产生不同质量差异[14]。因此,在质量研究中,待测样品应考虑研究对象种内变异的实际情况,取样应涵盖所用种内的不同类群,反映质量差异的幅度和变化规律。
2.1.2 产地中药材质量具有产地的依赖性,从某种意义上讲,同基原一样,产地也是中药材的基本属性之一,因此,才有“道地药材”的由来。但药用植物分布和散播有其自己系统进化的自然规律,特别是某些广布种,分布区地理跨度大,质量也有较大的差异。栽培药材也存在产地因素,特别是近些年来,因药材的供求变化,非道地产区或非原产地的引种栽培,也使栽培药材质量不一。因此,质量研究中,实验样品的产地覆盖度也至关重要。
2.1.3 生态条件生态因子是中药有效成分生物体内合成的重要条件,不仅土壤提供生物合成的原料来源,而光照、降雨、温湿等更是生物合成的反应条件。次生代谢产物的合成具有生态因子的敏感性,生态条件决定中药有效成分的含量和各成分之间的相对比例,进而决定中药的有效性。因此,质量研究中,实验样品产地的生态条件覆盖度亦非常重要,要考虑到样品产地的土壤、海拔、光照、坡向、生态群落等因素,保证实验样品的生态覆盖度。
2.2 取样代表性中药化学成分在中药基原的不同器官、组织、细胞中的分布不均一,不同器官、组织和细胞中有效成分的含量差异很大。在中成药生产和中药临床应用中,药材以数百公斤投料,而质量分析以克级取样测定,因此,如何能真实反映取样测定结果和投料药材的一致性,取样的代表性至关重要。
实验样品的取样方法直接决定研究结果的真实性。对于来源于生物有机体的中药材更为重要。实验样品的取样可分为野外(或田间)取样和实验室取样。野外取样一般应按居群取样和田间取样的规范方法;实验室取样应充分考虑到实验样品对于批次、器官、组织的代表性,特别是全草类药材,茎、叶、花、果不同器官中成分的含量差异很大,取样应还原到植株各器官的真实比例;成分在木质部、韧皮部、薄壁组织等不同组织部位的分布亦不均一,由于细胞壁的木化程度不同,组织部位的韧性和机械强度不同,样品粉碎难易程度、粒度等也存在差异,因此,实验室取样时需特别保证代表性和均一一致。
2.3 中药大品种生产过程“有效性获取”和“质量要素”的传递从药材到中成药还有中药生产的制备工艺过程,这一过程实现中药有效性的获取、变化和质量要素的传递。质量控制方法研究及质量标准确定应着眼于中药形成的全过程,以传递、溯源双向思维理念进行全程质量控制。药材的前处理、提取、纯化、浓缩、干燥直至制剂过程都会产生化学成分的获取、去除和复杂变化,工艺路线和工艺参数决定其结果,按照质量源于设计(QBD)的理念,“好的”质量控制手段和质量标准应体现全程质量控制和质量溯源。样品测定取样亦应遵循这一指导思想,增加各单元工艺过程及成品样品的覆盖度,以保证建立合理的质量标准。
样品测定后,建立完善的质量标准,对中药大品种质量标准进行全面提升。
3 中药大品种质量标准提升研究在以上研究思路指导下和在以上实验研究的基础上,对中药大品种疏风解毒胶囊和元胡止痛滴丸的质量标准进行全面提升研究。
3.1 疏风解毒胶囊质量标准提升研究 3.1.1 原料药材进行质量标准提升研究对虎杖、连翘、板蓝根、柴胡、败酱草、马鞭草、芦根、甘草8味药材进行了化学成分研究,通过液质指认分析,确定了虎杖等药材中共184个化合物[1-4];进一步建立了以上8味组成药材高效液相色谱(HPLC)指纹图谱评价体系[15-16],通过系统聚类分析和相似度评价系统建立各个药材对照指纹图谱共有模式,对每个药材的14批样品采用指纹图谱的方法进行质量评价;建立了马鞭草药材中戟马鞭草苷、马鞭草苷、毛蕊花糖苷3个成分的含量测定方法,方法简便、准确、重复性好。采用建立的方法对14批药材进行了测定;并照中国药典2010年版中虎杖、连翘、甘草、柴胡、板蓝根的含量测定方法,测定了5味药材共70批次的含量。对疏风解毒胶囊原料药材的质量标准进行了全面提升。
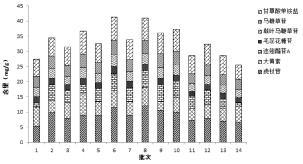
3.1.2 疏风解毒胶囊质量标准提升研究[17] 3.1.2.1 多指标成分含量测定依据筛选鉴定疏风解毒胶囊中潜在的抗炎活性成分,明确其抗炎药效物质基础主要有苯乙醇苷类(连翘酯苷E、连翘酯苷A、异连翘酯苷A、毛蕊花糖苷)、环烯醚萜苷类(戟叶马鞭草苷、马鞭草苷)、木脂素类(连翘苷)、黄酮类(3-羟基光甘草酚、牡荆苷)和蒽醌类(大黄素)化合物。在此基础上建立了疏风解毒胶囊HPLC多指标成分含量测定的方法[18],在同一色谱条件下同时测定虎杖苷、大黄素、连翘酯苷A、戟叶马鞭草苷、马鞭草苷、毛蕊花糖苷、甘草酸7个有效成分的方法,该方法简便、快捷、重复性好,可同时测定7种成分。建立了基于“有效性”的本品定量控制标准,以保证本品的有效性及其稳定均一性,为本品质量控制提供了保障。对近年的14批疏风解毒胶囊中的7种成分进行了含量测定。见图 8。
|
| 图 8 14批疏风解毒胶囊中的7种主要成分含量测定结果 Fig. 8 Determination of 7 constituents in Shufeng Jiedu capsule |
研究建立了疏风解毒胶囊指纹图谱质量控制分析方法[19],采用所建立的方法对14批疏风解毒胶囊样品进行了指纹图谱测定,采用相似度、聚类分析及主成分分析等数据处理方法对指纹图谱的模式识别进行研究,确定22个共有峰,以21号峰为参照物峰,建立标准指纹图谱(图 9)。

|
| 图 9 疏风解毒胶囊对照指纹图谱 Fig. 9 Control fingerprint of Shufeng Jiedu capsule |
通过对疏风解毒胶囊、全方药材及相应的阴性样品指纹图谱进行对照研究,对疏风解毒胶囊HPLC指纹图谱22个共有特征峰中的20个特征峰的来源进行了归属,其中来自于虎杖8个、连翘6个、马鞭草3个、败酱草1个、甘草2个;通过采用对照品及采用HPLC-MS法对色谱峰进行了指认,分别为大黄酚、大黄素-8-O-葡萄糖苷、大黄酸、连翘酯苷E、戟马鞭草苷、马鞭草苷、虎杖苷、甘草苷、连翘酯苷A、羟基化连翘酯苷A、毛蕊花糖苷、异连翘酯苷A、白藜芦醇、3-羟基光甘草酚、牡荆苷、甘草宁、异甘草苷、甘草素、芒柄花素、乌拉尔醇、大黄素、芦荟大黄素。
3.2 元胡止痛滴丸质量标准提升研究 3.2.1 原料药材质量标准研究对延胡索和白芷2味原料药材进行了化学成分研究,通过液质指认分析,确定了延胡索药材中29个化合物,均为生物碱类成分,白芷中25个化合物,均为香豆素成分;进一步建立了以上2味原料药材HPLC指纹图谱评价体系,通过系统聚类分析和相似度评价系统建立各个药材对照指纹图谱共有模式,分别对14批醋制延胡索和30批白芷样品采用指纹图谱的方法进行质量评价;建立了醋延胡索中7个指标成分(原阿片碱、黄连碱、黄藤素、去氢延胡索甲素、D-四氢药根碱、延胡索乙素及延胡索甲素)的HPLC含量测定方法[20],建立了白芷中4个成分(欧前胡素、异欧前胡素、白当归素、佛手柑内酯)的HPLC含量测定方法,方法简便、准确、重复性好。应用建立的方法测定了14批醋延胡索和30批白芷样品的含量,对元胡止痛滴丸原料药材的质量标准进行了全面提升。
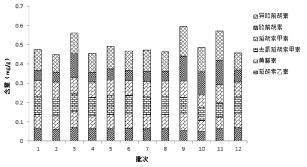
3.2.2 元胡止痛滴丸质量标准提升研究 3.2.2.1 多指标成分含量测定以确定的质量标志物为指标,分别建立了基于外标法和一测多评法(QAMS)的多指标成分含量测定方法[21],可同时测定元胡止痛滴丸中原阿片碱、黄藤素、去氢延胡索甲素、延胡索乙素、延胡索甲素、欧前胡素6个有效成分的含量。特别是QAMS法仅采用延胡索乙素为对照,即可实现对元胡止痛滴丸中的6个成分的定量控制,既节约了检验成本,又降低了实验操作的难度,该方法具有极大的推广应用价值。
|
| 图 10 12批元胡止痛滴丸6各指标成分含量测定结果 Fig. 10 Determination of 12 batch of constituents in Yuanhu Zhitong dropping pills |
建立了元胡止痛滴丸指纹图谱质量控制分析方法,采用所建立的方法对10批元胡止痛滴丸样品进行了指纹图谱测定,对指纹图谱进行了相似度评价,确定25个共有峰,对特征峰的来源进行了归属,其中来自于延胡索12个、白芷13个;并采用对照品及HPLC-MS法从元胡止痛滴丸指纹图谱25个共有峰中指认出20个化合物:原阿片碱、α-别隐品碱、药根碱、D-海罂粟碱、小檗碱、延胡索乙素、水合氧化前胡素、黄藤素、去氢延胡索甲素、白当归素、延胡索甲素、佛手柑内酯、白当归脑、别异欧前胡素、别欧前胡素、欧前胡素、8-甲氧基异欧前胡内酯、异欧前胡素、珊瑚菜素、蛇床子素。

|
| 图 11 元胡止痛滴丸对照指纹图谱 Fig. 11 Control fingerprint of Yuanhu Zhitong dropping pills |
综上所述,本研究从质量要素完整性表达及质量控制全过程的角度,通过化学成分研究、药效物质基础及质控指标的确定、多指标含量测定、指纹图谱等质控手段和方法,建立了从药材到成品的全过程的质量控制体系,对元胡止痛滴丸质量标准进行了全面的提升。
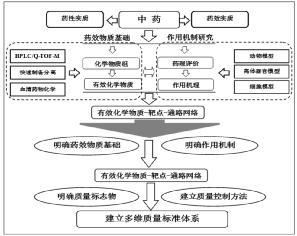
4 中药质量标准研究新的集成模式的建立根据中药大品种质量标准提升研究实践,建立了中药质量标准研究新的集成模式。以质量标志物概念为统领[22],将中药的药效和药性内涵均纳入质量评价研究;开展中药化学物质组及其生物效应相关性研究并经行关联性分析,确定药效物质基础,进一步进行中药化学成分的生源途径和特有性分析,确定质量评价指标;建立质量评价方法,建立实验样品取样规范,保证测定样品的代表性和覆盖度,进行样品测定分析,根据测定结果,建立完善的质量标准。见图 12。
|
| 图 12 中药质量研究集成模式 Fig. 12 Integrated model of TCM quality study |
| [1] | 郭敏娜, 刘素香, 赵艳敏, 等. 基于HPLC-Q-TOF-MS技术的柴胡化学成分分析[J]. 中草药, 2016, 47 (12): 2044–2052. |
| [2] | 张晨曦, 刘素香, 赵艳敏, 等. 基于液质联用技术的连翘化学成分分析[J]. 中草药, 2016, 47 (12): 2053–2060. |
| [3] | 赵艳敏, 刘素香, 张晨曦, 等. 基于HPLC-Q-TOF-MS技术的甘草化学成分分析[J]. 中草药, 2016, 47 (12): 2061–2068. |
| [4] | 张铁军, 朱月信, 刘岱琳, 等. 疏风解毒胶囊药效物质基础及作用机制研究[J]. 中草药, 2016, 47 (12): 2019–2026. |
| [5] | Zhang HB, Zhang TJ, Xu J, et al. Rapid analysis and identification of absorbed components and their metabolites in rat plasma and brain tissue after oral administration of Yuan-Hu-Zhi-Tong dropping pill using UPLC-Q-TOF/MS based multivariate statistical analysis[J]. Chinese Herbal Medicines, 2016, 8 (2): 154–163. DOI:10.1016/S1674-6384(16)60025-4 |
| [6] | Facchini P J, De Luca V. Opium poppy and madagascar periwinkle:model non-model systems to investigate alkaloid biosynthesis in plants[J]. Plant J, 2008, 54 (4): 763–784. DOI:10.1111/j.1365-313X.2008.03438.x |
| [7] | Liscombe D K, Facchini P J. Molecular cloning and characterization of tetrahydroprotoberberine cis-N-methyltransferase, an enzyme involved in alkaloid biosynthesis in opium poppy[J]. J Biol Chem, 2007 (282): 14741–14751. |
| [8] | 程巧, 曾建国, 乐捷. 异喹啉类生物碱生物合成、运输、储藏相关细胞生物学研究进展[J]. 植物学报, 2014, 49 (6): 720–728. |
| [9] | Dewan S, Sudha J, Sandeep G, et al. The biosynthesis of the alkaloids of Corydalis meifolia wall[J]. Tetrahedron, 1986, 42 (2): 675–680. DOI:10.1016/S0040-4020(01)87469-X |
| [10] | Tani C, Tagahara K. Studies on berberine derivatives and related alkaloids. VII. On the biosynthesis of protopine[J]. Chem Pharm Bull, 1974, 22 (10): 2457–2459. DOI:10.1248/cpb.22.2457 |
| [11] | Takao N, Iwasa K, Kamigauchi M, et al. Studies on the alkaloids of papaveraceous plants. XXV. Biosynthesis of the Alkaloids of Cory-dalis incisa Pers. and Chelidonium majus L. incorporations of te-trahydroprotoberberines, N-methosalts of tetrahydroprotoberberines, and protopine[J]. Chem Pharm Bull, 1976, 24 (11): 2859–2868. DOI:10.1248/cpb.24.2859 |
| [12] | 韩彦琪, 许浚, 张喜民, 等. 基于网络药理学的元胡止痛滴丸治疗原发性痛经的作用机制研究[J]. 药学学报, 2016, 51 (3): 380–387. |
| [13] | 韩彦琪, 许浚, 龚苏晓, 等. 基于HPLC-QTOF/MS及G蛋白偶联受体分析的延胡索物质基础及作用机制研究[J]. 药学学报, 2016, 51 (8): 1302–1308. |
| [14] | 张铁军, 高山林, 王文燕, 等. 物种概念及其在中药研究中的作用和意义[J]. 世界科学技术-中药现代化, 2004, 6 (3): 1–8. |
| [15] | 刘素香, 刘毅, 白雪, 等. 败酱草指纹图谱研究[J]. 中草药, 2016, 47 (12): 2074–2077. |
| [16] | 刘素香, 白雪, 刘毅, 等. 马鞭草HPLC指纹图谱建立及指标性成分的测定[J]. 中草药, 2016, 47 (12): 2069–2073. |
| [17] | 张铁军, 朱月信, 刘素香, 等. 疏风解毒胶囊的系统质量标准提升研究[J]. 中草药, 2016, 47 (12): 2027–2033. |
| [18] | 郭倩, 田成旺, 朱月信, 等. HPLC法同时测定疏风解毒胶囊中7种活性成分[J]. 中草药, 2015, 46 (8): 1174–1177. |
| [19] | 曹勇, 郭倩, 田成旺, 等. 疏风解毒胶囊HPLC指纹图谱研究[J]. 中草药, 2016, 47 (12): 2034–2039. |
| [20] | 陈俊, 许浚, 张静雅, 等. 基于一测多评法对延胡索中生物碱类成分的质量控制研究[J]. 中草药, 2016, 47 (3): 493–498. |
| [21] | 李思思, 许浚, 张铁军, 等. HPLC法同时测定元胡止痛滴丸中6种成分[J]. 中草药, 2015, 46 (21): 3198–3201. |
| [22] | 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker):中药产品质量控制的新概念[J]. 中草药, 2016, 47 (9): 1443–1457. |
 2017, Vol. 34
2017, Vol. 34