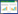文章信息
- 马浩玲, 张德芹, 丁丽琴, 陈新则, 吴晓磊, 伍明江, 邱峰
- MA Hao-ling, ZHANG De-qin, DING Li-qin, CHEN Xin-ze, WU Xiao lei, WU Ming-jing, QIU Feng
- HPLC-MS/MS法同时测定大鼠血浆中山楂叶提取物3种黄酮类成分及其药代动力学研究
- Simultaneous determination of three flavonoids in hawthorn leaves extract by HPLC-MS/MS method and analysis of their pharmacokinetics in plasma of rats
- 天津中医药, 2017, 34(4): 266-271
- Tianjin Journal of Traditional Chinese Medicine, 2017, 34(4): 266-271
- http://dx.doi.org/10.11656/j.issn.1672-1519.2017.04.16
-
文章历史
- 收稿日期: 2016-11-14
2. 天津中医药大学中药学院, 天津 300193
山楂叶为蔷薇科植物山里红(Crataegus pinnatifida Bge.Var.major N.E.Br.)或山楂(Crataegus pinnatifida Bge.)的干燥叶,具有活血化瘀,理气通脉,化浊降脂的功效[1],主要化学成分为黄酮类化合物,其中牡荆素、牡荆素-4"-O-葡萄糖苷、牡荆素-2"-O-鼠李糖苷作为山楂叶的主要活性成分[2],具有广泛的药理活性:抗炎、抗氧化、抗肿瘤、降血脂等[3-5];药代动力学利用动力学原理,研究药物在体内的吸收、分布、代谢和排泄与时间关系,为临床个体化给药的实现奠定基础[6-9]。目前对于山楂叶提取物体内药代动力学的研究主要集中在单剂量灌胃给药[10]和静脉注射给药[11],而中药山楂叶的用药以口服为主。因此本研究建立了高效液相色谱-串联质谱法(HPLC-MS/MS)同时测定大鼠血浆中牡荆素、牡荆素-4"-O-葡萄糖苷和牡荆素-2"-O-鼠李糖苷的方法,并对大鼠灌胃给予不同剂量山楂叶提取物后3种黄酮成分的药动学过程进行研究,为山楂叶的临床应用和开发提供实验依据。
1 材料与仪器 1.1 主要仪器液质联用仪:Shimadzu LC-20A高效液相色谱仪(日本SHIMADZU公司),API 4000三重四极杆串联型质谱仪(美国Applied BioSystem公司,配备电喷雾离子源、Analyst Software数据处理系统);XS205型电子天平(瑞士Mettler-Toledo公司);Sorvall RC 6+型离心机(美国Thermo公司);MX-S型涡旋混合器(美国SCILOGEX公司);超纯水系统(美国Millipore公司)。
1.2 药品与试剂牡荆素(Vitexin,VIT):购于天津化标生物技术有限公司,批号20151110;牡荆素-4"-O-葡萄糖苷(Vitexin-4"-O-Glucoside,VOG):购于阿拉丁®(Aladdin ®),批号11204018;牡荆素-2"-O-鼠李糖苷(Vitexin-2"-O-rhamnoside,VOR):购于中国药品生物制品检定所,批号111668-200602;黄芩苷(BAI):购于中国药品生物制品检定所,批号110715-201318;山楂叶提取物(HLE):购于山东步长药业公司,批号150907,经检测VIT、VOG、VOR含量分别占0.13%、4.317%、9.722%;甲醇(色谱纯,Fisher Scientific);乙腈(色谱纯,Fisher Scientific);甲酸(色谱纯,德国CNW公司);超纯水为Milli Q制备
1.3 实验动物SPF级雄性Wistar大鼠,体质量 (200±10)g,由中国人民解放军军事医学科学院实验动物中心提供,合格证编号:SCXK(军)2012-0004。
2 方法与结果 2.1 色谱条件Agilent ZORBAX XDB-C18(3.5 μm,2.1 mm×50 mm)色谱柱,Gemini C18(3.5 μm,4 mm× 30 mm)保护柱;流动相:A:乙腈;B:水(含0.1%甲酸);二元梯度洗脱:2.0%-20% A(0.01~1.5 min);20%-40% A(1.5~3.5 min);40%-95% A(3.5~4.5 min);95%-95% A(4.5~5.5 min);95%-2.0% A(5.5~5.51 min);2%-2% A(5.51~7.0 min)。流速:0.45 mL/min;柱温:40℃;进样量:10 μL。
2.2 质谱条件采用电喷雾离子源(ESI),负离子分析模式,多反应监测(MRM)扫描方式;参数设置:离子喷雾电压(IS):-4 200V;温度(TEM):550 ℃;碰撞气(CAD):Medium;气帘气(CUR):15.0 psi;气流1(GS1):55 psi;气流2(GS2):55 psi;加热(Ihe):On;母离子、子离子的质核比,去簇电压(DP)、碰撞能量(CE)见表 1。
| 成分 | 母离子质核比(m/z) | 子离子质核比(m/z) | 去簇电压(V) | 碰撞能量(V) |
| VIT | 430.9 | 311.0 | -105 | -33 |
| VOG | 593.4 | 413.4 | -113 | -35 |
| VOR | 577.3 | 413.4 | -94 | -35 |
| BAI(Internal standard) | 415.3 | 268.7 | -55 | -26 |
精密称取适量VIT、VOG、VOR和BAI对照品,加入适量甲醇充分溶解,分别配制成浓度均为0.5 mg/mL的储备液。分别精密吸取VIT、VOG、VOR储备液适量,加入50%甲醇水,采用倍数稀释法分别配制成8个浓度的系列对照品溶液,即VIT(5、10、25、100、250、1 000、2 500、5 000 ng/mL)、VOG和VOR(10、20、50、200、500、2 000、5 000、10 000 ng/mL)的标准系列溶液;另配制低(QCL)、中(QCM)、高(QCH)3个浓度的质控溶液,其中VIT浓度分别为10、250、4 000 ng/mL,VOG和VOR分别为20、500、8 000 ng/mL;内标BAI储备液采用甲醇稀释,配制成1 μg/mL的BAI甲醇溶液,作为内标工作液。以上溶液均密封后于4 ℃冰箱保存,备用。
2.4 山楂叶提取物供试液的制备精密称定山楂叶总黄酮提取物各6.25、12.50、25.00 g,分别加入25 mL 0.5%的羧甲基纤维素钠(CMC-Na)溶液研磨均匀,使药物浓度为0.25、0.50 1.00 g/mL,作为供试液,随用随配。
2.5 给药与样品采集受试大鼠18只,预适应1周,随机分为3组,即山楂叶提取物低、中、高剂量组。实验前12 h禁食,自由饮水,分别按1.0、2.0、4.0 g/kg(相当于1.296、2.593、5.185的VIT,43.167、86.333、172.667的VOG,97.222、194.444、388.889的VOR)灌胃给药,分别于给药前和给药后0.167、0.333、0.5、1、2、4、6、8、12、24、36、48 h经眼底静脉丛取血200 μL,并置于肝素化离心管中,6 000 r/min离心10 min,取出上层血浆,于-80 ℃冰箱保存,待测。
2.6 血浆样品处理方法室温下融化血浆样品,涡旋混匀,精确吸取50.0 μL大鼠血浆样品,依次加入10.0 μL维生素C溶液(1.4 mg/mL,水),5.0 μL 50%甲醇水溶液,涡旋30 s后,再加入150 μL BAI甲醇工作液沉淀蛋白,涡旋2 min,12 000 r/min离心10 min,吸取上清液20.0 μL进样测定。
2.7 方法学考察方法学验证包括基质特异性,灵敏度,线性,准确度,精密度,回收率,基质效应和稳定性,各项均按照2015版《中国药典》关于“生物样品定量分析方法验证指导原则”进行[12]。
2.7.1 专属性考察分别取空白血浆样品(处理时使用不加内标溶液的甲醇溶液沉淀蛋白)A、空白血浆中加入VIT、VOG和VOR最低浓度混合对照品工作液B、大鼠给药后1 h的血浆样品C,均按照血浆处理方法操作检测后,得到空白血浆、空白血浆+对照品、给药后1 h的血浆样品中各待测成分的提取离子流图,见图 1。血浆中所含待测成分和加入的内标BAI峰形良好、各通道保留时间不同(VIT:3.11 min;VOG:2.97 min;VOR:3.02 min;BAI:3.77 min),不受血浆中内源性物质干扰,方法专属性良好。
|
| 图 1 待测各成分提取离子色谱图:(A) 空白血浆;(B) 空白血浆+对照品;(C) 灌胃给予山楂叶提取物1 h后的血浆样品(VIT:牡荆素;VOG:牡荆素-4"-O-葡萄糖苷;VOR:牡荆素-2"-O-鼠李糖苷;BAI:黄芩苷) Fig. 1 Representative MRM chromatograms of analytes: (A) blank plasma sample; (B) blankplasma + reference substances; (C) plasma sample of 1 h afteroral administration of HLE (VIT: Vitexin; VOG: Vitexin-4"-O-Glucoside; VOR:Vitexin-2"-Orhamnoside; BAI: Baicalin) |
在空白大鼠血浆中加入按“ 2.3”配制的一系列对照品溶液,按照血浆样品处理方法操作后进样检测,通过计算待测成分与内标的峰面积比值,采用加权(1/x2)最小二乘法进行线性回归分析,求得各成分的回归方程即为标准曲线;根据信噪比S/N =10计算各成分的最低定量限(LLOQ)。VIT、VOG、VOR的标准曲线方程、相关系数、线性范围及定量下限结果见表 2。
| 成分 | 线性范围(ng/mL) | 标准曲线 | 相关系数(r) | 最低定量限(ng/mL) | 准确度(%,RE) | 精密度(%,RSD) |
| VIT | 0.5~500 | 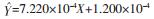
| 0.998 | 0.500 | 00.133 | 4.400 |
| VOG | 1~1000 | 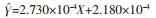
| 0.999 | 1.000 | 03.000 | 3.501 |
| VOR | 1~1000 | 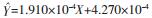
| 0.998 | 1.000 | -3.767 | 4.936 |
在空白大鼠血浆中加入最低定量限对照品溶液和低、中、高3个浓度的质控溶液,按照血浆样品处理方法操作后得到质控样品,进样检测,每个浓度各配制6份,每天1次,连续3 d,以当日标准曲线计算各样品的测定浓度,与配制浓度对照,求得方法的准确度,并计算方法的日内、日间精密度,其中准确度以RE [RE=(测定浓度-配制浓度)/配制浓度]表示。结果各成分的日内、日间精密度RSD<11.976%,RE在-12.567%~ 13.000%之间,符合生物样品分析测定要求。结果见表 3。
| 成分 | 质量浓度(ng/mL) | 日内 | 日间 | |||||
| 测定值(x±s,ng/mL) | 精密度(%,RSD) | 准确度(%,RE) | 测定值(x±s,ng/mL) | 精密度(%,RSD) | 准确度(%,RE) | |||
| VIT | 0.5 | 0.497±00.022 | 4.459 | -0.600 | 0.489±00.053 9 | 11.011 | -2.144 | |
| 1 | 0.962±00.074 | 7.713 | -3.833 | 0.925±00.063 1 | 6.821 | -7.506 | ||
| 25 | 25.267±01.167 | 4.620 | 1.067 | 24.250±02.022 | 8.337 | -3.000 | ||
| 400 | 384.167±10.458 | 2.722 | -3.958 | 373.778±20.570 | 5.503 | -6.556 | ||
| VOG | 1 | 1.086±00.072 | 6.631 | 8.583 | 1.029±00.117 | 11.402 | 2.894 | |
| 2 | 1.892±00.143 | 7.583 | -5.417 | 1.981±00.153 | 7.740 | -0.972 | ||
| 50 | 43.717±01.347 | 3.081 | -12.567 | 46.322±03.415 | 7.372 | -7.356 | ||
| 800 | 762.333±28.682 | 3.762 | -4.708 | 746.778±30.859 | 4.132 | -6.653 | ||
| VOR | 1 | 1.130±00.071 | 6.258 | 13.000 | 1.040±00.125 | 11.976 | 4.044 | |
| 2 | 1.903±00.225 | 11.798 | -4.833 | 1.939±00.219 | 11.268 | -3.028 | ||
| 50 | 44.700±01.950 | 4.363 | -10.600 | 46.700±04.563 | 9.771 | -6.600 | ||
| 800 | 774.667±42.688 | 5.511 | -3.167 | 746.611±47.605 | 6.376 | -6.674 | ||
取大鼠空白血浆,操作同“ 2.7.3”项,配制得到低、中、高3个浓度的质控样品(A);同时配制低、中、高3个浓度的质控溶液,不加空白血浆,直接按照上述方法处理,得到上清液(B);另取6份不同来源的大鼠空白血浆先利用纯甲醇沉淀蛋白,吸取上清液再加入低、高2个浓度的质控溶液,按上述方法处理,得到上清液(C);每个浓度平行操作6份,记录各样品与内标的峰面积,以A与B的比值计算提取回收率,以对应浓度的C与B的比值分别计算各成分和内标的基质效应因子(MF),以6批基质计算内标归一化基质效应因子(MF isnorm),进而评价基质效应。结果表明本实验条件下3种黄酮类成分的提取回收率均良好,血浆基质对其离子化及含量测定无影响。结果见表 4。
| 成分 | 质量浓度(ng/mL) | 回收率(x±s,%) | 精密度(%,RSD) | MF isnorm(x±s) | 精密度(%,RSD) |
| VIT | 1 | 99.728±5.052 | 5.066 | 0.055±4.302 | 4.302 |
| 25 | 112.469±2.297 | 2.043 | - | - | |
| 400 | 106.688±4.693 | 4.399 | 0.044±4.869 | 4.869 | |
| VOG | 2 | 109.786±1.946 | 1.773 | 0.116±10.268 | 10.268 |
| 50 | 111.329±1.873 | 1.682 | - | - | |
| 800 | 105.710±4.402 | 4.164 | 0.049±5.184 | 5.184 | |
| VOR | 2 | 105.842±1.952 | 1.844 | 0.078±6.856 | 6.856 |
| 50 | 110.031±3.325 | 3.022 | - | - | |
| 800 | 104.335±2.846 | 2.728 | 0.055±5.845 | 5.845 |
取大鼠空白血浆,操作同“ 2.7.3”项,配制得到低、高2个浓度的血浆质控样品,考察血浆中各成分在室温放置3 h稳定性、3次反复冻融稳定性及冰箱储存24 h稳定性。测定结果表 5,各成分在血浆中经过室温放置3 h、3次反复冻融及4 ℃储存24 h均稳定。
| 成分 | 质量浓度 (ng/mL) | 室温放置3 h | 冻融实验 | 4℃放置24 h | |||||
| 精密度 (%, RSD) | 准确度 (%, RE) | 精密度 (%, RSD) | 准确度 (%, RE) | 精密度 (%, RSD) | 准确度 (%, RE) | ||||
| VIT | 1 | 4.362 | 8.333 | 5.131 | 7.333 | 3.266 | 10.667 | ||
| 400 | 1.705 | -10.417 | 3.870 | -2.250 | 2.463 | -9.792 | |||
| VOG | 2 | 11.769 | -2.167 | 6.612 | 2.667 | 6.983 | -1.333 | ||
| 800 | 1.294 | -8.667 | 2.473 | -1.958 | 3.111 | -6.525 | |||
| VOR | 2 | 14.900 | -4.830 | 13.982 | 1.167 | 8.090 | -0.750 | ||
| 800 | 1.860 | -9.500 | 3.185 | -2.083 | 2.350 | -7.813 | |||
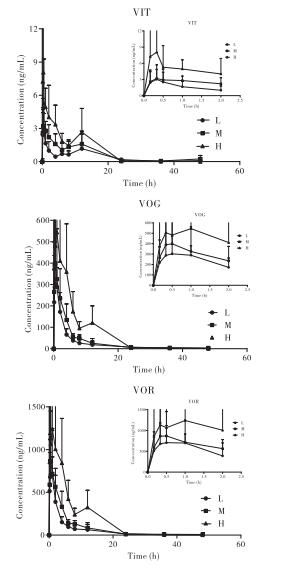
运用上述建立的HPLC-MS/ MS方法测定各时间点3种黄酮类成分的血药浓度,绘制平均血药浓度时间曲线,结果见图 2;采用药动学软件DAS(Ver 1.0)对所得各成分的血药浓度-时间数据进行房室模型拟合并计算主要药动学参数,同时利用软件SPSS Statistics 19.0对低、中、高剂量组的药动学参数进行统计分析,考察给药剂量对各成分药代动力学参数的影响是否有统计学差异。实验数据以均值±标准差(x±s)表示,多组间比较采用单因素方差分析(Oneway ANOVA),组间两两比较若方差齐采用LSD法,若方差不齐采用Dunnett’s T3法,P<0.05为差异有统计学意义。
|
| 图 2 大鼠单次灌胃给予山楂叶提取物后各有效成分的药时曲线(n=6) Fig. 2 Mean concentration-time profiles for the analytes in plasma of rats after a single oral administration of HLE (n=6) |
结果表明,大鼠灌胃HLE1.0、2.0、4.0 g/kg后,3种黄酮类成分在大鼠体内的药动学过程均符合一室模型,其中VIT药动学参数AUC0→t在中、高剂量组与低剂量组差异显著;对于MRT0→t,高剂量组同低、中剂量组差异显著;VOG和VOR药动学参数Cmax和AUC0→t在高剂量组中显著高于低剂量组,同时高剂量组AUC0→t也均显著高于中剂量组,但在实验剂量下各成分药动学参数与给药剂量不成正比,呈非线性相关,见表 6。
| 成分 | 给药剂量(mg/kg) | T1/2(h) | Tmax(h) | Cmax(ng/mL) | AUC(0-t)(ng/mL· h) | AUC(0-∞)(ng/mL· h) | MRT(0-t)(h) |
| VIT | 1.296 | 3.382±2.501 | 0.372±0.267 | 3.408±2.574 | 10.705±4.814 | 11.728±6.206 | 11.470±3.658 |
| 2.593 | 3.871±1.567 | 0.428±0.245 | 3.793±1.273 | 29.596±10.269** | 33.352±12.467 | 10.237±3.251 | |
| 5.185 | 4.611±1.509 | 0.461±0.236 | 9.447±8.583 | 30.686±14.899** | 36.544±22.788 | 6.176±1.800**# | |
| VOG | 43.167 | 2.718±1.825 | 0.528±0.245 | 358.780±272.336 | 993.037±501.398 | 996.570±499.021 | 6.329±2.142 |
| 86.333 | 3.050±0.975 | 0.778±0.647 | 396.000±177.253 | 1 447.051±509.690 | 1 449.641±509.783 | 6.544±2.173 | |
| 172.667 | 3.453±1.069 | 1.139±0.718 | 532.750±154.345* | 3 201.816±1 587.506**## | 3 253.687±1 637.716 | 6.066±1.219 | |
| VOR | 97.222 | 2.836±2.041 | 0.750±0.374 | 776.800±563.965 | 2 650.051±1 358.106 | 2 658.507±1 350.652 | 6.206±1.877 |
| 194.444 | 3.050±0.976 | 0.861±0.636 | 836.333±417.227 | 3 550.271±1 306.358 | 3 551.967±1 306.501 | 6.637±1.762 | |
| 388.889 | 3.711±1.536 | 1.139±0.718 | 1 390.000±482.494* | 7 689.838±4 056.733**# | 7 804.070±4 088.813 | 6.204±1.202 | |
| 注:与低剂量组比*P<0.05,**P<0.01;与中剂量组相比#P<0.05,##P<0.01。 | |||||||
考虑到中药化学成分的复杂性,单一成分的药动学研究太片面,并不能反映该味药整体的药动学特征,缺乏科学性和说服力,因此本研究从含量与药理方面出发,选择了山楂叶提取物中含量分别为第二、第一的专属性活性成分VOG和VOR,及其苷元VIT 3种主要成分作为药代标示物进行研究[13]。
实验对血浆样品处理方法进行了探索,考察了乙腈、甲醇沉淀血浆蛋白后直接进样和经氮吹后复溶进样检测的响应值,发现经甲醇处理的样品基质效应较小,灵敏度更高,可能由于甲醇处理血浆,不仅起到沉淀蛋白的作用,同时其对待测成分和内标具有良好的溶解性,发挥一定提取作用,从而减少血浆基质的影响[14]。而经氮吹处理的样品响应值只提高了1倍,未经氮吹处理的样品响应值也能达到实验测定要求,考虑到检测成本与时间,选用甲醇沉淀血浆蛋白未经氮吹处理的方法操作。
VOG和VOR是山楂叶总黄酮中含量较高、生物活性较强的化学成分,二者结构相近,具有类似的药动学特征;VIT作为二者共同的苷元成分,在大鼠肠黏膜通过被动扩散的方式转运进入体内,无特殊的吸收窗,但其在肠道的吸收较差,尤其在口服给药过程中,有报道建议制成注射剂使用[15],但目前中药多以口服为主,可通过改变药物剂型实现口服生物利用度的提高[16]。实验结果表明,VIT、VOG、VOR 3种黄酮类化合物在体内吸收迅速,低、中、高3个剂量组均在1 h左右达到最大吸收峰,但吸收量很少,Cmax与AUC(0-t)均在纳克级别,表明其吸收程度较差;同时3种成分均在12 h处又出现第2个吸收峰,尤其是高剂量组,与文献中报道黄酮类药物多存在双峰现象较为一致,肝肠循环可能是导致此现象的重要原因[17];3种成分在大鼠体内的药动学过程均符合一室模型,在实验剂量下各药动参数与给药剂量呈非线性相关,可能与扩散转运酶、代谢酶的饱和程度有关,具体机制有待进一步的研究。同时文献报道,某化学成分在单一药材与复方给药后的药动学可能存在差异,复方中配伍药材对该成分的吸收产生影响[18],而临床用药多以复方为主,山楂叶在临床的应用也是如此,因此,需以包含中药山楂叶的升清降浊方[19]或者糖脂清复方[20]为研究对象,并结合复方中的配伍比例等方面,进一步探讨其药动学特征,方能得到更加准确的数据,从而为临床治疗提供用药指导。
| [1] | 国家药典委员会. 中华人民共和国药典[S]. 一部. 北京: 中国医药科技出版社, 2015: 32. |
| [2] | 郝彧, 刘虹, 吴帅, 等. 大孔树脂纯化山楂叶提取物的工艺考察[J]. 天津中医药, 2009, 26 (4): 335–337. |
| [3] | 顾成波, 蔡曼, 袁肖寒, 等. 牡荆苷的植物资源及药理作用研究进展[J]. 中国中药杂志, 2015, 40 (3): 382–389. |
| [4] | Aslam MS, Ahmad MS, Mamat A S. Pharmacological Potential of Vitexin[J]. Indian Research Journal of Pharmacy & Science, 2015, 2 (2): 114–122. |
| [5] | 张敏丽, 闵清. 山楂叶总黄酮的药理作用研究进展[J]. 湖北科技学院学报 (医学版), 2015, 29 (2): 182–184. |
| [6] | 张燕, 刘欣, 叶娟. 中药不良反应现状分析与预防策略[J]. 天津中医药大学学报, 2011, 30 (2): 73–76. DOI:10.11656/j.issn.1673-9043.2011.02.03 |
| [7] | 刘昌孝. 中药的药代动力学研究在中药现代化中面临的任务[J]. 天津中医药, 2003, 20 (6): 1–5. |
| [8] | 刘昌孝. 我国药物动力学研究50年发展概述[J]. 天津中医药大学学报, 2008, 27 (3): 127–134. DOI:10.11656/j.issn.1673-9043.2008.03.03 |
| [9] | 张德芹. 中药复方药物动力学研究方法的探索[J]. 天津中医药大学学报, 2003, 22 (4): 10–12. DOI:10.11656/j.issn.1673-9043.2003.04.04 |
| [10] | Ma LY, Liu RH, Xu XD, et al. The pharmacokinetics of C-glycosyl flavones of Hawthorn leaf flavonoids in rat after single dose oral administration[J]. Phytomedicine:international journal of phytotherapy and phytopharmacology, 2010, 17 (8-9): 640–645. DOI:10.1016/j.phymed.2009.12.010 |
| [11] | Zhu S, Yan H, Niu K, et al. Simultaneous determination of seven components from hawthorn leaves flavonoids in rat plasma by LC-MS/MS[J]. Journal of chromatographic science, 2015, 53 (6): 909. DOI:10.1093/chromsci/bmu143 |
| [12] | 国家药典委员会. 中华人民共和国药典[S]. 四部. 北京: 中国医药科技出版社, 2015: 363-368. |
| [13] | 刘昌孝. 我国药代动力学研究发展的回顾[J]. 中国药学杂志, 2010, 45 (2): 81–89. |
| [14] | Liu X, Wang D, Zhang WJ, et al. LC determination and pharmacokinetic study of vitexin-4"-O-glucoside in rat plasma after oral administration[J]. Natural product research, 2012, 26 (10): 962–967. DOI:10.1080/14786419.2010.535165 |
| [15] | 王亚男, 甄毅岚, 李晓亮, 等. 牡荆素与牡荆素鼠李糖苷大鼠在体肠吸收对比研究[J]. 安徽医药, 2013, 17 (10): 1660–1663. |
| [16] | Duan J, Dang Y, Meng H, et al. A comparison of the pharmacokinetics of three different preparations of total flavones of Hippophae rhamnoides in beagle dogs after oral administration[J]. European journal of drug metabolism and pharmacokinetics, 2016, 41 (3): 239–249. DOI:10.1007/s13318-015-0254-9 |
| [17] | 黄勇, 何峰, 张治蓉, 等. HPLC-MS-MS同时检测大鼠血浆中荭草素、牡荆素和槲皮苷[J]. 中国实验方剂学杂志, 2012, 18 (1): 80–84. |
| [18] | 程丽丽, 许妍妍, 张艳军. 中药川乌多成分同时检测及药动学评价研究进展[J]. 天津中医药大学学报, 2014, 33 (1): 56–60. DOI:10.11656/j.issn.1673-9043.2014.01.19 |
| [19] | 杜娟, 张德芹, 文静, 等. 升清降浊方对MSG肥胖大鼠胰岛素增敏作用的影响[J]. 天津中医药大学学报, 2016, 35 (1): 27–30. DOI:10.11656/j.issn.1673-9043.2016.01.08 |
| [20] | 李玉红, 刘虹, 王茜, 等. 糖脂清过柱前后对KK-Ay小鼠血糖血脂药效学影响对比实验[J]. 天津中医药, 2012, 29 (4): 384–388. |
2. College of Chinese Materia Medica, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
 2017, Vol. 34
2017, Vol. 34