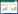文章信息
- 韩亚亚, 王磊, 张文杰, 郝佳, 刘二伟
- HAN Ya-ya, WANG Lei, ZHANG Wen-jie, HAO Jia, LIU Er-wei
- 松脂醇二葡萄糖苷大鼠胆汁内排泄研究
- Study on bile excretion of pinoresinol diglucoside of rats
- 天津中医药, 2017, 34(7): 491-494
- Tianjin Journal of Traditional Chinese Medicine, 2017, 34(7): 491-494
- http://dx.doi.org/10.11656/j.issn.1672-1519.2017.07.17
-
文章历史
- 收稿日期: 2017-05-20
2. 天津中医药大学第一附属医院, 天津 300193;
3. 天津市中药化学与分析重点实验室, 天津 300193
松脂醇二葡萄糖苷为杜仲中木脂素类成分之一,具有舒张血管,降低血压的作用[1-3]。关于杜仲提取物药理活性及作用机制已有报道,但松脂醇二葡萄糖苷的体内代谢过程及降压机制的研究目前仍然很少。Wang等[4]采用高效液相色谱-串联质谱法(HPLC-MS/MS)的方法对大鼠口服给药后的血浆动力学进行了初步研究,结果表明松脂醇二葡萄糖苷属于一室模型,给药12 h内消除95%。但是,目前对松脂醇二葡萄糖苷在胆汁内的排泄研究尚无报道。文章对松脂醇二葡萄糖苷及其代谢产物松脂醇单葡萄糖苷在大鼠胆汁排泄方面作用进行了研究[5],定量分析不同时间段内两者排泄情况,明确其在胆汁内排泄特征,进一步阐明松脂醇二葡萄糖苷及其代谢产物松脂醇单葡萄糖苷在体内的转化排泄过程, 研究结果为含有松脂醇二葡萄糖苷的药物研究开发和临床合理用药提供参考。
1 仪器、试药与实验动物 1.1 仪器液质联用仪(Agilent 1260高效液相色谱仪,Agilent 6430三重四极杆质谱仪);十万分之一天平(瑞士Mettler Toledo公司,AX-205);万分之一天平(德国Sartorius公司,BP121S);超纯水制造机(Millipore公司,Mill-QⅡ型);低温高速离心机(德国Sigma公司);涡旋混合仪(美国Labnet公司,VX-200);移液枪(德国Eppendorf公司);超低温冰箱(美国Thermo Heto公司,-86 ℃);硬脊膜外麻醉导管(常州市乐佳医疗器械有限公司)。
1.2 试药松脂醇二葡萄糖苷(实验室自制);松脂醇单葡萄糖苷(天津大学药学院苏艳芳教研室提供);华法林(上海Sigma公司);乌拉坦(天津市光复精细化工研究所);乙腈、甲醇(美国Fisher公司);乙酸(美国TEDIA试剂公司);超纯水(Mlillipore超纯水系统自制)。
1.3 实验动物雄性SD大鼠,8周龄,体质量为180~220 g。购自北京华阜康科技有限公司,实验前大鼠在天津中医药大学适应性培养1周[控温(23±2) ℃,控湿50%±10%],以适应环境。
2 实验方法与结果 2.1 色谱条件程序洗脱:流动相为乙腈(A),0.1%乙酸水(B);0~1.5 min,A相12%,1.5~2 min,A相12%~30%,2~3 min,A相30%~50%,3~10 min,A相50%~65%,10~12 min,A相65%~85%,12~20 min,A相至12%。柱温30 ℃,流速0.3 mL/min;进样量5 μL。
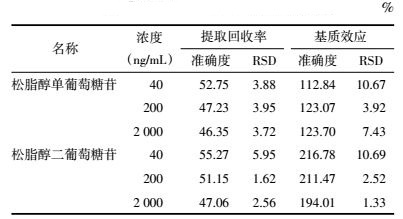
2.2 质谱条件电喷雾离子源(ESI),采用多级反应监测(MRM),负离子模式下监测,毛细管电压4.0 kV,氮气干燥气温度为350 ℃,氮气流速10 L/min。松脂醇二葡萄糖苷、松脂醇单葡萄糖苷和华法林的离子对质荷比、碰撞能量和碎裂电压见表 1。
 |
SD雄性大鼠禁食不禁水12 h后,用20%乌拉坦进行麻醉,沿腹中线打开腹腔,进行胆管插管手术,按照50 mg/kg的剂量灌胃给药松脂醇二葡萄糖苷的生理盐水溶液,给药后收集0~2、2~4、4~6、6~8、8~10、10~12、12~24 h胆汁样品并测量胆汁样品体积。吸取胆汁样品50 μL,于1.5 mL离心管中,加入10 μL华法林(50 ng/mL)涡旋混匀后静置5 min,混合液中加入乙腈140 μL继续涡旋混匀后静置10 min放入离心机内14 000 r/min离心10 min,离心后吸取上清液100 μL再加入乙腈400 μL涡旋混匀,14 000 r/min离心10 min,取上清液进样,进样量5 μL。
3 结果 3.1 专属性取大鼠空白胆汁,按照确定方法进行处理,进样后对松脂醇二葡萄糖苷、松脂醇单葡萄糖苷和华法林离子进行检测,结果显示胆汁内源性物质对3个化合物没有干扰,不影响结果测定,且化合物在此条件下测定峰形良好,适合测定,如图 1。

|
| 图 1 松脂醇二葡萄糖苷、松脂醇单葡萄糖苷和华法林离子检测图 Fig. 1 MRM chromatograms of pinoresinol diglucoside, pinoresinol single glucoside and warfarin A:空白胆汁;B:大鼠给药后的胆汁样品;C:空白胆汁中加入对照品 |
将不同浓度松脂醇二葡萄糖苷和松脂醇单葡萄糖苷的混合标准溶液加入空白胆汁中,按照样品处理方法步骤进行处理,并分析结果。以各化合物与华法林的峰面积比对浓度进行线性回归,权重系数为1/X,得到线性回归方程,松脂醇二葡萄糖苷:Y=0.035 9X+ 0.041 7,线性相关系数r2=0.998,松脂醇单葡萄糖苷:Y=0.354 1X+0.076 8,线性相关系数r2=0.999。胆汁中松脂醇二葡萄糖苷和松脂醇单葡萄糖苷在8~5 000 ng/mL范围内线性关系良好。松脂醇二葡萄糖苷、松脂醇单葡萄糖苷的定量限均为8 ng/mL,松脂醇单葡萄糖苷的检测限为4 ng/mL,松脂醇二葡萄糖苷的检测限为2 ng/mL。
3.3 精密度与准确度制备胆汁中分别含有高、中、低3个浓度的松脂醇二葡萄糖苷和松脂醇单葡萄糖苷质量控制样品,按照样品处理方法进行处理,每个浓度6份样品,通过标准曲线进行测定,连续测定3 d,计算其精密度和准确度,结果显示此方法适合胆汁中松脂醇二葡萄糖苷代谢成分的检测,见表 2。
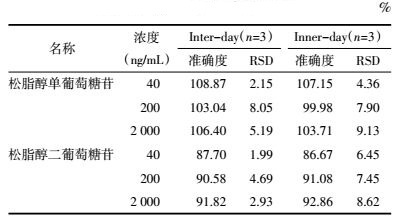
分别按照空白胆汁加入高、中、低3个浓度标准品后根据处理方法处理,将空白胆汁按方法处理后加入高、中、低浓度松脂醇二葡萄糖苷和松脂醇单葡萄糖苷混匀和将高中、低3个浓度标准品溶液稀释,分别处理3批待测样品,每批高、中、低浓度各3份进样,根据结果计算提取回收率和基质效应,结果见表 3。
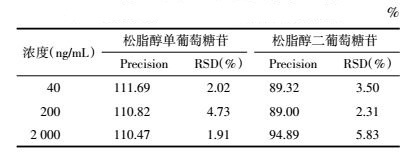
取空白胆汁,配制高、中、低浓度的松脂醇二葡萄糖苷和松脂醇单葡萄糖苷胆汁样品考察其在室温放置24 h稳定性,将样品实测值与实际值比较,RSD值小于15%符合要求,证明稳定性良好,检测结果准确,结果见表 4。
 |
实验建立了液质联用方法(LC-MS/MS)同时检测给药后大鼠胆汁中松脂醇二葡萄糖苷及其代谢产物松脂醇单葡萄糖苷,方法学在生物样品分析方法指导原则下进行了专属性、标准曲线、精密度、基质效应、提取回收率及稳定性等内容考察验证,将分析方法学用于胆汁中松脂醇二葡萄糖苷、松脂醇单葡萄糖苷的研究,证明所建立方法灵敏度可靠,符合生物样品测定要求,可用于胆汁中松脂醇二葡萄糖苷及其代谢产物松脂醇单葡萄糖苷的定量分析。
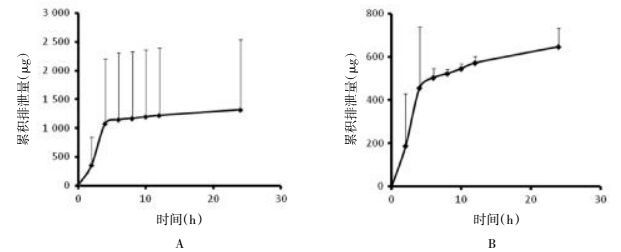
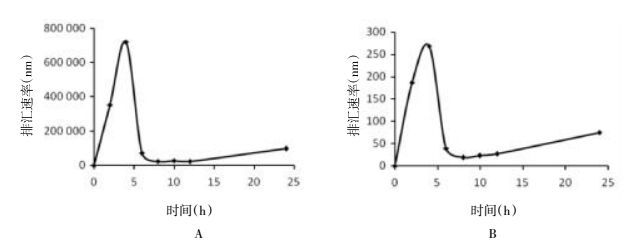
3.7 实验结果大鼠灌胃松脂醇二葡萄糖苷后,松脂醇二葡萄糖苷和松脂醇单葡萄糖苷均在胆汁中被发现,累积排泄量在给药之后不断增长,到6 h后保持一个平稳状态。排泄速率在第4 h到达顶峰,之后排泄速率迅速降低,6 h后保持一个较低的状态,实验后期大鼠排泄率有上升趋势。大鼠胆汁内松脂醇二葡萄糖苷、松脂醇单葡萄糖苷的累积排泄曲线见图 2,排泄速率曲线见图 3。
|
| 图 2 大鼠口服给药后在胆汁内的累积排泄曲线 Fig. 2 Cumulative excretion of pinoresinol diglucoside and pinoresinol single glucosidea in rats bile after oral administration A:松脂醇二葡萄糖苷累积排泄曲线;B:松脂醇单葡萄糖苷累积排泄曲线 |
|
| 图 3 大鼠口服给药后在胆汁内的排泄速率曲线 Fig. 3 Excretion rate of pinoresinol diglucoside and pinoresinol single glucosidea in rats bile after oral administration A:松脂醇二葡萄糖苷排泄速率曲线;B:松脂醇单葡萄糖苷排泄速率曲线 |
胆汁是一种由肝脏分泌的重要的消化液,其分泌是一个连续的、耗能的渗透过程,胆道许多成分胆汁酸盐、胆固醇、磷脂等在小肠大部分被重吸收,重吸收的成分通过门静脉再次进入肝脏内重新循环[6]。实验结果表明大鼠灌胃松脂醇二葡萄糖苷后,胆汁中同时检测到了松脂醇二葡萄糖苷原型化合物及其代谢产物松脂醇单葡萄糖苷的浓度,建立了同时检测胆汁中两者浓度的方法,并通过了方法学验证。按照100 mg/kg大鼠剂量口服给药松脂醇二葡萄糖苷单体后,24 h内松脂醇二葡萄糖苷平均累积排泄量为2 534 μg,松脂醇单葡萄糖苷仅为646 ng,计算胆汁24 h内松脂醇二葡萄糖苷排泄率为11.0%。松脂醇二葡萄糖苷在胆汁内主要以原型形式排出体外,松脂醇单葡萄糖苷为松脂醇二葡萄糖苷胆汁内的代谢产物,该过程是一个连续的长期的排泄过程,推测尿液和粪便中具有较高排泄量,需要进一步实验验证[7]。结果对于松脂醇二葡萄糖苷体内过程研究以及含有松脂醇二葡萄糖苷的中药临床应用具有指导意义。
| [1] | Li JF, Zhang JF, Wang JL, et a1. Effects of quercetin on intracellular free calcium concerntration in cultured rabbit aortic smooth muscle cells[J]. Chinese Journal Hypertention, 2000, 8 (1): 55–57. |
| [2] | 江春艳, 许激扬, 卞筱泓, 等. 杜仲降血压成分的组合及血管舒张作用[J]. 中国实验方剂学杂志, 2010, 16 (6): 218–220. |
| [3] | Chan EC, Pannangpetch P, Woodman OL. Rlaxation to flavones and flavonols in rat isolated thoracicaorta:mechanism of action and structure-activity relationships[J]. Cardiovasc Pharmacol, 2000, 35 (2): 326–330. DOI:10.1097/00005344-200002000-00023 |
| [4] | Wang JL, Liu EW, Zhang Y, et al. Validation of a HPLC-tandem MS/MS method for pharmacokinetics study of (+)-pinoresinol-di-β-D-glucopyranoside from Eucommia ulmoides Oliv extract in rats' plasma[J]. J Ethnopharmacol, 2012, 139 (2): 337–342. DOI:10.1016/j.jep.2011.10.037 |
| [5] | Liu K, Yan LQ, Yao GC, et al. Estimation of p-coumaric acid as metabolite of E-6-O-p-coumaroyl scandoside methyl ester in rat plasma by HPLC and its application to a pharmacokinetic study[J]. Journal of Chromatography B, 2006, 831 (1-2): 303–306. DOI:10.1016/j.jchromb.2005.12.018 |
| [6] | 陆伦根. 胆汁的分泌、排泄和调节及胆汁淤积发生机制[J]. 临床肝胆病杂志, 2011, 27 (6): 570–571. |
| [7] | 刘继平, 黄鑫, 薛梅, 等. 复方苦参注射液大鼠胆汁、尿液排泄研究[J]. 中药新药与临床药理, 2011, 12 (4): 424–428. |
2. The First Affiliated Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China;
3. Key Laboratory of Pharmacology of Traditional Chinese Medical Formulae, Ministry of Education, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
 2017, Vol. 34
2017, Vol. 34