文章信息
- 柴士伟, 杨帆, 于卉娟, 王跃飞
- CHAI Shiwei, YANG Fan, YU Huijuan, WANG Yuefei
- UPLC/ESI-Q-TOF MS法分析远志中的化学成分
- Analysis of chemical constituents of Radix Polygalae by UPLC/ESI-Q-TOF MS
- 天津中医药, 2018, 35(1): 60-64
- Tianjin Journal of Traditional Chinese Medicine, 2018, 35(1): 60-64
- http://dx.doi.org/10.11656/j.issn.1672-1519.2018.01.16
-
文章历史
- 收稿日期: 2017-10-23
2. 天津中医药大学, 天津市现代中药重点实验室-省部共建国家重点实验室培育基地, 天津 300193;
3. 天津国际生物医药联合研究院, 中药新药研发中心, 天津 300457
远志为临床常用中药之一,始载于《神农本草经》。《中国药典》(2015版)规定了远志为远志科植物远志(Polygala tenuifolia Willd.)或卵叶远志(Polygala sibirica L.)的干燥根,具有安神益智、祛痰、消肿等功效[1]。临床上常用于治疗由于心肾不交而引起的失眠、多梦、焦虑、神志迷糊、健忘惊悸、咳痰不爽等症[2-3],其主要化学成分包括糖酯、皂苷、口山酮类等[4-5]。文献报道,以西伯利亚远志糖A5、西伯利亚远志糖A6为代表的寡糖酯类成分和口山酮类成分是远志及远志科其他植物中的特征性化学成分[4, 6-9]。糖酯类化合物在抗痴呆、脑保护和抗抑郁方面表现出明显的生物活性[10-13];皂苷类化合物是远志发挥其镇静安神、祛痰止咳作用的主要药效物质[14-19];口山酮类化合物具有止痛、抗菌、抗肿瘤、抗病毒等作用[20-22]。
采用超高效液相色谱-电喷雾离子化-四级杆飞行时间串联质谱(UPLC/ESI-Q-TOF MS)法分析远志中化学成分,并综合文献总结归纳了远志药材中主要化合物的质谱裂解规律,阐明远志药材化学成分。
1 材料与方法 1.1 仪器采用UPLC/ESI-Q-TOF MS(美国Waters公司);万分之一天平(瑞士METTLER公司);十万分之一天平(瑞士METTLER公司);超纯水仪(美国Millipore公司);超声波清洗机(宁波新芝生物有限公司);台式离心机(上海安亭科学仪器厂);4 ℃医用冷藏箱(青岛海尔特种电器有限公司)。
1.2 试剂质谱级乙腈(美国Sigma-Aldrich公司);色谱级甲醇(美国Sigma-Aldrich公司);色谱级甲酸(美国Sigma-Aldrich公司);超纯水(实验室自制)。
1.3 试药对照品:西伯利亚远志糖A5(141102,SA5)、西伯利亚远志糖A6(141015,SA5)、西伯利亚远志口山酮B(140605,SX5)、远志口山酮XI(141104,PXXI)、3, 6′-二芥子酰基蔗糖(141024, DS)、细叶远志皂苷(141205,TF)、远志皂苷元(140717,SG)、远志酸(141127,PGA)、远志皂苷D(140623,PGD)购于成都普菲德生物技术有限公司,经高效液相色谱-紫外法(UPLC-UV)分析除了3,6′-二芥子酰基蔗糖(95.3%)外纯度均大于98%。样品:远志(购自亳州市药材市场,产地:山西)。
1.4 色谱条件色谱柱ACQUITY UPLC®BEH C18(2.1 mm×100 mm, 1.7 μm);流动相:乙腈(B)-0.1%甲酸水(A),梯度洗脱:(0~12 min,11%~29% B;12~13 min,29%~36% B;13~24 min,36%~43.5% B;24~25 min,43.5%~90% B);进样量:2 μL;流速:0.5 mL/min;柱温:40 ℃。
1.5 质谱条件电喷雾离子源(ESI)扫描方式;正离子模式毛细管电压:3.0 kV;负离子模式毛细管电压:-2.5 kV;离子源温度:120 ℃;脱溶剂气温度:400 ℃;脱溶剂气流量:700 L/h;锥孔气流量:50 L/h;碰撞气(氩气):0.20 mL/min。质量轴校正采用亮氨酸-脑啡肽(m/z [M+H]+=556.277 1,m/z [M-H]-=554.261 5)溶液。质量扫描范围:m/z 100~2 000 Da,数据分析:Masslynx V 4.1软件。
1.6 供试品溶液的制备取远志,粉碎,过60目筛,取0.5 g,精密称定,置25 mL容量瓶中,加入适量甲醇,密塞,超声处理(功率300 W,频率40 kHz)30 min,放至室温,甲醇定容至刻线,摇匀,涡旋1 min后14 000 r/min离心10 min,取上清液,即得。
1.7 对照品储备液的制备分别取SA5、SA6、SX5、PXXI、DS、TF、SG、PGA、PGD各5 mg,精密称定,加甲醇和少量DMSO溶解并配制成每1 mL分别含有SA5 0.050 mg、SA6 0.052 mg、SX5 0.050 mg、PXXI 0.063 mg、DS 0.049 mg、TF 0.054 mg、SG 0.049 mg、PGA 0.052 mg、PGD 0.056 mg的混合对照品溶液,即得。
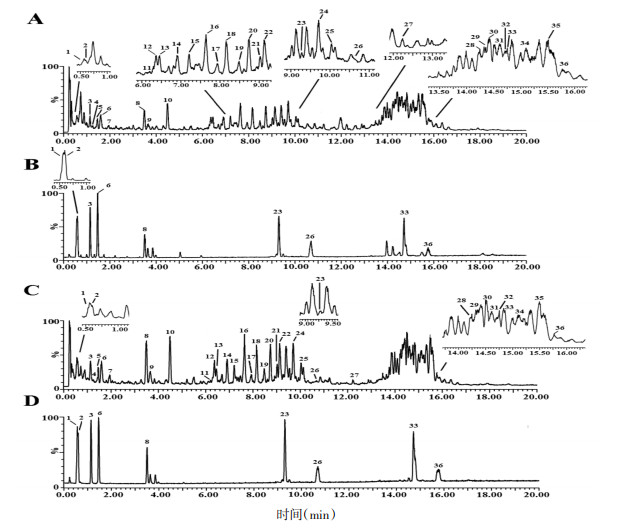
2 实验结果 2.1 远志化学成分的UPLC/ESI-Q-TOF MS分析采用UPLC/ESI-Q-TOF MS对远志的化学成分进行质谱定性鉴别,供试品溶液总离子流图分别见图 1(A)、图 1(C),对照品溶液总离子流图分别见图 1(B)、图 1(D)。共检测到36个化合物,鉴定和推测了29个化合物,包括14个糖酯、4个口山酮、9个皂苷、2个苷元。通过与对照品的保留时间、质谱碎片信息的比对,确证了SA5、SA6、SX5、PXXI、DS、TF、SG、PGA、PGD化合物。参考相关文献[23-27],根据色谱保留时间、质谱数据以及裂解规律,推测了20个化合物。所检测到的化合物的保留时间、准分子离子和加合离子的精确质量数、误差、理论分子量、分子式和二级质谱数据见表 1。
|
| 图 1 供试品溶液正离子模式(A)、对照品溶液正离子模式(B)、供试品溶液负离子模式(C)、对照品溶液负离子模式(D)总离子流图 Fig. 1 UPLC/ESI-Q-TOF MS total ion chromatograms of RP extracts (A) in positive ion mode and (C) in negative ion mode, base peak intensity chromatograms of mixed standards (B) in positive ion mode and (D) in negative ion mod |
| 编号 | tR(min) | [M+H]+/[M+Na]+/[M+NH4]+ | [M-H]-/[M-H+HCOOH]- | 分子式 | 化合物 | |||||
| 实测值(Error,ppm) | 理论值(Error,ppm) | MS2 | 实测值(Error,ppm) | 理论值(Error,ppm) | MS2 | |||||
| 1* | 0.548 | 541.153 4(0.2) | 571.163 9 | 339.109 0[M+H-C6H12O6]+,177.056 3[M+H-C6H12O6-C6H10O5]+ | - | - | - | C23H32O15 | SA6 | |
| 2* | 0.609 | 571.163 8(-0.2) | 539.140 1 | 369.119 5[M+H-C6H12O6]+,207.067 1[M+H-C6H12O6-C6H10O5]+ | - | - | - | C24H26O14 | SXB | |
| 3* | 1.152 | 539.140 2(0.2) | 437.108 4 | 407.098 8[M+H-C5H8O4]+,287.056 7[M+H-C5H8O4-C4H8O4]+,257.045 9[M+H-C5H8O4-C5H10O5]+ | - | - | - | C20H20O11 | irisxanthone | |
| 4 | 1.379 | 437.109 3(2.1) | 569.150 6 | 317.067 2,287.057 9,221.083 1 | 435.093 3(1.4) | 435.092 7 | 345.060 7,315.050 7,272.032 3 | C25H28O15 | polygalaxanthone Ⅲ [24] | |
| 5 | 1.428 | 569.151 6(1.8) | 569.150 6 | 437.108 8,419.099 0,317.067 5,287.057 0 | 567.136 2(2.1) | 567.135 0 | 435.093 5,345.061 6,315.050 6,272.032 5,258.061 9 | C25H28O15 | PXXI | |
| 6* | 1.482 | 569.150 7(0.2) | 691.185 0 | 437.108 7[M+H-C5H8O4]+;317.067 0[M+H-C5H8O4-C4H8O4]+;287.056 5[M+H-C5H8O4-C5H10O5]+ | - | - | - | C30H36O17 | tenuifoliside B [23-24] | |
| 7 | 1.959 | 691.185 1(0.1) | 777.221 8 | 369.118 8,207.063 3 | 667.187 4(0) | 667.187 4 | 637.178 5 | C34H42O19 | DS | |
| 8* | 3.502 | 777.220 2(-2.1) | 747.211 2 | 369.119 2[M+H-C17H22O10]+,207.066 7[M+H-C17H22O10-C6H10O5]+ | - | - | - | C33H40O18 | arillanin A [24] | |
| 9 | 3.664 | 747.210 4(-1.1) | 705.200 7 | 369.119 5,339.109 1,207.066 9,177.056 5,145.030 1 | 723.213 2(-0.6) | 723.213 6 | 547.166 6,223.060 9,205.050 2,175.039 7,160.016 1 | C31H38O17 | tenuifoliside A [23-24] | |
| 10 | 4.476 | 705.199 8(-1.3) | 1 272.419 4 | 665.207 6,383.135 3,221.083 3,190.064 3 | 681.203 7(0.9) | 681.203 1 | 443.119 0,137.024 2,179.034 6,239.055 7 | C56H70O32 | tenuifoliose T [24] | |
| 11 | 6.284 | 272.417 2(-1.7) | 791.237 5 | 617.332 9,413.123 1,289.072 0,259.061 1,177.056 2,147.045 6 | 1 253.376 5(-0.6) | 1 253.377 2 | 1 223.363 9,1 077.328 4,955.291 0,647.199 8,451.122 7,307.081 1,287.054 7,257.043 9 | C35H44O19 | tenuifoliside C [23-24] | |
| 12 | 6.374 | 791.236 5(-1.3) | 756.271 5 | 751.243 5,383.134 9,369.118 9,221.082 6,207.066 6 | 767.240 4(0.7) | 767.239 9 | 529.156 3,205.050 0 | C34H42O18 | ND | |
| 13 | 6.458 | 756.269 7(-2.4) | 1 497.471 9 | 557.312 7,411.277 2,397.128 9,204.103 3,147.045 7,131.050 8 | 737.229 1(-0.3) | 737.229 3 | 661.197 9,615.192 3,555.297 1,467.140 1,147.044 8,121.029 1 | C67H84O38 | ND | |
| 14 | 6.920 | 497.473 6(1.1) | 1 297.403 4 | 1 479.460 3,1 272.415 9,1 132.389 5,1 102.377 6,775.228 4,587.322 8 | 1 495.453 1(-2.1) | 1 495.456 2 | 1 253.377 1,1 379.407 1,1 203.362 2,1 161.351 3 | C58H72O33 | ND | |
| 15 | 7.212 | 297.403 7(0.2) | 1 309.403 4 | 515.302 6,413.124 5 | 1 295.388 2(0.3) | 1 295.387 8 | 1 119.340 6 | C59H72O33 | tenuifoliose J [23-24] | |
| 16 | 7.644 | 309.401 7(-1.3) | 719.216 3 | 1 291.391 2,798.281 0,413.124 2,397.129 6,309.098 8,147.046 0 | 1 307.392 0(3.2) | 1 307.387 8 | 1 161.352 1,1 119.341 4,1 101.330 6,997.304 8,842.237 5 | C32H40O17 | ND | |
| 17 | 7.928 | 719.214 6(-2.4) | 1 356.440 5 | 321.242 7 | 741.223 6(-0.8) | 741.224 2 | 695.218 1,543.171 8 | C60H74O34 | tenuifoliose B [23-24] | |
| 18 | 8.159 | 356.440 7(0.1) | 1 309.403 4 | 1 321.401 0,1 159.346 7,681.195 9,585.180 7,545.165 8,413.124 7 | 1 337.400 6(1.7) | 1 337.398 3 | 1 295.390 4,1 161.353 6,1 119.342 4,1 101.332 4,997.305 6 | C59H72O33 | tenuifoliose Ⅰ [23-24] | |
| 19 | 8.474 | 309.404 8(1.1) | 1 284.622 5 | 501.322 1,413.124 4,351.108 7,177.055 7,147.046 0 | 1 307.388 7(0.7) | 1 307.387 8 | 1 263.566 2,1 161.350 0,969.467 4,673.200 6,423.288 8,307.080 8 | C59H94O29 | ND | |
| 20 | 8.736 | 284.621 3(-0.9) | 1 356.440 5 | 941.471 7,663.374 4,501.322 2,289.072 9,443.316 0 | 1 265.581 1(0.6) | 1 265.580 3 | 1 235.566 8,971.482 5,499.165 7,455.315 4,425.304 7 | C60H74O34 | tenuifoliose D [23-24] | |
| 21 | 9.028 | 356.439 2(-1.0) | 541.153 3 | 1 339.412 5,747.229 8,681.194 3,413.123 4,381.118 4,177.056 1 | 1 337.398 2(-0.1) | 1 337.398 2 | 1 161.351 1,1 039.312 3,893.275 9,997.302 4,795.234 7 | C22H30O14 | SA5 | |
| 22 | 9.134 | 1 351.4 106(-2.5) | 1 351.414 0 | 1 333.401 9,868.283 5,687.194 2,597.181 2,545.164 9,413.123 5 | 1 349.402 5(3.1) | 1 349.398 3 | 1 161.354 9,1 101.514 3,1 039.317 7,731.223 8,674.198 0 | C61H74O34 | tenuifoliose H [24] | |
| 23* | 9.297 | 1 209.588 6(-1.5) | 1 209.590 4 | 1 077.546 8[M+H-C5H8O4]+;945.504 2[M+H-2C5H8O4]+ | - | - | - | C57H92O27 | PGD | |
| 24 | 9.710 | 1 381.423 3(-0.9) | 1 381.424 5 | 413.123 7,147.045 7,177.056 2 | 1 379.408 2(-0.5) | 1 379.408 9 | 1 203.361 1,1 161.350 8 | C62H76O35 | Tenuifoliose A [24] | |
| 25 | 10.032 | 1 268.625 0(-2.0) | 1 268.627 5 | 501.321 9,455.316 9,437.305 8 | 1 249.586 7(1.1) | 1 249.585 3 | 828.351 3,455.314 7,425.304 1 | C59H94O28 | ND | |
| 26* | 10.698 | 698.410 6(-1.4) | 698.411 6 | 663.370 7[M+NH4-H2O-NH3]+;501.321 3[M+NH4-C6H12O6-NH3]+ | C36H56O12 | TF | ||||
| 27 | 12.215 | 910.296 3(-2.0) | 910.298 1 | 587.175 3,345.098 3,207.067 4,177.056 2 | 891.254 5(-1.6) | 891.255 9 | 223.060 0,205.049 7,175.039 7 | C41H47O22 | ND | |
| 28 | 14.246 | 1 722.774 4(-0.3) | 1 722.775 0 | 1 247.580 4,909.322 7,747.270 0,663.374 1,501.320 6,453.176 0, | - | - | - | C80H120O39 | senegin Ⅳ [24] | |
| 29 | 14.326 | 1 866.812 5(-0.4) | 1 866.817 3 | 1 725.705 4,1 669.715 7,1 555.696 9,1 023.352 2,939.460 8,747.269 9 | - | - | - | C86H128O43 | onjisaponin L [24-26] | |
| 30 | 14.421 | 1 650.754 2(0.2) | 1 650.753 9 | 1 509.652 1,1 469.659 5,1 307.603 5,999.493 4,687.451 8,807.290 3 | - | - | - | C77H116O37 | onjisaponin O [24-26] | |
| 31 | 14.630 | 1 636.737 8(-0.3) | 1 636.738 3 | 1 307.602 4,1 145.549 9,999.491 8,867.451 4,809.442 1,645.237 3 | - | - | - | C76H114O37 | onjisaponin R [25-26] | |
| 32 | 14.758 | 1 590.734 0(0.8) | 1 590.732 8 | 1 449.621 8,1 247.585 3,893.326 3,747.268 4,663.373 2,501.321 6 | - | - | - | C75H112O35 | onjisaponin B [24] | |
| 33* | 14.760 | 489.321 5(-0.2) | 489.321 6 | 443.316 3[M+H-HCOOH]+;425.305 4[M+H-HCOOH-H2O]+;397.310 2[M+H-HCOOH-H2O-CO]+ | - | - | - | C29H44O6 | PGA | |
| 34 | 15.115 | 1 704.769 2(2.8) | 1 704.764 5 | 1 488.701 2,939.463 7,867.449 6,791.296 8,663.374 3,585.218 3 | - | - | - | C80H118O38 | onjisaponin Ng [24] | |
| 35 | 15.581 | 1 750.770 8(0.5) | 1 750.770 0 | 1 623.680 7,1 451.633 7,1 053.356 0,999.486 6,663.374 1,501.320 7 | - | - | - | C81H120O40 | onjisaponin Fg/W [24, 27] | |
| 36* | 15.760 | 554.324 9(0.2) | 554.324 8 | 501.322 2[M+H-HCl]+;491.293 4[M+H-HCOOH]+,455.317 5[M+H-HCl-HCOOH]+ | - | - | - | C30H45ClO6 | SG | |
| 注:“*”与对照品比对;“-”无信号;“ND”未鉴定。 | ||||||||||
本实验建立了一种高效、快速的UPLC-Q/TOF MS方法,通过结合标准品的质谱图及查阅相关文献,鉴定和推测了远志药材中29个化学成分,并总结了远志中糖酯、口山酮、皂苷类化合物的质谱裂解规律,为远志药材进一步研究和其他中药研究奠定了基础。
| [1] | 国家药典委员会. 中华人民共和国药典(一部)[S]. 北京: 中国医药科技出版社, 2015. |
| [2] | 刘大伟, 康利平, 马百平. 远志化学及药理作用研究进展[J]. 国际药学研究杂志, 2012, 39 (1): 32–36. |
| [3] | 韩丽丽, 李真, 管仁伟, 等. 中药远志的研究进展[J]. 中国野生植物资源, 2010, 29 (6): 1–4. |
| [4] | 杨学东, 张丽杰, 梁波, 等. 远志科植物中的寡糖酯类成分[J]. 中草药, 2002, 33 (10): 92–96. |
| [5] | 孙长清, 彭晓敏, 朱乃亮, 等. 远志中西伯利亚远志糖A5和西伯利亚远志糖A6的含量测定方法研究[J]. 中国中药杂志, 2012, 37 (11): 1607–1609. |
| [6] | 姜勇, 屠鹏飞. 远志研究进展[J]. 中草药, 2001, 32 (8): 90–92. |
| [7] | 刘明, 徐伟, 梁娜, 等. 远志的化学成分研究[J]. 中国现代中药, 2010, 12 (9): 18–21. |
| [8] | 姜艳艳, 戴莹, 巴寅颖, 等. 基于开心散-远志类药有效组分特征图谱的远志质量表征研究[J]. 北京中医药大学学报, 2011, 34 (8): 544–547. |
| [9] | 姜艳艳, 段以以, 刘洋, 等. 远志化学成分分离与结构鉴定[J]. 北京中医药大学学报, 2011, 34 (2): 122–125. |
| [10] | 刘屏, 王东晓, 郭代红, 等. 远志3, 6'-二芥子酰基蔗糖在药物诱发抑郁模型上的药效评价[J]. 中国药学杂志, 2008, 43 (18): 1391–1394. DOI:10.3321/j.issn:1001-2494.2008.18.008 |
| [11] | Naito R, Tohda C. Characterization of anti-neurodegenerative effects of Polygala tenuifolia in Abeta (25-35)-treated cortical neurons[J]. Biological&pharmaceutical Bulletin, 2006, 29 (9): 1892–1896. |
| [12] | Wei X, Hu JF, Yuan YH, et al. Polygala saponin XXXⅡ from Polygala tenuifolia root improves hippocampal-dependent learning and memory[J]. Acta Pharmacologica Sinica, 2009, 30 (9): 1211–1219. DOI:10.1038/aps.2009.112 |
| [13] | Ikeya Y, Takeda S, Tunakawa M, et al. Cognitive improving and cerebral protective effects of acylated oligosaccharides in Polygala tenuifolia[J]. Biological&pharmaceutical Bulletin, 2004, 27 (7): 1081–1085. |
| [14] | 窦智, 胡长明, 文莉, 等. 高效液相色谱法测定生远志及其炮制品中远志皂苷B的含量[J]. 中国医院药学杂志, 2014, 34 (19): 1676–1678. |
| [15] | 傅晶, 张东明, 陈若芸. 远志属植物的皂苷类成分及其药理作用研究进展[J]. 中草药, 2006, 37 (1): 144–146. |
| [16] | 韩毅丽, 梁璐, 张丹丹, 等. 超声提取远志总皂苷的研究[J]. 山西医药杂志, 2010, 39 (11): 1051–1052. |
| [17] | 冯丹, 郑德, 周洪雷, 等. 远志总皂苷有效部位质量控制研究[J]. 时珍国医国药, 2014, 25 (9): 2149–2151. |
| [18] | 孔辉, 郑德, 周洪雷, 等. 远志总皂苷大孔吸附树脂纯化工艺研究[J]. 辽宁中医杂志, 2014, 41 (10): 2196–2199. |
| [19] | Chung IW, Moore NA, Oh WK. Behavioural pharmacology of polygalasaponins indicates potential antipsychotic efficacy[J]. Pharmacology, Biochemistry, and Behavior, 2002, 71 (1-2): 191–195. DOI:10.1016/S0091-3057(01)00648-7 |
| [20] | 李照亮, 董宪喆, 王东晓, 等. 远志寡糖酯类化合物及远志口山酮Ⅲ CYP450酶的活性影响研究[J]. 中国中药杂志, 2014, 39 (22): 4459–4463. |
| [21] | 杨学东, 徐丽珍, 杨世林. 远志属植物中口山酮类成分及其药理研究进展[J]. 天然产物研究与开发, 2000, 12 (5): 88–94. |
| [22] | 林敬开. 中药远志活性成分与安全性研究[D]. 北京: 中国中医科学院, 2011. http://med.wanfangdata.com.cn/Paper/Detail?id=DegreePaper_Y1950642 |
| [23] | 林黎琳. 远志属两种植物的口山酮类成分研究[D]. 北京: 中国协和医科大学, 2005. |
| [24] | 刘筱筱, 夏忠庭, 何毅, 等. 远志UPLC多指标成分的测定及指纹图谱研究[J]. 中草药, 2016, 47 (12): 2167–2174. DOI:10.7501/j.issn.0253-2670.2016.12.026 |
| [25] | 李创军, 杨敬芝, 庾石山, 等. 远志中的三萜皂苷和寡糖多酯类成分[J]. 中国天然药物, 2011, 9 (5): 321–328. |
| [26] | Li CJ, Yang JZ, Yu SS, et al. Triterpenoid saponins with neuroprotective effects from the roots of Polygala tenuifolia[J]. Planta Med, 2008, 74 (2): 133–141. DOI:10.1055/s-2008-1034296 |
| [27] | Liu JY, Yang XD, He JM, et al. Structure analysis of triterpene saponins in Polygala tenuifolia by electrospray ionization ion trap multiple-stage mass spectrometry[J]. J Mass Spectrom, 2007, 42 (7): 861–873. DOI:10.1002/(ISSN)1096-9888 |
2. Tianjin State Laboratory of Modern Chinese Medicine-Province and Ministry co-established State Key Laboratory Cultivation Base, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China;
3. Research and Development Center of Traditional Chinese Medicine, Tianjin International Joint Academy of Biotechnology and Medicine, Tianjin 300457, China
 2018, Vol. 35
2018, Vol. 35