文章信息
- 黄洋, 李红
- HUANG Yang, LI Hong
- 平目汤2号对非活动期Graves眼病相关指标的影响
- Effects of Pingmu Decoction-Ⅱ on the laboratory indicators related to the non-active Graves' ophthalmopathy
- 天津中医药, 2018, 35(11): 819-821
- Tianjin Journal of Traditional Chinese Medicine, 2018, 35(11): 819-821
- http://dx.doi.org/10.11656/j.issn.1672-1519.2018.11.06
-
文章历史
- 收稿日期: 2018-06-30
Graves眼病又称甲状腺相关性眼病,是多种免疫异常引起的自身免疫性疾病,其特征是眼球后及眼眶周围眼组织的浸润性病变,主要表现为眼眶内脂肪组织、结缔组织及眼外肌体积的增加[1]。研究发现Graves病患者中约有25%~50%可伴随Graves眼病症状[2]。而近年来由于环境污染、生活节奏紧张、碘盐摄取增多和遗传因素等造成Graves眼病的发病率逐年增高,在成年病例的眼眶疾病中,Graves眼病发病率在国内外均居首位[3]。
Graves眼病按病情发展可以分为活动期和非活动期。平目汤2号是笔者导师李红教授的经验方,具有温阳益气、化痰祛瘀的功效,主要用于非活动期Graves眼病和使用激素等免疫抑制剂后无效或复发的患者。
虽然到目前为止Graves眼病的发病机制尚不十分明确,但目前有学者认为其发病是细胞免疫和体液免疫共同作用的结果,其中以细胞免疫为主,主要是T细胞的各分化亚群介导不同的免疫反应参与了疾病的过程[4]。又有多项研究证实[5-6],Graves眼病患者的血液呈高黏状态,有血小板聚集现象。故本研究通过检测Graves眼病患者治疗前后的血液流变学指标、CD3+、CD4+、CD8+、CD4+/CD8+等变化来探讨平目汤2号治疗非活动期Graves眼病的相关机制。现将观察结果报告如下。
1 资料与方法 1.1 一般资料76例观察病例全部来源于2004年12月—2007年8月本院内分泌门诊和住院的患者,年龄18~65岁。去除脱落病例后共65例纳入统计学分析。试验组34例,其中男16例,女18例,平均年龄(33.53±8.19)岁,平均病程(3.10±0.75)a;对照组31例,其中男13例,女18例,平均年龄(34.39±8.02)岁,平均病程(2.92±0.86)a,两组平均年龄及病程差别无统计学意义(P > 0.05)。参照《实用内科学》中的相关标准来制定Graves病浸润性突眼的诊断标准[7]。Graves眼病突眼活动性的诊断标准参照1992年AdHoC委员会推荐的临床评分标准:自发性的眼球后疼痛感,眼球运动时疼痛,眼睑红斑,眼睑水肿或发胀,结膜充血,球结膜水肿,眼阜水肿。以上7条每条各计1分,共7分。积分≥4分的判断为活动期,积分<4分的判断为非活动期。所有患者在进入试验前均未用过免疫抑制剂,且血清甲状腺激素水平(血清游离三碘甲腺氨酸、血清游离甲状腺素)正常至少2个月。
1.2 试验方法采用随机对照、双盲双模拟设计。采用随机数字表法分为试验组和对照组,用信封法隐匿随机分组方案,由专人保管。全部受试者维持Graves病基础治疗,并据入组号使用相应药物。平目汤2号颗粒剂及模拟药由四川美大康制药厂制成,泼尼松模拟药由本院制剂室制作。泼尼松片由上海信谊制药厂生产(批号:0712)。试验组予平目汤2号,每次1袋,每日2次,同时前4周服泼尼松模拟药每次10 mg,每日3次,以后每周减泼尼松模拟药5 mg,至每次10 mg/d维持。对照组服泼尼松10 mg/次,每日3次,4周后每周减泼尼松5 mg,至10 mg/d维持。同时服平目汤2号模拟药每次1袋,每日2次。两组疗程均为12周。所有受试者均于疗程前后取清晨空腹静脉血。血液流变学运用北京普利生LBY-N6C全自动血清洗血流变仪检测。CD3+、CD4+、CD8+采用美国BD FACSCalibur流式细胞仪检测。严格按操作说明书操作。
1.3 统计学方法数据采用SPSS 19.0统计分析软件处理,计量资料符合正态分布的采用均数±标准差(x±s)进行统计描述。组内比较采用配对t检验,组间比较采用独立样本t检验。计数资料采用χ2检验。所有的统计检验均采用双侧检验,P < 0.05为差异有统计学意义。
2 结果 2.1 两组治疗前后血液流变学的比较患者治疗前的全血低切黏度、全血高切黏度、血浆黏度、聚集指数这4项,两组之间比较均无统计学差异(P > 0.05)。治疗后试验组4项指标均显著下降,与治疗前比较差别有统计学意义(P < 0.01),对照组治疗前后差别无统计学意义。治疗后两组相比,差别有统计学意义(P < 0.01)。试验组治疗前后差值与对照组相比,差别有统计学意义(P < 0.01)。故试验组在改善非活动期Graves眼病患者血液流变学指标方面的疗效优于对照组,见表 1。

|
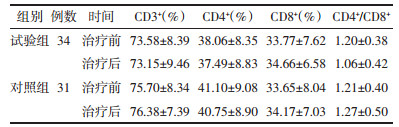
两组治疗前后CD3+、CD4+、CD8+、CD4+/CD8+组间及组内相比,差别无统计学意义(P > 0.05),见表 2。
|
对照组5例因疗效较差,退出试验,1例因失眠退出试验,1例因未复查实验室指标,脱落率为18.42%。试验组4例未复查实验室指标,脱落率为10.53%。
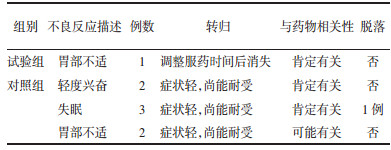
2.4 两组治疗后不良反应发生情况比较对照组轻度兴奋2例、失眠3例、胃部不适2例,患者反应轻微尚可耐受,故未予处理。试验组胃部不适1例,经调整服药时间后消失。两组不良反应发生率试验组低于对照组(P < 0.05)。见表 3。
中医学对于非活动期Graves眼病缺乏系统性记载,导师认为非活动期浸润性突眼病迁延日久,伤及气阴,导致气阴两虚,血行不畅,瘀滞经络。目为宗脉之所聚,目睛血瘀,则目突迁延日久;或又因阴损及阳,阳气亏虚,寒痰凝聚,阻滞经络,瘀血内停,凝结于目,终致目突经久不愈。故阳气亏虚、痰瘀阻滞是本病主要病机[8]。平目汤2号由生黄芪、丹参、仙灵脾等6味中药组成,方中黄芪益气健脾,丹参活血化瘀,仙灵脾补虚温阳,全方共奏温阳益气、化痰祛瘀之功。
研究证实,Graves眼病患者可能因甲状腺素分泌过多引起交感神经和肾上腺髓质系统兴奋,血液中的儿茶酚胺显著增加,导致微小动脉痉挛,微循环障碍,血流速度减慢,血液呈现出高黏高聚的状态[5-6],故治疗时尤当注重活血散瘀以改善血液循环,提高临床疗效。试验结果显示平目汤2号治疗后全血低切黏度、全血高切黏度、血浆黏度、聚集指数均显著下降,对照组治疗后与治疗前无明显差异,试验组显著优于对照组。故推测平目汤2号治疗非活动期Graves眼病机制之一为改善血液循环。
有研究显示[9],在早期Graves眼病患者体内,CD4+T细胞增多,CD8+T细胞减少,CD4+/CD8+较正常增高,又以CD4+T细胞分泌的Th1细胞因子介导的细胞免疫为主。故早期Graves眼病的治疗可采用免疫抑制剂,或特定的细胞因子、细胞因子抑制剂或诱导剂,来调节T细胞亚群之间的平衡,下调CD4+T细胞产生的细胞因子,可减轻突眼的症状。本研究对象为非活动期Graves眼病(病程大于2 a的晚期Graves病突眼),研究结果显示两组治疗后及组间CD3+、CD4+、CD8+、CD4+/CD8+相比,差异无统计学意义,与上述早期Graves病突眼研究结果不同。目前对于非活动期Graves眼病免疫系统功能异常的发病机制尚不清楚,本试验结果有待于今后进一步研究。
此外试验结果显示,两组不良反应发生率差异有统计学意义,试验组优于对照组。本研究推测平目汤2号治疗非活动期Graves眼病机制之一可能是改善血液循环,且药物安全性高,价格低廉,是治疗非活动期Graves眼病的有效药物,具有开发、推广价值。
| [1] | Rahn RS, Heufelder AE. Pathogenesis of Graves' ophthalmopathy[J]. NEngl JMed, 1993, 329 (20): 1468–1475. DOI:10.1056/NEJM199311113292007 |
| [2] | Rahn RS. Graves' ophthalmopathy[J]. NEngl JMed, 2010, 362 (8): 726–738. DOI:10.1056/NEJMra0905750 |
| [3] | Bartalena L, Pinchera A, Marcocci C. Management of Graves' ophthalmopathy:reality and perspective[J]. Endocrine Rev, 2000, 21 (2): 168–199. |
| [4] | Aniszewski JP, Valyasevi RW, Bahn RS. Relationship between disease duration and predominant orbital T cell subset in Graves' ophthalmopathy[J]. Clin Endocrinol Metab, 2000, 85 : 2776–2780. |
| [5] | 徐爱华, 李锐松, 秦正誉, 等. 甲亢患者血液流变学的改变及其临床意义[J]. 中华内分泌代谢杂志, 1990, 6 (2): 107–108. |
| [6] | 高琳, 闵迅, 姜黔峰, 等. 甲亢病人血液流变学研究[J]. 贵州医药, 1998, 22 (3): 177. |
| [7] | 陈灏珠. 实用内科学[M]. 北京: 人民卫生出版社, 2001: 9. |
| [8] | 陈秋颖, 李红. 李红治疗非活动期Graves眼病经验撷要[J]. 四川中医, 2014, 32 (1): 4–5. |
| [9] | 周素娴, 夏宁, 梁瑜祯, 等. Graves眼病患者T细胞亚群的研究[J]. 中华内分泌代谢杂志, 2006, 22 : 126–127. DOI:10.3760/j.issn:1000-6699.2006.02.012 |
 2018, Vol. 35
2018, Vol. 35