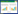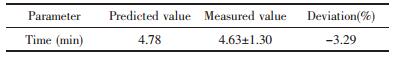文章信息
- 老蕊娟, 赵芳, 金鑫, 陆佳, 刘睿
- LAO Ruijuan, ZHAO Fang, JIN Xin, LU Jia, LIU Rui
- 基于星点设计效应面-人工神经网络法的复方活血化瘀喷膜剂的制备
- Preparation of Compound Huoxue Huayu spraying-film (CHH-SF) preparation based on central composite design and artificial neural network modeling
- 天津中医药, 2018, 35(12): 951-955
- Tianjin Journal of Traditional Chinese Medicine, 2018, 35(12): 951-955
- http://dx.doi.org/10.11656/j.issn.1672-1519.2018.12.21
-
文章历史
- 收稿日期: 2018-05-24
2. 武警后勤学院军事药学教研室, 天津 300309
传统药酒具有行血活络的功效,且易于吸收和发散,因此酒剂常用于治疗风湿痹痛,但携带、贮存不便,使用时易沾染衣物,且作用时间短,不易于质量控制,亟需改进[1]。传统酒剂以乙醇为溶剂,易于挥发,不良气味明显,对皮肤黏膜刺激性较强[2]。喷膜剂是一种新剂型,结合了气雾剂与膜剂的剂型特点[3],喷于局部皮肤,即可形成一层薄膜,既能保护创面,又能释放药物而起到局部或全身治疗作用。另外,该剂型也可避免口服给药所引起的胃肠道刺激和肝脏首过效应。同时采用透皮给药技术,大幅度延长了药物作用时间,增强了给药均匀度,使药效更加持久。本实验以当归红花酒作为模型药物,以成膜性、成膜时间为主要指标确定复方活血化瘀喷膜剂(CHH-SF)最优处方量,以期为临床提供新型高效、安全可靠的皮肤用药。
1 仪器与材料 1.1 仪器BT125D型分析天平(德国Sartorius公司);SPD-M20A高效液相色谱仪(日本岛津公司);KH3200B型超声波清洗器(昆山禾创超声仪器有限公司)。
1.2 材料红花、当归(市售);聚乙烯吡咯烷酮(PVPK30)(成都市科龙化工试剂厂);聚乙烯醇(PVA-124)(西陇科学股份有限公司);羟丙甲纤维素(HPMC)(北京凤礼精求商贸有限责任公司);乙醇(色谱纯,天津化学试剂批发公司)。
2 方法与结果 2.1 复方活血化瘀喷膜剂的制备 2.1.1 复方活血化瘀处方的提取液的制备称取当归15 g,红花15 g,粉碎,粗粉过40目药检筛,称量,以1:16质量比加入乙醇(60%)浸泡1周,抽滤,分装。
2.1.2 复方活血化瘀喷膜剂的制备称取处方量PVPK30、PVA-124、HPMC,将其加入到加10 mL上述复方活血化瘀处方提取液中充分溶胀,搅拌,超声,使其全部溶解后,分装即得[4]。
2.2 成膜性评价利用生物显微镜对各供试品成膜后表面形态进行观察,以流动性、成膜时间、均一性等指标为评价指标,对成膜材料PVPK30进行初步评价[5-7]。此外,分别对加入PVA-124和HPMC后混合基质的成膜性能进行研究。
2.3 单因素试验根据成膜性初步考察结果设计单因素试验,固定其他用量不变,按“2.1”项下方法制备喷膜剂,进行成膜时间考察。
2.3.1 PVPK30用量的考察按2.1.1项下制备复方活血化瘀喷膜剂,固定处方中PVA-124含量为5%,HPMC含量为0.3%,分别对浓度为3%、5%、7%、9%和11%的PVPK30进行考察,研究成膜材料PVPK30用量对成膜性的影响。
2.3.2 PVA-124用量的考察按2.1.1项下制备复方活血化瘀喷膜剂,固定PVPK30含量为7%,HPMC含量为0.3%,分别对浓度为1%、3%、5%、7%和9%的PVA -124进行考察,研究成膜材料PVA-124用量对成膜时间的影响。
2.3.3 HPMC用量的考察按2.1.1项下制备复方活血化瘀喷膜剂,固定PVPK30含量为9%,PVA-124含量为5%,分别对浓度为0.1%、0.3%、0.5%和0.7%的HPMC进行考察,研究成膜材料HPMC用量对成膜时间的影响。
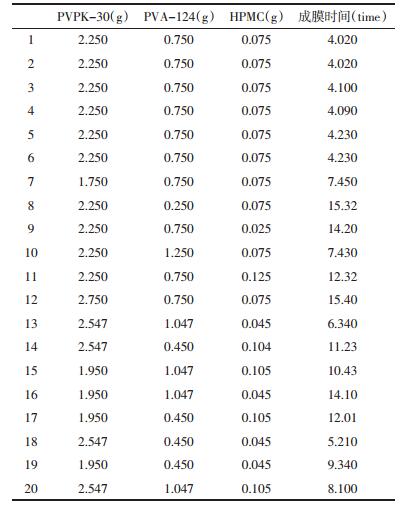
2.4 星点设计-效应面优化(CCD)根据2.2.2-2.2.3项下单因素考察实验结果分析,选择对影响显著的3个因素为考察对象,以PVPK30用量(X1),PVA-124用量(X2),HPMC用量(X3)为自变量,以成膜时间Y1为评价指标,采用星点设计-效应面法对复方活血化瘀喷膜剂进行处方优化[8]。根据星点设计的原理[9],各因素设置5水平,用代码值±a,±1,0来表示。对于三因素的星点设计a=1.682,代码所代表的实际操作物理量见表 1。
使用由遗传算法修改的BP神经网络对复方活血化瘀喷膜剂进行优化。优化程序由Metlab b2012b(MathWorks)编写。选择3种可控处方因素(PVPK-30用量,PVA用量,HPMC用量)进行优化。基于成膜时间作为指标,通过随机选择3个因子获得3个代表性原始数据[10]。处方输入神经网络用于处方优化神经网络的结构和参数的优化构建了神经网络模型。
2.6 CCD与ANN的比较基于与人工神经网络模型(ANN)的预测输出,计算各种参数,如均方根误差(RMSE),预测标准误差(SEP)和平均绝对相对偏差(AARD),比较RSM与ANN方法对复方活血化瘀喷膜剂的模拟效果[11]。RMSE、SEPA、ARD分别由公式(1)、(2)、(3)求出。
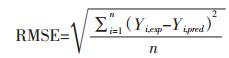 |
(1) |
 |
(2) |
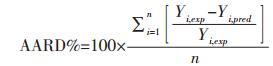 |
(3) |
实验结果表明,PVPK30与提取药液相容性好,选择其为主要成膜材料,将基质中PVPK30含量分别设定为1%、3%、5%、7%、9%时,随着PVPK30浓度的升高,流动性逐渐降低,肉眼可观察到气泡逐渐消,制剂均匀度增加,但显微镜下观察仍有大量气泡,且各组成膜时间均>20 min,在以上含各浓度的PVPK30的基质中,加入0.2%的HPMC后,所得制剂肉眼观察无显著性差别,而将所得各组喷膜剂置于显微镜下观察,发现大多数气泡消失,高浓度组仍具有较高的均一性。由于不同浓度的PVPK30单独作为成膜材料成膜时间均过长,故在处方中加入PVA-124。实验结果表明,在含0.2%的HPMC的各不同浓度(1%、3%、5%、7%、9%)的PVPK30基质中,加入7%的PVA-124后,成膜时间均呈现不同程度的缩短,大部分处方的成膜时间减少到10 min以下。所以本实验选择PVPK30、PVA-124和HPMC作为混合成膜基质材料,并对各成分比例进行进一步优化。
3.2 单因素考察实验结果表明,各基质用量对成膜时间的影响较大。当固定处方中PVA-124含量为5%,HPMC含量为0.2%,PVPK30含量为3%、5%、7%、9%、11%时,成膜时间分别为8.22 min、10.17 min、13.23 min、7.23 min、8.57 min;当固定处方中PVPK30含量为7%,HPMC含量为0.3%,PVA-124含量为1%、3%、5%、7%、9%时,成膜时间分别为4.73 min、4.62 min、4.52 min、6.00 min、4.63 min;当固定PVPK30含量为9%,PVA-124含量为5%,HPMC含量为0.1%、0.3%、0.5%、0.7%时,成膜时间分别为4.32 min、4.08 min、5.50 min、5.58 min、4.87 min。根据实验结果,筛选出各基质较优用量范围分别为PVPK30(7%~11%),PVA-124(1%~5%),HPMC(0.1%~0.5%)。
3.3 星点实验星点设计结果见表 2。根据实验结果以成膜时间为因变量Y,运用Design-Expert 7.0.0软件对各个因素进行多元二次方程拟合,得到的方程式,见公式(4):
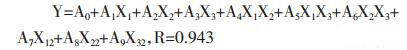 |
(4) |
|
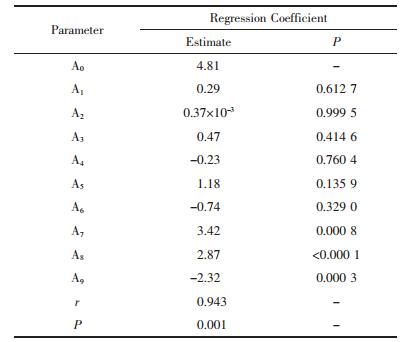
各方程拟合及相关系数,见表 3。
|
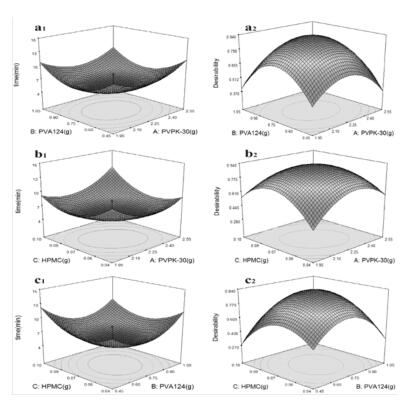
由Design Expert 7.0.0软件得出的复方活血化瘀喷膜剂星点设计三维效应图见图 1。从优化方程的3个影响因素的系数和效应面图可知,PVA-124对成膜时间影响最小,PVPK30和HPMC对成膜时间影响较大,当HPMC浓度为0.3%时,PVPK30和PVA124用量对成膜时间影响较大。
|
| 图 1 成膜时间独立变量三维效应面图 Fig. 1 Surface response chart of independent variables on film formation time a1、b1、c1分别为PVPK30与PVA-124含量、PVPK30与HPMC含量、PVA124与HPMC含量对成膜时间的三维效应面图;a2、b2、c2分别是PVPK30与PVA-124含量、PVPK30与HPMC含量及PVA124与HPMC含量以时间最小值为期望值的三维效应面图 |
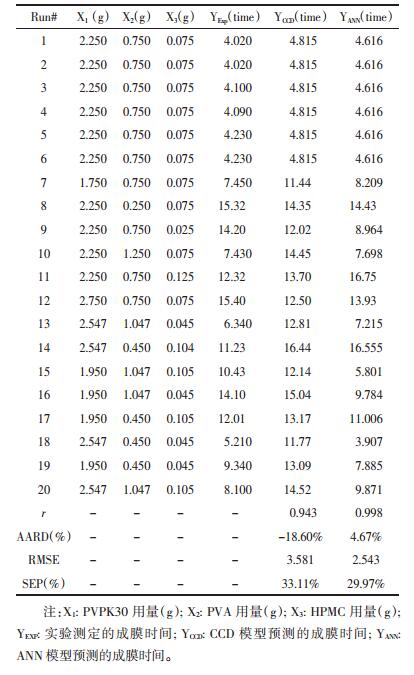
60.0%的数据集用于训练网络,20.0%用于神经网络模型的测试和验证。发现由3个输入层(HPMC%,PVA-124%和PVPK30%)和1个输出层(成膜时间)组成的4-10-2 ANN(包括偏置神经元)模型能够更准确的预测估计成膜时间。如表 4所示,R值为0.998,在每种情况下均接近1(1.0),ANN预测值(成膜时间)与实验数据具有较高的一致性。此外,还检查了不同自变量对输出的相对影响。观察到输入参数的影响程度遵循该顺序:PVA124(50.0%)>PVPK30(27.0%)>HPMC(23.0%)。
|
RMSE,SEP和AARD的计算结果如表 4所示。与CCD模型相比,ANN模型具有较低的RMSE(2.54),SEP(29.94)和AARD(4.69)。CCD模型的r值为0.943,而ANN模型的r值为0.998,更接近于1,说明了ANN模型的可靠性和适用性。这些结果证实,两种模型与实验数据都吻合良好。但与CCD模型相比,人工神经网络模型的实验值和预测值之间的偏差非常小。所以与CCD相比,人工神经网络具有更好的预测能力。
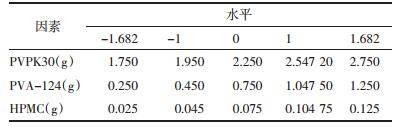
3.6 最优处方及验证基于人工神经网络模拟,最优处方见表 5。按照所优化的处方,制备3批复方活血化瘀喷膜剂,并对实际成膜时间进行测定,结果见表 6,成膜时间的预测值和实测值的偏差均较小,说明实验所得数学模型可以很好的预测各因素和评价指标之间的关系,适用于复方活血化瘀喷膜剂处方的优化。
目前,喷膜剂成膜材料的关键在于能在皮肤温度下迅速成膜。所成膜要求均匀、表面光滑、细腻、完整[12]。成膜材料[13-14]中应用较为广泛的有聚乙烯毗咯烷酮类(PVP)、聚乙烯醇类(PVA)。PVP类和PVA类两者均为水溶性高分子材料,具有优异的溶解性、低毒性、成膜性、化学稳定性、生理惰性和粘连能力等特性。一般作为成膜材料使用的型号有PVPK-30、PVA-124、PVA-1788及PVA-1788低粘度型等[15-16]。同时,卡波姆、羧甲基纤维素钠、壳聚糖和甲壳素等,由于柔软性好、本身具有吸附伤口渗出物、减少创面渗出、促进创面愈合的作用,也常作为混合成膜材料使用。在本研究中,使用复合基质材料,即PVPK30、PVA-124和HPMC,使三者优势相结合。单独使用PVPK30,成膜时间较长,且喷膜剂均一性较差。加入HPMC可明显消除喷膜剂中气泡,增加制剂均一性。而PVPK30、PVA-124和HPMC三者的联合使用,可显著缩短成膜时间。
星点设计-效应面法[17-19]是在析因设计的基础上,加上星点及中心点而形成的实验次数较少、可进行线性或非线性拟合的实验设计方法,在制剂处方和工艺的优化中应用广泛。人工神经网络[20]由MATLAB软件完成的一个监督多层感知器,由输入,隐藏和输出层组成。人工神经网络的功能不受限制,可以灵活地捕捉复杂的模式,并且可以在模拟中保持稳定。尽管缺少数据,它仍能找到模式。在本实验中,人工神经网络具有更好的预测性能,可应用于更多制剂的处方优化及筛选。
实验中,根据星点设计效应面-人工神经网络法,复方活血化瘀喷膜剂的最优处方为PVPK30 2.24 g、PVA-124 0.75 g、HPMC 0.07 g,成膜时间为4.63 min。
5 结论本实验制得的复方活血化瘀喷膜剂黏度适宜,使用方便,成膜时间短,均一性好。剂型改造后,制得的复方活血化瘀喷膜剂较药酒原方滞留时间明显增长,药效发挥时间明显延长。星点设计效应面和人工神经网络法与实验数据都吻合良好,均可用于该制剂处方的优化和预测。但在本实验中,人工神经网络模型的实验值和预测值之间的偏差更小,预测更准确。
| [1] | 蔡鹰, 陆瑜, 龚琳, 等. 复方大黄烫伤喷膜的制备工艺优选[J]. 时珍国医国药, 2016, 27 (8): 1899–1900. |
| [2] | 朱玉莲.化瘀消肿喷膜剂的研究[D].重庆医科大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10631-1016783502.htm |
| [3] | 林华燕, 魏刚, 何坦, 等. 大黄不同提取液的成膜材料筛选[J]. 广东药学院学报, 2012, 28 (5): 470–474. DOI:10.3969/j.issn.1006-8783.2012.05.002 |
| [4] | 樊荣丹, 陈鹰, 张樱子, 等. 复方消伤痛喷膜剂的制备与质量控制[J]. 中国药师, 2014, 17 (5): 779–781. |
| [5] | 高倩.黄马缓释喷膜剂的研制[D].重庆: 重庆医科大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10631-1016783504.htm |
| [6] | 张世川, 国大亮, 刘岩, 等. 喷膜剂制备工艺与质量控制研究进展[J]. 药物评价研究, 2015, 38 (4): 435–438. |
| [7] | 崔曰新.盐酸利多卡因喷膜剂的制备[D].广州: 广东药科大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10573-1016730499.htm |
| [8] | Xue M, Hu S, Lu Y, et al. Development of chitosan nanoparticles as drug delivery system for a prototype capsid inhibitor[J]. International Journal of Pharmaceutics, 2015, 495 (2): 771–782. DOI:10.1016/j.ijpharm.2015.08.056 |
| [9] | 李琦, 裴河欢, 李静, 等. 星点设计-效应面法优选盐余甘子的炮制工艺[J]. 中南药学, 2018, 16 (4): 473–477. |
| [10] | Oladipo AA, Gazi M. Nickel removal from aqueous solutions by alginate-based composite beads:Central composite design and artificial neural network modeling[J]. Journal of Water Process Engineering, 2015, 8 (9): e81–e91. |
| [11] | Shet VB, Palan AM, Rao SU, et al. Comparison of response surface methodology and artificial neural network to enhance the release of reducing sugars from non-edible seed cake by autoclave assisted HCl hydrolysis[J]. Biotech, 2018, 8 (2): 127. |
| [12] | 蔡鹰, 陆瑜, 龚琳, 等. 复方大黄烫伤喷膜的制备工艺优选[J]. 时珍国医国药, 2016, 27 (8): 1899–1900. |
| [13] | 樊荣丹.复方消伤痛喷膜剂的研究[D].湖北中医药大学, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10507-1014325516.htm |
| [14] | 张子龙.大黄、关黄柏、泽兰、侧柏叶及双柏喷膜剂经皮渗透特征图谱特性研究[D].广州: 广州中医药大学, 2012. |
| [15] | 齐笑, 赵雪, 赵雪琪, 等. 喷膜剂的研究进展[J]. 实用药物与临床, 2018, 21 (4): 463–466. |
| [16] | 樊荣丹, 陈晨, 张樱子, 等. 喷膜剂中成膜材料的研究进展[J]. 中国药师, 2014, 17 (3): 492–495. |
| [17] | 张永萍, 徐剑, 谢伟杰. 星点设计-效应面法优化吲哚美辛亲水凝胶贴剂基质处方及成型工艺[J]. 医药导报, 2018, 37 (5): 593–599. |
| [18] | 杨志欣, 王海威, 张文君, 等. 星点设计-效应面优化苦参总生物碱组分磷脂复合物研究[J]. 中药材, 2018, 41 (3): 670–674. |
| [19] | 陈静怡, 郭贤源, 任翔, 等. 星点设计-效应面法优化积雪草苷脂质体镶囊的制备工艺[J]. 中草药, 2018, 49 (3): 569–574. |
| [20] | Novis S, Machado F, Costa VB, et al. Applying an artificial neural network model for developing a severity score for patients with hereditary amyloid polyneuropathy[J]. Amyloid-journal of Protein Folding Disorders, 2017, 24 (3): 1–9. |
2. Military Medicine Section, Logistics University of Chinese People's Armed Police Force, Tianjin 300309, China
 2018, Vol. 35
2018, Vol. 35