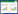文章信息
- 李晨萌, 田金洲, 魏明清, 倪敬年, 张学凯, 李婷, 时晶
- LI Chenmeng, TIAN Jinzhou, WEI Mingqing, NI Jingnian, ZHANG Xuekai, LI Ting, SHI Jing
- 补肾平肝方联合盐酸多奈哌齐治疗阿尔茨海默病精神行为症状的有效性观察
- Effectiveness of notifying kidney and calming liver recipe combined with donepezil in the treatment of Alzheimer's disease with behavioral and psychological symptoms
- 天津中医药, 2019, 36(10): 951-954
- Tianjin Journal of Traditional Chinese Medicine, 2019, 36(10): 951-954
- http://dx.doi.org/10.11656/j.issn.1672-1519.2019.10.04
-
文章历史
- 收稿日期: 2019-02-26
阿尔茨海默病(AD)是一种隐匿起病的以进行性认知功能损害为突出表现的神经变性病,临床主要表现除认知减退外,还包括日常生活能力受损及精神行为症状。AD的精神行为症状(BPSD)包括幻觉、妄想、激越、焦虑、抑郁、淡漠、易怒、异常行为运动[1],高达90%的AD患者在病程中至少伴随一种BPSD[2]。BPSD是AD患者住院治疗以及机构入住的最主要原因[3],不仅降低患者生活质量,也给照料者及社会带来巨大的负担。胆碱酯酶抑制剂是被推荐用于AD精神行为症状的首要药物,在控制认知下降和BPSD方面疗效肯定[4]。本院记忆门诊擅长中西药并用治疗AD伴发精神行为症状,常用的治法为补肾平肝法。本研究旨在分析补肾平肝方联合盐酸多奈哌齐治疗AD伴BPSD的效果是否优于单纯西药治疗。
1 资料与方法 1.1 病例来源以2016年9月——2018年6月就诊于北京中医药大学东直门医院记忆门诊的轻、中度AD伴BPSD且中医辨证为肾虚阳亢的患者92例为研究对象,根据疗法分组,观察组50例,采用补肾平肝方联合盐酸多奈哌齐治疗,对照组42例,单纯采用盐酸多奈哌齐治疗,疗程均为12周。对其临床资料进行回顾性分析。
1.2 诊断标准1) AD伴BPSD的诊断标准:AD的诊断采用国际上公认的美国国立神经病、语言交流障碍和卒中研究所-老年性痴呆与相关疾病协会(NINCDS-ADRDA)[5]拟定的“很可能AD”的诊断标准。精神行为症状的诊断根据神经精神调查量表(NPI)[6],具有其中任何一项精神行为症状即可诊断。2)痴呆严重程度判断:根据国际通用的临床痴呆评估量表(CDR)[7]进行评定:1分代表轻度痴呆,2分代表中度痴呆,3分代表重度痴呆。3)中医证候诊断标准:中医证候评估标准采用痴呆证候要素评定量表(PES-D-11)[8],证候积分大于等于7分,表明该证候成立。
1.3 纳入标准1) 符合NINCDS-ADRDA很可能AD的诊断标准。2)年龄在50~85岁之间。3)轻度或中度的AD患者,即CDR得分为1或2分。4)PES-D-11量表肾虚、阳亢证候积分≥7分。5)具有至少一项BPSD,且NPI量表得分≥4分。6)海金斯基缺血量表(HIS)[9]得分≤4分。7)汉密尔顿抑郁量表(HAMD)[10]得分≤12分。8)按照本研究治疗方法服药,且治疗前后神经心理学测试资料保留完整的患者。
1.4 排除标准1) 存在影响认知功能的其他神经变性疾病;2)脑血管疾病认知功能损害;3)严重心血管疾病、甲状腺功能减低、一氧化碳中毒影响认知功能者;4)精神疾病所致的精神行为症状;5)治疗前两周服用抗精神病药物。
1.5 脱落情况未按照本研究规定的治疗方法服药,观测时点未进行复诊者视为脱落。观察组脱落6例,对照组脱落8例。
1.6 治疗方法 1.6.1 对照组服用盐酸多奈哌齐(商品名:安理申,卫材(中国)药业有限公司生产,5 mg/片),1次/日,每次1片,睡前服用(若患者存在严重的失眠,可改为晨起顿服)。
1.6.2 观察组观察组在对照组基础上给予补肾平肝中药方颗粒剂(北京康仁堂药业有限公司生产)。主要药物包括:生地黄30 g,山茱萸30 g,肉苁蓉20 g,远志15 g,天麻20 g,钩藤30 g,黄芩15 g,珍珠粉0.6 g分冲,生甘草6 g。100 mL温水冲服,早、晚饭半小时服用。
1.6.3 治疗疗程治疗疗程为12周。
1.7 评价指标1) 简易精神状态检查表(MMSE)[11]量表评估总体认知功能,评分越高表示总体认知功能越好。2)采用NPI量表评估精神行为症状,此量表包括妄想、幻觉、激越、抑郁/烦躁不安、焦虑、欣快/情感高涨、淡漠/漠不关心、去抑制、易激惹、异常行为运动,共10项精神行为因子,还包括夜间行为活动、食欲/饮食改变2项植物神经改变,各项目评价的内容包括症状出现频率(F)、严重程度(S),每个项目的得分等于频率和严重度之积(F×S)。
1.8 统计方法采用SPSS 21.0统计软件进行数据分析,计数资料用构成比或率表示,组间比较采用χ2检验;计量资料用均值±标准差(x±s)表示,正态分布计量资料的比较采用t检验,偏态分布计量资料比较采用秩和检验。P<0.05为差异具有统计学意义。
2 结果 2.1 两组患者人口学资料比较对照组42例患者中男22例,女20例,平均年龄为(71.21±8.30)岁;观察组患者50例,其中男26例,女24例,平均年龄为(70.72±7.76)岁。两组患者人口学资料(包括性别、年龄、教育年限、体重指数、吸烟史、高血压史、糖尿病史、痴呆严重程度、MMSE、NPI)相比较,差异均无统计学意义(P>0.05),具有可比性,见表 1。
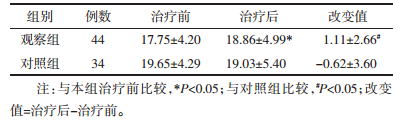
两组患者治疗前、治疗后的总体认知功能MMSE评分比较,差异均无统计学意义(P>0.05),观察组治疗后MMSE评分,较治疗前有显著升高(P<0.05)。观察组MMSE分数升高情况与对照组相比,差异有统计学意义(P<0.05),见表 2。
|
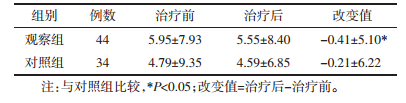
组间比较,两组患者治疗前和治疗后精神行为症状NPI总分均无统计学差异(P>0.05);组内比较,两组患者治疗后NPI总分均较治疗前降低,且观察组降低更明显(P<0.05),见表 3。
|
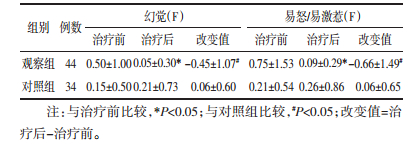
分别对NPI量表的10项精神行为因子以及2项植物神经改变发生的频率(F)、严重程度(S)进行分析,结果显示,观察组治疗后幻觉(F)和易怒/易激惹(F)较治疗前显著降低(P<0.05),幻觉(F)和易怒/易激惹(F)的减少情况与对照组比较,差异有统计学意义(P<0.05),而其他精神行为因子和植物神经改变发生的频率和严重程度比较,未显示出统计学差异。见表 4。
|
AD主要表现为认知损害,同时精神行为症状也是其常见的伴随症状,其中最常见的是易激惹、激越、焦虑、异常行为运动[12]。目前关于AD精神行为症状的中医证候和治疗研究较为缺乏,根据中医学异病同治的思想,其治疗上也多参考郁证、癫狂的治疗。笔者认为AD的精神行为症状尤其是阳性症状(幻觉、易激惹等)主要与“火”有关,因肝主情志,肝阳上亢,上扰神明,则出现急躁易怒、妄闻妄见、烦躁不安等精神行为症状,亦可导致头晕目眩、颞顶头痛、耳鸣如潮等躯体症状,故当用平肝泻火治法;而认知损害则主要责之于肾虚,因肾藏精,精生髓,髓养脑,脑为元神之府,故当补肾填精治法。因此,治疗AD伴精神行为症状可从补肾和平肝入手,双管齐下。
本研究所用补肾平肝方中生地黄、山茱萸、肉苁蓉补肾填精,肾精充盈,上充脑髓,则可发挥益肾健脑功效;天麻、钩藤平肝清热,黄芩清肝泻火,使肝经之热得清而不致偏亢;远志安心气,定神益智,交通心肾,珍珠粉分冲辅助清肝泻火、镇心定惊。以上诸药合用,共奏补肾平肝之效。
现代药理学研究发现,生地黄有效成分梓醇具有抗氧化、抗炎、抗凋亡和其他神经保护作用,在对抗神经缺血缺氧损伤(如老年痴呆)中起到重要作用[13]。山茱萸环烯醚萜苷能促进脑缺血小鼠的学习记忆能力,减少海马区神经元死亡数量[14]。肉苁蓉总苷胶囊治疗48周可以延缓中度AD患者认知功能减退、海马体积萎缩[15]。天麻和钩藤作为基础药对,其有效成分天麻素和钩藤碱可通过多种机制发挥神经保护作用,并改善记忆障碍,对老年痴呆有一定疗效[16]。并且钩藤能抑制谷氨酸兴奋毒性[17],研究表明其具有镇静作用[18],因此可能对痴呆阳性精神行为症状发挥一定作用。基于以上研究,本研究采用的补肾平肝中药对AD伴精神行为症状的改善作用或许可以得到解释。
认知测试是评估阿尔茨海默病患者病情的关键步骤,MMSE是目前应用最广泛的综合认知评估量表[11]。本研究观察组患者经过12周治疗后MMSE分数平均提高1.11分,而对照组患者MMSE分数有所降低,表明联合用药可以提高患者综合认知功能。此研究结果具有较重要的意义,因为有临床研究[19-20]显示MMSE分数的微小改变对于AD的医疗花费有至关重要的影响。神经心理学评定是评估BPSD的主要方式,其中NPI量表作为全面评估BPSD变化的工具,已成为目前大多数抗痴呆药物疗效评价的指标之一[21]。本研究结果显示,单用盐酸多奈哌齐及联合中药治疗12周后,AD患者NPI分数改变值分别为(-0.21±6.22)和(-0.41±5.10),两者比较差异有统计学意义(P<0.05),表明联合用药对AD精神行为症状的改善作用优于单纯使用盐酸多奈哌齐,其中能显著降低幻觉和易激惹发生次数。
本研究结果初步表明,补肾平肝方联合盐酸多奈哌齐对阿尔茨海默病伴精神行为症状患者的认知功能和精神行为症状具有较好的改善效果。由于本研究纳入的样本较少,随访周期较短,因此治疗的长期疗效,尚需要大样本的长期随机对照研究来验证。
| [1] |
Carotenuto A, Rea R, Traini E, et al. The effect of the association between donepezil and choline alphoscerate on behavioral disturbances in alzheimer's Disease:Interim Results of the ASCOMALVA Trial[J]. J Alzheimers Dis, 2017, 56(2): 805-815. DOI:10.3233/JAD-160675 |
| [2] |
Fernández M, Gobartt AL, Balañá M, COOPERA Study Group. Behavioural symptoms in patients with Alzheimer's disease and their association with cognitive impairment[J]. BMC Neurol, 2010, 10(1): 87. |
| [3] |
Zhou T, Wang J, Xin C, et al. Effect of memantine combined with citalopram on cognition of BPSD and moderate Alzheimer's disease:a clinical trial[J]. Exp Ther Med, 2019, 17(3): 1625-1630. |
| [4] |
田金洲. 中国痴呆诊疗指南[M]. 北京: 人民卫生出版社, 2017: 258-274.
|
| [5] |
McKhann G, Drachman D, Folstein M, et al. Clinical diagnosis of Alzheimer's disease:report of the NINCDS-ADRDA Work Group under the auspices of Department of Health and Human Services Task Force on Alzheimer's Disease[J]. Neurology, 1984, 34(7): 939-944. DOI:10.1212/WNL.34.7.939 |
| [6] |
Cummings JL, Mega M, Gray K, et al. The Neuropsychiatric Inventory[J]. Neurology, 1994(12): 2308. |
| [7] |
Hughes CP, Berg L, Danziger WL, et al. A new clinical Scale for the staging of dementia[J]. Br J Psychiatry, 1982, 140(6): 566-572. DOI:10.1192/bjp.140.6.566 |
| [8] |
田金洲, 时晶, 张新卿, 等. 轻度认知损害临床研究指导原则(草案)[J]. 中西医结合学报, 2008, 6(1): 9-14. |
| [9] |
Hachinski VC, Iliff LD, Zilhka E, et al. Cerebral Blood Flow in Dementia[J]. Arch Neurol, 1976, 1(6024): 1487-1488. |
| [10] |
Hamilton M. A rating scale for depression[J]. J Neurol Neurosurg Psychiatry, 1960, 23(12): 56-62. |
| [11] |
Folstein MF, Folstein SE, McHugh PR. "Mini-mental state". A practical method for grading the cognitive state of patients for the clinician[J]. J Psychiatr Res,, 1975, 12(3): 189-198. DOI:10.1016/0022-3956(75)90026-6 |
| [12] |
陈丽坚, 萧鲲, 张翠玲, 等. 阿尔茨海默病患者的精神行为症状与照料者苦恼程度关系分析[J]. 实用医学杂志, 2018, 34(16): 2794-2798. DOI:10.3969/j.issn.1006-5725.2018.16.040 |
| [13] |
黄传君, 赵方正, 张才擎. 生地黄有效成分梓醇药理作用机制研究进展[J]. 上海中医药杂志, 2017, 51(2): 93-97. |
| [14] |
杨明明, 袁晓旭, 赵桂琴, 等. 山茱萸化学成分和药理作用的研究进展[J]. 承德医学院学报, 2016, 33(5): 398-400. |
| [15] |
Li N, Wang J, Ma J, et al. Neuroprotective effects of cistanches herba therapy on patients with moderate alzheimer's Disease[J]. Evid Based Complement Alternat Med, 2015, 1-12. |
| [16] |
曾嫱, 李利民, 曾永长, 等. 天麻钩藤药对防治老年痴呆的药理作用机制概述[J]. 辽宁中医杂志, 2019, 61(9): 1-9. |
| [17] |
Lee J, Son D, Lee P, et al. Alkaloid fraction of Uncaria rhynchophylla protects against N-methyl-D-aspartate-induced apoptosis in rat hippocampal slices[J]. Neurosci Lett, 2003, 348(1): 51-55. DOI:10.1016/S0304-3940(03)00613-X |
| [18] |
宋立人, 洪洵, 丁绪亮, 等. 现代中药学大词典[M]. 北京: 人民卫生出版社, 2001: 367.
|
| [19] |
Jönsson L, Lindgren P, Wimo A, et al. Costs of Mini Mental State Examination-related cognitive impairment[J]. Pharmacoeconomics, 1999, 16(4): 409-416. DOI:10.2165/00019053-199916040-00008 |
| [20] |
Wolstenholme J, Fenn P, Gray A, et al. Estimating the relationship between disease progression and cost of care in dementia[J]. British Journal of Psychiatry, 2002, 181(2): 36-42. |
| [21] |
Cummings JL. Drug therapy:Alzheimer's disease[J]. N Engl J Med, 2004, 351: 56-67. DOI:10.1056/NEJMra040223 |
 2019, Vol. 36
2019, Vol. 36