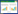文章信息
- 王亚昆
- WANG Yakun
- 病毒合剂联合磷酸奥司他韦治疗儿童甲型流行性感冒的临床观察
- Observation on the clinical effect of Oseltamivir Phosphate combined with Virus Mixture in the treatment of children influenza A
- 天津中医药, 2019, 36(8): 763-766
- Tianjin Journal of Traditional Chinese Medicine, 2019, 36(8): 763-766
- http://dx.doi.org/10.11656/j.issn.1672-1519.2019.08.10
-
文章历史
- 收稿日期: 2019-04-23
流行性感冒(简称流感)对全球人类的发病率和病死率有重大影响,世界卫生组织估计每年约有10亿人被感染,多达50万人死于流感[1],流感病毒由于抗原漂移(以血凝素和神经氨酸酶蛋白的点突变为特征)和抗原转移(由于人畜共患病病毒和人类病毒之间的基因重组导致的重大转移)而不断进化[1],虽然疫苗接种是预防流感的基石,但疫苗接种率往往不理想,而且鉴于流感病毒不断发展,目前的疫苗可能并非100%有效[2]。因此在大流行性感染的早期阶段,当对抗大流行性病毒株的疫苗仍然不可用时,抗病毒药物对于治疗流感十分重要。从20世纪80年代到21世纪初,由于发现表面糖蛋白神经氨酸酶(NA)在流感病毒复制中的关键作用,以及其对NA晶体结构的识别能力,导致靶向性NA抑制剂(NAI)如奥司他韦、帕拉米韦和扎那米韦的发展[2-5]。磷酸奥司他韦(达菲)是首个口服有效的特异性流感病毒NA抑制剂,而中成药的使用尚无统一的标准,本研究中达菲联合病毒合剂治疗流感获得了良好的临床效果,现报道如下。
1 资料和方法 1.1 一般资料选取本院自2018年12月—2019年3月门急诊或住院治疗确诊为流感甲型流感病毒感染的患儿60例作为研究对象,所有患儿均详细询问病史、体格检查、血常规+镜检+C反应蛋白(CRP)+降钙素原(PCT)、咽拭子甲型流感病毒核酸检测[逆转录-聚合酶链式反应(RT-PCR)法],门急诊血常规及咽拭子均在2 h内出具化验结果,诊断标准符合《流行性感冒诊断和治疗指南(2011年版)》[6]。本研究所有患儿家属均签署知情同意书。
1.2 纳入与排除标准纳入标准:1)具有流感样表现的学龄前期患儿,咽拭子甲型流感病毒核酸检测阳性(RT-PCR法)。2)起病48 h内,体温>39.0 ℃,血常规白细胞不高或减低。3)无严重基础疾病。排除标准:1)已使用其他抗病毒药物。2)合并细菌感染。3)已知对本研究所用中药成分或西药过敏者。4)符合《流行性感冒诊断和治疗指南(2011年版)》中有关重症流感诊断标准者。5)免疫缺陷或近3月内服用免疫抑制剂或糖皮质激素患儿。6)合并下气道感染。
1.3 分组和治疗方案本研究总共纳入病例73例,全部病例均符合研究纳入标准,采用随机数字法分为对照组及治疗组(治疗组37例,对照组36例),剔除资料不全者6例、脱落7例,最终纳入60例(治疗组30例,对照组30例)。对照组中男13例,女17例,年龄15~76个月,平均年龄(40.77±17.07)个月,血常规白细胞总数(6.67±1.41)×109/L。治疗组中男14例,女16例,年龄16~74月,平均年龄(39.9±16.98)个月,白细胞总数(6.35±1.56)×109/L。两组患儿在性别、年龄、白细胞总数之间的差异无统计学意义(P>0.05),具有可比性,见表 1。
对照组给予磷酸奥司他韦(商品名:达菲,上海罗氏制药有限公司,国药准字J20140121)治疗,用法依据《流行性感冒诊断和治疗指南(2011年版)》,疗程5 d。治疗组在对照组的基础上联合病毒合剂(天津市儿童医院,津药制字Z20070306)治疗,用法:3岁以下每日50 mL,3岁以上每日100 mL,分2~3次服用,疗程5 d。所有患儿均随访14 d,治疗无效患儿均收入院治疗。
1.4 疗效判定标准 1.4.1 中医症状分级量化标准参照2002版《中药新药临床研究指导原则》[7],观察比较两组治疗效果,评价采用症状积分判定方法,评判依据为:无症状0分、轻度1分、中度2分、重度3分,评判鼻塞、喷嚏、流涕、咽痛、咳嗽、发热、恶寒、头痛、肌肉关节酸痛、全身乏力10项症状的总积分。
1.4.2 中医证候疗效判定标准中医证候疗效判定标准,根据2002版《中药新药临床研究指导原则》[7]和国家中医药管理局发布的2012版《中医病证诊断疗效标准》[8]制定。痊愈:临床症状、体征消失或基本消失,证候疗效积分减少≥95%。显效:临床症状、体征明显改善,证候疗效积分减少≥70%。有效:临床症状、体征均有好转,证候疗效积分减少≥30%。无效:临床症状、体征无明显改善,甚或加重,证候疗效积分减少不足30%。总有效率(%)=(痊愈例数+显效例数+有效例数)/总例数×100%。
1.5 不良反应观察所有患儿均在治疗过程中观察药物的不良反应发生情况。
1.6 统计学处理采用SPSS 22.0统计软件进行分析,计量资料用均数±标准差(x±s)表示,组间比较采用t检验,计数资料以例数和百分比(%)表示,组间比较用χ2检验,P < 0.05代表差异有统计学意义。
2 结果 2.1 两组患儿临床疗效情况比较治疗后,对照组治愈9例,显效11例,有效2例,总有效率73.3%;治疗组治愈13例,显效13例,有效2例,总有效率93.3%,两组总有效率比较差异有统计学意义(P<0.05),见表 2。
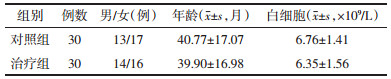
两组患儿治疗前证候疗效积分的比较差异无统计学意义(P>0.05),治疗后证候疗效积分的比较差异有统计学意义(P<0.05),治疗后证候积分的差值比较差异有统计学意义(P<0.05),见表 3。
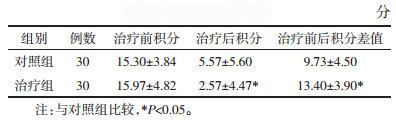
|
两组患儿治疗后发热、咳嗽、鼻塞、恶寒、肌肉关节酸痛症状缓解时间比较差异有统计学意义(P<0.05),见表 4。
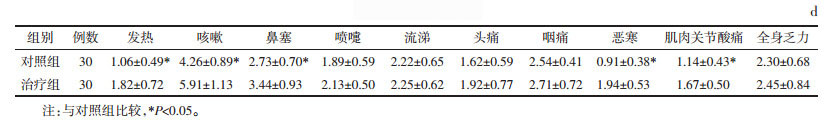
|
所有患儿在治疗过程中均未发现药物的不良反应。
3 讨论流感是由流感病毒引起的急性呼吸道传染病,容易在人与人之间传播。流感的流行病学特点为突然暴发,迅速扩散,造成不同程度的流行,具有季节性,发病率高但病死率低。流感病毒属于正黏病毒科,为单股、负链、分节段的RNA病毒。根据核蛋白和基质蛋白分为甲、乙、丙3型。根据甲型流感病毒表面的血凝素和NA蛋白结构及其基因特征又可分成许多亚型,目前已发现甲型流感病毒血凝素16个亚型(H1~16)、NA 9个亚型(N1~9)[9]。带有流感病毒颗粒的飞沫吸入呼吸道后,病毒的NA破坏神经氨酸,使黏蛋白水解,糖蛋白受体暴露。甲、乙型流感病毒通过血凝素结合上皮细胞含有唾液酸受体的细胞后启动感染[10]。甲和乙型流感的临床特点是突然出现发热、头痛、肌痛、咳嗽和食欲减退等全身性症状,体温可达39~40 ℃,常有咽喉痛、鼻塞、流涕、胸骨后不适等,严重病例可发生下呼吸道合并症,如气管炎和支气管肺炎。常见的肺外并发症有心肌炎、肾功能衰竭、心包炎、脑膜炎和Reye综合征等[11]。婴幼儿流感的临床症状往往不典型,可仅为反复高热不退或出现高热惊厥,而缺少流感样症状。新生儿流感少见,往往只表现为嗜睡、拒奶、呼吸暂停等,易合并肺炎。小儿流感病毒引起的合并症及重症病例更常见,而早期治疗(症状出现后48 h内)住院的复杂流感患儿病死率降低了52%[12],因此在发病36 h或48 h内尽早使用抗流感病毒药物治疗可缩短病程,减少并发症。
NA催化人呼吸道细胞上糖缀合物的末端唾液酸残基的分解,促进病毒进入宿主细胞,并破坏宿主细胞上的血凝素受体,导致子代病毒颗粒的释放和随后的感染传播[3, 5]。NA抑制剂达菲抑制感染细胞的病毒释放,并降低病毒复制率,对甲、乙型流感均具活性。许多随机、双盲、安慰剂对照试验均报道其用于流感样病例,能有效缓解症状、明显缩短病程、减少并发症的发生和抗菌药物的使用。本研究结果表明达菲的抗病毒作用较好,与国外报道基本相同,能明显缩短病程、改善症状。达菲在儿童中应用的常见不良反应包括胃肠道症状、咳嗽、支气管炎等,在儿童个别病例可出现自我伤害和谵妄事件[13]。因样本含量少,两组患儿均未出现明显的不良反应。
流感属中医学“时行感冒”范畴,时行感冒的病机是邪毒经口鼻或皮毛而入,卫气被郁,故微恶风寒,发热或壮热;卫气被郁,毛窍开合失司,故无汗或少汗;邪未外泄,病毒熏蒸于上,故头痛、咽痛;邪毒袭肺,肺气不宣,故咳嗽;病毒之邪伤及阴血,故舌质红或红绛,苔薄黄或黄厚,邪毒在卫表,故脉浮数、滑或滑数,脉为病毒盈盛之症。病毒合剂为本院自行配制的中药制剂,由金银花、连翘、白茅根、水牛角粉、石膏等组成。方中金银花可清热解毒、发散风热、抗菌、增强免疫力,连翘内清郁热、外疏肌表,白茅根生津止渴、清热止咳、清热利尿、清肺胃热,水牛角粉可清热解毒、定惊安神、凉血止血,石膏可清泻肺热,诸药共伍,具有较好的抗病毒效果,还可调节患者免疫功能、抗炎、定惊、退热、止咳、利尿,为治疗流感有效药物。本研究结果提示病毒合剂联合达菲治疗流感临床效果明显优于达菲单药治疗,考虑可能与目前流行的季节性甲型流感病毒毒株普遍具有耐药性有关。
综上所述,病毒合剂联合达菲治疗流感的临床效果确切,可有效缩短患者主要症状消失时间,且不良反应少,值得临床借鉴推广应用。
| [1] |
Ghebrehewet S, MacPherson P, Ho A. Influenza[J]. BMJ, 2016, 355: i6258. |
| [2] |
Hurt AC. The epidemiology and spread of drug resistant human influenza viruses[J]. CurrOpinVirol, 2014, 8: 22-29. |
| [3] |
McLaughlin MM, Skoglund EW, Ison MG. Peramivir:an intravenous neuraminidase inhibitor[J]. Expert Opin Pharmacother, 2015, 16(12): 1889-1900. DOI:10.1517/14656566.2015.1066336 |
| [4] |
Babu YS, Chand P, Bantia S, et al. BCX-1812(RWJ-270201):a novel, highly potent, orally active, and selective influenza neuraminidase inhibitor through structure-based drug design[J]. J Med Chem, 2000, 43(19): 3482-3486. DOI:10.1021/jm0002679 |
| [5] |
Chand P, Kotian PL, Dehghani A, et al. Systematic structurebased design and stereoselective synthesis of novel multisubstituted cyclopentane derivatives with potent antinifluenza activity[J]. J Med Chem, 2001, 44(25): 4379-4392. DOI:10.1021/jm010277p |
| [6] |
卫生部流行性感冒诊断与治疗指南编撰专家组. 流行性感冒诊断与治疗指南(2011年版)[J]. 中华结核和呼吸杂志, 2011, 34(10): 725-734. DOI:10.3760/cma.j.issn.1001-0939.2011.10.004 |
| [7] |
郑筱萸.中药新药临床研究指导原则(试行)[S].北京: 中国医药科技出版社, 2002: 364-366.
|
| [8] |
国家中医药管理局. 中医病症诊断疗效标准[M]. 北京: 中国医药科技出版社, 2012: 11.
|
| [9] |
David MK, Peter MH, Fields V. Philadelphia(USA): Lippincott Williams and Wilkins, 2007: 1718.
|
| [10] |
Douglas D, Richman JR, Whitley GF. Clinical virology[J]. Washington:ASM Press, 2009, 943-975. |
| [11] |
Duchini A, Viermes ME, Nyberg LM, et al. Hepatic decompensation in patients with cirrhosis during infection with influenza A[J]. Arch Intern Med, 2000, 160(1): 113-115. DOI:10.1001/archinte.160.1.113 |
| [12] |
Muthuri SG, Venkatesan S, Myles PR, et al. Effectiveness of neuraminidase inhibitors in reducing mortality in patients admitted to hospital withinfluenza AH1N1pdm09 virus infection:a meta-analysis of individual participant data[J]. Lancet Respir Med, 2014, 2: 395-404. DOI:10.1016/S2213-2600(14)70041-4 |
| [13] |
詹思延. 奥司他韦安全性再聚焦——药物流行病学视角[J]. 药物不良反应杂志, 2012, 14(1): 1-3. DOI:10.3969/j.issn.1008-5734.2012.01.001 |
 2019, Vol. 36
2019, Vol. 36