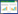文章信息
- 刘文莉, 只德贤, 王丽莉, 刘昌孝, 何新
- LIU Wenli, ZHI Dexian, WANG Lili, LIU Changxiao, HE Xin
- 香柑内酯在不同种属肝微粒体中的代谢差异研究
- Study of the differences in bergapten metabolites in liver microsomes of different species and genera
- 天津中医药, 2019, 36(9): 921-924
- Tianjin Journal of Traditional Chinese Medicine, 2019, 36(9): 921-924
- http://dx.doi.org/10.11656/j.issn.1672-1519.2019.09.21
-
文章历史
- 收稿日期: 2019-05-17
2. 广东药科大学中药学院, 广州 510006;
3. 天津药物研究院释药技术与药代动力学国家重点实验室, 天津 300193;
4. 天津商业大学生物技术与食品科学学院, 天津 300134
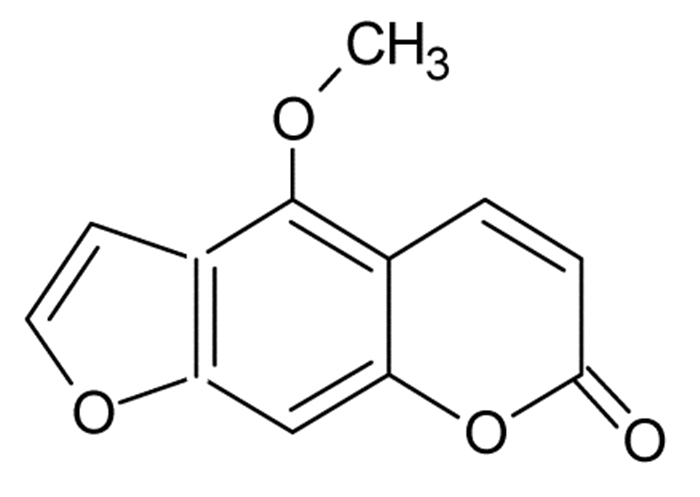
香柑内酯是从伞形科和芸香科植物中发现的一种具有生物活性的天然化合物,不仅存在于许多传统中药植物如独活、防风、白芷中,而且在许多蔬菜和水果也有发现[1-2]。香柑内酯结构如图 1所示,属于呋喃香豆素类化合物。香柑内酯具有很强的光敏性,能与长波紫外光结合,在临床上主要用于治疗牛皮癣,白癜风和T细胞淋巴瘤等[3-7]。
|
| 图 1 香柑内酯 Fig. 1 Structure of bergapten |
肝脏中存在的细胞色素P450酶(CYP450酶)是人体中最重要的肝脏微粒体混合功能酶系统,能作用于各种外源性化合物,使其在肝脏内进行生物转化,对药物在机体内的代谢起到极其重要的作用[8-10]。药物代谢过程中存在的种属差异,对于药物的安全性评价、药效学及药物动力学研究具有重要的意义[11-12]。当动物与人体实验结果存在明显差异时,如何将动物实验的结果外推至人体是一个难题。确切地估计药物代谢的种属差异,对评价动物实验数据、科学地预测药物毒理学、药物动力学、药理学特性是至关重要的[13-14]。
为了更好地理解香柑内酯的肝代谢及实验动物和人体之间可能存在的差异,本文利用人、恒河猴、食蟹猴、豚鼠、大鼠、小鼠、比格犬7种动物肝微粒体,采用肝微粒体体外孵育法研究了香柑内酯在不同种属微粒体中的代谢差异。
1 材料与仪器 1.1 仪器及耗材6520四级肝飞行时间液质联用(Q-TOF HPLC/MS,美国安捷伦公司,MassHunter B.02.01SP3色谱工作站);高速离心机(ALLEGRA-64R,美国BECKMAN公司);海尔-80 ℃超低温保存箱(青岛海尔股份有限公司);微型旋涡混合仪(WH-3,上海沪西分析仪器厂有限公司);十万分之一天平(AX205,瑞士Mettler Toledo公司);DKB-501A型超级恒温水槽(上海精宏实验设备有限公司);Millipore Milli-Q/30 L超纯水机(法国Millipore公司);96孔深孔培养板(美国Corning公司);电子恒温水浴锅(天津市泰斯特仪器有限公司)。
1.2 药品与试剂香柑内酯(5-甲氧基补骨脂素)标准品(>98 %)、卡马西平(内标)购于中国食品药品检定研究院;人肝微粒体、恒河猴肝微粒体、食蟹猴肝微粒体、小鼠肝微粒体、SD大鼠肝微粒体及比格犬肝微粒体,均购于瑞德肝脏疾病研究(上海)有限公司;还原型辅酶Ⅱ(NADPH)、二甲基亚砜(DMSO),购自美国Sigma公司;甲醇、乙腈、为为色谱纯等购于天津康科德科技发展有限公司;所有其他溶剂和化学试剂均为分析纯或以上。
2 方法 2.1 香柑内酯在7种肝微粒中的孵育反应香柑内酯(终浓度为50 μmol/L)溶于DMSO(终浓度不超过0.5%),并在磷酸盐缓冲液(pH 7.4,0.1 mol/L)中稀释。将50 μL标准溶液与50 μL 7种肝微粒体(终浓度为2 mg/mL)混合,分别在37 ℃预孵育5 min。然后,向上述反应混合物中加入100 μL NADPH(终浓度为1 mmol/L)。在37℃孵育120 min后,使用400 μL冰甲醇终止反应。在4℃下10 000 g离心10 min后,上清液通过0.22 μm过滤器过滤,并通过UPLC/Q-TOF MS进行分析。对照组不加香柑内酯。分别将5 μL上述溶液注入Q-TOF UPLC/MS和HPLC/MS/MS进行分析。
2.2 香柑内酯在7种哺乳动物肝微粒体中的代谢产物测定 2.2.1 色谱条件色谱柱:Agilent Proshell 120(2.1 mm×100 mm,1.7 μm);柱温:30 ℃;流动相A为0.1 %甲酸溶液,流动相B为甲醇;流速:0.2 mL/min;梯度洗脱,0~3min,90% A,3~14min,90 %→10 %A,14~17 min,10 %A,17~17.01 min,10 %→90 %A,17.01~20 min,90 %A;进样量:5 μL。
2.2.2 质谱条件电喷雾离子源(ESI);正离子模式和负离子模式;碰撞能量,25 eV;毛细管电压,3.2 kV;离子源温度:300 ℃;脱溶剂气温度:350 ℃;脱溶剂气流速:480 L/h;锥空气流速:600 L/h。
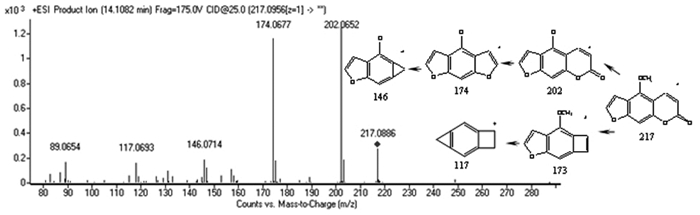
3 结果 3.1 香柑内酯在7种肝微粒体中代谢产物结构鉴定在正离子ESI+下,香柑内酯(tR=14.108 2 min)在m/z 217.095 6处具有质子化分子[M+H]+。香柑内酯主要通过去甲基(-CH3)和脱掉中性分子CO生成m/z 202.065 2,174.067 7,146.071 4,117.693 2处的特征产物离子。
如图 2所示,基于香柑内酯的代谢产物裂解和特征性质谱分离特征,推断这些代谢产物的碎片信息和断裂过程。
|
| 图 2 香柑内酯Q-TOF质谱和碎片信息 Fig. 2 Q-TOF mass spectrometry and fragment information of bergaptenin |
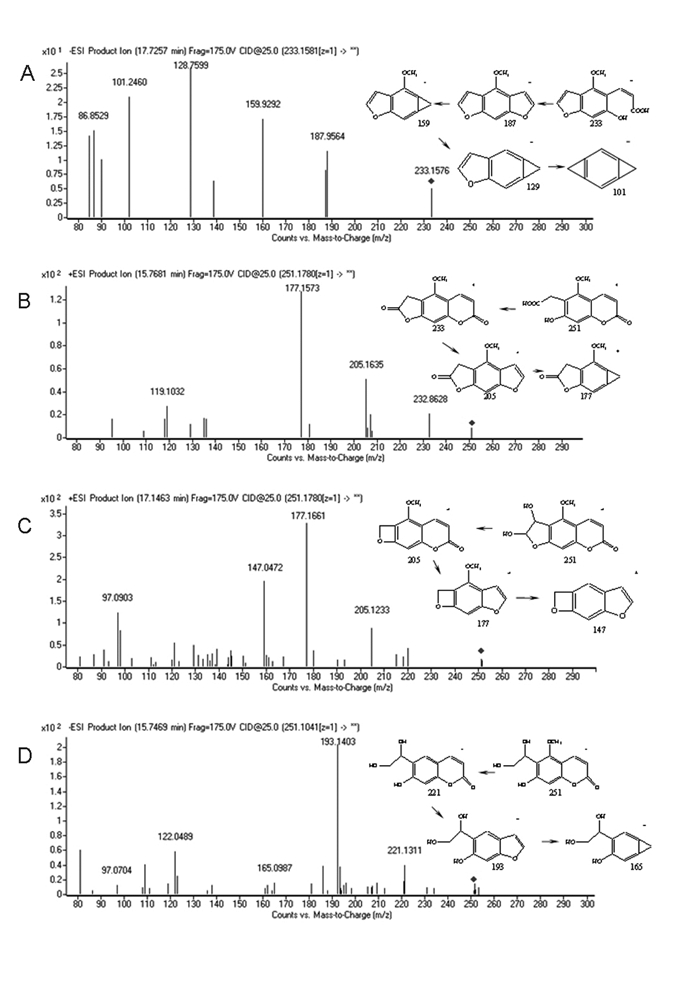
香柑内酯与7种肝微粒体孵育后,共检测到4种代谢产物:M1(苯环羟基化),M2(内酯环水解),M3(内酯环的羟基化)和M4(呋喃环氧化)。代谢产物的结构详细分析如图 3所示。代谢产物的结构详细分析如图 3所示。
|
| 图 3 香柑内酯代谢产物的Q-TOF的质谱图(A)M1、(B)M2、(C)M3、(D)M4 Fig. 3 Q-TOF mass spectrum of the metabolites of bergaptenin:(A) M1, (B) M2, (C) M3, (D) M4 |
代谢产物M1准分子离子峰[M-H]-为m/z 233.158 1的离子,表明加入H2O分子,主要碎片离子为m/z 187.956 4,159.929 2,128.759 9,101.246 0,确认内酯环水解产物的形成。代谢产物M2和M3准分子离子峰[M+H]+和[M-H]-分别为m/z 251.178 0和m/z 249.127 5。碎片数据表明,香柑内酯转化为γ-酮戊二酸和环氧化物中间体,并形成羟基香豆素乙酸和二氢二醇。代谢产物M4准分子离子峰[M-H]-为m/z 251.104 1,与在呋喃环上羟基化产物的形成一致,也是二氢二醇(M3)的氧化产物。
3.2 香柑内酯在不同肝微粒体中代谢产物种类及含量比较 3.2.1 香柑内酯在不同肝微粒体中代谢产物的种类比较由表 1可以看出,人肝微粒体、大鼠肝微粒体及比格犬肝微粒体中均发现4种代谢产物(M1、M2、M3、M4)。恒河猴肝微粒体、食蟹猴肝微粒体及小鼠肝微粒体中均发现3种代谢产物(M2、M3、M4),而在豚鼠肝微粒体中仅发现两种代谢产物(M3、M4)。从代谢产物的种类上分析,香柑内酯在大鼠、比格犬肝微粒体的代谢产物种类与人肝微粒体代谢产物种类相同。表 1总结了在7种肝微粒体中鉴定的香柑内酯代谢产物的化学式,准确的质量和保留时间(tR)。
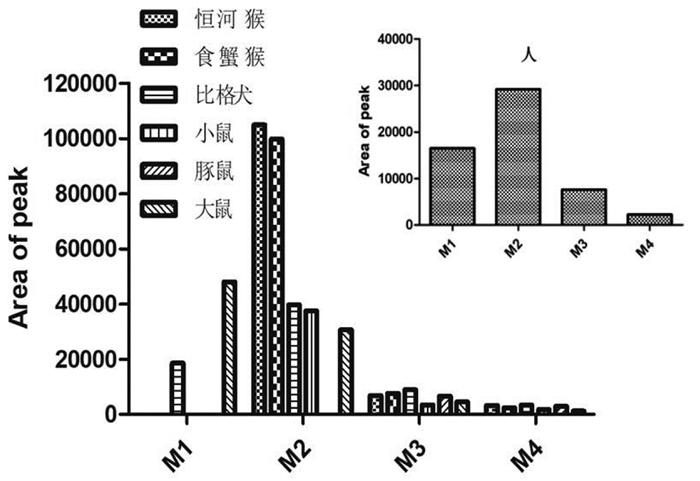
如图 4所示,香柑内酯在人肝微粒体中代谢产物M1的含量与比格犬和大鼠比较接近;香柑内酯在人肝微粒体中代谢产物M2的含量与比格犬、小鼠及大鼠接近。代谢产物M3、M4在七种肝微粒体中的含量都较为接近。综上所述,从代谢产物的含量上分析,比格犬和大鼠肝微粒体中的代谢产物与人肝微粒体中的代谢产物含量比较接近。
|
| 图 4 香柑内酯在不同肝微粒体中代谢产物含量比较(n=3) Fig. 4 Comparison of metabolite contents of bergaptenin in different liver microsomes(n=3) |
伞形科药用植物植物包括北沙参、白芷等在中医药中应用十分广泛,如消炎癣湿药膏等复方中药,其主要药效成分为呋喃香豆素类化合物。香柑内酯为来源于伞形科药用植物中的呋喃香豆素类化合物,在临床上多用于治疗皮肤病,同时具有抗菌降血压等作用。
药物进入体内主要经由肝脏进行代谢,在这一过程中肝脏中的CYP450酶发挥着及其重要作用[15-17]。其中,CYP1A2占CYP450酶总量的13%,参与包括咖啡因、非那西丁、奥美拉唑等20多种临床常用药物的代谢。CYP2E1约占CYP450酶总量的7%,具有超过70种外源性底物,CYP3A4参与50%以上临床用药的Ⅰ相代谢[18]。一些香豆素类化合物的体内代谢与CYP450酶相关,如补骨脂素等为CYP450酶的抑制剂[19]。
由于存在种属差异,香柑内酯在不同动物肝微粒体中的代谢也不相同。通过从代谢产物种类及含量上分析,香柑内酯在比格犬和大鼠肝微粒体中的代谢与在人肝微粒的代谢较为相近。开展药物代谢的种属差异研究,有助于阐明药物的毒副作用,对于药物的安全性评价、药效学及药物动力学研究具有重要的意义,为新药开发提供数据支持,同时为动物实验的结果外推至人体提供理论支持。
| [1] |
林黎, 钱晓萍, 刘宝瑞. 中药独活的化学成分及其抗肿瘤活性的研究进展[J]. 现代肿瘤医学, 2011, 19(2): 373-376. |
| [2] |
刘双利, 姜程曦, 赵岩, 等. 防风化学成分及其药理作用研究进展[J]. 中草药, 2017, 48(10): 2146-2152. DOI:10.7501/j.issn.0253-2670.2017.10.032 |
| [3] |
Ohnishi A, Matsuo H, Yamada S, et al. Effect of furanocoumarin derivatives in grapefruit juice on the uptake of vinblastine by Caco-2 cells and on the activity of cytochrome P4503A4[J]. British Journal of Pharmacology, 2010, 130(6): 1369-1377. |
| [4] |
杨秀伟, 徐波, 冉福香, 等. 40种香豆素类化合物对人表皮癌细胞系A432细胞株和人乳腺癌细胞系BCAP细胞株增殖抑制活性的筛选[J]. 中国现代中药, 2006(12): 9-10, 18. DOI:10.3969/j.issn.1673-4890.2006.12.004 |
| [5] |
杨秀伟, 徐波, 冉福香, 等. 11种香豆素类化合物对人膀胱癌细胞系E-J细胞株生长抑制活性的筛选[J]. 中西医结合学报, 2007(1): 56-60. |
| [6] |
董伟, 汤喜兰, 赵国巍, 等.白芷香豆素类化合物对乳腺癌细胞的化疗增敏作用研究[J/OL].中国临床药理学与治疗学, 2019(2): 140-146[2019-03-08].
|
| [7] |
Heald P, Rook A, Perez M, et al. Treatment of erythrodermic cutaneous T-cell lymphoma with extracorporeal photochemotherapy[J]. Journal of the American Academy of Dermatology, 1992, 27(3): 427-433. DOI:10.1016/0190-9622(92)70212-X |
| [8] |
Letteron P, Descatoire V, Larrey D, et al. Inactivation and induction of cytochrome P-450 by various psoralen derivatives in rats[J]. Journal of Pharmacology & Experimental Therapeutics, 1986, 238(2): 685-692. |
| [9] |
Mays DC, Hilliard JB, Wong DD, et al. Bioactivation of 8-methoxypsoralen and irreversible inactivation of cytochrome P-450 in mouse liver microsomes:modification by monoclonal antibodies, inhibition of drug metabolism and distribution of covalent adducts[J]. Journal of Pharmacology & Experimental Therapeutics, 1990, 254(2): 720-731. |
| [10] |
Tinel M, Belghiti J, Descatoire V, et al. Inactivation of human liver cytochrome P-450 by the drug methoxsalen and other psoralen derivatives[J]. Biochemical Pharmacology, 1987, 36(6): 951-955. DOI:10.1016/0006-2952(87)90190-0 |
| [11] |
何芋岐, 曾瑶, 凌蕾, 等. 睾酮代谢的种属差异研究(英文)[J]. 遵义医学院学报, 2017, 40(5): 463-468. DOI:10.3969/j.issn.1000-2715.2017.05.001 |
| [12] |
樊慧蓉, 董世奇, 李全胜, 等. 甘草素在体外不同种属肝微粒体中的代谢差异研究[J]. 中草药, 2017, 48(2): 320-326. |
| [13] |
张晓璐, 乐江. 细胞色素P450的工具药选择及种属差异的研究进展[J]. 中国药理学与毒理学杂志, 2012, 26(5): 697-701. DOI:10.3867/j.issn.1000-3002.2012.05.019 |
| [14] |
Yang AH, Chen JX, Ma YT, et al. Studies on the metabolites difference of psoralen/isopsoralen in human and six mammalian liver microsomes in vitro by UHPLC-MS/MS[J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 141: 200-209. DOI:10.1016/j.jpba.2017.04.026 |
| [15] |
Wang LL, Hai Y, Huang NN, et al. Human cytochrome P450 enzyme inhibition profile of three flavonoids isolated from Psoralea corylifolia:in silico predictions and experimental validation[J]. New Journal of Chemistry, 2018, 42(13): 10922-10934. DOI:10.1039/C7NJ00884H |
| [16] |
Hai Y, Feng S, Wang LL, et al. Coordination Mechanism and bio-evidence:reactive γ-ketoenal intermediated hepatotoxicity of psoralen and isopsoralen based on computer approach and bioassay[J]. Molecules, 2017, 2(9): 1451. |
| [17] |
Feng S, He X, Zhong PR, et al. A Metabolism-Based synergy for total coumarin extract of radix angelicae dahuricae and ligustrazine on migraine treatment in rats[J]. Molecules, 2018, 23(5): 1004. DOI:10.3390/molecules23051004 |
| [18] |
梁容佳, 陈俊秀, 只德贤, 等. 异鼠李素对人肝微粒体CYPs活性及大鼠原代肝细胞毒性作用研究[J]. 药物评价研究, 2017, 40(5): 627-632. |
| [19] |
Feng S, He X. Mechanism-based inhibition of CYP450:an indicator of drug-induced hepatotoxicity[J]. Current Drug Metabolism, 2013, 14(9): 921-945. DOI:10.2174/138920021131400114 |
2. School of Traditional Chinese Medicine, Guangdong Pharmaceutical University, Guangzhou 510006, China;
3. Drug Delivery Technology and Pharmacokinetics, Tianjin Institute of Pharmaceutical Research, Tianjin 300193, China;
4. School of Biotechnology Food Science, Tianjin University of Commerce, Tianjin 300134, China
 2019, Vol. 36
2019, Vol. 36