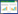文章信息
- 张永苗, 张兵, 梁春霞, 彭辉, 王仁兴, 薛志峰, 刘志东
- ZHANG Yongmiao, ZHANG Bing, LIANG Chunxia, PENG Hui, WANG Renxing, XUE Zhifeng, LIU Zhidong
- 基于HPLC-UV特征图谱与主成分分析的蔓荆子配方颗粒的质量控制研究
- Quality evaluation of Viticis Fructus formula granules based on HPLC-UV characteristic spectrum and principal component analysis
- 天津中医药, 2019, 36(9): 925-931
- Tianjin Journal of Traditional Chinese Medicine, 2019, 36(9): 925-931
- http://dx.doi.org/10.11656/j.issn.1672-1519.2019.09.22
-
文章历史
- 收稿日期: 2019-05-22
2. 天津中医药大学, 天津市现代中药重点实验室-省部共建国家重点实验室培育基地, 天津 301617
蔓荆子为马鞭草科牡荊属多年生落叶小灌木单叶蔓荆(Vitex trifolia L. var. simplicifolia Cham.)或蔓荆(Vitex trifolia L.)的干燥成熟果实[1],主产于山东、广西、广东、福建、江西、浙江等地。蔓荆子在《神农本草经》中被列为上品,谓“荆实,味苦,微寒,主筋骨间寒热,湿痹据挛,明目坚齿,利九窍,去白虫,久服轻身耐老”[2]。蔓荆子中主要含有酚类、木脂素类、黄酮类、萜类等化学成分[3-9]。现代研究表明,蔓荆子具有镇痛、抗炎、降压、祛痰、抗肿瘤、抗衰老和改善微循环的药理作用[10-13],常用于疏散风热、清理头目、止痛的功效。蔓荆子中主要含有原儿茶酸、对羟基苯甲酸、蔓荆子黄素3种活性成分,其中原儿茶酸具有抗菌[14]、抗炎[15]、抗氧化[16]、抑制肿瘤、镇痛[17]、保护缺血和缺氧神经元细胞[18-19]等作用,对羟基苯甲酸具有神经保护和抗炎作用[20],蔓荆子黄素具有抗炎[21-24]、抗氧化、镇痛、抗肿瘤[24-30]、免疫调节[18]的作用,它们是蔓荆子发挥药效的物质基础。
相比传统汤剂,中药配方颗粒具有方便服用、高效、易携带和安全可控等优点。本文在参照古法的基础上,采用生品粉碎后进行水提、过滤浓缩、干燥制粒,可充分提取蔓荆子的有效成分,提高其配方颗粒的质量。蔓荆子配方颗粒在性味归经,功能主治方面与蔓荆子药材一致。本文通过测定不同产地批次蔓荆子的配方颗粒中原儿茶酸、对羟基苯甲酸和蔓荆子黄素进行含量和指纹图谱,并结合主成分分析方法对其指纹图谱特征变量进行降维处理,寻求其在化学成分方面的共性与差异,根据相似相聚原理,区分优劣,为蔓荆子配方颗粒的质量控制和评价提供依据。
1 实验仪器与试药安捷伦1260LC-VWD液相色谱仪(美国安捷伦公司);安捷伦1260LC-DAD液相色谱仪(美国安捷伦公司);B-290型喷雾干燥仪(瑞士Buchi公司);GL2-25干法制粒机(张家港开创机械制造有限公司);FA124型万分之一天平(天津亿诺科学仪器有限公司);XP205十万分之一电子分析天平(瑞士Mettler Toledo公司);Milli-Q超纯水机(美国Millipore公司)。
对羟基苯甲酸对照品(批号2169,含量以99.2%计)、原儿茶酸对照品(批号5668,含量以100%计)、蔓荆子黄素对照品(批号5185,含量以99.6%计)均购自上海诗丹德标准技术服务有限公司。糊精(西安天正药业有限公司),乙腈、甲醇、磷酸、甲酸均为色谱纯(购自Fisher Scientific公司),水为超纯水。10批蔓荆子药材均由黑龙江珍宝岛药业股份有限公司提供,编号分别为A1~A10,来源见表 1。按2015年版《中国药典》一部蔓荆子鉴别项下方法检验,鉴定为品为马鞭草科植物单叶蔓荆(Vitex trifolia L. var. simplicifolia Cham.)或蔓荆(Vitex trifolia L.)的干燥成熟果实。按其含量测定项下测定蔓荆子黄素的含量,结果显示,蔓荆子药材中蔓荆子黄素含量均大于0.030%,符合药典标准。
取原儿茶酸15.26 mg、对羟基苯甲酸11.82 mg、蔓荆子黄素对照品10.46 mg,精密称定,分别置于50、25和50 mL量瓶中,加60%甲醇分别制成每1 mL含原儿茶酸0.305 2 mg、对羟基苯甲酸0.469 0 mg、蔓荆子黄素0.208 4 mg的对照品储备液。
2.1.2 混标溶液的配制分别精密吸取上述各对照品储备液2、5和2 mL适量于50 mL量瓶中,加60%甲醇制成每1 mL含原儿茶酸12.21 μg、对羟基苯甲酸46.90 μg、蔓荆子黄素8.335 μg的混合对照品溶液①。分别精密吸取上述各对照品储备液10、25和10 mL于100 mL量瓶中,加60%甲醇制成每1 mL含原儿茶酸30.52 μg、对羟基苯甲酸117.3 μg、蔓荆子黄素20.84 μg的混合对照品溶液②。
2.1.3 配方颗粒的制备取A1~A10蔓荆子药材粉碎成粗粉,加12倍水,回流提取2 h,趁热滤过,减压浓缩汤剂密度至1.020 g/cm3,按药(干膏量)与糊精1:1比例加入,混合均匀后,喷雾干燥,以干燥粉末进行干法制粒(每克配方颗粒相当于5 g蔓荆子饮片),所得10批颗粒依次编号记为S1~S10。
2.1.4 供试品溶液的制备精密称取蔓荆子配方颗粒粉末0.3 g,置于具塞锥形瓶中,精密加入25 mL 60%甲醇,密封,称质量,超声处理45 min(功率400 W,频率40 kHz),放冷,再次称质量,用60%甲醇补足减失质量,静置后取上清液,以0.22 μm孔径的滤膜过滤,即得供试品溶液。
2.1.5 色谱条件Agilent ZOBRAX Plus C18色谱柱(5 μm,4.6 mm×250 mm),流动相为0.1%磷酸水(A)-乙腈(B),梯度洗脱,0~3 min(93% A),3~13 min(93%-90% A),13~25 min(90%-83% A),25~35 min(83%-74% A),35~40 min(74%-60% A),40~45 min(60%-40% A),45~55 min(40%-10% A),流速1.0 mL/min,柱温35 ℃,进样量10 μL,程序性检测波长,0~9 min(254 nm),9~9.01 min(254~258 nm),9.01~20 min(258 nm),20~20.01min(258~260 nm),20.01~55 min(260 nm)。理论塔板数按对羟基苯甲酸峰计算应不低于3 000。
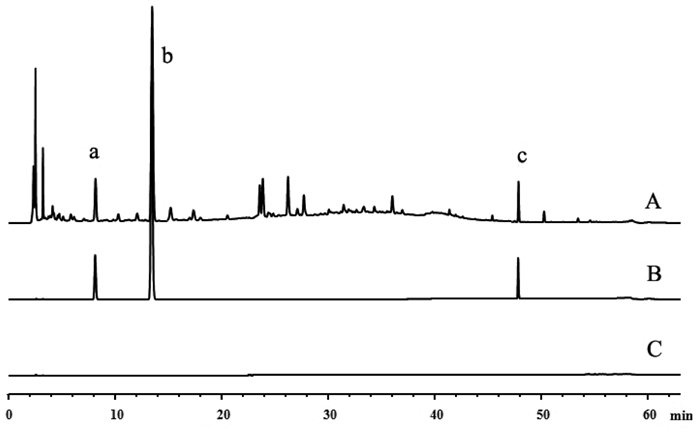
2.1.6 专属性考察取混合对照品溶液①和江西SQ80703的蔓荆子配方颗粒(S8)制备的供试品溶液,按“2.1.5”项下色谱条件分析。由图 1可知,原儿茶酸、对羟基苯甲酸、蔓荆子黄素混合对照品溶液、蔓荆子配方颗粒供试品溶液在相同的保留时间都有色谱峰,同时无溶剂峰干扰,表明方法专属性良好。
|
| A.蔓荆子配方颗粒供试品溶液;B.混合对照品;C.空白60%甲醇;a.原儿茶酸;b.对羟基苯甲酸;c.蔓荆子黄素 图 1 专属性考察图谱 Fig. 1 HPLC chromatograms exclusive investigation |
精密称取对照品原儿茶酸10.12 mg、对羟基苯甲酸25.42 mg、蔓荆子黄素10.26 mg,置于100 mL量瓶,加60%甲醇溶解,得每1 mL含原儿茶酸、对羟基苯甲酸和蔓荆子黄素分别为0.101 2 mg、0.252 2 mg、0.102 2 mg的混合对照品储备液。将混合对照品储备溶液分别进行2倍、5倍、10倍、25倍、50倍、100倍稀释,得系列浓度溶液,按“2.1.5”项下色谱条件测定峰面积,以溶液浓度为(μg/mL)横坐标、其峰面积(mAU)为纵坐标,得原儿茶酸、对羟基苯甲酸和蔓荆子黄素的线性回归方程分别为Y=37.208X-2.269 1(r2=0.999 9)、Y=60.517X-6.483 0(r2=0.999 9)和Y=30.455X-1.644 8(r2=0.999 9)。表明原儿茶酸、对羟基苯甲酸和蔓荆子黄素分别在1.012~50.60 μg/mL、2.522~126.1 μg/mL和1.022~51.09 μg/mL范围内线性关系良好。
2.1.8 精密度考察取混合对照品溶液①,按“2.1.5”项下色谱条件,连续进样6次,计算对羟基苯甲酸、原儿茶酸和蔓荆子黄素峰面积的RSD分别为0.25%、0.27%和0.23%,表明仪器精密度良好。
2.1.9 稳定性考察精密吸取S8的供试品溶液10 μL,分别在0、2、4、6、8、10、12、24、48和72 h进样,进样室温度与室温一致,测定对羟基苯甲酸、原儿茶酸和蔓荆子黄素的峰面积,计算对羟基苯甲酸、原儿茶酸和蔓荆子黄素峰面积的RSD分别为0.22%、0.28%和0.39%,表明供试品溶液在室温条件下72 h内稳定。
2.1.10 重复性考察精密称取S8的蔓荆子配方颗粒粉末6份,按“2.1.4”项下制备供试品溶液,按“2.1.5”项下色谱条件测定。结果蔓荆子配方颗粒中原儿茶酸、对羟基苯甲酸和蔓荆子黄素的平均含量分别为0.102 5%、0.390 1%和0.070 38%,RSD分别为0.64%、0.63%和0.72%,表明方法重复性良好。
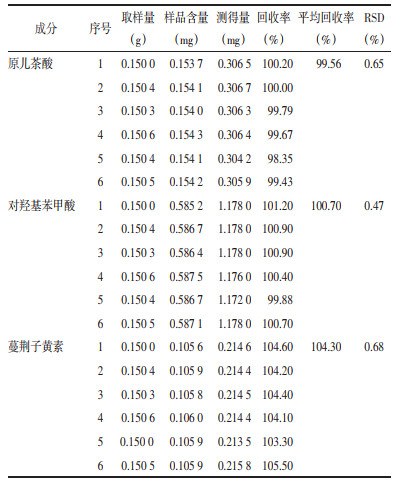
2.1.11 加样回收率考察精密称取S8的蔓荆子配方颗粒粉末0.15 g,按“2.1.4”项下方法制备供试品溶液,分别精密加入混合对照品溶液②5 mL,平行制备6份,按“2.1.5”项下色谱条件测定。计算原儿茶酸、对羟基苯甲酸和蔓荆子黄素的回收率分别为99.56%、100.7%和104.3%,RSD分别为0.65%、0.47%和0.68%,结果表明方法准确度良好。见表 2。
|
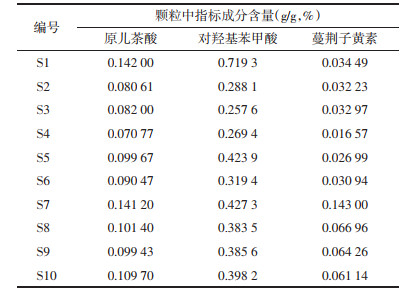
取S1~S10的蔓荆子配方颗粒,按“2.1.4”项下方法制备供试品溶液,按“2.1.5”项下色谱条件进行测定,计算10批蔓荆子配方颗粒中对羟基苯甲酸、原儿茶酸和蔓荆子黄素的含量。各批次蔓荆子配方颗粒中的原儿茶酸含量范围在0.070 77%~0.142 0%之间、对羟基苯甲酸含量在0.257 6%~0.719 3%之间、蔓荆子黄素含量在0.016 57%~0.143 0%之间。10批蔓荆子颗粒中的原儿茶酸含量相差2.0倍,对羟基苯甲酸含量相差2.8倍,蔓荆子黄素含量相差8.6倍,说明不同产地批次的蔓荆子所制备的配方颗粒有效成分含量差异大。见表 3。
|
其中江西产地的蔓荆子所制备的蔓荆子配方颗粒(S7~S10)3种主要活性成分含量均较高,明显优于原药材为安徽的配方颗粒(S1~S3)和原药材为广西的配方颗粒(S4~S6)。根据《中国药典》2015版对蔓荆子药材进行质量检查,其中江西产地的蔓荆子药材质量优于安徽和广西等地药材,结果如表 1所示。药材质量检查结果与颗粒剂含量测定结果一致,表明使用江西产地的优质药材所制备的配方颗粒质量也较优。
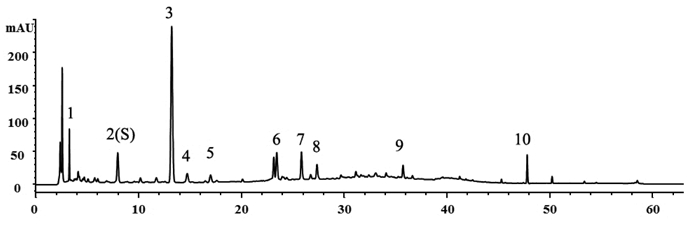
2.2 蔓荆子配方颗粒指纹图谱的建立与测定 2.2.1 指纹图谱的建立取S8蔓荆子配方颗粒,按照“2.1.4”项下方法制作供试品溶液,按“2.1.5”项下色谱条件进行测定,记录色谱图,确定了其中10个峰面积较大的特征峰,其中峰2、峰3、峰10分别是原儿茶酸、对羟基苯甲酸、蔓荆子黄素。见图 2。
|
| 峰2.原儿茶酸;峰3.对羟基苯甲酸;峰10.蔓荆子黄素 图 2 蔓荆子配方颗粒的指纹图谱 Fig. 2 Fingerprint chromatogram of Viticis Fructus formula granules |
原儿茶酸是蔓荆子药材及其配方颗粒中的主要有效成分之一,各个批次的蔓荆子药材所制备的蔓荆子配方颗粒中均含有此峰,峰面积占总峰面积适宜,无其他干扰峰,因此确定原儿茶酸作为指纹图谱参照峰。
2.2.2 专属性考察取混合对照品溶液①和S8蔓荆子配方颗粒制备的供试品溶液,按“2.1.5”项下色谱条件分析。混合对照品溶液、供试品溶液在相同的保留时间都有色谱峰,并无溶剂峰干扰,专属性良好,如图 1所示。
2.2.3 精密度考察取S8蔓荆子配方颗粒制备的供试品溶液,按“2.1.5”项下色谱条件分析,连续进样6次,得指纹图谱。计算得供试品溶液中各共有峰相对保留时间的RSD在0.078%~0.14%之间,相对峰面积的RSD在0.15%~1.1%之间,表明仪器精密度良好。
2.2.4 稳定性考察取S8蔓荆子配方颗粒制备的供试品溶液,按“2.1.5”项下色谱条件分析,分别在0、2、4、6、8、10、12、24、48、72 h进样,进样室温度与室温一致,测得指纹图谱,计算得供试品溶液中各共有峰相对保留时间的RSD在0.14%~1.1%之间,相对峰面积的RSD在0.53%~5.8%之间,表明样品溶液在室温条件下72 h内稳定。
2.2.5 重复性考察取S8蔓荆子配方颗粒按“2.1.4”项下方法平行制备6份供试品溶液,按“2.1.5”项下色谱条件分析,计算得供试品溶液中各共有峰相对保留时间的RSD在0.032%~0.13%之间,相对峰面积的RSD在0.21%~0.75%之间,表明方法重复性良好。
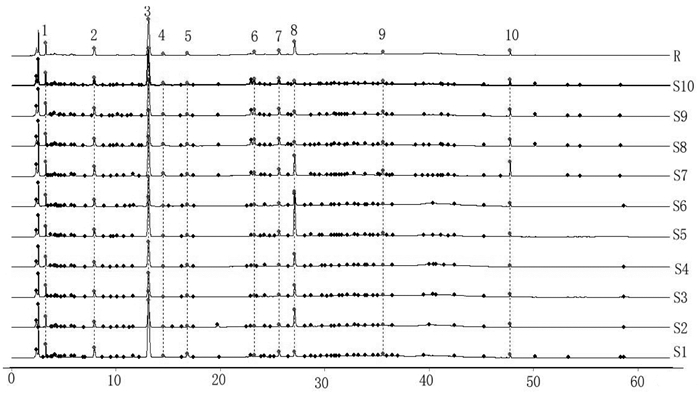
2.2.6 指纹图谱相似度评价取S1~S10的蔓荆子配方颗粒,按“2.1.4”项下方法制备供试品溶液,按“2.1.5”项下色谱条件进行测定,将色谱数据导入“中药色谱指纹图谱相似度评价系统(2012版)”,建立10批蔓荆子配方颗粒(S1~S10)的指纹图谱叠加图,见图 3。得到蔓荆子配方颗粒对照指纹图谱(R),每批样品与R比较,计算10批颗粒剂指纹图谱相似度,S1~S10样品相似度结果分别是0.975,0.984,0.993,0.992,0.914,0.996,0.992,0.976,0.976,0.978。10批蔓荆子配方颗粒的指纹图谱相似度差异不大,表明其化学成分含量总体稳定。
|
| 图 3 蔓荆子配方颗粒的指纹图谱叠加图和对照指纹图谱R Fig. 3 Fingerprints overlay and contrast fingerprint R of Viticis Fructus formula granules |
主成分分析是考察多个变量间相关性的一种多元降维统计方法,通过研究少数几个主成分来揭示多个变量间的内部结构,描述最大的变异量,能够有效研究样本组分上的差别[31]。中药指纹图谱可较全面地表征中药中的多种化学成分,指纹图谱结合主成分分析可评价药物之间的相似性和差异性,是适合中药特点的质量控制方法[32-35]。
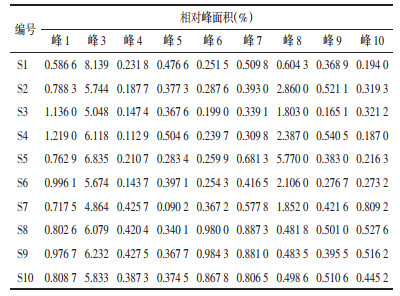
主成分分析方法对蔓荆子配方颗粒指纹图谱中的10个特征峰进行分析,特征峰信息见图 3,以2号峰(原儿茶酸)为参照峰,得到各特征峰的相对峰面积,见表 4。采用SIMCA 14.0软件,以各特征峰的相对峰面积为变量,对10批蔓荆子配方颗粒的指纹图谱特征峰进行主成分分析。选取3个主成分建立分析模型,结果累计贡献率达82.4%,能代表特征峰的信息。分别利用3个主成分(PC1,PC2,PC3)进行区分,将变量投影在二维空间上,拟合分析生成10批蔓荆子配方颗粒的主成分分析得分图和载荷图,分别用来观察蔓荆子配方颗粒所用药材的产区分布状况和分析各个特征峰对产地区分所起的贡献作用。
|
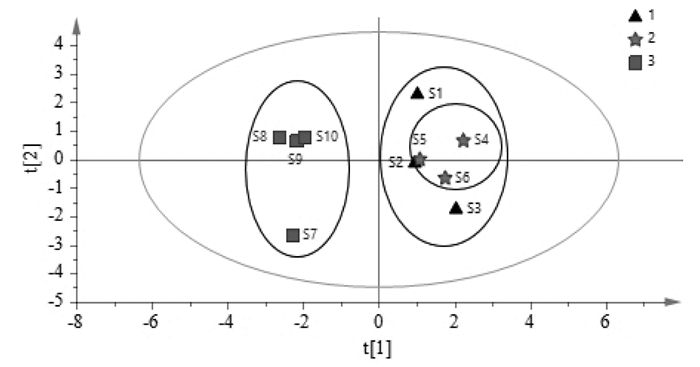
主成分分析的得分图见图 4,根据相似相聚原理,明显分为2类,江西产地蔓荆子的配方颗粒(S7~S10)样品聚为一类,安徽和广西产地蔓荆子的配方颗粒(S1~S6)聚为一类。广西产地蔓荆子的配方颗粒(S4~S6)分散比较集中,安徽产地蔓荆子的配方颗粒(S1~S3)同产区的差异相对较大。根据10批蔓荆子颗粒剂含量测定结果可知,江西的蔓荆子药材质量较优,用该产地蔓荆子药材制备配方颗粒,测得颗粒中3种活性成分含量均较高,指纹图谱相似度较高,主成分分析方法通过对指纹图谱特征峰进行分析,将江西产地的蔓荆子制备的颗粒剂聚在一起,表明江西产地蔓荆子的颗粒剂化学成分含量稳定,质量均一性良好,故可判断出江西产地蔓荆子药材制备的配方颗粒较其安徽和广西产地的优质。
|
| 图 4 10批蔓荆子配方颗粒HPLC特征峰主成分分析得分图 Fig. 4 Score plot of HPLC characteristic peaks of 10 batches of Viticis Fructus formula granules |
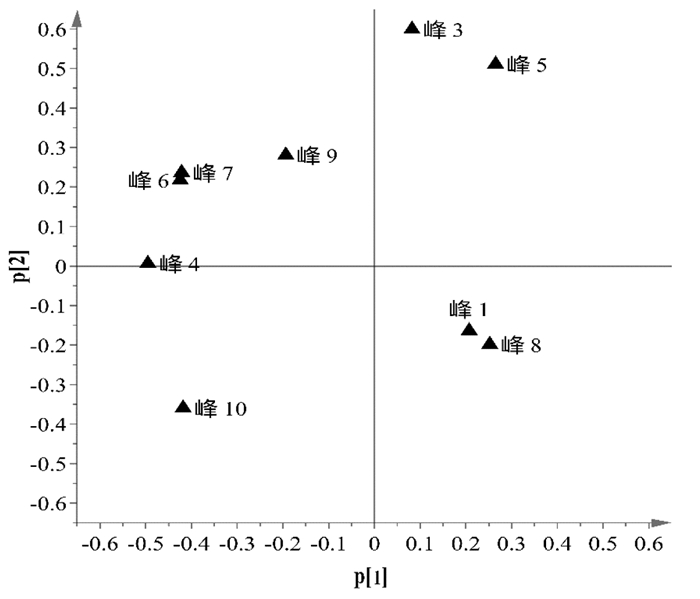
主成分分析载荷图见图 5,距离载荷图原点越远的变量,其绝对值越大,对分类模型总体方差贡献程度越高,代表该特征峰对产地分布所起的作用越大。由图可知,所选的特征峰峰均对分类模型有较高的贡献度,贡献度最大的3个峰分别为峰3(对羟基苯甲酸)、峰5、峰10(蔓荆子黄素),鉴于峰5化合物成分尚不明确,且在蔓荆子药材及配方颗粒中含量相对较低,难以准确定性定量,而峰3、峰10为蔓荆子药材及配方颗粒的主要活性成分,含量较高,对分类模型贡献度最大。本研究选择的10个共有峰具有明显的特征性,可作为该模型的特征变量。
|
| 图 5 10批蔓荆子配方颗粒HPLC特征峰主成分分析载荷图 Fig. 5 Loading plot of HPLC characteristic peaks of 10 batches of Viticis Fructus formula granules |
通过3D全波长(190~400 nm)扫描,得原儿茶酸、对羟基苯甲酸和蔓荆子黄素最大吸收波长分别为260 nm、254 nm和258 nm,故采用程序性波长对含量测定和指纹图谱进行准确、便捷、高效的研究。
蔓荆子配方颗粒既保留了原药材的功用,又能安全、有效、便捷、质量可控地应用于临床。根据蔓荆子炮制的文献考证,蔓荆子在唐代及以前以生用破碎为主,宋代以后又增加炒制、酒浸的炮制方法[36],如今蔓荆子的生品和微炒后的炮制品应用较多,炒制虽会提高蔓荆子总黄酮含量[7, 37],但其镇痛效果明显下降[38]。本实验以水为提取溶剂,采用粉碎蔓荆子药材的方式来提高其有效成分的提取效率。
鉴于中药汤剂中含有较多的糖类和鞣质成分,湿法制粒难度大,为防止颗粒剂花粒现象,故采用内加辅料法喷雾干燥、干法制粒。甘露醇、蔗糖、乳糖、糊精和淀粉均是常用的稀释剂,乳糖易溶于水,化学性质稳定,无吸湿性,但乳糖含糖量较高,不适合高血压、龋齿等患者的长时间服用。甘露醇溶解效果好,内加辅料得率低,损失大,成型率、外观效果均较差。淀粉的溶解效果较差,影响颗粒的溶解度,而糊精的溶解性比淀粉好,综合考虑,最终确定糊精作为制备蔓荆子配方颗粒的辅料。
原儿茶酸、对羟基苯甲酸和蔓荆子黄素作为蔓荆子配方颗粒的主要活性成分,定量分析这3种主要活性成分是保证蔓荆子配方颗粒安全、有效应用的前提。根据颗粒剂中单个化学成分的高低来难以判断药物质量,指纹图谱能较全面的反映蔓荆子配方颗粒的化学成分及其相对比例,鉴于个体样本本身的差异,可通过选择图谱中特征峰对其进行整体性评价。鉴于中药材的产地对药物的质量和疗效有影响[39-40],本文以不同产地蔓荆子药材制备的配方颗粒为例,基于HPLC-UV法的含量测定结合指纹图谱分析与主成分分析的评价方法,在一定程度上表征了10批蔓荆子配方颗粒在化学成分方面的共性与差异,可区分出由江西产地的蔓荆子所制备的配方颗粒质量最佳,均一性良好,基于三者的综合信息,可以为蔓荆子配方颗粒甄选原药材、质量控制和评价提供相应的依据。
| [1] |
国家药典委员会.中华人民共和国药典: 2015版(一部)[S].北京: 中国医药科技出版社, 2015: 363.
|
| [2] |
曹元宇. 神农本草经[M]. 山海: 上海科学出版社, 1987: 220.
|
| [3] |
蔡凡, 严启新. 蔓荆子黄酮类化学成分的研究[J]. 广东药科大学学报, 2017, 33(3): 314-316. |
| [4] |
周玲利, 曹晓诚, 袁庆, 等. 蔓荆子总黄酮阻断FoxM1-MMP2信号轴抑制SMMC-7721源性肝癌干样细胞迁移和侵袭[J]. 湖南师范大学学报(医学版), 2018, 15(2): 6-9. DOI:10.3969/j.issn.1673-016X.2018.02.002 |
| [5] |
苑青青.结构多样的二萜类成分的发现及活性研究[D].上海: 中国科学院大学(中国科学院上海药物研究所), 2017. http://cdmd.cnki.com.cn/Article/CDMD-80123-1017820641.htm
|
| [6] |
陈怀远, 涂林锋, 肖春荣, 等. 单叶蔓荆子的化学成分研究[J]. 中国中药杂志, 2018, 43(18): 3694-3700. |
| [7] | |
| [8] |
李雅, 李风光. 蔓荆子化学成分研究新进展[J]. 广东化工, 2016, 43(17): 82-86. DOI:10.3969/j.issn.1007-1865.2016.17.038 |
| [9] |
赵利新.单叶蔓荆叶化学成分及蔓荆子的质量控制研究[D].济南: 山东中医药大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10441-1014116184.htm
|
| [10] |
官扬, 胡慧明, 潘婷, 等. 蔓荆子的药理作用及其临床应用研究进展[J]. 江西中医药, 2013, 44(4): 72-73. DOI:10.3969/j.issn.0411-9584.2013.04.034 |
| [11] |
田华, 杜婷, 黄开合, 等. 蔓荆子的药理作用研究进展[J]. 中国医药导报, 2013, 10(9): 29-30. DOI:10.3969/j.issn.1673-7210.2013.09.012 |
| [12] |
盛习锋, 陈蓉. 蔓荆子化学成分及药理活性的研究进展[J]. 湖南中医杂志, 2007, 23(3): 107-108. DOI:10.3969/j.issn.1003-7705.2007.03.064 |
| [13] |
房士明, 樊官伟, 姚进龙, 等. 蔓荆的化学成分及药理活性研究进展[J]. 中草药, 2015, 46(24): 3757-3765. DOI:10.7501/j.issn.0253-2670.2015.24.025 |
| [14] |
饶春晖, 陆淼炯, 杨燕. 原儿茶酸对金黄色葡萄球菌性肺炎模型小鼠的保护作用及相关机制研究[J]. 浙江中西医结合杂志, 2018, 28(11): 911-915, 987-988. DOI:10.3969/j.issn.1005-4561.2018.11.005 |
| [15] |
张宏宁, 安春娜, 徐曼, 等. 原儿茶酸抗PC12细胞氧化损伤作用[J]. 中国新药杂志, 2014, 23(3): 347-350. |
| [16] |
陈益耀, 陈轶, 何周桃, 等. 原儿茶酸、白杨素对非酒精性脂肪肝细胞模型的抗氧化作用[J]. 中西医结合肝病杂志, 2018, 28(5): 294-296, 322. |
| [17] |
Khan AK, Rashid R, Fatima N, et al. Pharmacological activities of protocatechuic acid[J]. Acta Pol Pharm, 2015, 72(25): 643-650. |
| [18] |
王晗.原儿茶酸对脂肪干细胞体外增殖和迁移的影响[D].大连: 大连理工大学, 2008. http://cdmd.cnki.com.cn/article/cdmd-10141-2009040448.htm
|
| [19] |
张佩玲.原儿茶酸抑制Aβ诱导的PC12细胞的毒性作用及机制研究[D].广州: 广州中医药大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10572-1016208182.htm
|
| [20] |
Aimee NW, Matthew CB, Noelle Punessen, et al. Comparison of the neuroprotective and anti-inflammatory effects of the anthocyanin metabolites, protocatechuic acid and 4-Hydroxybenzoic acid[J]. Oxidative Medicine and Cellular Longevity, 2017(2017): 1-13. |
| [21] |
Ma JM, Yin GH, Lu ZB, et al. Casticin prevents DSS induced ulcerative colitis in mice through inhibitions of NF-κB pathway and ROS signaling[J]. Phytotherapy Research:PTR, 2018, 32(9): 1770-1783. DOI:10.1002/ptr.6108 |
| [22] |
Dai Y, Cheng RD, Gao J, et al. Casticin inhibits PDGF-induced proliferation and migration of airway smooth muscle cells[J]. European Journal of Pharmacology, 2018(830): 39-46. |
| [23] |
Wang JS. Casticin alleviates lipopolysaccharide-induced inflammatory responses and expression of mucus and extracellular matrix in human airway epithelial cells through Nrf2/Keap1 and NF-κB pathways[J]. Phytotherapy Research:PTR, 2018, 32(7): 1346-1353. DOI:10.1002/ptr.6067 |
| [24] |
Chan WC, Wong SK, Chan HT. Casticin from Vitex species:a short review on its anticancer and anti-inflammatory properties[J]. Journal of Integrative Medicine, 2018, 16(3): 147-152. DOI:10.1016/j.joim.2018.03.001 |
| [25] |
Junko K, Fumiko S, Masataka M, et al. G2-M arrest and antimitotic activity mediated by casticin, a flavonoid isolated from Viticis Fructus(Vitex rotundifolia Linne fil.)[J]. Cancer Letters, 2004, 208(1): 59-64. DOI:10.1016/j.canlet.2004.01.012 |
| [26] |
Zhang J, Cui YH, Sun SW, et al. Casticin inhibits the epithelial-mesenchymal transition in ovarian carcinoma via the hedgehog signaling pathway[J]. Oncology Letters, 2018, 15(4): 4495-4502. |
| [27] |
Gong Q, Cao XZ, Cao JG, et al. Casticin suppresses the carcinogenesis of small cell lung cancer H446 cells through activation of AMPK/FoxO3a signaling[J]. Oncology Reports, 2018, 40(3): 1401-1410. |
| [28] |
许刚, 张云锋, 孟磊, 等. 蔓荆子黄素抑制p53突变型人肺癌细胞生长及其机制研究[J]. 西北药学杂志, 2016, 31(2): 161-164. DOI:10.3969/j.issn.1004-2407.2016.02.015 |
| [29] |
孟繁敏.蔓荆子黄素诱导人前列腺癌PC-3细胞的凋亡和对G2/M期阻滞作用[D].沈阳: 辽宁师范大学, 2013. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y2377106
|
| [30] |
杨远超.蔓荆子黄素对单核巨噬细胞增殖和凋亡影响的研究[D].北京: 北京中医药大学, 2018. http://cdmd.cnki.com.cn/Article/CDMD-10026-1018192320.htm
|
| [31] |
张小确, 高枝荣, 夏云贵. 主成分分析方法及其在各仪器分析中的应用[J]. 河北工业科技, 2007, 24(6): 345-350, 354. DOI:10.3969/j.issn.1008-1534.2007.06.009 |
| [32] |
袁亚洲.指纹图谱结合化学计量学在中药质量控制中的研究[D].南昌: 南昌大学, 2009. http://cdmd.cnki.com.cn/Article/CDMD-11902-2009241879.htm
|
| [33] |
王元清, 韩彬, 向荣, 等. 总量统计矩结合聚类分析与主成分分析评价虎杖饮片一致性与差异性[J]. 中草药, 2015, 46(19): 2863-2869. DOI:10.7501/j.issn.0253-2670.2015.19.008 |
| [34] |
吴玲芳, 林琛, 袁永兵, 等. 叶下珠指纹图谱及模式识别研究[J]. 中草药, 2015, 46(4): 572-575. |
| [35] |
邹妍, 鄢海燕. 基于PCA及PLS-DA算法分析决明子炒制前后化学成分的变化[J]. 中国医院药学杂志, 2018, 38(19): 2027-2030. |
| [36] |
王作承, 常瑞莲, 张桂菊. 蔓荆子及其炮制品炮制沿革及现代研究[J]. 药学研究, 2018, 37(11): 673-675. |
| [37] |
王婷, 唐力英, 郭日新, 等. 炮制对蔓荆子中主要黄酮成分水溶出率的影响[J]. 中国药物警戒, 2017, 14(4): 215-217, 241. DOI:10.3969/j.issn.1672-8629.2017.04.007 |
| [38] |
龚拥军, 王新军. 蔓荆子镇痛作用的炮制方法探讨[J]. 中国现代药物应用, 2012, 6(4): 134-135. DOI:10.3969/j.issn.1673-9523.2012.04.120 |
| [39] |
赵凯, 周莲. 不同产地杜仲叶药效成分的分类与评估[J]. 兰州文理学院学报(自然科学版), 2018, 32(5): 64-67. |
| [40] |
朱启亮, 黄玉梅, 高明, 等. 不同产地、部位和采收期益母草中药效成分研究[J]. 中药材, 2017, 40(12): 2828-2831. |
2. Tianjin State Key Laboratory of Modern Chinese Medicine-Province and Ministry Co-Established State Key Laboratory Cultivation Base, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
 2019, Vol. 36
2019, Vol. 36