文章信息
- 余洪刚, 付大海, 杨利生, 宋超, 唐俊峰, 秦晓娟
- YU Honggang, FU Dahai, YANG Lisheng, SONG Chao, TANG Junfeng, QIN Xiaojuan
- 复明汤调控TGF-β1/Smad3通路抑制肺成纤维细胞活化及肺上皮损伤减轻博来霉素诱导的肺纤维化
- Fuming decoction inhibits the activation of lung fibroblast and lung epithelial injury to alleviate bleomycin-induced pulmonary fibrosis through regulating TGF-β1/Smad3 pathway
- 天津中医药, 2020, 37(12): 1412-1419
- Tianjin Journal of Traditional Chinese Medicine, 2020, 37(12): 1412-1419
- http://dx.doi.org/10.11656/j.issn.1672-1519.2020.12.20
-
文章历史
- 收稿日期: 2020-07-13
2. 陕西中医药大学中药药理学研究室, 咸阳 712000;
3. 汉中市人民医院呼吸内科, 汉中 723000
特发性肺纤维化(IPF)是一种上皮纤维母细胞性疾病,是由于肺泡上皮细胞受到多种微小损伤并随后诱导过度的成纤维细胞活性所致[1-2]。肺上皮损伤后,重要的纤维变性介质如转化生长因子β1(TGF-β1)由上皮细胞、成纤维细胞和其他细胞类型释放[3],在博来霉素损伤的小鼠和IPF患者的肺组织中均显著上调[4-6]。研究前期临床实践发现复明汤(FMT)治疗肺纤维化疗效确切,其出自《医林改错》,重用补气药与少量活血药相伍,佐以通络平喘,补气而不壅滞,活血亦不伤正,合而用之,诸症向愈,临床治疗肺纤维化疗效确切,然而其作用机制不明限制其临床应用。本研究拟阐明FMT在体外对TGF-β1信号转导、TGF-β1诱导的肺成纤维细胞活化和上皮损伤的影响,并进一步验证FMT在博莱霉素损伤的小鼠体内在肺纤维化中的潜在作用。
1 材料和方法 1.1 复明汤制备枸杞子、女贞子、丹参、当归、决明子各15 g,菟丝子、牡丹皮、茯苓、白术、菊花、木贼、石菖蒲各10 g,黄芪12 g,三七6 g,甘草6 g,加入10倍量蒸馏水浸泡30 min后煎煮2次,每次90 min,合并后,以旋转蒸发仪将其浓缩,使生药浓度分别为1、2、3、4和5 g/mL的FMT。
1.2 细胞系和小鼠小鼠胚胎成纤维细胞NIH-3T3,小鼠肺成纤维细胞MLg和人肺泡上皮细胞(AEC)A549系从ATCC获得。用CAGA荧光素酶报告基因转染NIH-3T3细胞,以生成CAGA-NIH-3T3报告细胞。在37 ℃的恒温箱中,在含10 %胎牛血清(FBS)和抗生素(100 U/mL青霉素和100 μg/mL链霉素)的Dulbecco改良Eagle培养基(DMEM)中常规培养细胞。8周龄的雄性C57BL/6 J小鼠购自上海斯莱克实验动物有限公司。将所有小鼠饲养于无病原体设施中。所有手术均在7.5 %水合氯醛麻醉下进行。
1.3 博来霉素的给药和实验设计小鼠肺纤维化模型参照文献建立[7]。简而言之,小鼠以10%乌拉坦腹腔麻醉后,向小鼠气管内注射溶解在生理盐水(0.9 % NaCl)中的单剂量博来霉素(2.5或5 U/kg),注射后迅速将小鼠直立并旋转,使药液在肺中均匀分布,待动物自然清醒后,随机分为两组,对照组和FMT组。FMT组小鼠经灌胃给予2 mL 5 g/mL的FMT,而对照组小鼠则给予等体积的蒸馏水。在博来霉素处理后的指定时间,处死小鼠用于随后的实验。
1.4 荧光素酶测定CAGA-NIH-3T3细胞接种在96孔板中,达到80%融合后,血清饥饿24 h。此后,在含0.1% FBS的DMEM中用不同生药浓度的FMT处理细胞1 h,并用5 ng/mL TGF-β1处理细胞24 h。在处理结束时,将细胞裂解并在双荧光素酶报告基因测定(Promega)中测定。反应的最初20 s期间的总发光在照度光度计中测量。
1.5 细胞活力分析将MLg细胞接种在96孔板中,并用不同生药浓度的FMT预处理1 h,然后在有或无TGF-β1(10 ng/mL)的条件下共培养,使用3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化物(MTT)细胞增殖和细胞毒性测定试剂盒确定细胞活力。
1.6 RNA提取和定量实时聚合酶链反应使用TRIzol试剂从细胞中提取总RNA。使用随机寡核苷酸引物和M-MLV逆转录酶合成第一链互补DNA(cDNA)。qRT-PCR以20 μL的体积进行,其中包含5 pmol引物,10 ng cDNA和SYBR Green PCR主混合物。使用2-ΔΔCt方法相对于β-actin确定基因表达。靶基因及其引物序列如下。Acta2:5’-GCTGGTGATGATGCTCCCA-3’和5’-GCCCATTCCAACCATTACTCC-3’;Col1a1:5’-CCAAGAAGACATCCCTGAAGTCA-3’和5’-TGCACGTCATCGCACACACA-3’;Fn1:5’-GTGTAGCACAACTTCCAATTACG- AA-3’和5’-GGAATTTCCGCCTCGAGTCT-3’;Actb(细胞):5’-AGGCCAACCGTGAAAAGATG-3’和5’-AGAGCATAGCCCTCGTAGATGG-3’;CDH1:5’-CGAGAGCTACACGTTCACGG-3’和5’-TGCA- CGTCATCGCACACA-3’;CDH2:5’-TCAGGCGTC- TGTAGAGGCTT-3’和5’-ATGCACATCCTTCGAT- AAGACTG-3’;SNAI1:5’-TCGGAAGCCTAACTA- CAGCGA-3’和5’-AGATGAGCATTGGCAGCGAG-3’;ACTB(动物):5’-CATGTACGTTGCTATCCAG- GC-3’和5’-CTCCTTAATGTCACGCACGAT-3’。
1.7 蛋白印迹(Western blot)法从细胞和培养上清液中提取蛋白质,收集培养基并在4 ℃下以14 000×g离心3 min以去收集细胞,使用RIPA裂解液从培养基中获得总蛋白,并使用BCA法测定蛋白质浓度。通过SDS-PAGE分离等量的蛋白质,并将其转到PVDF膜上。将膜在室温下用5%脱脂奶封闭1 h,并在4 ℃下与一抗孵育过夜。磷酸化(p)-Smad2(3108),Smad2(3122),p-Smad3(9520),Smad3(9513),ERK(4370S),ERK(4695),p-p38(4631S),p38(9212),p-c-Jun N-terminal kinase(JNK;9251S),JNK(9252),E-cadherin(3195),N-cadherin(13116)和SNAIL(3879)购自Cell Signaling Technology。Type 1 collagen(ab21286)和fibronectin(ab2413)抗体购自Abcam。GAPDH(UM4002)和β-tubulin(UM4003)抗体购自Utibody Biotechnology。α-SMA(sc-32251)抗体购自Santa Cruz Biotechnology,β-actin(AC026)抗体购自ABclonal Technology。随后,将膜与HRP偶联的二抗在室温下孵育2 h,并使用增强型化学发光试剂盒(Pierce)检测蛋白质信号。
1.8 细胞迁移实验通过划痕修复实验评估迁移。MLg细胞是接种在6孔板中并培养24 h。用无菌微量移液器吸头刮擦细胞单层后,在存在和不存在TGF-β1(10 ng/mL)的情况下,用FMT(5 g/mL)处理细胞36 h于显微镜下观察,使用Image J软件进行图像分析。
1.9 肺功能评估使用Anires2005系统对小鼠进行麻醉,气管切开,并用计算机控制的小动物呼吸机进行机械通气,以确定肺功能。该系统可以自动计算并显示肺参数,例如呼吸动态顺应性(Cdyn)、肺阻力(RL)和呼气阻力(RE)。
1.10 组织学检查左肺以0.4 mL 10 %福尔马林固定。将组织固定过夜,包埋在石蜡中,然后切片以用苏木精伊红(HE)或Masson 3色染色。使用ImagePro Plus 6.0软件(Media Cyber netics)分析数字图像,概述肺的总体和纤维化区域,并对每个肺的纤维化像素相对于总像素进行求和,以获得纤维化的百分比。
1.11 羟脯氨酸测定使用常规羟脯氨酸方法在右肺中清除血液中的胶原蛋白含量。将肺在120 ℃下干燥16 h时,将切碎于3 mL 6 N HCl中的肺组织在120 ℃下再孵育16 h。然后将样品冷却并通过5.0 μm注射过滤器过滤,然后用NaOH调节pH值至6.5~8.0。随后,加入磷酸缓冲盐溶液(PBS)至总体积为10 mL,并通过分光光度法测量吸光度,用氯胺-T进行羟脯氨酸测定。使用含有已知量的纯化胶原蛋白的样品确定胶原蛋白水解的完全性和羟脯氨酸的回收率。
1.12 支气管肺泡灌洗液收集和细胞计数将气管插管并在室温下用0.8 mL无菌PBS灌洗3次。将样品以300×g离心5 min,并收集无细胞的上清液。沉淀以PBS洗涤,然后悬浮在200 μL PBS中,用血细胞计数器和异细胞计数进行总细胞计数。对于不同的细胞计数,每个悬浮液的涂片均用HE染色,并根据标准形态学标准将500个细胞分类为巨噬细胞,嗜中性粒细胞或淋巴细胞。
1.13 酶联免疫吸附测定使用酶联免疫吸附测定(ELISA)试剂盒(BioLegend,USA),根据说明书测量BALF中白细胞介素(IL)-1β,干扰素-γ(IFN-γ)和肿瘤坏死因子-α(TNF-α)的水平。将BALF样品添加至包被有捕获抗体的测定板的孔中。过夜孵育后,将测定板洗涤3次,并加入检测抗体。在室温下孵育1 h并洗板3次后,将抗生蛋白链菌素-HRP加入孔中。用四甲基联苯胺底物显色,并在450、570 nm下测量吸光度。
1.14 统计学方法使用Prism 7.0进行统计分析,数据以均数±标准差(x±s)表示。采用Shapiro-Wilk法进行正态性检验,满足正态分布的数据,两组间比较采用两独立样本t检验,多组间比较采用单因素方差分析,组间两两比较采用LSD法;不满足正态分布的数据,两组间比较采用Mann-Whitney检验,多组间比较采用Kruskal-Wallis H检验,组间两两比较进行Dunn检验,使用对数秩检验比较生存曲线,P < 0.05为差异具有统计学意义。
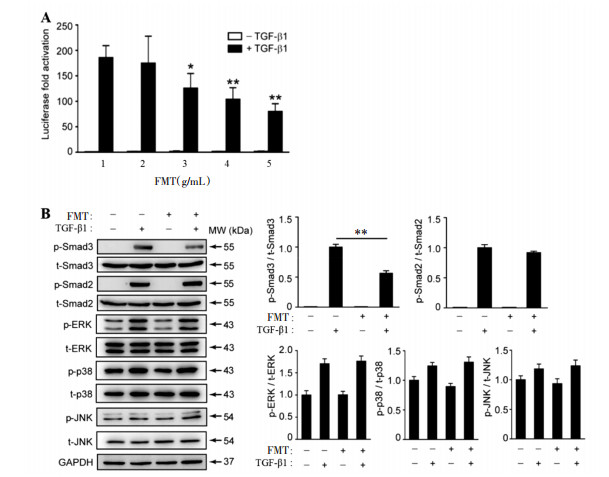
2 结果 2.1 FMT抑制TGF-β1激活的Smad3信号传导评估FMT对用(CAGA)12-荧光素酶报告基因转染的NIH-3T3细胞中TGF-β1信号通路的影响,其包含12个Smad结合位点。结果表明,该报告基因在TGF-β1处理后被激活,但被FMT以浓度依赖的方式抑制,表明FMT可通过拮抗TGF-β1信号通路发挥其潜在抗纤维化作用。见图 1A。
|
| 注:A.双荧光素酶基因检测FMT对TGF-β1信号通路的影响;B. FMT对小鼠肺成纤维细胞MLg细胞系中Smad2/3依赖途径和非Smad信号传导(如MAPK级联)的影响。*P < 0.05,**P < 0.01。 图 1 复明汤在体外抑制TGF-β1激活的Smad3信号传导 Fig. 1 Fuming decoction inhibits Smad3 signaling by TGF-β1 activation in vitro |
为进一步探索细胞内信号转导机制,研究了FMT对小鼠肺成纤维细胞MLg细胞系中Smad2/3依赖途径和非Smad信号传导(如MAPK级联)的影响。TGF-β1有效地增加了磷酸化的Smad2、ERK1/2、JNK和p38的水平,并可显著抑制TGF-β1诱导的Smad3磷酸化,同时对TGF-β1诱导的其他下游因子的磷酸化作用较小。结果表明,FMT主要通过抑制典型的TGF-β1- Smad2/3途径,特别是通过抑制Smad3活化来阻断TGF-β1信号传导。见图 1B。
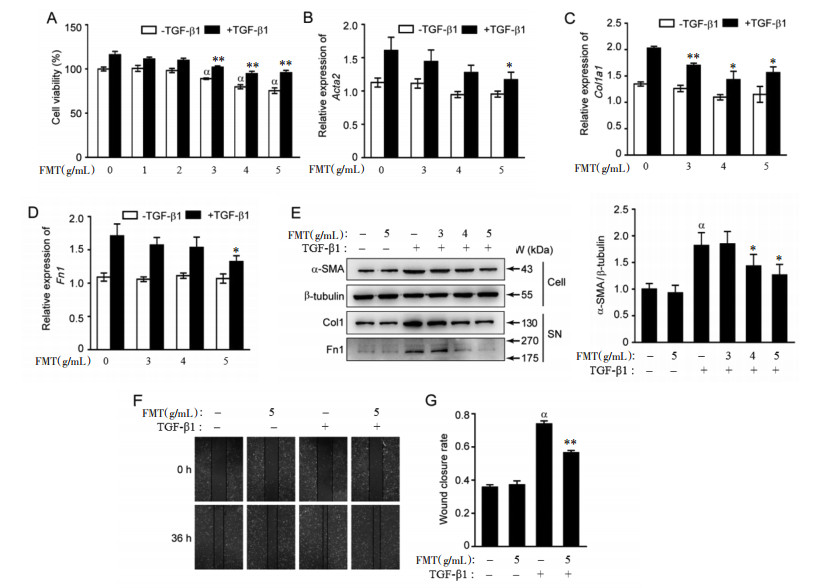
2.2 FMT减弱TGF-β1诱导的肺成纤维细胞活化成纤维细胞和成肌纤维细胞是主要的反射细胞,在组织损伤后和IPF患者中被激活,导致ECM产生增加和迁移潜力增强。为了检查FMT是否介导了与成纤维细胞活化有关的TGF-β1信号传导阻滞,建立经TGF-β1处理的成纤维细胞体外模型。FMT的生药浓度范围为1~5 g/mL,在生药浓度>2 g/mL时对MLg细胞的生存能力具有更大的影响,见图 2A。如图 2B和E所示,在TGF-β1处理后,α-SMA的mRNA和蛋白表达显著增加,但在FMT干预下显着降低,表明FMT抑制了TGF-β1诱导的成肌纤维细胞分化。TGF-β1增加了两种主要ECM成分的Ⅰ型胶原和纤连蛋白的mRNA和蛋白质水平,当用FMT治疗时,它们的表达显著降低,见图 2C、D、E。另外,图 2F和图 2G显示,FMT处理36 h后,TGF-β1刺激的成纤维细胞迁移速率降低,表明FMT抑制成纤维细胞迁移。
|
| 注:A.有无TGF-β1存在,FMT对细胞活力影响;qRT-PCR分析acta2(B)、Col1a1(C)和Fn1(D)的mRNA表达;E.α-SMA和β-tubulin蛋白表达水平;F、G划痕修复实验测定复明汤对成纤维细胞迁移的影响,36 h后确定划痕修复率,确定迁移率。*P < 0.05,**P < 0.01。 图 2 复明汤体外抑制TGF-β1诱导的成纤维细胞活化、ECM产生及成纤维细胞迁移 Fig. 2 Fuming decoction inhibits TGF-β1 induced fibroblast activation, ECM production, and fibroblast migration in vitro |
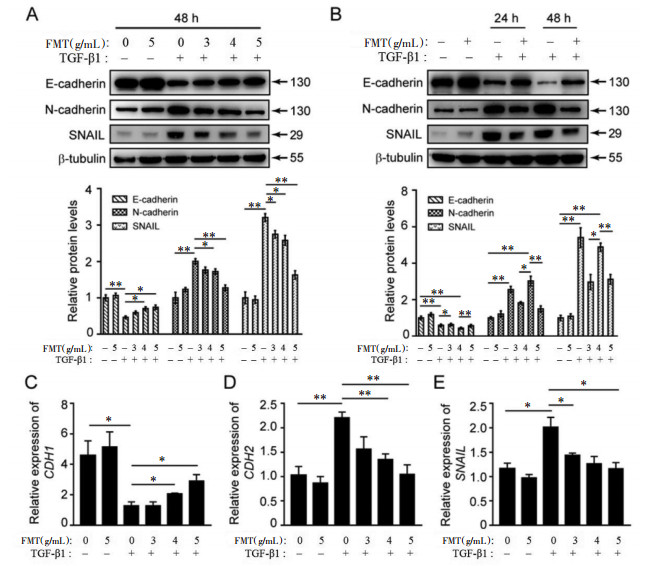
研究表明,肺泡上皮细胞(AEC)损伤可能是肺纤维化发病机制中的重要早期特征。受损的AECs被激活并可能经历许多细胞和分子变化,例如同时丢失上皮标记和获得间充质标记[8]。为了确定FMT对TGF-β1信号的阻断是否导致对上皮损伤的保护,向TGF-β1处理的A549细胞中添加了FMT。结果表明,TGF-β1诱导了上皮激活,表现为上皮标记物(E-cadherin)的表达减少、间充质标记物(N-cadherin)的表达增加及TGF-β的增加β1下游转录因子SNAIL。FMT干预以浓度和时间依赖性方式显著抑制了TGF-β1诱导的上皮损伤,见图 3A和B。实时荧光定量聚合酶链反应(qRT-PCR)分析进一步证明,TGF-β1在A549细胞中显着下调E-钙黏蛋白的mRNA表达,并上调N-钙黏蛋白和SNAIL的表达,见图 3C、D、E,表明FMT可保护肺泡上皮A549细胞免受TGF-β1诱导的损伤。
|
| 注:不同生药浓度(A)及不同作用时间(B)后,对E-adherin、N-cadherin及SNAIL等蛋白表达影响;qRT-PCT检测CDH1(C)、CDH2(D)及SNAI1(E)mRNA的相对表达量。*P < 0.05,**P < 0.01。 图 3 复明汤体外抑制TGF-β1诱导的上皮损伤 Fig. 3 Fuming decoction inhibits TGF-β1 induced epithelial damage in vitro |
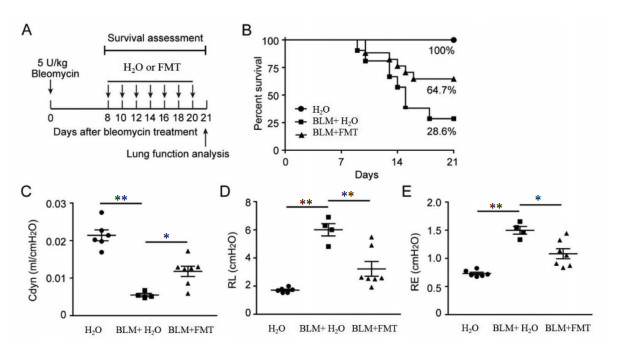
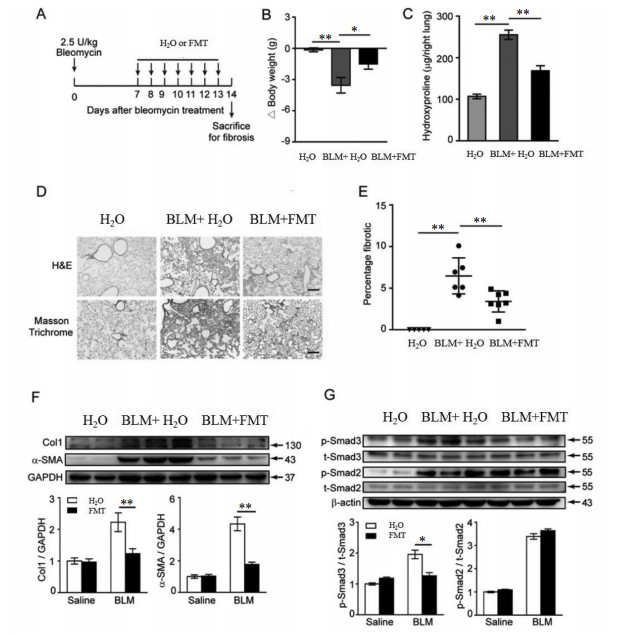
在体内进一步评估了FMT的抗纤维化作用。经气管内施用博来霉素诱导小鼠肺纤维化,发现经FMT治疗的小鼠对大剂量博来霉素(5 U/kg)诱导的肺损伤的敏感性显著降低,表现出更好的存活率,见图 4A和B。而且,经FMT处理的小鼠表现出肺功能的改善,如Cdyn升高和RL/RE值降低,见图 4C、D、E。与仅用博来霉素处理的小鼠(2.5 U/kg)相比,博来霉素处理后7 d经FMT治疗的小鼠可恢复纤维化诱导的体质量减轻和胶原蛋白减少确定,见图 5A、B、C、D。对肺纤维化切片的面积进行定量,说明了FMT治疗后肺纤维化减弱,见图 5E。Col1和α-SMA蛋白水平降低进一步支持FMT处理可减轻小鼠中肺纤维化,见图 5F。同时检查FMT对体内Smad2/3磷酸化水平的影响,发现FMT可显著降低由博来霉素诱导的磷酸化Smad3,证实其可通过抑制TGF-β1信号通路改善纤维化,见图 5G。
|
| 注:A.治疗剂量时间表;B. 21d后不同处理方法小鼠的生存率;肺功能参数,包括Cdyn(C)、RL(D)、RE(E)的变化。*P < 0.05,**P < 0.01。 图 4 FMT提高博来霉素损伤小鼠的存活率并改善其肺功能 Fig. 4 Fuming decoction improves the survival rate of bleomycin (BLM) injured mice and improves their lung function |
|
| 注:A.给药方案;B.小鼠体质量变化;C.肺组织中羟脯氨酸含量变化;D. HE染色结果;E.肺切片中纤维化区域的百分比;F.肺组织中Col1和α-SMA蛋白表达水平;G.肺组织中磷酸化Smad3和Smad2的表达。*P < 0.05,**P < 0.01。BLM:博来霉素。 图 5 FMT减弱博来霉素诱导的小鼠肺纤维化的产生 Fig. 5 Fuming decoction attenuates bleomycin (BLM) -induced lung fibrosis in mice |
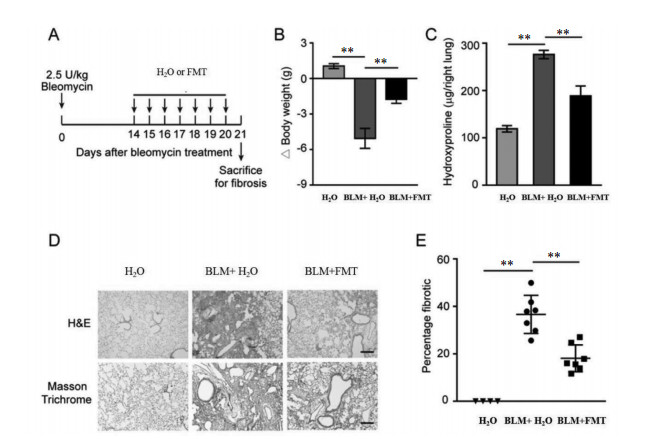
为了评估FMT是否可以逆转已经建立的纤维化,在博莱霉素处理后14 d给药FMT,1周后处死小鼠,并收集样品用于纤维化分析,见图 6A。结果表明FMT可显著减少肺纤维化,见图 6B、C、D、E。
|
| 注:A.给药方案;B.小鼠体质量变化;C.肺组织中羟脯氨酸含量变化;D. HE和Masson 3色染色的肺部代表性图像;E.肺切片中肺纤维化区域百分比。*P < 0.05,**P < 0.01。BLM:博来霉素。 图 6 FMT可减弱博来霉素诱导的已成型小鼠肺纤维化 Fig. 6 Fuming decoction can attenuate bleomycin (BLM)-induced formed pulmonary fibrosis in mice |
中药目前被认为是用于药物筛选和开发的宝贵资源,并且已经开发出旨在干扰TGF-β1信号通路的策略来治疗IPF。研究表明黄芩苷和大黄素可以减轻博来霉素诱导的肺纤维化[9-10],而丹酚酸B能够保护百草枯引起的肺损伤[11],其作用机制均与TGF-β1信号的失活有关。本研究从多方面证实FMT对进行性肺纤维化具有抗纤维化作用,FMT可拮抗TGF-β1信号转导,降低Smad3磷酸化水平,在体外抑制了TGF-β1诱导的上皮损伤、成肌纤维细胞活化、ECM产生、成纤维细胞迁移,并最终在体内证实上述活性。
TGF-β1通过刺激其下游介质Smad2/3发挥其在器官纤维化(包括肺纤维化)中的生物学活性[12],这两种Smad在ECM产生和组织纤维化中具有不同的作用[13-14]。本研究发现,在体外和体内模型中Smad3而非Smad2是FMT靶向的潜在细胞内传感器,与最近相关研究结果一致,Smad3为ECM产生和组织纤维化中TGF-β1信号传导的关键介质[15-16]。同时本研究发现FMT可通过对AEC损伤以及对成纤维细胞分化和活化的作用来减轻肺纤维化,其可显著逆转TGF-β1诱导的成肌纤维细胞分化,ECM产生和体外成纤维细胞迁移,从而抑制成纤维细胞的功能。这些作用可能是FMT抵抗博来霉素在体内的纤维化作用能力的基础,甚至可以减少博来霉素诱导已形成的纤维化。同时,当进行预防性应用时,FMT对博莱霉素诱导的小鼠肺纤维化没有保护作用。IPF一度被认为是一种非炎性疾病,因为肺纤维化不能对皮质类固醇激素疗法产生反应[17]。然而,最近对免疫细胞功能的研究导致重新评估了炎症细胞在肺纤维化发展中的作用。而FMT似乎并未影响博来霉素模型中炎性细胞的初始流入和细胞因子的产生,这提示FMT可以在不加剧炎症的剂量下减轻纤维化,从而避免了与全面抑制TGF-β1相关的潜在风险。
综上所述,本研究表明FMT可减轻博来霉素诱导的小鼠肺纤维化和功能障碍,其作用机制可能是通过调控TGF-β1/ Smad3信号通路,进而保护上皮损伤、抑制成肌纤维细胞分化、ECM沉积和成纤维细胞迁移。结合中药复方的低毒性及逆转肺纤维化的能力,FMT具有临床治疗进行性肺纤维化患者的潜力,本研究为FMT治疗肺纤维化的临床应用奠定理论基础。
| [1] |
RICHELDI L, COLLARD H R, JONES M G. Idiopathic pulmonary fibrosis[J]. The Lancet, 2017, 389(10082): 1941-1952. DOI:10.1016/S0140-6736(17)30866-8 |
| [2] |
LYNCH D A, S ERZELLATI N, TRAVIS W D, et al. Diagnostic criteria for idiopathic pulmonary fibrosis:a Fleischner Society White Paper[J]. The Lancet Respiratory Medicine, 2018, 6(2): 138-153. DOI:10.1016/S2213-2600(17)30433-2 |
| [3] |
HU H H, CHEN D Q, WANG Y N, et al. New insights into TGF-β/Smad signaling in tissue fibrosis[J]. Chemico-biological Interactions, 2018, 292: 76-83. DOI:10.1016/j.cbi.2018.07.008 |
| [4] |
SELMAN M, PARDO A, KAMINSKI N. Idiopathic pulmonary fibrosis:aberrant recapitulation of developmental programs[J]. PLoS Medicine, 2008, 5(3). |
| [5] |
GUO J, FANG Y, JIANG F, et al. Neohesperidin inhibits TGF-β1/Smad3 signaling and alleviates bleomycin-induced pulmonary fibrosis in mice[J]. European Journal of Pharmacology, 2019, 864: 172712. DOI:10.1016/j.ejphar.2019.172712 |
| [6] |
LI N, FENG F, WU K, et al. Inhibitory effects of astragaloside Ⅳ on silica-induced pulmonary fibrosis via inactivating TGF-β1/Smad3 signaling[J]. Biomedicine & Pharmacotherapy, 2019(119): 109387. |
| [7] |
QU Y, ZHANG L, KANG Z, et al. Ponatinib ameliorates pulmonary fibrosis by suppressing TGF-β1/Smad3 pathway[J]. Pulmonary Pharmacology & Therapeutics, 2015(34): 1-7. |
| [8] |
WOLTERS P J, COLLARD H R, JONES K D. Pathogenesis of idiopathic pulmonary fibrosis[J]. Annual Review of Pathology:Mechanisms of Disease, 2014(9): 157-179. |
| [9] |
HUANG X, HE Y, CHEN Y, et al. Baicalin attenuates bleomycin-induced pulmonary fibrosis via adenosine A2a receptor related TGF-β1-induced ERK1/2 signaling pathway[J]. BMC Pulmonary Medicine, 2016, 16(1): 132. DOI:10.1186/s12890-016-0294-1 |
| [10] |
GUAN R, WANG X, ZHAO X, et al. Emodin ameliorates bleomycin-induced pulmonary fibrosis in rats by suppressing epithelial-mesenchymal transition and fibroblast activation[J]. Scientific Reports, 2016(6): 35696. |
| [11] |
LIU B, CAO B, ZHANG D, et al. Salvianolic acid B protects against paraquat-induced pulmonary injury by mediating Nrf2/Nox4 redox balance and TGF-β1/Smad3 signaling[J]. Toxicology and Applied Pharmacology, 2016(309): 111-120. |
| [12] |
FLEMING N I, JORISSEN R N, MOURADOV D, et al. SMAD2, SMAD3 and SMAD4 mutations in colorectal cancer[J]. Cancer Research, 2013, 73(2): 725-735. DOI:10.1158/0008-5472.CAN-12-2706 |
| [13] |
MENG X M, HUANG X R, CHUNG A C K, et al. Smad2 protects against TGF-β/Smad3-mediated renal fibrosis[J]. Journal of the American Society of Nephrology, 2010, 21(9): 1477-1487. DOI:10.1681/ASN.2009121244 |
| [14] |
DUNCAN M R, FRAZIER N S, ABRAMSON S, et al. Connective tissue growth factor mediates transforming growth factor β-induced collagen synthesis:down-regulation by cAMP[J]. The FASEB Journal, 1999, 13(13): 1774-1786. DOI:10.1096/fasebj.13.13.1774 |
| [15] |
HU H H, CHEN D Q, WANG Y N, et al. New insights into TGF-β/Smad signaling in tissue fibrosis[J]. Chemico-biological Interactions, 2018(292): 76-83. |
| [16] |
KANG J H, JUNG M Y, YIN X, et al. Cell-penetrating peptides selectively targeting SMAD3 inhibit profibrotic TGF-β signaling[J]. The Journal of Clinical Investigation, 2017, 127(7): 2541-2554. DOI:10.1172/JCI88696 |
| [17] |
BYRNE A J, MAHER T M, LLOYD C M. Pulmonary macrophages:a new therapeutic pathway in fibrosing lung disease[J]. Trends in Molecular Medicine, 2016(22): 303-316. |
2. Department of Traditional Chinese Medicine Pharmacology, Shaanxi University of Chinese Medicine, Xianyang 712000, China;
3. Department of Respiratory Medicine, Hanzhong People's Hospital, Hanzhong 723000, China
 2020, Vol. 37
2020, Vol. 37