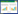文章信息
- 陆雪琴, 赵亮, 周洁, 段彦娟, 张春燕, 朱建勇, 翟晓翔
- LU Xueqin, ZHAO Liang, ZHOU Jie, DUAN Yanjuan, ZHANG Chunyan, ZHU Jianyong, ZHAI Xiaoxiang
- 多指标综合加权评分法优选复方夏枯草洗剂提取工艺研究
- Optimizing extraction process of Compound Xiakucao Lotion by comprehensive evaluation of multiple mark
- 天津中医药, 2020, 37(12): 1431-1435
- Tianjin Journal of Traditional Chinese Medicine, 2020, 37(12): 1431-1435
- http://dx.doi.org/10.11656/j.issn.1672-1519.2020.12.23
-
文章历史
- 收稿日期: 2020-07-14
2. 南京中医药大学, 南京 210023;
3. 上海中医药大学附属第七人民医院中心实验室, 上海 200137
复方夏枯草洗剂处方由夏枯草、丹参、威灵仙、木贼、板蓝根、大青叶、皂角刺、鸭跖草、薏苡仁、制香附共10味中药组成,为上海市第七人民医院皮肤科临床验方。该复方中药外用治疗寻常疣具有临床疗效好、对皮肤无刺激性的优点,可以极大提高患者、尤其儿童的顺应性,减轻痛苦,提高疗效。本研究旨在按照国家食品药品监督管理总局对医疗机构应用传统工艺配制中药制剂的要求,拟将复方夏枯草洗剂研制成院内制剂,使该制剂规范化应用于临床,保证药物的安全性、稳定性、有效性和可控性。本研究采用正交实验设计,以迷迭香酸、丹酚酸B的含量及出膏率为考察指标[1-2],对料液比、提取时间、提取次数等因素进行考察,优选复方夏枯草洗剂的最佳提取工艺,确保该药物的工艺稳定,质量可控[3-4]。
1 材料 1.1 仪器高效液相色谱仪(Agilent 1260),美国安捷伦公司;电子天平(CP225D),北京赛多利斯仪器系统有限公司;超声清洗仪(DL720-A),上海之信仪器有限公司;旋转蒸发仪(N-1300-WB),日本EYELA公司;电热恒温水浴锅(HWS28型),上海一恒科学实验有限公司;电热恒温干燥箱(DNG-9140A),上海精宏实验设备有限公司。
1.2 药物与试剂对照品迷迭香酸(批号:111871-201706)、丹酚酸B(批号:111562-201716),均购于中国食品药品检定研究院;甲醇为色谱纯试剂,美国Fisher公司;水为超纯水,其余试剂均为分析纯。夏枯草等10味药材均购自上海康桥药业有限公司,符合2015版《中华人民共和国药典》相关规定。
2 方法与结果 2.1 含量测定 2.1.1 色谱条件色谱柱为安捷伦ZORBAX Eclipse Plus C18(250 mm × 4.6 mm,5 μm);流动相:以0.1%磷酸溶液为流动相A,以甲醇为流动相B,洗脱程序见表 1;流速:1.0 mL/min;柱温:28.0 ℃;检测波长:286 nm;进样量:10 μL。
精密称取迷迭香酸、丹酚酸B对照品适量,加50%甲醇溶液溶解,配制成浓度分别为115 μg/mL,1 700 μg/mL混合对照品溶液,备用。
2.1.3 供试品溶液的制备称取1日处方量药材共155 g,加10倍量水,煎煮2次,每次1 h,合并滤液,减压浓缩至100 mL,精密吸取1 mL浓缩液,置5 mL的容量瓶中,加50%甲醇溶液定容至5 mL,即得。
2.1.4 阴性对照品溶液的制备称取除夏枯草、生丹参之外的药材,按照“2.1.3”项下方法,制备缺夏枯草、生丹参的阴性对照溶液。
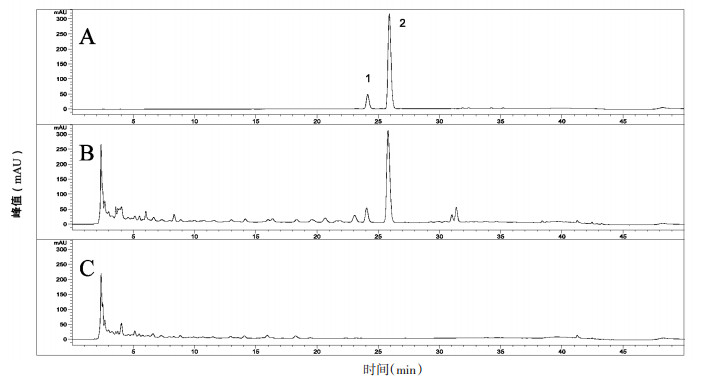
2.2 迷迭香酸、丹酚酸B专属性实验分别吸取混合对照品溶液,供试品溶液,阴性对照品溶液各10 μL,按“2.1.1”项下进行分析,2种指标性成分与其相邻的色谱峰分离系数均大于1.5,并且各组分互不干扰,理论塔板数符合要求,阴性无干扰,专属性良好。见图 1。
|
| 注:A.混合对照品溶液;B.供试品溶液;C.阴性对照品溶液;1.迷迭香酸;2.丹酚酸B。 图 1 复方夏枯草洗剂的高效液相色谱图 Fig. 1 HPLC chromatograms of Compound Xiakucao Lotion |
精密吸取1、2.5、5、10、12.5、15、20 μL的混合对照品溶液,注入液相色谱仪,按照“2.1.1”项下的方法进行测定,记录峰面积。以进样量为横坐标(X),以峰面积为纵坐标(Y),绘制标准曲线,得各组分线性方程、相关系数、线性范围分别为Y迷迭香酸=674.85X-2.427 7,r=1.000 0,0.115~2.3 μg;Y丹酚酸B=319.26X-7.741 6,r=1.000 0,1.7~34 μg,在相应进样范围内线性关系良好。
2.3.2 精密度实验精密吸取“2.1.2”项下混合对照品溶液5 μL,按“2.1.1”项下色谱条件重复进样6次,记录峰面积,计算迷迭香酸、丹酚酸B的RSD分别为0.31%、0.22%,表明仪器的精密度良好。
2.3.3 重复性实验按“2.1.3”项下的方法分别制备6份供试品溶液,分别进样10 μL,记录迷迭香酸、丹酚酸B的峰面积,计算迷迭香酸、丹酚酸B的RSD分别为0.53%、0.59%,表明方法重复性良好。
2.3.4 稳定性实验取“2.1.3”项下方法配制供试品溶液,分别于室温放置0、2、4、8、16、32 h。按“2.1.1”项下色谱条件进样10 μL,测定峰面积,计算迷迭香酸、丹酚酸B的RSD分别为1.24%、0.54%,表明供试品溶液在32 h内稳定。
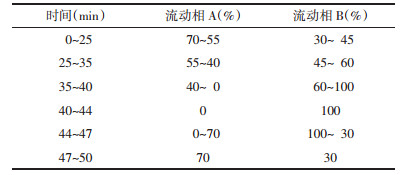
2.3.5 加样回收率实验取已知指标成分含量的供试品溶液1份,在线性范周内分别加入一定量的迷迭香酸、丹酚酸B对照品溶液,各6份,按“2.1.1”项下色谱条件测定含量,结果见表 2。迷迭香酸和丹酚酸B的平均回收率为101.6%和97.3%,RSD分别为2.16%和1.89%,说明本方法回收率良好。
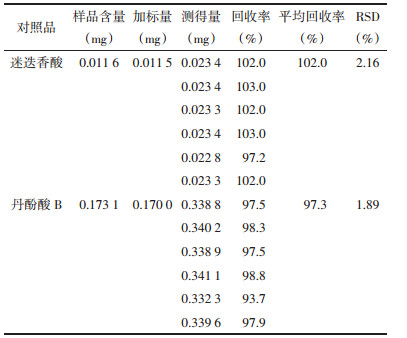
称取1日处方量药材,约155 g,共6份,补足吸水量,料液比分别按1:4、1:6、1:8、1:10、1:12和1:14煎煮1次,每次0.5 h,煎液浓缩至100 mL。按“2.1.3”项下方法分别配制迷迭香酸、丹酚酸B的供试品溶液。按“2.1.1”项下方法进行含量测定,结果见表 3。实验显示,1:4、1:6提取两种主成分含量偏低,1:14提取两种主成分提高不明显,经选择选取1:8、1:10和1:12为正交实验料液比进一步考察。
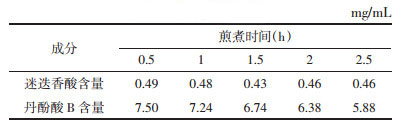
称取1日处方量药材,约155 g,共5份,补足吸水量,加10倍水,煎煮1次,分别煎煮0.5、1、1.5、2、2.5 h,煎液浓缩至100 mL。按“2.1.3”项下方法分别配制迷迭香酸、丹酚酸B的供试品溶液。按“2.1.1”项下方法进行含量测定,结果见表 4。实验显示,两种主成分含量随煎煮时间的增加有明显的下降趋势,所以选择0.5、1、1.5 h为正交实验提取时间进一步考察。
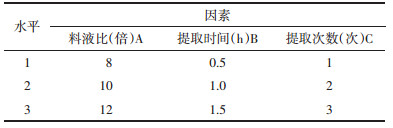
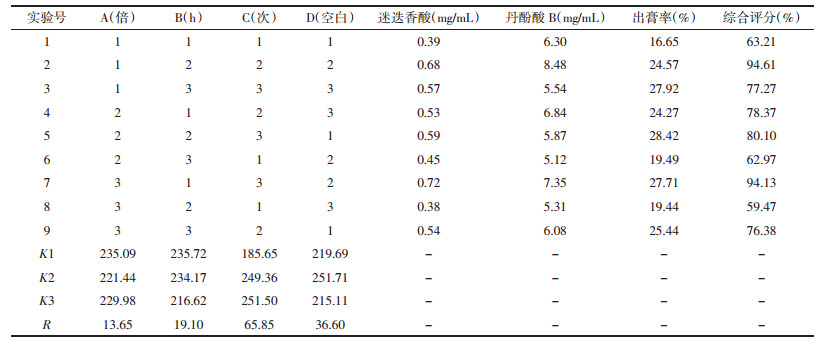
以复方夏枯草洗剂处方药材浓缩提取液中迷迭香酸、丹酚酸B的含量及干膏得率为指标,采用L9(34)正交实验进行考察料液比,提取时间,提取次数等因素,优选出最佳的提取工艺,因素水平见表 5。
按照“2.1.3”项下的方法,对正交设计各组的方案进行提取,制备各组供试品溶液,按照“2.1.1”项下的色谱条件进行含量测定,记录峰面积,计算各供试品溶液中迷迭香酸、丹酚酸B的含量,结果见表 6。
|
精密量取各组浓缩提取液25 mL,分别置已干燥至恒质量的蒸发皿中,水浴蒸干,置105 ℃的烘箱中干燥至恒质量,取出,置干燥器中冷却后,迅速称定质量,计算出膏率,结果见表 6。
2.5.4 正交实验结果分析根据指标因素对提取工艺影响贡献的大小的差异分配权重系数,复方夏枯草洗剂由夏枯草、生丹参、威灵仙、木贼等10味药组成,夏枯草与生丹参为君药,分别选取两味药材的主成分迷迭香酸和丹酚酸B为定量质控指标;干浸膏收率也可反应本方中有效成分的提取效率,故也选定为考察指标,并给予相应权重系数。即迷迭香酸含量(W1)的权重系数为0.4,丹酚酸B含量(W2)的权重系数为0.4,干浸膏收率(W3)的权重系数率为0.2进行加权求和[2],综合评分W(%)= 0.4W1/Wmax1+0.4W2 /Wmax2+0.2W3 /Wmax3。综合加权评价结果见表 9和表 10。
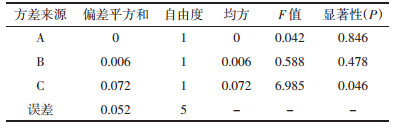
由表 7中结果分析可知,料液比和提取时间对提取效果无显著影响。各因素对综合评分的影响依次为C>B>A,最优提取工艺为C3B1A1,即1:8,0.5 h,3次。最后确定最佳提取工艺为加8倍水,煎煮0.5 h,提取3次。
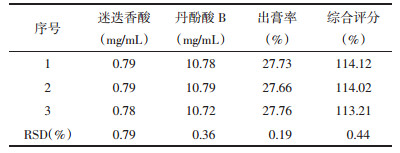
称取1日处方量药材,共3份,按照确定的最佳提取工艺C3B1A1进行验证实验,即加入8倍量的水,提取3次,每次0.5 h,提取液合并浓缩至100 mL,按照“2.1.3”项下的方法制备供试品溶液,按照“2.1.1”项下方法测定迷迭香酸、丹酚酸B的含量。实验结果见表 8,综合评分值达113.21%~114.12%,结果显示,该工艺准确可靠,可行性好,可用于工业化生产。
复方夏枯草洗剂中的君药为夏枯草和生丹参,结合文献资料,本文选用夏枯草、生丹参中主要成分迷迭香酸和丹酚酸B作为含量检测指标[1-2],其含量测定方法主要参考《中华人民共和国药典》2015年版(一部)相关药材项下含量测定方法[5],2种指标性成分的检测波长药典中分别为330 nm和286 nm[5],经过实验发现采用波长286 nm,能很好地同时检测到两味药材中主成分的含量,故采用此波长来检测复方夏枯草洗剂样品,同时结合相关文献[6-8]进行制定。
寻常疣是一种发生于皮肤浅表的慢性良性赘生物,由人类乳头瘤病毒(HPV)感染引起[9]。作为皮肤病门诊中最常见的皮肤病之一,寻常疣虽然易于诊断,但由于可自身接种,临床上治疗非常棘手,复发率居高不下,对患者的生活质量造成极大的影响。目前,临床上尚无特异性抗病毒药物可用于HPV感染,寻常疣有较多的治疗方法,主要包括有两类手段,一类是使用物理或化学方式直接损坏表皮的疣体,另一类是使用免疫调节剂改善人体的细胞免疫功能[10]。前者属于有创治疗,存在诸多弊端,如治疗过程较为痛苦、容易形成创面、恢复周期长、容易感染等,并且有着较高的复发率。而使用免疫调节剂的有效率不佳,患者面临较高的治疗成本和时间成本。中药外用治疗寻常疣有一定的优势,具有毒副作用小、费用低廉、疗效显著等特点,应借助现代科学实验技术进一步深入研究。
复方夏枯草洗剂为上海市第七人民医院皮肤科的经验方,前期临床研究结果表明复方夏枯草洗剂能够有效减轻寻常疣的角质增生与炎症反应,疗效显著。本研究采用多指标综合加权评分法优选复方夏枯草洗剂提取工艺,确定最佳提取方法,为复方夏枯草洗剂的开发提供完备的实验基础,使其作为院内制剂更规范化应用于临床。
| [1] |
戴晶晶, 朱建勇, 张春燕, 等. 正交试验优选冬柏通淋颗粒提取工艺[J]. 亚太传统医药, 2017, 13(8): 26-29. DAI J J, ZHU J Y, ZHANG C Y, et al. Optimizing extraction process of Dongbai Tonglin Granules by orthogonal test[J]. Asia-Pacific Traditional Medicine, 2017, 13(8): 26-29. |
| [2] |
张春燕, 张冰冰, 路建饶, 等. 多指标综合加权评分法优选宁神颗粒提取工艺研究[J]. 上海中医药杂志, 2019, 53(1): 96-100. ZHANG C Y, ZHANG B B, LU J R, et al. Optimizing extraction process of Ningshengranule by comprehensive evaluation of multiple mark[J]. Asia-Pacific Traditional Medicine, 2019, 53(1): 96-100. |
| [3] |
RU M, WANG K, BAI Z, et al. A tyrosine aminotransferase involved in rosmarinic acid biosynthesis in Prunella vulgaris L[J]. Scientific Reports, 2017, 7(1): 4892. |
| [4] |
丁永桢.丹酚酸B防治人乳头瘤病毒感染及其机制研究[D].广州: 南方医科大学, 2018: 16-31. DING Y Z. The activity and mechanistic investigation of Salvianolic Acid B on human papillomavirus infection[D]. Guangzhou: Southern Medical University, 2018: 16-31. |
| [5] |
国家药典委员会.中华人民共和国药典(一部)[S].北京: 中国医药科技出版社, 2015: 76-77. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (Part Ⅰ)[S]. Beijing: China Medical Science Press, 2015: 76-77. |
| [6] |
孙芸, 施洋, 宫海燕, 等. 高效液相色谱法测定天香丹颗粒中红景天苷和丹参酮ⅡA的含量[J]. 新疆医科大学学报, 2015, 38(4): 449-451. SUN Y, SHI Y, GONG H Y, et al. Determination of Salidroside and TanshinoneⅡA in Tianxiangdangranule by HPLC[J]. Journal of Xinjiang Medical University, 2015, 38(4): 449-451. |
| [7] |
张静, 袁珂, 金永春, 等. UPLC法同时测定冬凌草中5种有效成分的含量[J]. 药物分析杂志, 2011(4): 641-644. ZHANG J, YUAN K, JIN Y C, et al. UPLC simultaneous determination of five effective constituents in Rabdosiarubescens[J]. Chinese Journal of Pharmaceutical Analysis, 2011(4): 641-644. |
| [8] |
张冰冰, 路建饶, 朱建勇, 等. 多指标综合加权评分法优选肾衰乙方的提取工艺[J]. 药学服务与研究, 2020, 20(1): 23-27. ZHANG B B, LU J R, ZHU J Y, et al. Optimization of the extraction technology of Shenshuaiyi decoction by comprehensive evaluation of multiple indexes[J]. Pharmaceutical Care and Research, 2020, 20(1): 23-27. |
| [9] |
赵辨. 中国临床皮肤病学[M]. 2版. 南京: 江苏科学技术出版社, 2017: 436-440. ZHAO B. China Clinical Dermatology[M]. 2nd Edition. Nanjing: Phoenix Science Press, 2017: 436-440. |
| [10] |
STERLING J C, GIBBS S, HUSSAIN S, et al. British Association of Dermatologists' guidelines for the management of cutaneous warts 2014[J]. British Journal of Dermatology, 2014, 171(4): 696-712. |
2. Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. Central Laboratory, Seventh People's Hospital of Shanghai University of Traditional Chinese Medicine, Shanghai 200137, China
 2020, Vol. 37
2020, Vol. 37