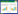文章信息
- 尹超, 王朋宇, 胡艳云, 马朝朋, 王晓妍
- YIN CHAO, WANG Pengyu, HU Yanyun, MA Chaopeng, WANG Xiaoyan
- 黄连地黄汤对糖尿病性心肌病大鼠心肌CTGF及FN1表达的影响
- Effect of Huanglian Dihuang Decoction on the expression of CTGF and FN1 in myocardium of rat with diabetic cardiomyopathy
- 天津中医药, 2020, 37(6): 698-703
- Tianjin Journal of Traditional Chinese Medicine, 2020, 37(6): 698-703
- http://dx.doi.org/10.11656/j.issn.1672-1519.2020.06.23
-
文章历史
- 收稿日期: 2020-01-15
糖尿病性心肌病是发生于糖尿病患者,不能用高血压性心脏病、冠状动脉粥样硬化性心脏病及其他心脏病变来解释的心肌疾病[1]。其在代谢紊乱及微血管病变之基础上引起心肌广泛灶性坏死,出现心功能异常,最终进展为心力衰竭及心源性休克,甚至猝死[2]。充血性心力衰竭为糖尿病心肌病的主要临床表现[3]。由于心肌灶性坏死、纤维瘢痕形成,引起心肌电生理特性不均一而导致心律失常[4]。在糖尿病患者中,女性并发充血性心力衰竭的概率约为男性的2倍。黄连地黄汤组成为黄连(去须)、生地、天花粉、五味子(去梗)、川当归、人参(去芦)、干葛、白茯苓(去皮)、麦门冬(去心)、甘草,功效为滋阴清热,生津止渴,治阴虚火旺之消渴。现代常用于糖尿病性心肌病属阴虚火旺证者[5]。
1 材料及方法 1.1 实验动物SPF级SD大鼠80只,雌性,体质量180~220 g,购于北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0011。
1.2 受试药物及试剂柠檬酸,购于天津大茂化学试剂厂,批号:20171024。柠檬酸三钠,购于天津大茂化学试剂厂,批号:20170706。。链脲佐菌素(STZ),美国Sigma公司,批号:170325。水合氯醛:购于天津大茂化学试剂厂,批号:20161219。低密度脂蛋白胆固醇(LDL-C)测定试剂盒,购于南京建成生物工程研究所,批号:20171221。总胆固醇(TC)测定试剂盒,购于南京建成生物工程研究所,批号:20171203。超氧化物歧化酶(SOD)测定试剂盒,购于南京建成生物工程研究所,批号:20171117。丙二醛(MDA)测试盒,购于南京建成生物工程研究所,批号:20171215。葡萄糖,购于天津市永大化学试剂有限公司,批号:20170213。结缔组织生长因子抗体(CTGF),购于北京博奥森生物技术有限公司,批号:20171228。纤维连接蛋白抗体(FN1),购于北京博奥森生物技术有限公司,批号:20171115。盐酸二甲双胍片,购于中美上海施贵宝制药有限公司,批号:20170421。盐酸苯那普利片,购于北京诺华制药有限公司生产,批号:20170716。TMS-P超敏试剂盒,购于福建迈新生物技术开发有限公司,批号:12/2017。磷酸缓冲盐溶液(PBS),购于北京Solarbio科技有限公司,批号:20171005。无水乙醇,购于天津市永大化学试剂有限公司,批号:20170910。
黄连地黄汤人用法用量为黄连(去须)、生地、天花粉、五味子(去梗)、川当归、人参(去芦)、干葛、白茯苓(去皮)、麦门冬(去心)、甘草各3 g,用水600 mL煎,去渣温服,每日2次。本研究所需药物浓度分别为生药0.27、0.54、1.08 g/mL,取以上药物各45.36 g,共计453.6 g,分2次煎煮,合计加水9 072 mL,合并2次煎液,浓缩至420 mL,制成浓度为生药1.08 g/mL的浓缩液,每周制备1次,分为7等份密封冷藏保存,灌胃时用蒸馏水等倍稀释为生药0.54 g/mL和生药0.27 g/mL。
1.3 仪器金华科迪KD-P生物组织摊片机。安稳+型血糖仪,三诺生物传感股份有限公司。金华科迪KD-202型病理切片机。金华科迪KD-H生物组织烤片机。BX53型奥林巴斯显微镜。
1.4 实验方法 1.4.1 分组、造模、给药80只雌性SPF级SD大鼠,随机选取10只为空白对照组,其余大鼠随机分为模型组、黄连地黄汤低剂量组(2.7 g/kg生药)、黄连地黄汤中剂量组(5.4 g/kg生药)、黄连地黄汤高剂量组(10.8 g/kg生药)、二甲双胍合并苯那普利对照组(90 mg/kg,0.9 mg/kg),每组14只。先用高脂高糖饲料(普通饲料66.5%、猪油10%、蔗糖15%、蛋黄7%、胆酸钠0.5%、胆固醇1%)喂养6周,然后大鼠禁食12 h,除空白对照组外其余大鼠腹腔注射浓度为44 mg/kg的STZ,STZ使用0.1 mol/L柠檬酸钠缓冲液(pH=4.0)配置[6]。注射STZ的第3天,测大鼠空腹血糖,血糖大于11.1 mmol/L认为2型糖尿病模型成功,剔除血糖不合格大鼠,各给药组灌胃体积为10 mL/kg,空白对照组及模型组灌胃等体积的蒸馏水,血糖符合标准的大鼠继续喂饲高脂高糖饲料,边造模边给药12周,末次给药后测大鼠空腹血糖。实验结束时大鼠用5%水合氯醛(6 mL/kg)麻醉,腹主动脉取血,检测血清LDL-C、TC、SOD、MDA,最后取心脏用福尔马林溶液固定,用于苏木精-伊红(HE)染色及免疫组化检测心肌CTGF及FN1表达。
1.4.2 心肌组织HE染色切片脱蜡至水,常规HE染色。中性树胶封片后在光学显微镜下观察心肌细胞损伤程度。
1.4.3 免疫组化法测定心肌细胞CTGF及FN1表达切片脱蜡至水。3% H2O2室温孵育5 min。蒸馏水冲洗,PBS缓冲液冲洗3次,每次3 min。10%山羊血清封闭,室温孵育10 min,倾去血清。滴加Ⅰ抗(CTGF 1:300;FN1 1:400),于37 ℃孵育2 h。PBS缓冲液冲洗3次,每次3 min。滴加适量生物素标记的Ⅱ抗,于37 ℃孵育30 min。PBS缓冲液冲洗3次,每次3 min。滴加适量的辣根酶标记的链霉素工作液,于37 ℃孵育30 min。PBS缓冲液冲洗3次,每次3 min。DAB显色剂显色,蒸馏水冲洗,苏木精复染,脱水,二甲苯透明,中性树胶封片。免疫组化图片采用ImageJ软件进行灰度值分析[7]。
1.5 统计学方法所有数据采用SPSS 22.0软件进行统计处理,实验数据以均数±标准差(x±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD法,P < 0.05为差异有统计学意义。
2 实验结果 2.1 黄连地黄汤对糖尿病性心肌病大鼠模型血糖及血脂的影响见表 1。与空白对照组相比模型组空腹血糖值显著升高(P < 0.01);与模型组相比,黄连地黄汤中剂量组、黄连地黄汤高剂量组、二甲双胍合并苯那普利对照组空腹血糖值显著降低(P < 0.01)。与空白对照组相比,模型组治疗后LDL-C显著升高(P < 0.01),与模型组相比黄连地黄汤低剂量组、黄连地黄汤中剂量组、黄连地黄汤高剂量组、二甲双胍合并苯那普利对照组治疗后LDL-C显著降低(P < 0.05)。与空白对照组相比模型组血清TC显著升高(P < 0.01),与模型组相比黄连地黄汤高剂量组、二甲双胍合并苯那普利对照组治疗后血清TC显著降低(P < 0.05)。
| mmol/L | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
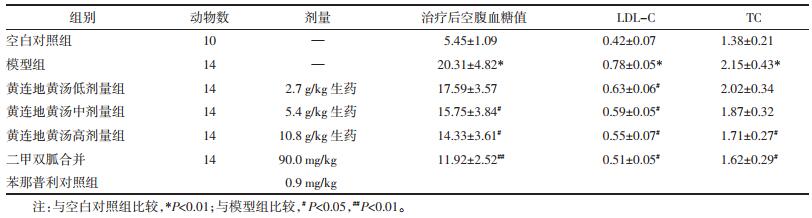
见表 2。与空白对照组相比,模型组MDA显著增加(P < 0.01)。与模型组相比,黄连地黄汤高剂量组和二甲双胍合并苯那普利对照组MDA显著降低(P < 0.05)。与空白对照组相比,模型组SOD显著降低(P < 0.01)。与模型组相比,黄连地黄汤中剂量组、黄连地黄汤高剂量组和二甲双胍合并苯那普利对照组血清SOD显著增加(P < 0.05)。
| mmol/L | |||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||
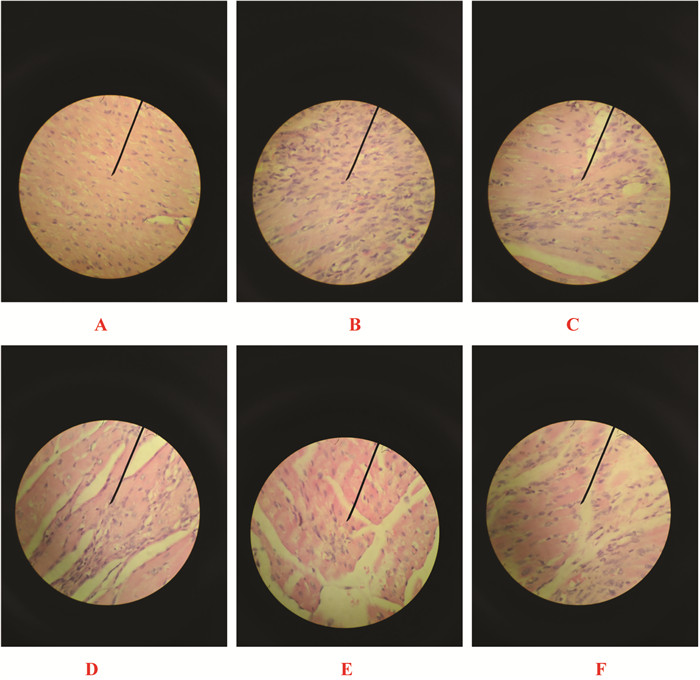
见图 1。空白对照组大鼠心肌细胞无病变;模型对照组大鼠部分心肌细胞溶解消失,且呈现单核细胞浸润;各治疗组大鼠心肌均出现局灶性损伤及单核细胞浸润,但其损伤程度较模型组有所减轻。
|
| 注:A:空白对照组;B:模型组;C:黄连地黄汤低剂量组;D:黄连地黄汤中剂量组;E:黄连地黄汤高剂量组;F:二甲双胍合并苯那普利对照组。 图 1 黄连地黄汤对糖尿病性心肌病大鼠心肌损伤的影响 Fig. 1 Effect of Huanglian Dihuang Decoction on myocardial damage in diabetic cardiomyopathy rats |
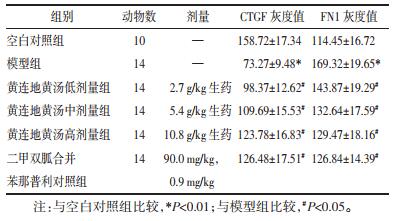
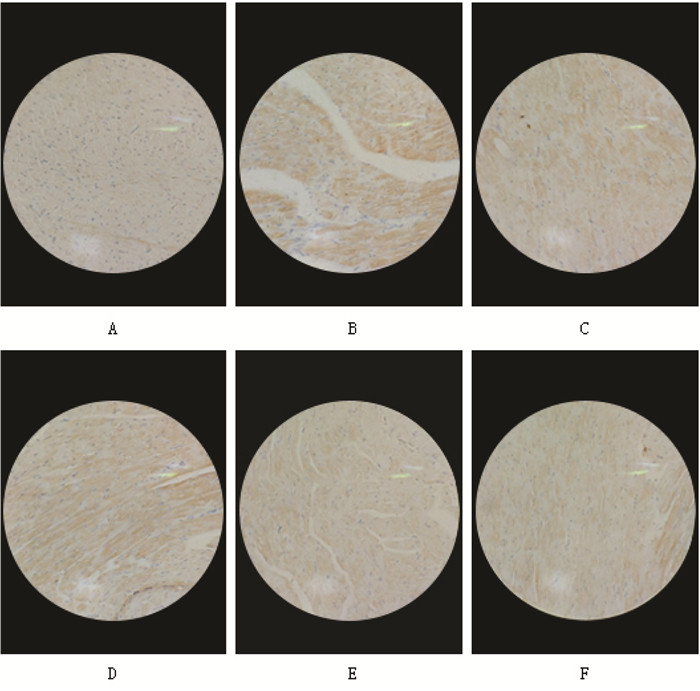
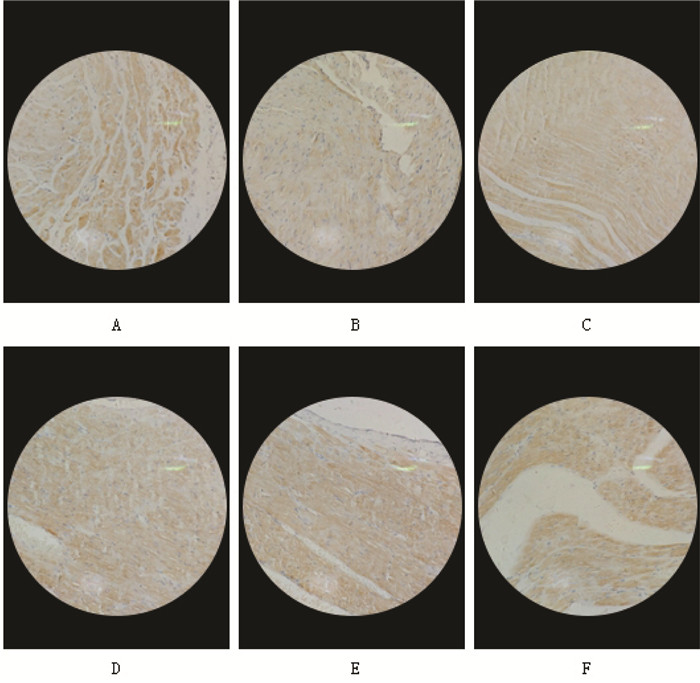
见表 3,图 2、3。与空白对照组相比,模型组心肌细胞CTGF表达显著增加(P < 0.01)。与模型组相比,黄连地黄汤低剂量组、黄连地黄汤中剂量组、黄连地黄汤高剂量组和二甲双胍合并苯那普利对照组心肌细胞CTGF表达显著降低(P < 0.05)。与空白对照组相比,模型组心肌细胞FN1表达显著降低(P < 0.01)。与模型组相比,黄连地黄汤低剂量组、黄连地黄汤中剂量组、黄连地黄汤高剂量组和二甲双胍合并苯那普利对照组心肌细胞FN1表达显著增加(P < 0.05)。
|
|
| 注:A:空白对照组;B:模型组;C:黄连地黄汤低剂量组;D:黄连地黄汤中剂量组;E:黄连地黄汤高剂量组;F:二甲双胍合并苯那普利对照组。 图 2 黄连地黄汤对糖尿病性心肌病大鼠心肌细胞CTGF表达的影响(×200) Fig. 2 Effect of Huanglian Dihuang Decoction on CTGF expression in cardiomyocytes in diabetic cardiomyopathy rats(×200) |
|
| 注:A:空白对照组;B:模型组;C:黄连地黄汤低剂量组;D:黄连地黄汤中剂量组;E:黄连地黄汤高剂量组;F:二甲双胍合并苯那普利对照组。 图 3 黄连地黄汤对糖尿病性心肌病大鼠心肌病大鼠心肌细胞FN1表达的影响(×200) Fig. 3 Effect of Huanglian Dihuang Decoction on FN1 expression in cardiomyocytes in diabetic cardiomyopathy rats(×200) |
糖尿病性心肌病是指发生于糖尿病患者,在代谢紊乱及微血管病变之基础上引发心肌广泛灶性坏死,出现亚临床的心功能异常,最终进展为心力衰竭,重症患者甚至猝死[8]。心肌细胞代谢紊乱糖尿病患者的收缩蛋白发生糖基化,导致其功能异常。心肌细胞钙转运缺陷随着心肌细胞外葡萄糖水平的升高直接导致细胞内钙离子浓度的改变,2型糖尿病的心肌细胞钠钙交换受到抑制,钙离子(Ca2+)浓聚于肌浆网,Ca2+超负荷的心肌肌浆网,心肌舒张时张力增高,心脏的顺应性下降[9]。糖尿病患者心肌存在弥漫性心肌壁内小血管病变。糖尿病病程较久由糖基化的胶原沉积引起心肌间质纤维化[10]。糖尿病患者血脂增高能促进血管壁细胞对脂质的摄取,极低密度脂蛋白胆固醇(VLDL-C)转变为胆固醇酯,LDL-C糖化损害肝细胞上的相关受体对其识别从而使LDL-C代谢减慢[11]。LDL-C与另外受体结合被巨噬细胞优先吞噬和降解,堆积在巨噬细胞内成为泡沫细胞进而促进动脉粥样硬化(AS)斑块的形成[12]。糖尿病患者在血糖控制不良时,三酰甘油含量增加,氧化脂蛋白酶活性增高,LDL-C增加,均成为血管内皮细胞和血管平滑肌细胞的胞质毒性因素。糖尿病心肌病为与代谢相关的广泛性心肌损害,心肌细胞肥大、变性、灶性坏死、坏死区为纤维组织取代。针对糖尿病性心肌病目前无特效的治疗方法,虽然尚不明确血糖控制是否改变糖尿病性心肌病的病程,仍应及时控制高血糖[13]。治疗高血压是本病的基本治疗措施。研究表明中度肥胖的糖尿病患者左室舒张期明显僵硬,糖尿病患者较正常人群患高脂血症的概率高,因此需进行降血脂治疗[14]。黄连地黄汤对血糖血脂血压均有影响,黄连煎剂和小檗碱还有降低血糖的作用,黄连水浸液可使血清胆固醇含量降低。当归流浸膏有抗心律不齐和降压作用[15]。当归能抗心肌缺血缺氧。葛根素可抗高血压,防治AS,葛根素可明显限制犬实验性急性心肌梗死范围[16]。本研究结果表明黄连地黄汤可显著降低糖尿病性心肌病模型大鼠空腹血糖值、LDL-C及TC含量,同时提高糖尿病性心肌病模型大鼠抗氧化能力。
CTGF对成纤维细胞具有趋化及促有丝分裂作用,CTGF与包括心脏、肾脏及肝脏等在内的许多组织器官纤维化发生发展密切相关[17]。CTGF因具有明显的趋化性,能诱导成纤维细胞增殖。外源性CTGF可刺激大鼠肝星状细胞(HSC)增殖及黏附。CTGF在肝纤维化发生发展中起着重要的作用[18]。FN是一种纤维连接蛋白,参与细胞黏附、分化、伤口愈合、凝血和机体防卫。主要分布于结缔组织和大部分基底膜上,纤维连接蛋白有促进巨噬细胞的吞噬功能,促进细胞与纤维基质间连接的生理作用[19]。纤连蛋白与机体创伤修复有密切关系。纤维连接蛋白可用于治疗血液系统和心脑血管系统疾病。随着血管硬化程度的增加FN1含量呈下降趋势。血浆FN1缺乏会引起微血管完整性的破坏和通透性升高,导致血浆大量外渗,血液浓缩,黏度增高,有效循环血量减少,血浆与组织液内平衡失调,引起机体休克等危险情况[20]。糖尿病患者的成纤维细胞外基质蛋白的合成发生改变,FN1与胶原的比例降低,即胶原相对含量升高[21]。在糖尿病和下肢静脉溃疡中,FN1含量明显降低。本研究结果表明黄连地黄汤可显著降低糖尿病性心肌病模型大鼠心肌细胞结缔组织生长因子的表达,显著增加心肌细胞细胞黏附蛋白的表达,具有明显的抗心肌损害及心肌细胞纤维化的作用。
综上所述,黄连地黄汤可通过降低糖尿病性心肌病模型大鼠空腹血糖值、LDL-C、TC含量及心肌细胞CTGF的表达,增加其抗氧化能力及心肌细胞FN1的表达,最终产生抗心肌细胞损害及纤维化的作用。
| [1] |
徐娜, 白淑芝. 糖尿病心肌病发病机制的研究进展[J]. 医学综述, 2019, 25(3): 520-524. XU N, BAI S Z. Research progress in pathogenesis of diabetic cardiomyopathy[J]. Medical Recapitulate, 2019, 25(3): 520-524. DOI:10.3969/j.issn.1006-2084.2019.03.021 |
| [2] |
王静娜, 侯瑞田, 史亦男, 等. 糖尿病心肌病发病机制及病理改变研究进展[J]. 心血管病学进展, 2016, 37(4): 412-415. WANG J N, HOU R T, SHI Y N, et al. Research progress on pathogenesis and pathological changes of diabetic cardiomyopathy[J]. Advances in Cardiovascular Diseases, 2016, 37(4): 412-415. |
| [3] |
张凤丽, 周迎生, 赵一楠. 糖尿病心肌病——心脏损害的"暗礁"[J]. 慢性病学杂志, 2014, 15(8): 587-595. ZHANG F L, ZHOU Y S, ZHAO Y N. Diabetic cardiomyopathy:the "reef" of heart damage[J]. Chronic Pathematology Journal, 2014, 15(8): 587-595. |
| [4] |
李顺宝, 李田昌. 糖尿病性心肌病的病理生理机制[J]. 中国心血管杂志, 2011, 16(2): 149-151. LI S B, LI T C. Pathophysiological mechanism of diabetic cardiomyopathy[J]. Chinese Journal of Cardiovascular Medicine, 2011, 16(2): 149-151. DOI:10.3969/j.issn.1007-5410.2011.02.022 |
| [5] |
殷献军. 糖尿病心肌病中西医诊疗进展[J]. 中西医结合心脑血管病杂志, 2017, 15(13): 1576-1580. YIN X J. Progress in diagnosis and treatment of diabetic cardiomyopathy in Chinese and Western medicine[J]. Chinese Journal of Integrative Medicine on Cardio-Cerebrovascular Disease, 2017, 15(13): 1576-1580. DOI:10.3969/j.issn.1672-1349.2017.13.010 |
| [6] |
霍梦露, 王瑞瑶, 李超, 等. 小檗碱对高糖高脂饲料联合链脲佐菌素诱导的糖尿病心肌病大鼠的保护作用[J]. 中国临床保健杂志, 2019, 22(3): 377-382. HUO M L, WANG R Y, LI C, et al. The protective effect of berberine on diabetic cardiomyopathy rats induced by streptozotocin and high-glucose-high-fat diet[J]. Chinese Journal of Clinical Healthcare, 2019, 22(3): 377-382. DOI:10.3969/J.issn.1672-6790.2019.03.023 |
| [7] |
顾国萍, 张丽华. Cx30.2和Cx45在急性心肌梗死大鼠心脏结区组织中的表达[J]. 中国医药导报, 2015, 12(6): 22-30. GU G P, ZHANG L H. Expression of Cx30.2 and Cx45 in heart tissues of rats with acute myocardial infarction[J]. China Medical Herald, 2015, 12(6): 22-30. |
| [8] |
谭慧琼, 罗晓亮. 继发性心肌病[J]. 中国实用内科杂志, 2012, 32(7): 502-504. TAN H Q, LUO X L. Secondary cardiomyopathy[J]. Chinese Journal of Practical Internal Medicine, 2012, 32(7): 502-504. |
| [9] |
周斌全, 胡申江. 糖尿病大鼠心肌超微结构及钙离子调控蛋白基因表达的改变[J]. 浙江大学学报(医学版), 2005, 34(5): 454-458. ZHOU B Q, HU S J. Alterations of myocardial ultrastructure and gene expression of calcium handling proteins in diabetic rat heart[J]. Journal of Zhejiang University (Medicine Sciences), 2005, 34(5): 454-458. DOI:10.3785/j.issn.1008-9292.2005.05.015 |
| [10] |
吕青兰, 孙丽, 蒋碧梅, 等. 核仁素对小鼠糖尿病性心肌病心肌肥大与纤维化发生的影响[J]. 中国病理生理杂志, 2017, 33(7): 1231-1236. LYU Q L, SUN L, JIANG B M, et al. Role of nucleolin on myocardial hypertrophy and fibrosis in type II diabetic cardiomyopathy mice[J]. Chinese Journal of Pathophysiology, 2017, 33(7): 1231-1236. DOI:10.3969/j.issn.1000-4718.2017.07.013 |
| [11] |
李顺宝, 李田昌. 小檗碱对糖尿病早期心肌病大鼠保护及其机制研究[J]. 中国医药导刊, 2011, 13(2): 301-302. LI S B, LI T C. The protective effect and mechanism of borberine for early diabetic cardiomyopathy rats[J]. Chinese Journal of Medicinal Guide, 2011, 13(2): 301-302. DOI:10.3969/j.issn.1009-0959.2011.02.071 |
| [12] |
李诗, 石岩. Tribbles同源蛋白3与糖尿病及其并发症研究进展[J]. 中医药临床杂志, 2018, 30(10): 1965-1969. LI S, SHI Y. Research progress of Tribbles Homology Protein 3 and diabetes mellitus and its complications[J]. Clinical Journal of Traditional Chinese Medicine, 2018, 30(10): 1965-1969. |
| [13] |
王慧, 丁选胜. 糖尿病心肌病治疗药物研究进展[J]. 药学进展, 2018, 42(11): 860-867. WANG H, DING X S. Research progress in therapeutic drugs for diabetic cardiomyopathy[J]. Progress in Pharmaceutical Sciences, 2018, 42(11): 860-867. |
| [14] |
杨跃进, 王红, 宋光远. 糖尿病心肌病[J]. 中国糖尿病杂志, 2012, 20(10): 794-796. YANG Y J, WANG H, SONG G Y. Diabetic cardiomyopathy[J]. Chinese Journal of Diabetes, 2012, 20(10): 794-796. DOI:10.3969/j.issn.1006-6187.2012.10.022 |
| [15] |
沙雯君, 朱英倩, 雷涛. 黄连素对2型糖尿病湿热困脾证患者胰高血糖素样肽的影响[J]. 上海中医药大学学报, 2018, 32(6): 7-10. SHA W J, ZHU Y Q, LEI T. Effects of berberine on glucagon-like peptide in patients with type 2 diabetes mellitus with syndrome of dampness-heat disturbing spleen[J]. Academic Journal of Shanghai University of Traditional Chinese Medicine, 2018, 32(6): 7-10. |
| [16] |
童凤雪, 张砾丹, 邹欣, 等. 黄连不同方法提取物治疗2型糖尿病大鼠的比较研究[J]. 中西医结合研究, 2019, 11(2): 78-85. TONG F X, ZHANG L D, ZOU X, et al. Comparative study on extracts from different methods of rhizoma coptidis in the treatment of type 2 diabetic rats[J]. Research of Integrated Traditional Chinese and Western Medicine, 2019, 11(2): 78-85. DOI:10.3969/j.issn.1674-4616.2019.02.006 |
| [17] |
梁媛媛. 结缔组织生长因子在大鼠糖尿病心肌病中的作用机制[J]. 中国老年学杂志, 2018, 38(6): 1465-1467. LIANG Y Y. Mechanism of connective tissue growth factor in diabetic cardiomyopathy in rats[J]. Chinese Journal of Gerontology, 2018, 38(6): 1465-1467. DOI:10.3969/j.issn.1005-9202.2018.06.077 |
| [18] |
戴榕, 王超, 周军, 等. 硫氢化钠对慢性心力衰竭大鼠心肌纤维化及结缔组织生长因子表达的影响[J]. 疑难病杂志, 2018, 17(12): 1370-1374. DAI R, WANG C, ZHOU J, et al. Effects of sodium hydrosulfide on myocardium fibrosis and expression of connective tissue growth factor in rats with chronic heart failure[J]. Chinese Journal of Difficult and Complicated Cases, 2018, 17(12): 1370-1374. DOI:10.3969/j.issn.1671-6450.2018.12.017 |
| [19] |
靳陶然, 刘宽芝. 糖尿病心肌病心肌间质重构[J]. 国外医学·心血管疾病分册, 2005, 32(4): 26-28. JIN T R, LIU K Z. Myocardial interstitial remodeling in diabetic cardiomyopathy[J]. International Journal of Cardiovascular Disease, 2005, 32(4): 26-28. |
| [20] |
周俊岭, 马礼坤. 瑞舒伐他汀抑制去氧皮质酮诱导大鼠心肌纤维化的作用影响[J]. 安徽医科大学学报, 2013, 48(10): 1183-1186. ZHOU J L, MA L K. Effect of rosuvastatin on inhibiting deoxycorticosterone-induced myocardial fibrosis in rats[J]. Acta Universitatis Medicinalis Anhui, 2013, 48(10): 1183-1186. |
| [21] |
许侠, 刘国良. 糖尿病伴穿通性疾病的特征、识别及处理[J]. 实用糖尿病杂志, 2018, 14(1): 7-8. XU X, LIU G L. Characteristics, recognition and management of diabetes mellitus with perforating diseases[J]. Journal of Practical Diabetology, 2018, 14(1): 7-8. |
 2020, Vol. 37
2020, Vol. 37