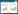文章信息
- 孙大娟, 樊静娜, 王帅, 迟莉丽
- SUN Dajuan, FAN Jingna, WANG Shuai, CHI Lili
- 基于JAK1/STAT6通路探讨安肠愈疡汤对HT-29细胞炎症模型的影响及机制研究
- Discussion on the effect and mechanism research of Anchang Yuyang Recipe on HT-29 cell inflammation model based on the JAK1/STAT6 pathway
- 天津中医药, 2020, 37(8): 936-942
- Tianjin Journal of Traditional Chinese Medicine, 2020, 37(8): 936-942
- http://dx.doi.org/10.11656/j.issn.1672-1519.2020.08.21
-
文章历史
- 收稿日期: 2020-03-14
2. 山东中医药大学第一临床医学院, 济南 250014
溃疡性结肠炎(UC)是一种慢性非特异性肠道炎症性疾病[1]。目前认为UC的发病是由遗传易感性、环境因素、自身免疫调节失衡、肠道菌群紊乱等多方面因素相互影响共同作用引起的肠黏膜屏障损伤[2],故Giovanni又称UC为“屏障器官性疾病”[3]。肠道黏膜屏障的完整性在UC的发病机制中起着重要作用,故修复损伤的肠道黏膜屏障是治疗UC的关键所在。安肠愈疡汤是导师迟莉丽教授临证治疗UC总结的经验方,具有健脾益气、清解化湿、调气活血的功效,临床疗效显著[4-5]。课题组前期研究发现安肠愈疡汤可明显下调UC大鼠致炎因子白细胞介素(IL)-1β、IL-8、肿瘤坏死因子-α(TNF-α)的表达,上调抗炎因子IL-10、IL-13的表达,上调肠黏膜修复因子肠三叶因子(TFF3)、黏蛋白2(MUC2)的表达,具有较好的抗炎及促进黏膜修复的作用[6-9]。但是对于安肠愈疡汤调控TFF3分子的上游调控通路研究尚不明确,有研究表明蛋白酪氨酸激酶1(JAK1)/信号转导和转录活化因子6(STAT6)信号通路广泛参与细胞生长、分化、增殖、炎症和调节免疫功能等过程,在UC的发病中调控着重要的免疫应答反应[10-13]。本实验在前期研究基础上,使用脂多糖(LPS)诱导建立人结直肠腺癌细胞(HT-29细胞)炎症模型,从体外实验观察安肠愈疡汤对JAK1/ STAT6通路的影响,并探讨其作用机制。
1 材料 1.1 细胞HT-29细胞(上海中桥新舟生物科技有限公司,批号:Cat.#ZQ0057)。
1.2 药物制备安肠愈疡汤(生黄芪30 g,炒白术30 g,薏苡仁30 g,败酱草30 g,黄连9 g,黄芩9 g,木香9 g,槟榔15 g,地榆炭15 g,白及12 g,当归9 g,炒白芍12 g,防风6 g,生甘草9 g)药材购于山东中医药大学附属医院,煎煮、过滤、浓缩后置于旋转蒸发仪中蒸发至浓稠不流动状态,烘干制成浸膏。称量后完全溶解于DMEM培养基中,使用无菌注射器取溶解后液体通过0.22 μm滤膜除菌制成无菌药品溶液,干预时使用DMEM培养基配置成相应浓度的含药培养基进行孵育。5-氨基水杨酸(5-AS,商品名:美沙拉秦,批号:Cat.SA5260,Lot.518A021,购自北京索莱宝科技有限公司)溶解于二甲基亚砜(DMSO),后溶解于DMEM培养基中再配置成相应浓度进行干预。
1.3 试剂四甲基噻唑蓝MTT(批号:Lot. #303H0525,购自北京索莱宝科技有限公司),PrimeScriptTM RT reagent Kit with gDNA Eraser[Perfect Real Time,批号:Cat.# RR047A,Lot.#AI12361A,购自宝日医生物技术(北京)有限公司(takara中国)],辣根酶标记山羊抗兔IgG(批号:Cat.#ZB-2301,购自北京中杉金桥生物技术有限公司),人类IL-13、TFF3酶联免疫吸附(ELISA)试剂盒(批号分别为:Cat.E-EL-H0104c,Lot.3YVV1HYY3U及Cat.E-ELH1108c,Lot.LRQW8J1JW6,购自武汉伊莱瑞特生物科技股份有限公司),兔多克隆IL-13、JAK1抗体(批号分别为:ab106732、ab47435,购自英国Abcam公司),兔单克隆STAT6、TFF3抗体(批号分别为:ab32520、ab108599,购自英国Abcam公司);异硫氰酸荧光素(FITC)标记山羊抗兔免疫球蛋白G(IgG)(H+L)(批号:Cat.A0562,购自上海碧云天生物科技有限公司);4’,6-二脒基-2-苯基吲哚(DAPI)染色液(批号:Cat.C1005,购自上海碧云天生物科技有限公司)。
1.4 仪器EVOSTM FLoid倒置荧光显微镜(购自美国Thermo Fisher Scientific公司),Bio -Rad Mini - PROTEAN Tetra电泳系统(购自美国Bio-Rad公司),Fluor Chem Q蛋白印迹成像和定量分析系统(购自美国Protein simple公司),Light Cycler 480Ⅱ荧光定量聚合酶链反应(PCR)仪(购自德国Roche公司)。本研究在山东中医药大学附属医院实验中心完成。
2 方法 2.1 HT-29细胞炎症模型建立HT-29细胞培养于含10%胎牛血清的DMEM培养基中,加入LPS 20 μg/mL[14-15]孵育24 h(LPS组),以未经LPS处理的细胞作为对照组。提取核糖核酸(RNA)应用实时荧光定量聚合酶链反应(Q-RT-PCR)技术检测IL-8、IL-13 mRNA的表达。
2.2 安肠愈疡汤浓度的筛选在前期研究基础上,安肠愈疡汤分设0.01、0.1、1、5、10、25、50 mg/mL 7个浓度梯度,以正常未处理HT-29细胞为对照组,采用MTT法观察不同浓度安肠愈疡汤对HT-29活力的影响,并采用Q-RT-PCR法检测IL-8 mRNA表达变化。
2.3 分组及干预实验细胞分为6组,空白组:加入完全培养基孵育,不做任何处理;模型组:给予LPS(20 μg/mL)干预24 h;安肠愈疡汤各浓度组:LPS(20 μg/mL)干预24 h后再给予安肠愈疡汤(低、中、高浓度)孵育24 h;5-AS组:LPS(20 μg/mL)干预24 h后再给予5-AS(1 mg/L)孵育24 h。
2.4 应用ELISA法检测各组IL-13、TFF3的分泌水平取细胞培养上清1 000 × g离心20 min,取上清液,根据ELISA试剂盒说明书检测IL-13、TFF3的表达水平。
2.5 应用免疫荧光检测各组IL-13、TFF3的荧光强度各组以1×104/孔细胞密度接种到铺好细胞爬片的24孔板内,干预24 h后弃培养基,多聚甲醛固定、TritonX-100通透、山羊血清封闭,每孔加入一抗(1:200),湿盒4 ℃孵育过夜,FITC标记的二抗室温避光孵育1 h,DAPI染核5 min,抗荧光衰减封片剂封片后于荧光显微镜下采集图像,应用Image J软件分析抗体表达。
2.6 Q-RT-PCR检测各组IL-13、JAK1、STAT6、TFF3mRNA的表达收集干预24 h的细胞,按Trizol说明书提取细胞总RNA,按照cDNA合成试剂盒说明书合成cDNA模板,以此cDNA模板采用Light Cycler 480Ⅱ荧光定量PCR仪进行扩增,以GAPDH作为对照,采用2-ΔΔCt法计算组间对应基因的表达差异。实验用各引物序列见表 1。
提取各组细胞总蛋白,BCA法测定蛋白浓度,制备蛋白上样缓冲液,配制SDS-PAGE凝胶,取等量蛋白电泳,湿转、封闭后放入到IL-13(1:1 000)、TFF3(1:5 000)、JAK1(1:2 000)、STAT6(1:1 000)、β-actin(1:1 000)的一抗孵育盒中4 ℃过夜,次日洗膜,室温孵育二抗1 h,洗膜。发光液显色,凝胶系统成像。使用Image J软件分析条带灰度值。
2.8 统计学方法采用SPSS 23.0软件进行统计分析,数据以均数±标准差(x±s)表示,两组间比较采用两独立样本t检验,多组间比较若方差齐采用单因素方差分析,组间两两比较采用LSD法,多组间比较若方差不齐采用秩和检验。P<0.05为差异具有统计学意义。
3 结果 3.1 HT-29细胞炎症模型的建立与对照组比较,模型组细胞IL-8 mRNA表达明显上调(P<0.01),IL-13 mRNA表达明显下调(P<0.01),说明炎症模型建立成功,见表 2。

|
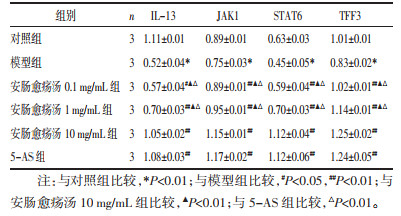
与对照组比较,模型组对HT-29细胞具有明显促增殖作用(P<0.01);与模型组相比,安肠愈疡汤在浓度为0.01、0.1、1、5、10 mg/mL时对HT-29具有明显的促增殖作用(P<0.01),在25、50 mg/mL时有抑制作用(P<0.01)。0.01、0.1、10 mg/mL 3组组间比较差异有统计学意义(P<0.01),0.1 mg/mL与1 mg/mL组间比较差异有统计学意义(P<0.05)。1 mg/mL组与5 mg/mL组之间比较差异无统计学意义(P>0.05)。选择安肠愈疡汤0.1、1、10 mg/mL进行后续实验,见表 3。
|
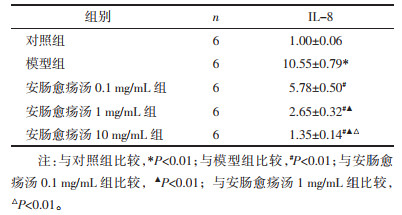
分别采用安肠愈疡汤0.1、1、10 mg/mL浓度干预LPS诱导的HT-29 24 h后,采用Q-RT-PCR检测IL-8 mRNA表达,结果显示:与对照组比较,模型组IL-8 mRNA表达上调(P<0.01);与模型组比较,安肠愈疡汤0.1、1、10 mg/mL组表达均下调(P<0.01);3组间两两比较有差异(P<0.01)。因此选取0.1、1、10 mg/mL为后期实验低、中、高浓度,见表 4。
|
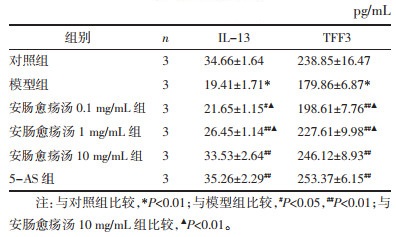
与对照组比较,模型组IL- 13、TFF3表达减少(P<0.01);与模型组相比,各用药组IL-13、TFF3分泌均增多(P<0.05或P<0.01);安肠愈疡汤高浓度组IL-13、TFF3表达高于中、低浓度组(P<0.01),安肠愈疡汤高浓度组IL-13、TFF3表达与5-AS组比较无统计学差异(P>0.05)。见表 5。
|
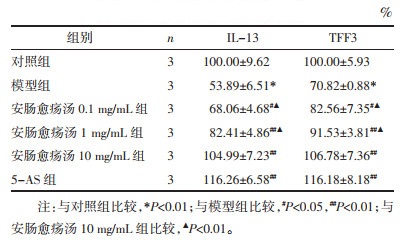
以对照组荧光强度为100%,免疫荧光分析结果显示:与对照组相比,模型组IL-13、TFF3荧光强度降低(P<0.01);与模型组相比,各用药组IL-13、TFF3荧光强度均增强(P<0.05或P<0.01);安肠愈疡汤高浓度组IL-13、TFF3荧光强度高于中、低浓度组(P<0.01),安肠愈疡汤高浓度组IL-13、TFF3荧光强度低于美沙拉秦组,但差异无统计学意义(P>0.05)。见表 6、图 1、图 2。
|

|
| 图 1 安肠愈疡汤对LPS诱导HT-29细胞IL-13荧光强度 Fig. 1 The fluorescent intensity of IL-13 in HT-29 cells induced by LPS with AYR |

|
| 图 2 安肠愈疡汤对 LPS 诱导 HT-29 细胞内 TFF3表达影响 Fig. 2 The fluorescent intensity of TFF3 in HT-29 cells induced by LPS with AYR |
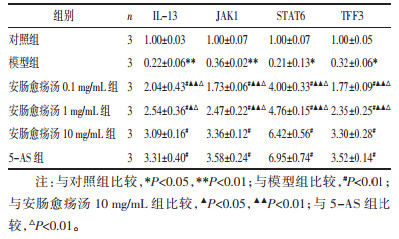
与对照组比较,模型组IL -13、JAK1、STAT6、TFF3 mRNA和蛋白表达均下调,差异有统计学意义(P<0.05或P<0.01);与模型组相比,各用药组IL-13、JAK1、STAT6、TFF3 mRNA和蛋白表达均上调(P<0.05或P<0.01);安肠愈疡汤高浓度组IL -13、JAK1、STAT6、TFF3 mRNA和蛋白表达高于中、低浓度组,差异有统计学意义(P<0.05或P<0.01),高浓度组IL-13、JAK1、STAT6、TFF3 mRNA和蛋白表达与5-AS组无统计学差异(P>0.05)。中药中、低浓度组IL-13、JAK1、STAT6、TFF3 mRNA和蛋白的表达低于5-AS组,差异有统计学意义(P<0.01)。见表 7、表 8、图 3。

|
| 注:1:对照组;2:模型组;3:安肠愈疡汤0.1 mg/mL组;4:安肠愈疡汤1 mg/mL组;5:安肠愈疡汤10 mg/mL组;6:5-AS组。 图 3 各组蛋白的表达 Fig. 3 Protein expression in each group |
UC的治疗目标是在诱导及维持临床症状缓解的基础上强调黏膜愈合[16-17],修复损伤的肠道黏膜屏障是UC治疗的关键。安肠愈疡汤是治疗UC的经验方,临床疗效确切,前期临床研究[4-5]发现其对UC患者内镜黏膜愈合及组织病理学炎症的缓解均有着良好的疗效。前期实验研究[6-9]发现安肠愈疡汤能上调血清中抗炎因子IL-13以及肠道黏膜修复因子TFF3、MUC2的表达,具有良好的抗炎及促进黏膜修复的作用。但是对于安肠愈疡汤调控TFF3分子的上游调控通路研究尚不明确,研究表明IL-13可通过STAT6途径上调TFF3 mRNA及蛋白水平的表达[18]。蛋白酪氨酸激酶(JAK)/信号转导和转录活化因子(STAT)信号通路涉及实体肿瘤、淋巴瘤以及炎症性疾病[19]等的发病机制,研究发现JAK1/STAT6通路在UC的发病中起着重要调控作用[8-11, 20]。JAK1/ STAT6主要由IL-4、IL-13激活[21]以启动信号转导和转录的功能。STAT6在Th2细胞的分化中有着重要的影响,影响B细胞抗原呈递的细胞表面分子表达,调节IL-10等炎症因子的表达[22]。有研究发现STAT6-/-的小鼠在三硝基苯磺酸(TNBS)诱导后出现了肠道黏膜伤口的愈合延迟,与对照组比较抗炎细胞因子IL-10显著下降。还有研究发现通过调控JAK1/STAT6通路调节一氧化氮合成酶(iNOS)和干扰素-γ(IFN-γ)的生成发挥对肠黏膜炎症的保护作用[23]。本研究在前期研究基础上进一步从体外实验探讨安肠愈疡汤对JAK1/STAT6通路的影响。
既往研究[14-15]采用LPS干预HT-29细胞构建体外炎症模型,LPS刺激细胞后可导致大量炎症因子如IL-1、IL-6、IL-8的释放,而且还会进一步生成并释放炎症因子如白三烯等[24],是常用的构建细胞炎症模型的诱导因子。在既往基础上课题组又进行了炎症模型的验证,IL-8是重要的炎症趋化因子,由LPS刺激HT-29细胞后激活TLR4/NF-κB通路产生[25],IL-13是重要的抗炎因子,本研究中发现LPS干预HT-29细胞后出现致炎因子IL-8上升以及抗炎因子IL-13下降,提示模型构建成功。国内炎症性肠病治疗指南推荐5-AS作为轻中度UC的一线用药,有良好的抗炎调节免疫作用,有研究表明5- AS可以通过抑制前列腺素的合成及白三烯的释放从而起到抗炎作用,还能抑制炎症因子的释放减轻肠道黏膜炎症反应[26],因此选择5-AS作为阳性对照药物。
本研究结果显示,安肠愈疡汤可能通过上调IL-13的分泌,激活JAK1/STAT6通路,促进黏膜修复因子TFF3的分泌,减轻HT-29细胞炎症模型的炎症反应,发挥保护作用。安肠愈疡汤具有剂量依赖性的作用特点,高浓度组作用优于中、低浓度组,但与5-AS组比较未见明显优势。本实验初步探讨了安肠愈疡汤对LPS诱导的HT-29细胞炎症模型可能的保护机制,显示出安肠愈疡汤对肠道黏膜良好的修复作用。今后将从UC大鼠模型体内实验进一步探讨安肠愈疡汤对肠道黏膜屏障的保护机制。
| [1] |
MAGRO F, GIONCHETTI P, ELIAKIM R, et al. Third European evidence-based consensus on diagnosis and management of ulcerative colitis. Part 1:definitions, diagnosis, extra-intestinal manifestations, pregnancy, cancer surveillance, surgery, and ileo-anal pouch disorders[J]. Journal of Crohns & Colitis, 2017, 11(6): 649. |
| [2] |
ATREYA R, NEURATH M F. Chemokines in inflammatory bowel diseases[J]. Nature Reviews Immunology, 2014, 14(5): 329-342. DOI:10.1038/nri3661 |
| [3] |
ACTIS G C, PELLICANO R, ROSINA F. Inflammatory bowel diseases:current problems and future tasks[J]. World Journal of Gastrointestinal Pharmacology & Therapeutics, 2014, 5(3): 169. |
| [4] |
孙大娟, 迟莉丽. 安肠愈疡汤合加味生肌散治疗溃疡性结肠炎30例[J]. 山东中医药大学学报, 2009, 33(5): 402-403. SUN D J, CHI L L. Treatment of 30 cases of ulcerative colitis with Anchang Yuyang Decoction and Jiawei Shengji Powder[J]. Journal of Shandong University of Traditional Chinese Medicine, 2009, 33(5): 402-403. |
| [5] |
迟莉丽.安肠愈疡汤口服合生肌散灌肠治疗溃疡性结肠炎的疗效观察及机制研究[D].济南: 山东中医药大学, 2004. CHI L L. The curative effects and the mechanism research in treating UC by coupling use of An-Chang-Yu-Yang-Tang with Sheng-Ji-San[D]. Jinan: Shandong University of Traditional Chinese Medicine, 2004. |
| [6] |
迟莉丽, 戴霞. 安肠愈疡汤口服合加味生肌散灌肠对实验性溃疡性结肠炎大鼠的影响[J]. 中华中医药杂志, 2009, 24(10): 1337-1339. CHI L L, DAI X. Study on effect and mechanism of Anchang Yuyang Decoction with Jiawei ShengjiPowder on ulcerative colitis in rats[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2009, 24(10): 1337-1339. |
| [7] |
石敏, 迟莉丽, 戴霞, 等. 安肠愈疡汤合加味生肌散对实验性溃疡性结肠炎大鼠的药效学研究[J]. 时珍国医国药, 2010, 21(9): 2286-2288. SHI M, CHI L L, DAI X, et al. Pharmacodynamics study of Anchang Yuyang Decoction and Jiawei Shengji Powder on experimental ulcerative colitis in rats[J]. Lishizhen Medicine and Materia Medica Research, 2010, 21(9): 2286-2288. DOI:10.3969/j.issn.1008-0805.2010.09.075 |
| [8] |
迟莉丽, 孙大娟, 程艳, 等. 中药安肠愈疡汤对溃疡性结肠炎大鼠结肠组织中TFF3、MUC2及TLR4基因表达的影响[J]. 胃肠病学, 2016, 21(2): 85-89. CHI L L, SUN D J, CHENG Y, et al. Effect of Anchang Yuyang Decoction on colon tissue TFF3, MUC2 and TLR4 expressions in rats with ulcerative colitis[J]. Chinese Journal of Gastroenterology, 2016, 21(2): 85-89. DOI:10.3969/j.issn.1008-7125.2016.02.005 |
| [9] |
迟莉丽, 孙大娟, 梁峻尉, 等. 中药安肠愈疡汤对溃疡性结肠炎大鼠结肠组织中IL-6、IL-13含量及NF-κB表达的影响[J]. 世界中医药, 2016, 11(1): 113-116. CHI L L, SUN D J, LIANG J W, et al. Effect of Anchang Yuyang Decoction on the expression of IL-6, IL-13 and NF-κB in ulcerative colitis mice[J]. World Chinese Medicine, 2016, 11(1): 113-116. DOI:10.3969/j.issn.1673-7202.2016.01.030 |
| [10] |
ELROD J W, LAROUX F S, HOUGHTON J, et al. DSS-induced colitis is exacerbated in STAT-6 knockout mice[J]. Inflammatory Bowel Diseases, 2010, 11(10): 883-889. |
| [11] |
FAN H, LIANG L, TANG Q, et al. Effects of Wumeiwan on the expression ofSTAT6 in rats with ulcerative colitis[J]. Research of Integrated Traditional Chineseand Western Medicine, 2011, 3(3): 127-131. |
| [12] |
杨立, 肖明明. STAT6蛋白在实验性结肠炎大鼠中的表达及其对细胞因子IFN-γ和IL-4的影响[J]. 胃肠病学和肝病学杂志, 2015, 24(11): 1341-1345. YANG L, XIAO M M. Expression of STAT6 in the intestinal mucosa of rats with TNBS induced experimentalcolitis and its influence on cytokines IFN-γ and IL-4[J]. Chinese Journal of Gastroenterology and Hepatology, 2015, 24(11): 1341-1345. |
| [13] |
COSINROGER J, ORTIZMASIA D, CALATAYUD S, et al. The activation of Wnt signaling by a STAT6-dependent macrophage phenotype promotes mucosal repair in murine IBD[J]. Mucosal Immunology, 2016, 9(4): 986-998. DOI:10.1038/mi.2015.123 |
| [14] |
HALLER D, HOLT L, PARLESAK A. Differential effect of immune cells on non-pathogenic Gram-negative bacteria-induced nuclear factor-κB activation and pro-inflammatory gene expression in intestinal epithelial cells[J]. Immunology, 2004, 112(2): 310-320. |
| [15] |
WU W, ZHEN Z, NIU T, et al. κ-Carrageenan enhances lipopolysaccharide-induced Interleukin-8 secretion by stimulating the Bcl10-NF-κB pathway in HT-29 cells and aggravates freundii-induced inflammation in mice[J]. 2017, 2017(1-4): 863-865. DOI:10.1155/2017/8634865 |
| [16] |
胡品津, 钱家鸣, 吴开春, 等. 我国炎症性肠病诊断与治疗的共识意见(2012年·广州)[J]. 内科理论与实践, 2013, 8(1): 61-75. HU P J, QIAN J M, WU K C, et al. Consensus on the diagnosis and treatment of inflammatory bowel disease in China (Guangzhou, 2012)[J]. Journal of Internal Medicine Concepts & Practice, 2013, 8(1): 61-75. |
| [17] |
吴开春, 梁洁, 冉志华, 等. 炎症性肠病诊断与治疗的共识意见(2018年·北京)[J]. 中国实用内科杂志, 2018, 38(9): 796-813. WU K C, LIANG J, RAN Z H, et al. Chinese consensus on diagnosis and treatment of inflammatory bowel disease(Beijing, 2018)[J]. Chinese Journal of Practical Internal Medicine, 2018, 38(9): 796-813. |
| [18] |
BLANCHARD C, DURUAL S, ESTIENNE M, et al. IL-4 and IL-13 up-regulate intestinal trefoil factor expression:requirement for STAT6and de novo protein synthesis[J]. Journal of Immunology, 2004(172): 3775-3783. DOI:10.4049/jimmunol.172.6.3775 |
| [19] |
VILLARINO A V, KANNO Y, O'SHEA J J. Mechanisms and consequences of Jak-STAT signaling in the immune system[J]. Nature Immunology, 2017, 18(4): 374-384. |
| [20] |
BANERJEE S, BIEHL A, GADINA M, et al. JAK-STAT signaling as a target for inflammatory and autoimmune diseases:current and future prospects[J]. Drugs, 2017, 77(2): 521-546. |
| [21] |
GOENKA S, KAPLAN M H. Transcriptional regulation by STAT6[J]. Immunologic Research, 2011, 50(1): 87-96. DOI:10.1007/s12026-011-8205-2 |
| [22] |
ARCHAMBAUD C, SANSONI A, MINGUENEAU M, et al. STAT6 deletion converts the Th2 inflammatory pathology afflicting LatY136F mice into alymphoproliferative disorder involving Th1 and CD8 effector T Cells[J]. The Journal of Immunology, 2009, 182(5): 2680-2689. DOI:10.4049/jimmunol.0803257 |
| [23] |
ELROD J W, LAROUX F S, HOUGHTON J, et al. DSS-induced colitis is exacerbated in STAT-6 knockout mice[J]. Inflammatory Bowel Diseases, 2010, 11(10): 883-889. |
| [24] |
SHIH M F, CHEN L Y, TSAI P J, et al. In vitro and in vivo therapeutics of β-thujaplicin on LPS-induced inflammation in macrophages and septic shock in mice[J]. International Journal of Immunopathology and Pharmacology, 2012, 25(1): 39-48. DOI:10.1177/039463201202500106 |
| [25] |
HU L L, SUN C, WANG S N, et al. Lipopolysaccharide neutralization by a novel peptide derived from phosvitin[J]. International Journal of Biochemistry & Cell Biology, 2013, 45(11): 2622-2631. |
| [26] |
HEIKE B, CHRISTOPH B, MICHAEL V, et al. Mesalazine inhibits activation of transcription factor NF-kappaB in inflamed mucosa of patients with ulcerative colitis[J]. American Journal of Gastroenterology, 2000, 95(12): 3452-3457. |
2. The First Clinical Medical School, Shandong University of Traditional Chinese Medicine, Jinan 250014, China
 2020, Vol. 37
2020, Vol. 37