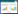文章信息
- 何朝凯, 刘春香, 王辉, 张俊华
- HE Chaokai, LIU Chunxiang, WANG Hui, ZHANG Junhua
- 中医药治疗乳腺癌随机对照试验结局指标分析
- Outcome measures analysis of ranomized controlled trials in traditional Chinese medicine treating breast cancer
- 天津中医药, 2021, 38(10): 1299-1304
- Tianjin Journal of Traditional Chinese Medicine, 2021, 38(10): 1299-1304
- http://dx.doi.org/10.11656/j.issn.1672-1519.2021.10.16
-
文章历史
- 收稿日期: 2021-04-30
2. 中国医学科学院北京协和医院, 北京 100730
目前,在医疗、护理、康复、营养以及精神卫生等健康领域的临床研究中普遍存在结局指标选择、测量和报告不一致、不实用性、不规范性等问题,甚至一些至关重要的结果可能被低估或完全忽视[1-6]。为了得到实用性、可靠性更高的研究结果,使之成为患者、医疗健康专业者和卫生政策制定者等决策时的重要参考依据,研究者在进行临床试验和系统评价时需要高度重视结局指标报告的规范化[7]。
核心指标集(COS)是一组关于健康卫生行业中特定领域的所有临床试验被要求测量和报告的最少化、共识化的指标集合[8]。COS研究通过候选条目产生、两轮Delphi问卷调查、举办多方共识会议这3个阶段与18条最基本的报告条目要求来产生标准化的指标集合,从而在临床研究结局指标的选择和报告上达成共识[9],以提高同类研究指标的一致性和实用性[10],避免同类研究结果因异质性无法进行合并与比较所造成的不必要的资源浪费[11-12]。
中医药临床研究的结局指标问题同样较多,且有一定的特殊性,迫切需要探索形成符合自身特点的COS[13-14]。本研究采用COS研究的方法,通过对近5年中医药治疗乳腺癌随机对照试验(RCT)进行收集,分析研究报告的结局指标及存在的问题,为构建中医药防治乳腺癌核心指标集奠定基础。
1 资料与方法 1.1 纳入与排除标准 1.1.1 纳入标准1)研究类型:随机对照试验,语言限定为英文和中文。2)患者类型:明确符合乳腺癌诊断标准的患者,不受乳腺癌病理类型、乳腺癌临床分期、病程、年龄、种族和地域的限制。3)干预措施:观察组单独或联合使用中医药相关疗法,包括中药方剂和中成药,对照措施不进行限制。4)结局指标:提取纳入研究中报告的所有结局指标。
1.1.2 排除标准1)合并其他疾病的研究。2)以针灸、推拿、中药熏洗、穴位注射、穴位贴敷等为干预措施的研究。3)学位论文。4)综述性文章。5)重复发表的研究。
1.2 文献检索采用自由词和主题词结合的方式检索Cochrane Library、Pubmed、Embase、Web of Science、SinoMed、万方数据和中国知网(CNKI)数据库。检索时间为2014年1月—2019年10月。中文检索词为“乳腺癌”“乳腺肿瘤”“临床试验”“临床研究”“临床观察”“临床评价”“临床调查”“随机对照试验”“中医”“中药”等。英文检索词为“Breast Neoplasms”“Breast Cancer”“Breast Tumor” “Traditional Chinese Medicine”“herbal medicine”“zhongyi”“zhongyao”“Clinical Trial”“Randomized Controlled Trial”等。
1.3 文献筛选与资料提取由两名评价者独立阅读题目和摘要,排除明显不符合纳入标准的研究,对可能符合纳入标准的研究阅读全文,确定是否纳入,并提取资料,交叉核对。如遇分歧,经讨论解决。
采用预先设计的Excel表格对纳入文献进行资料提取,主要内容包括:1)研究的基本信息,包括题目、第一作者、发表年限、发表期刊等。2)研究对象的基线情况,包括人口学特征如例数、年龄,以及临床特征如病理分型、临床分期、病程、中医证型等。3)干预措施,包括药物名称、疗程、频次、用量等。4)结局指标及其测量方法和评价时间点。
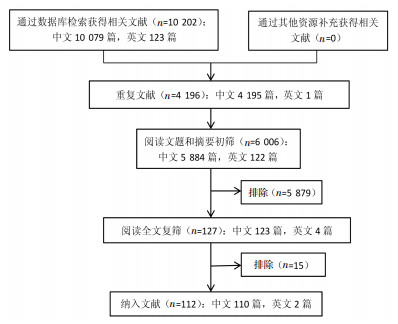
2 结果 2.1 文献筛选流程根据检索策略初检获得10 202篇相关文献,删除重复文献后,根据纳入排除标准,经筛选后最终纳入112篇文献,其中中文110篇,英文2篇。见图 1。
|
| 图 1 文献筛选流程 Fig. 1 Literature screening flow |
112个RCT研究中共包含9 430例患者,其中观察组4 738例,对照组4 692例,年龄范围17~80岁。样本量范围为20~620例,研究的平均样本量为84例。
2.2.2 病程共有23个(23/112,21%)研究报告了病程,具体病程为0~25年,89个研究未报告病程。
2.2.3 病理分型共53个(53/112,47%)研究报告了乳腺癌患者的病理分型,主要包括乳头状癌、髓样癌、小管癌、黏液腺癌、鳞状细胞癌、浸润性导管癌、浸润性小叶癌和腺癌等。
2.2.4 临床分期65个(65/112,58%)研究报告了具体临床分期,根据国际抗癌联盟(UICC)和美国癌症联合会(AJCC)联合制定的乳腺癌TNM分期法分为Ⅰ~Ⅳ期。
2.2.5 中医证型报告中医证型的研究共25个(25/112,22%),包括气阴两虚、气血两虚、正气亏虚、中阳气虚、气虚、血虚、肾虚、肾阴虚、肝肾阴虚、肝郁痰凝、肝瘀痰凝、肝郁脾虚、肝郁气滞、瘀毒蕴结、冲任失调、正虚毒炽、心脾两虚、脾虚痰湿、脾胃虚弱、脾胃湿热、脾胃虚寒,共21种证型。
2.2.6 干预措施干预措施分为中药汤剂和中成药两种类型,分别有62个和49个研究,另有1项研究采用汤剂结合中成药疗法。其中中成药22个为注射液,28个为口服制剂。
2.2.7 疗程除5个研究未报告疗程相关信息外,其余107项RCT均报告试验疗程。疗程为7 d~5年,具体分布为:疗程≤2周有3个(2.6%),疗程2~4周有7个(6.3%),疗程4~8周有34个(30.4%),疗程8周~6个月有53个(47.3%),疗程6个月以上共10个(8.9%)。
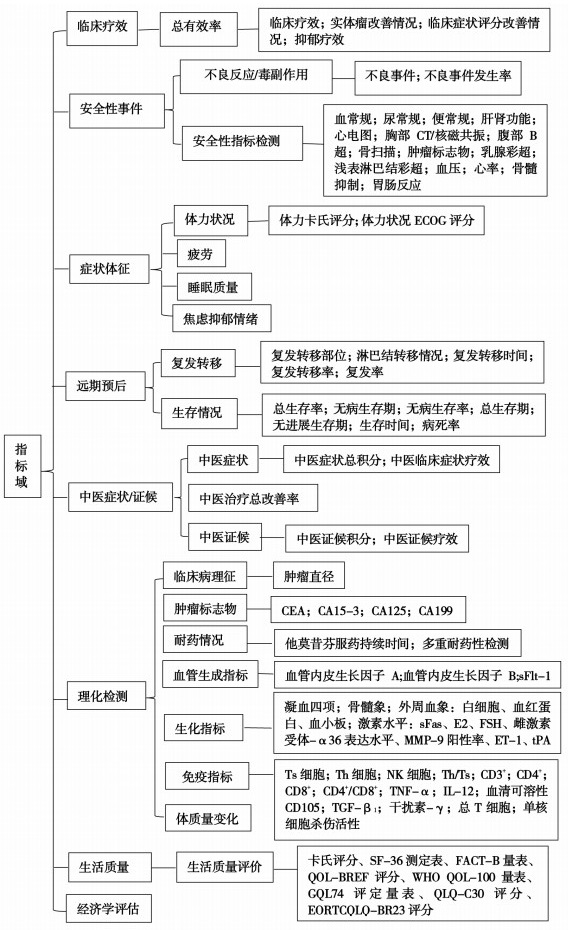
2.3 结局指标 2.3.1 指标域纳入研究报告的所有结局指标共61项,单个研究报告的最少结局指标为1个,最多为7个,每项研究平均报告3个。根据指标的功能属性,将纳入研究的所有结局指标归类为临床疗效、中医症状/证候、症状体征、理化检测、生活质量、远期预后、经济学评估和安全性事件8个域。见图 2。
|
| 注:ECOG评分:美国东部肿瘤协作组织体力状态评分量表;CEA:癌胚抗原;CA15-3:糖类抗原15-3;CA125:糖类抗原125;CA199:糖类抗原199;Ts细胞:抑制性T淋巴细胞;Th细胞:辅助性T淋巴细胞;NK细胞:自然杀伤细胞;CD3+:成熟T淋巴细胞;CD4+:辅助性T淋巴细胞;CD8+:细胞毒性T细胞;TNF-α:肿瘤坏死因子α;IL-12:白细胞介素-12;TGF-β1:转化生长因子β1蛋白;sFlt-1:人血管内皮生长因子可溶性受体1;sFas:血浆可溶性死亡分子;E2:雌二醇;t-PA:组织型纤溶酶原激活剂;MMP-9:基质金属蛋白酶;FSH:促卵泡激素;ET-1:内皮素-1;SF-36测定表:健康调查测定简表;FACT-B量表:乳腺癌患者生命质量测定量表;QOL-BREF评分:生存质量测定量表简表;WHO QOL-100量表:世界卫生组织生存质量测定量表;GOL-74评定量表:生活质量综合评定量表;QLQ-C30评分:欧洲癌症治疗研究组织生命质量测定量表;EORTC-QLQ-BR23评分:乳腺癌特异性量表。 图 2 指标域 Fig. 2 Outcome measures field |
在所有纳入文献中,结局指标使用率排前15位的依次为:临床疗效、不良反应、生活质量、肿瘤标志物、生存情况、免疫功能指标、安全性评价、复发转移情况、中医证候积分、中医证候疗效、中医症状积分、血管生成指标、体力状况、骨髓抑制、睡眠质量。见表 1。
其中,临床疗效的评价标准以世界卫生组织拟定的实体瘤客观评价标准为依据,主要分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),临床受益率=CR+PR+SD。
2.3.3 指标组合结局指标组合使用情况的统计结果显示,有10个研究同时使用临床疗效、不良反应、生活质量3个指标;有4个研究同时使用临床疗效、不良反应两个指标;有4个研究同时使用临床疗效、不良反应、安全性评价3个指标;有3个研究同时使用临床疗效、不良反应、免疫功能3个指标。具体的结局指标组合类型多达82种。不同指标组合使用频数详见开放科学(资源服务)标识码(OSID)。
2.3.4 测量时间点频次排列前5位的有效性指标测量时间点如下。1)临床疗效:83项研究采用临床疗效指标,测量的时间点共14个,3项研究未报告时间点,其中20个研究(24.1%)选择在治疗6周后测量,15个研究(18.1%)为治疗12周后测量,12个研究(14.5%)为治疗8周后测量,10个研究(12.0%)为治疗9周后测量。2)肿瘤标志物:26项研究共报告9个测量时间点,9个研究(34.6%)选择在治疗6周后测量,其次为治疗9周后(5/26,19.2%)。3)免疫功能指标:22项研究共9个测量时间点,以治疗6周后进行测量的最多(6/22,27.3%),其次为9周(4/22,18.2%)。4)中医证候积分:8个研究选择了中医证候积分指标,2项(25%)研究在治疗6周后进行测量。5)中医证候疗效:8个研究选择了中医证候疗效指标,2项(25%)研究在治疗6周后进行测量,另有2项(25%)研究在治疗9周后进行测量。详见OSID。
3 讨论有学者在对中医药治疗心绞痛临床试验COS研究中指出,原始研究所报告的结局指标存在差异性大、不规范和不实用等问题[13, 15]。本研究中同样发现相似的问题,但以指标组合过于随意、指标测量方法差异性大和指标报告不规范这3个问题更为突出。
本研究在对中医药治疗乳腺癌随机对照试验的结局指标分类整理过程中发现,原始研究在选择和报告结局指标时主要存在以下6个方面的问题。
1)缺乏终点指标,临床实用性不强。对于肿瘤的疗效评价,最具临床价值的指标是预后,而现有研究中过多的中间指标被研究者所使用,缺少对生存期等的报告。本研究中,仅17项(15.2%)纳入研究报告了患者生存期,10项(8.9%)报告了生存率,2项(1.8%)报告了死亡情况。
2)指标组合过于随意。在112个RCT中就出现了多达82种不同的指标组合类型,组合条目有2~7条不等,随意性较大。其中,仅4个指标组合使用的类型就有29种,且在所有组合类型中单个组合的使用频次普遍不高。如使用频次最高的临床疗效、不良反应、生活质量这一组合指标仅为10次,其余大多为1次。
3)同一指标的测量时间点不统一,缺少远期效应观测。如临床疗效这一指标的测量时间点就多达14个,且大部分研究的指标测量时间点多在12周以内。对于肿瘤治疗来说,长期随访的结果评价是关键,但目前中医药治疗乳腺癌的研究,缺乏对远期预后结果的测量与评价。
4)相同指标测量方法差异性大。如在进行生活质量评价时,研究者采用了8个不同的测评量表。部分结局指标的评价标准也不尽相同,也存在自拟评价标准的情况。
5)指标报告不规范。主要体现在指标变量类型随意转换、指标名称不规范和不同指标存在相似交叉条目这3个方面。如临床疗效、生存情况和中医症状疗效等连续性变量被转化成等级资料进行报告,多用显效、有效、无效、总有效率、总生存率等形式。同一指标存在错用或乱用不同名称进行报告的情况,如部分研究将KPS评分报告为生活质量评分,而另一部分研究却报告为体力状况或功能状态评分。此外,还有研究在报告结局指标时存在条目交叉重复报告的情况。如生活质量评分中包含了躯体功能、心理功能、社会功能和物质生活状态4个维度,在临床疗效、中医症状疗效和睡眠质量评分等条目中均有重复交叉的内容。
6)自拟症状或证侯积分,缺乏能体现中药特色效果的特异性指标。在所有纳入研究中,仅18%左右的研究报告了中医相关指标。
本研究还对所有指标的使用频次进行了统计,为核心指标集条目池的构建提供数据支持。这些在原始文献中使用频次高的指标将被推荐为候选指标条目进入初选条目池,然后通过Delphi调查和多方共识会议,最终形成中医药治疗乳腺癌的临床研究COS。
4 局限性与展望本研究纳入的原始研究类型较为单一,且文献限定为近5年发表,样本的代表性存在一定的局限。未来的研究应该进一步扩充纳入研究的类型,如病例报告文献、注册研究方案等,同时扩大文献的年限跨度进行补充和对比研究,为COS的制定提供更为全面的初始条目池。
5 结论中医药治疗乳腺癌相关临床研究所报告的结局指标主要存在终点指标过少、远期效应测量缺乏等临床实用性差的问题;同时还存在组合过于随意、测量方法差异性大、表达不规范、数量不一致以及测量时间点跨度大等异质性过高的问题。因此,需要构建公认的中医药核心指标集,以提高中医药临床研究的质量,减少不必要的资源浪费。
| [1] |
BEUSCART J B, DALLEUR O, BOLAND B, et al. Development of a core outcome set for medication review in older patients with multimorbidity and polypharmacy: a study protocol[J]. Clinical Interventions in Aging, 2017, 12: 1379-1389. DOI:10.2147/CIA.S135481 |
| [2] |
KARAS J, ASHKENAZI S, GUARINO A, et al. Developing a core outcome measurement set for clinical trials in acute diarrhoea[J]. Acta Paediatrica, 2016, 105(4): e176-e180. DOI:10.1111/apa.13349 |
| [3] |
SMITH S M, WALLACE E, SALISBURY C, et al. A core outcome set for multimorbidity research(COSmm)[J]. Annals of Family Medicine, 2018, 16(2): 132-138. DOI:10.1370/afm.2178 |
| [4] |
WEBSTER L, GROSKREUTZ D, GRINBERGS-SAULL A, et al. Development of a core outcome set for disease modification trials in mild to moderate dementia: a systematic review, patient and public consultation and consensus recommendations[J]. Health Technology Assessment, 2017, 21(26): 1-192. DOI:10.3310/hta21260 |
| [5] |
BLACKWOOD B, MARSHALL J, ROSE L. Progress on core outcome sets for critical care research[J]. Current Opinion in Critical Care, 2015, 21(5): 439-444. DOI:10.1097/MCC.0000000000000232 |
| [6] |
GARGON E, GURUNG B, MEDLEY N, et al. Choosing important health outcomes for comparative effectiveness research: a systematic review[J]. PLoS One, 2014, 9(6): e99111. DOI:10.1371/journal.pone.0099111 |
| [7] |
KIRKHAM J J, DAVIS K, ALTMAN D G, et al. Core outcome set-standards for development: the COS-STAD recommendations[J]. PLoS One, 2017, 14(11): e1002447. |
| [8] |
KIRKHAM J J, GORST S, ALTMAN D G, et al. COS-STAR: a reporting guideline for studies developing core outcome sets (protocol)[J]. Trials, 2015, 16: 373. DOI:10.1186/s13063-015-0913-9 |
| [9] |
KIRKHAM J J, GORST S, ALTMAN D G, et al. Core outcome set-standards for reporting: the COS-STAR statement[J]. PLoS One, 2016, 13(10): e1002148. |
| [10] |
CHIAROTTO A, OSTELO R W, TURK D C, et al. Core outcome sets for research and clinical practice[J]. Brazilian Journal of Physical Therapy, 2017, 21(2): 77-84. DOI:10.1016/j.bjpt.2017.03.001 |
| [11] |
CHALMERS I, GLASZIOU P. Avoidable waste in the production and reporting of research evidence[J]. Lancet, 2009, 374(9683): 86-89. DOI:10.1016/S0140-6736(09)60329-9 |
| [12] |
HIRSCH B R, CALIFF R M, CHENG S K, et al. Characteristics of oncology clinical trials: insights from a systematic analysis of ClinicalTrials.gov[J]. JAMA Internal Medicine, 2013, 173(11): 972-979. DOI:10.1001/jamainternmed.2013.627 |
| [13] |
张明妍, 张俊华, 张伯礼. 2015年中药治疗稳定性心绞痛临床试验结局指标文献研究[J]. 中国中西医结合杂志, 2018, 38(2): 191-197. ZHANG M Y, ZHANG J H, ZHANG B L. Outcome measures of clinical trials of stable angina pectoris treated by Chinese medicine in 2005:literature research[J]. Chinese Journal of Integrated Traditional and Western Medicine, 2018, 38(2): 191-197. |
| [14] |
邢冬梅, 张俊华, 张伯礼. 中医临床研究核心结局指标集形成路径[J]. 中华中医药杂志, 2014, 29(5): 1352-1355. XING D M, ZHANG J H, ZHANG B L. Approach to developing core outcome sets for clinical trials of traditional Chinese medicine[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2014, 29(5): 1352-1355. |
| [15] |
王可仪, 金鑫瑶, 王虎城, 等. 中医药治疗不稳定型心绞痛临床研究指标分析[J]. 天津中医药, 2020, 37(10): 1150-1155. WANG K Y, JIN X Y, WANG H C, et al. Analysis of clinical index of Chinese medicine in treatment of unstable angina pectoris[J]. Tianjin Journal of Traditional Chinese Medicine, 2020, 37(10): 1150-1155. DOI:10.11656/j.issn.1672-1519.2020.10.17 |
2. Peking Union Medical College Hospital, Chinese Academy of Medical Sciences, Beijing 100730, China
 2021, Vol. 38
2021, Vol. 38