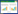文章信息
- 汤艳莉, 王继明, 杨萃, 庄庭怡, 付金萍
- TANG Yanli, WANG Jiming, YANG Cui, ZHUANG Tingyi, FU Jinping
- 连花清瘟制剂对COVID-19疗效的Meta分析
- Effect of Lianhua Qingwen preparation on COVID-19: a Meta-analysis
- 天津中医药, 2021, 38(11): 1414-1420
- Tianjin Journal of Traditional Chinese Medicine, 2021, 38(11): 1414-1420
- http://dx.doi.org/10.11656/j.issn.1672-1519.2021.11.12
-
文章历史
- 收稿日期: 2020-12-10
新型冠状病毒肺炎(COVID-19)是指感染2019新型冠状病毒(SARS-CoV-2)导致的肺炎,其临床表现以发热、干咳、乏力等为主要症状,少数患者可伴见鼻塞、流涕、腹泻等上呼吸道和消化道症状。COVID-19的出现和迅速增加给全球公共卫生、研究界和医学界带来了挑战。在临床治疗方面,临床多采用对症支持治疗及综合干预。
连花清瘟制剂(颗粒剂型、胶囊剂型)由连翘、金银花、炙麻黄、炒苦杏仁、石膏、板蓝根、绵马贯众、鱼腥草、广藿香、大黄、红景天、薄荷脑、甘草等组成,可以清瘟解毒,宣肺泄热[1]。现代药理学研究表明,本方具有较好的广谱抗病毒、抑菌、退热、抗炎、止咳、化痰、调节免疫等作用,可用于呼吸系统病毒性疾病的治疗[2]。连花清瘟制剂对甲型流感病毒(H1N1、H3N2)、乙型流感病毒、禽流感病毒(H5N1、H9N2、H7N9)、冠状病毒等以及多种普通感冒病毒都具有广谱抗病毒作用,且同时可以有效抑制多种细菌[3]。在COVID-19的治疗过程中,连花清瘟制剂已被《新型冠状病毒感染的肺炎诊疗方案》(第四版)列为推荐用药。
目前,国内外有许多临床和实验研究对连花清瘟制剂治疗COVID-19进行了报道[4-6],但由于受到检索策略、临床研究方法、样本量等因素局限,其对COVID-19的临床证据有待进一步深化。本研究通过系统检索国内外文献,纳入连花清瘟制剂干预COVID-19的临床随机对照试验(RCT)研究进行系统综述及Meta分析,以期对中药连花清瘟制剂干预COVID-19的临床效果提供依据,并对相应的基础实验研究起到一定的指导作用。
1 资料与方法 1.1 纳入与排除标准 1.1.1 研究类型国内外公开发表的关于连花清瘟制剂(颗粒剂型、胶囊剂型)治疗COVID-19的RCT,在研究过程中不限于是否采用盲法,出版语言为中文或英文。
1.1.2 研究对象1)符合《新型冠状病毒感染的肺炎诊疗方案》中的COVID-19的诊断标准。2)性别、民族不限。
1.1.3 干预措施1)试验组为连花清瘟制剂(颗粒剂型、胶囊剂型),服药方式、剂量及方案均按照说明书给药;对照组为常规西药治疗,或常规西药联合中药安慰剂治疗。2)两组均采用常规西药治疗或标准治疗,试验组在此基础上加用连花清瘟制剂。
1.1.4 结局指标1)主要结局指标:发热(症状积分、退烧时间)。2)次要结局指标:咳嗽(症状积分、改善时间),乏力(症状积分、改善时间)、临床有效率、肺部CT、轻症转重症例数、炎症指标。3)安全性指标:不良反应发生的例数及临床表现。
1.1.5 排除标准1)个案报道、病例系列研究等非随机对照临床试验。2)综述、述评、动物实验、细胞实验等基础研究类型文献。3)治疗组干预措施中除连花清瘟制剂外,还包括其他中药、中成药、中药注射液、针灸、拔罐、穴位贴敷等干预措施的临床文献。4)临床研究的对照组合并采用包含其他中医药治疗方法的文献。5)重复发表的文献。
1.2 检索策略主要采取计算机检索的方式。检索的外文数据库包括PubMed、MEDLINE、荷兰医学文摘Embase、考科蓝协作网(Cochrane Collaboration)等数据库;中文数据库包括中国知网(CNKI)、维普(VIP)、万方医学网、中国生物医学文献数据库(CBM)。检索语言为中文和英文。文献检索时限均从建库至2020年5月。中文检索词:连花清瘟制剂、连花清瘟、连花清瘟颗粒、连花清瘟胶囊、新型冠状病毒肺炎、新冠肺炎、COVID-19、2019冠状病毒病、新型冠状病毒、随机对照试验、临床观察;英文检索词:Lianhua Qingwen preparations、Lianhua Qingwen、Lianhua Qingwen granule、Lianhua Qingwen capsule、novel coronavirus pneumonia、coronavirus diseases 2019、COVID-19、novel coronavirus、2019-nCoV、SARS-CoV-2、randomized controlled trial、controlled trial、randomized、randomly、trial。
1.3 文献筛选、资料及数据提取及质量评价由2名研究者独立进行文献检索、阅读题目及摘要,对可能符合纳入标准的文献进一步阅读全文。当意见不一致时,通过讨论,或者通过第三者参与讨论解决。选定文献之后,由2名研究者独立按事先设定的资料提取表格提取相关资料,提取资料后,再进行交叉核对。当出现两者意见不一致时,通过讨论,或者通过第三者参与讨论解决。相关资料的提取内容包括:作者、发表年份、病例来源、随机化方法、随机分配方案的隐藏情况、是否采用盲法(研究者、患者、分析者)、是否采用安慰剂、分组、样本量、干预方式(药物名称、剂量、给药途径和疗程)、受试者年龄、性别、基线资料等基本情况、失访/退出情况、结局指标、安全性指标等。根据《Cochrane干预措施系统评价手册》[7]中的文献质量评价标准,由2名研究者分别对纳入文献的临床试验质量进行评价。当意见不一致时,通过讨论,或者通过第三者参与讨论解决。
1.4 统计学方法采用Review manager 5.3软件对该项目纳入的临床试验资料进行Meta分析。计数资料采用相对危险度(RR)表示效应量。计量资料以加权均数差值(WMD)及其95%可信区间(CI)为统计效应量。各研究间的异质性则采用χ2检验。当Meta分析结果显示无异质性,即异质性检验P > 0.1或I2<50%时,选择固定效应模型进行效应量的合并分析;反之,则认为存在异质性,可选择随机效应模型计算其合并效应量,并谨慎解释研究结果。如果纳入研究的临床试验数量较多,则采用漏斗图分析可能的发表偏倚,否则不予进行分析。
2 结果 2.1 文献检索结果初检英文文献65篇,中文文献97篇;最终纳入研究文献5篇[9-13],其中,英文文献1篇,中文文献4篇。5项研究中共824例患者,治疗组424例,对照组400例。见图 1。
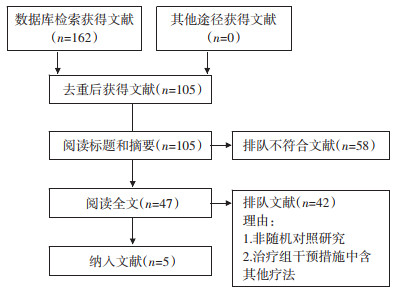
|
| 图 1 文献筛选流程图 Fig. 1 Literature screening flow chart |
所纳入的临床研究的基本特征见表 1。根据《Cochrane干预措施系统评价手册》,对所纳入的5项RCT进行方法学的质量评价,结果如图 2所示。所有的临床试验均提及“随机”,其中,有2篇临床研究明确报道了随机序列生成的方法[8, 12];随机分配方案的隐藏均没有报道;实施偏倚评价,仅有1篇英文文献报道了单盲[8],其余文献均未报道双盲及安慰剂对照;所有5篇文献[8-12]报道的研究均为试验组在对照组基础西药治疗上加用中药干预;随访偏倚评价,所有文献报告了纳入研究与完成研究的例数,均不存在脱落现象;所有文献均报道研究方案的所有结局指标。
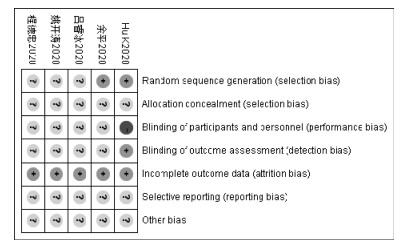
|
| 图 2 纳入研究的质量评价 Fig. 2 Quality evaluation of included studies |
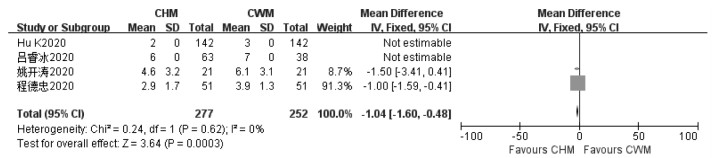
5项研究均报道了连花清瘟制剂对发热的临床疗效。4项研究报道了退热时间[8-11];1项研究报道了退热的例数[10];1项研究报道了发热症状积分[12]。其中,在退热时间方面,异质性检验P=0.62,I2=0%,采用固定效应模型进行Meta分析。结果显示,试验组与对照组比较退热时间更短,差异有统计学意义(MD=-1.04,95%CI=-1.60~ -0.48,P=0.000 3)(见图 3),表明联合应用连花清瘟制剂治疗具有显著缩短退热时间的作用。在退热例数方面,虽然差异没有统计学意义,但试验组较对照组显示出更好的退热趋势。在发热症状积分方面,与对照组相比,试验组发热积分显著低于对照组。
|
| 图 3 连花清瘟制剂对COVID-19患者发热影响的Meta分析 Fig. 3 Meta-analysis of the influence of Lianhua Qingwen preparation on fever in COVID-19 patients |
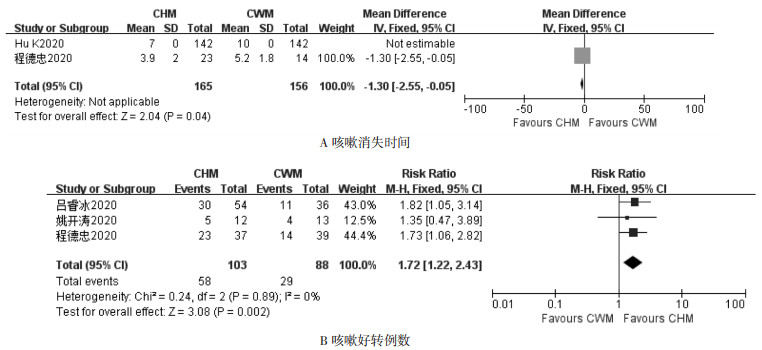
5项研究均报道了连花清瘟制剂对咳嗽的临床疗效。2项研究报道了咳嗽症状消失时间[8-9];3项研究报道了咳嗽好转的例数[9-11];1项研究报道了咳嗽症状积分[12]。其中,在咳嗽症状消失时间方面,采用固定效应模型进行Meta分析。结果显示,试验组与对照组相比咳嗽消失时间更短,差异有统计学意义(MD=-1.30,95%CI=-2.55~ -0.05,P=0.04),见图 4A,表明联合应用连花清瘟制剂治疗具有显著缩短咳嗽时间的作用。在咳嗽好转例数方面,异质性检验P=0.89,I2=0%,采用固定效应模型进行Meta分析。结果显示,试验组与对照组相比,差异没有统计学意义(RR=1.72,95%CI=1.22~2.43,P=0.002),见图 4B,表明联合应用连花清瘟制剂治疗具有显著减少咳嗽患者例数的作用。在咳嗽症状积分方面,与对照组相比,试验组咳嗽积分显著优于对照组。
|
| 图 4 连花清瘟制剂对COVID-19患者咳嗽影响的Meta分析 Fig. 4 Meta-analysis of the effect of Lianhua Qingwen preparation on cough in COVID-19 patients |
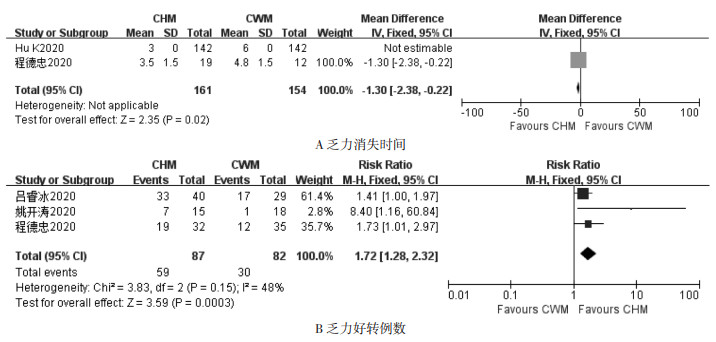
5项研究均报道了连花清瘟制剂对乏力的临床疗效。2项研究报道了乏力症状消失时间[8-9];3项研究报道了乏力好转的例数[9-11];1项研究报道了乏力症状积分[12]。其中,在乏力症状消失时间方面,采用固定效应模型进行Meta分析。结果显示,与对照组相比,试验组乏力消失时间更短,差异有统计学意义(MD=-1.30,95%CI=-2.38~ -0.22,P=0.02),见图 5A,表明联合应用连花清瘟剂治疗具有显著缩短乏力症状持续时间的作用。在乏力好转例数方面,异质性检验P=0.15,I2=48%,采用固定效应模型进行Meta分析。结果显示,试验组与对照组相比,差异没有统计学意义(RR=1.72,95%CI=1.28~2.32,P=0.000 3),见图 5B,表明联合应用连花清瘟制剂治疗具有显著减少乏力患者例数的作用。在乏力症状积分方面,与对照组相比,试验组乏力积分显著优于对照组。
|
| 图 5 连花清瘟制剂对COVID-19患者乏力影响的Meta分析 Fig. 5 Meta-analysis of the effect of Lianhua Qingwen preparation on fatigue in COVID-19 patients |
3项研究[8-9, 12]报告了临床有效率,研究间异质性较小(P=0.88,I2=0%),采用固定效应模型进行Meta分析。结果显示,试验组与对照组比较临床有效率差异具有统计学意义(RR=1.23,95%CI=1.12~1.34,P<0.000 1),见图 6,表明联合应用连花清瘟制剂治疗能够显著提升临床有效率。
|
| 图 6 连花清瘟制剂对COVID-19患者临床有效率影响的Meta分析 Fig. 6 Meta-analysis of the effect of Lianhua Qingwen preparation on the clinical effective rate in COVID-19 patients |
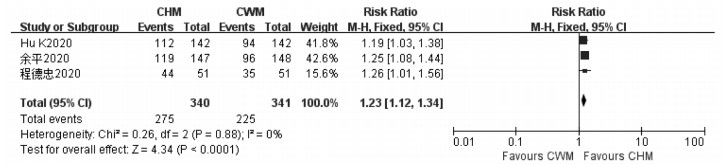
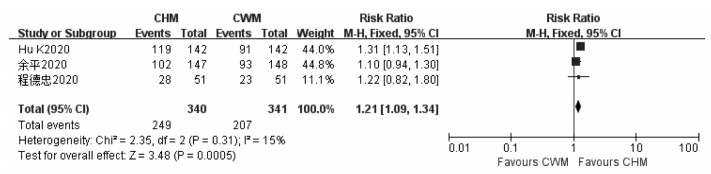
3项研究[8-9, 12]报告了肺部CT的临床疗效,研究间异质性较小(P=0.31,I2=15%),采用固定效应模型进行Meta分析。结果显示,试验组与对照组相比肺部CT好转例数更多,差异有统计学意义(RR=1.21,95%CI=1.09~1.34,P=0.000 5),见图 7,表明联合应用连花清瘟制剂治疗具有显著改善肺部CT的作用。
|
| 图 7 连花清瘟制剂对COVID-19患者肺部CT影响的Meta分析 Fig. 7 Meta-analysis of the effect of Lianhua Qingwen preparation on lung CT in COVID-19 patients |
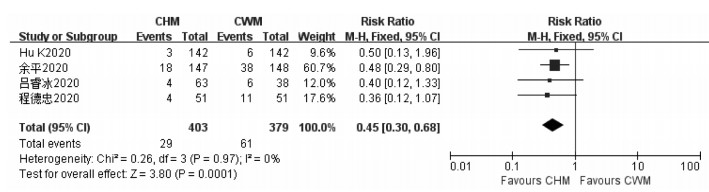
4项研究[8-9, 11-12]报告了轻症转重症例数,研究间异质性较小(P=0.97,I2=0%),采用固定效应模型进行Meta分析。结果显示,试验组与对照组相比轻症转重症例数更少,差异有统计学意义(RR=0.45,95%CI=0.30~0.68,P=0.000 1),见图 8,表明联合应用连花清瘟制剂治疗具有降低轻症转重症例数的作用。
|
| 图 8 连花清瘟制剂对COVID-19患者轻症转重症例数影响的Meta分析 Fig. 8 Meta-analysis of the effect of Lianhua Qingwen preparation on the number of patients with COVID-19 from mild to severe |
1项研究[12]报告了炎症指标,包括白细胞(WBC)及淋巴细胞(LYM)计数,C反应蛋白(CRP)及血小板(PCT)水平。与对照组比较,试验组在改善炎症指标方面显著优于对照组,WBC及LYM计数均得以显著上升,CRP及PCT水平均得以显著下降。
2.4 安全性评价共有2项研究[8, 11]报告了不良事件的发生情况,其中1项临床研究未发现不良反应[11],仅有1项临床研究详细描述不良反应[8]。共计142例,其中65例发生于试验组,77例发生于对照组。试验组中,Hu K等[8]的研究报告的不良反应包括肝功能异常、肾功能不全、头痛、恶心、呕吐、腹泻、食欲不振。两组均未出现严重不良反应,两组比较无统计学差异。
3 讨论与严重急性呼吸综合征(SARS)以及中东呼吸综合征(MERS)相似,COVID-19均由冠状病毒感染所致,其同源性高达85%以上,并可通过感染呼吸道上皮细胞而诱发肺炎[13]。COVID-19患者的主要临床症状包括发热、咳嗽、乏力,部分患者还会出现鼻塞、流涕、腹泻等表现。然而,在临床上仍缺乏治疗COVID-19的特效药物情况下,如何有效阻断疾病进展,减少轻症转重症的并发症是临床医生需要解决的问题。
在古代中医学中就有数千年的防治疫病的历史经验。《素问·刺法论》记载:“五疫之至,皆相染易,无问大小,病状相似。”汉代张仲景《伤寒论》中也有治疗外寒内热证型的麻杏石甘汤。至明代,医家吴又可在《温疫论》专门论述瘟疫防治,认为瘟疫为天地之间的异气、厉气、疫疠之气所致。清代吴鞠通提倡三焦辨证治疗外感温热病,并创制辛凉平剂银翘散为主治之方。
连花清瘟制剂即是来自于麻杏石甘汤与银翘散的加味方,具有卫气同治、表里双解、先证用药、截断病势、整体调节、多靶治疗等优势。根据Meta分析的结果,在常规西药标准治疗(对症治疗、支持治疗、抗病毒治疗、抗菌治疗等)的基础上联合连花清瘟制剂,不仅具有显著改善患者发热症状,缩短发热时间,而且还能减轻咳嗽、乏力症状,提高临床有效率,改善肺部CT,显著减少轻症转重症患者的例数。此外,此项Meta分析结果还提示联合应用连花清瘟制剂,能够升高WBC及LYM计数,显著降低CRP及PCT水平,提示该方具有一定的抗炎作用。在安全性评价上,共有2篇文献对安全性问题进行了报道,但仅有1篇Hu K的文献对不良事件进行详细描述,包括肝肾功能损伤,头痛及恶心、呕吐等消化道症状。虽然没有严重不良事件发生,其不良反应可能与疾病进展等因素相关,且作者认为其安全性较好,但考虑到多数临床研究未对不良事件进行详细的描述与报道,故对其安全性有待进一步强化。
本研究还存在如下局限性值得关注:在纳入文献的方法学质量方面,以中文文献研究为主,在随机序列方案的生成方法、随机分配方案的隐藏、盲法的实施等方面存在一定的局限。但该项目纳入的英文文献研究为随机、单盲、多中心、随机对照临床研究,在方法学上相对较高,具有较高的临床证据等级。在临床研究的纳入人群方面,目前主要以中国人群为主,可能具有一定的偏倚。在病死率方面,由于纳入人群均为轻型和普通型,尚未观察到该药对病死率的影响。在干预措施方面,由于基础治疗的常规西药不完全一致,导致研究结果存在潜在偏倚。在随访方面,鉴于COVID-19患者具有一定的“复阳”问题,所纳入的研究欠缺长期随访的临床资料,未对远期预后进行评价。
笔者通过对中药连花清瘟制剂干预COVID-19的有效性进行分析和对安全性进行评价,结果显示在常规西药标准治疗基础上联合中药连花清瘟制剂具有一定的改善症状、减少重症发生率、改善肺部CT及炎症指标等作用,且安全性较好。本研究对临床运用连花清瘟制剂治疗COVID-19提供了一定的循证依据。
| [1] |
贾振华, 吴以岭. 络病理论指导外感温病研究[J]. 环球中医药, 2010, 3(1): 26-28. JIA Z H, WU Y L. Study on exogenous febrile disease guided by collateral disease theory[J]. Global Traditional Chinese Medicine, 2010, 3(1): 26-28. DOI:10.3969/j.issn.1674-1749.2010.01.007 |
| [2] |
丁月文, 曾丽娟, 李润峰, 等. 连花清瘟颗粒抗呼吸道合胞病毒感染BALB/c小鼠的药效作用研究[J]. 广州中医药大学学报, 2016, 33(4): 540-544. DING Y W, ZENG L J, LI R F, et al. Pharmacodynamic action of Lianhua Qingwen Granule on BALB/c mice infected with respiratory syncytial virus[J]. Journal of Guangzhou University of Traditional Chinese Medicine, 2016, 33(4): 540-544. |
| [3] |
莫红缨, 柯昌文, 郑劲平, 等. 连花清瘟胶囊体外抗甲型流感病毒的实验研究[J]. 中药新药与临床药理, 2007, 18(1): 6-9. MO H Y, KE C W, ZHENG J P, et al. Experimental study on the anti influenza a virus of Lianhua Qingwen Capsule in vitro[J]. Traditional Chinese Drug Research and Clinical Pharmacology, 2007, 18(1): 6-9. |
| [4] |
杨猛, 杨少华, 杨眉, 等. 中药连花清瘟治疗新型冠状病毒肺炎的系统评价[J]. 中国药物评价, 2020, 37(2): 126-130. YANG M, YANG S H, YANG M, et al. Systematic review on the treatment of novel coronavirus pneumonia with Lianhua Qingwen[J]. Chinese Journal of Drug Evaluation, 2020, 37(2): 126-130. |
| [5] |
漆国栋, 漆伟, 江琼, 等. 连花清瘟结合西医方案对新冠肺炎普通型患者疗效的系统评价[J]. 中医药临床杂志, 2020, 32(7): 1195-1199. QI G D, QI W, JIANG Q, et al. Systematic review of Lianhua Qingwen combined with Western medicine for COVID-19 general type patients[J]. Clinical Journal of Traditional Chinese Medicine, 2020, 32(7): 1195-1199. |
| [6] |
张文斌, 刘利男, 王震, 等. 连花清瘟联合西医治疗新冠肺炎普通型患者疗效及安全性Meta分析[J]. 海南医学院学报, 2020, 26(14): 1045-1050. ZHANG W B, LIU L N, WANG Z, et al. Meta-analysis of the efficacy and safety of Lianhua Qingwen combined with Western medicine in the treatment of common patients with novel coronavirus pneumonia[J]. Journal of Hainan Medical University, 2020, 26(14): 1045-1050. |
| [7] |
HIGGINS J, GREEN S. Cochrane handbook for systematic reviews of interventions[M]. Chichester UK: Wiley and Sons, 2008.
|
| [8] |
HU K, GUAN W J, BI Y, et al. Efficacy and safety of Lianhuaqingwen capsules, a repurposed Chinese herb, in patients with coronavirus disease 2019:A multicenter, prospective, randomized controlled trial[J]. Phytomendicine, 2021, 85: 153242. DOI:10.1016/j.phymed.2020.153242 |
| [9] |
程德忠, 王文菊, 李毅, 等. 51例新型冠状病毒肺炎患者应用中药连花清瘟疗效分析: 多中心回顾性研究[J]. 天津中医药, 2020, 37(5): 509-516. CHENG D Z, WANG W J, LI Y, et al. Efficacy of Lianhua Qingwen in treating 51 cases of coronavirus disease 2019:a multicenter retrospective study[J]. Tianjin Journal of Traditional Chinese Medicine, 2020, 37(5): 509-516. |
| [10] |
姚开涛, 刘明瑜, 李欣, 等. 中药连花清瘟治疗新型冠状病毒肺炎的回顾性临床分析[J]. 中国实验方剂学杂志, 2020, 26(11): 8-12. YAO K T, LIU M Y, LI X, et al. Retrospective clinical analysis of Lianhua Qingwen in treating coronavirus disease 2019[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2020, 26(11): 8-12. |
| [11] |
吕睿冰, 王文菊, 李欣. 连花清瘟颗粒联合西药常规疗法治疗新型冠状病毒肺炎疑似病例63例临床观察[J]. 中医杂志, 2020, 61(8): 655-659. LYU R B, WANG W J, L X. Clinical observation of Lianhua Qingwen granule combined with Western medicine in the treatment of 63 suspected cases of coronavirus disease 2019[J]. Journal of Traditional Chinese Medicine, 2020, 61(8): 655-659. |
| [12] |
余平, 李叶子, 万少兵, 等. 连花清瘟颗粒联合阿比多尔治疗轻度新型冠状病毒肺炎的疗效观察[J]. 中国药学杂志, 2020, 55(12): 1042-1045. YU P, LI Y Z, WAN S B, et al. Effects of Lianhua Qingwen Granules plus arbidol on treatment of mild corona virus disease-19[J]. Chinese Pharmaceutical Journal, 2020, 55(12): 1042-1045. |
| [13] |
TANG B, BRAGAZZI N L, LI Q, et al. An updated estimation of the risk of transmission of the novel coronavirus (2019-nCov)[J]. Infectious Disease Modelling, 2020, 5: 248-255. DOI:10.1016/j.idm.2020.02.001 |
 2021, Vol. 38
2021, Vol. 38