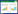文章信息
- 袁薪蕙, 刘志超, 黄宇虹, 王保和, 杜犀
- YUAN Xinhui, LIU Zhichao, HUANG Yuhong, WANG Baohe, DU Xi
- 雷公藤多苷片治疗肾病综合征增效减毒作用系统评价
- A systematic review of the synergism and attenuation effects of Tripterygium Glycosides Tablet on the nephrotic syndrome
- 天津中医药, 2021, 38(2): 213-218
- Tianjin Journal of Traditional Chinese Medicine, 2021, 38(2): 213-218
- http://dx.doi.org/10.11656/j.issn.1672-1519.2021.02.16
-
文章历史
- 收稿日期: 2020-11-20
2. 天津中医药大学第二附属医院临床药理科, 天津 300150
肾病综合征(NS)是由肾小球滤过膜受损而导致大量蛋白质从尿中丢失的临床综合征[1],表现为高度水肿、大量蛋白尿、高脂血症、低蛋白血症[2]。现代医学治疗肾病综合症主要通过改善饮食、利尿消肿、降低尿蛋白、激素抗炎、抑制免疫损伤为主[3]。雷公藤多苷(TG)可从抗炎抑炎、免疫调节等途径对肾脏疾病进行干预,但具有一定的毒性[4]。因此本研究对目前已有的TG的临床研究展开系统评价,根据TG治疗NS有效性和安全性的系统综述进一步验证其增效减毒作用。
1 资料与方法 1.1 原始研究纳入标准研究类型为随机对照试验(RCT);研究对象为明确诊断为NS的患者(包含原发性、难治性、复发性NS),年龄、性别不限(包含老年、成人、儿童等);对照组干预措施是未使用TG的基础治疗如降压、利尿、抗感染等,或NS的常规治疗如使用糖皮质激素泼尼松等,试验组为对照组相同干预措施加用TG;主要评价指标为总有效率、完全缓解率、24 h尿蛋白定量、不良反应发生率;试验组与对照组对照药使用剂量相同,试验组只加用TG单一变量;随访期限不限;原始文献语种为中文、英文。
1.2 原始研究排除标准研究对象为非NS患者的临床试验;研究雷公藤单味药、其配伍方剂或雷公藤其他成分的临床试验;以TG为对照,研究其他药物的临床试验;系统综述;非RCT;试验组与对照组阳性对照药剂量不统一,不能排除两组疗效变化是阳性药剂量不同引起,还是加用雷公藤引起的临床试验。
1.3 原始研究证据检索策略计算机检索中国知网(CNKI)、万方、维普3个中文数据库和PubMed、Cochrane Library两个英文数据库。检索关键词要求题目中出现“雷公藤”并含“肾病综合征”字样;且全文出现“随机”并含“对照”字样。英文检索关键词为题目中出现“Nephrotic Syndrome”并含“Tripterygium”字样。原始研究年份为从各数据库建库时间开始至2018年12月31日。
1.4 文献筛选与数据提取根据题目和摘要初筛,筛除不符合纳入标准的文献。对剩余文献查出原文,阅读原文,确定符合纳排标准的文献。采用双人双筛选,有意见分歧时咨询第3方。如缺乏资料,尽量与原作者联系咨询。使用Excel软件制作提取表,包含作者、年份、样本量、性别、年龄、干预措施、疗程、随访时间、结局指标。
1.5 文献质量评价采用Cochrane协作网推荐的偏倚风险评价工具[5-6]对纳入文献质量进行评价。评价员使用该工具对每篇原始研究以下7个方面分别做出“low risk”“high risk”“unclear risk”的评价:1)是否使用随机方法。2)是否进行分配隐藏。3)是否对受试者与研究人员采用盲法。4)是否对结果评估采用盲法。5)数据是否完整。6)是否存在选择性报告。7)是否存在其他偏倚。
1.6 统计学方法使用RevMan 5.3软件进行Meta分析。异质性检验采用Q检验,计算Q值和I2值。若I2=0,说明无异质性,采用固定效应模型;I2 < 50%,说明异质性在可以接受的范围内;I2≥50%,说明存在明显异质性,采用随机效应模型。若有明显异质性,应进一步分析异质性来源,剔除异质性来源的文献,控制异质性在可接受范围内或为可忽略的数值,使用固定效应模型重新进行Meta分析。计量资料以均数差(MD)和95%置信区间(CI)表示;计数资料以相对危险度(RR)和95%CI表示。统计各结局指标的RR值(计数资料)或MD值(计量资料)和CI区间做森林图。发表偏倚分析使用漏斗图,若对称,则提示不存在发表偏倚;若不对称,则提示存在发表偏倚。
2 研究结果按照检索策略检索得到文献共274篇,含中文265篇,英文9篇。有1篇无法获得,实际获得文献273篇,含知网99篇,万方93篇,维普73篇,PubMed 5篇,Cochrane Library 3篇。最终纳入文献数38篇。筛选流程如图 1。
|
| 图 1 原始文献筛选流程图 Fig. 1 Flow diagram of literature screening |
纳入的38个原始研究,总样本含量3 307例,其中试验组1 660例,对照组1 647例。
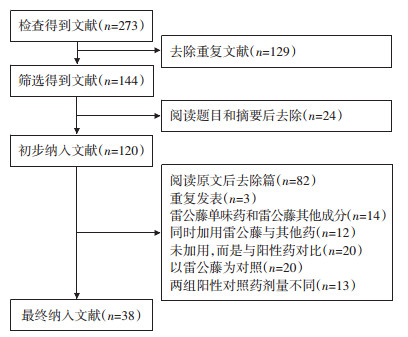
2.2 纳入文献质量评价用RevMan5.3软件采用Cochrane协作网推荐的偏倚风险评估方法对纳入文献的方法学质量进行评价。纳入的38篇文献中,15篇明确报告用随机数字表法进行随机;19篇只出现“随机”字样,未阐述随机方法;3篇提到根据时间随机;1篇未显示随机。33篇文献结果数据完整或与其研究目标一致,4篇未显示是否完整,只有1篇文献研究结果报告不完整。10篇文献缺少重要疗效指标数据,不排除选择性报告的可能性。1篇出现其他偏倚(基线不一致)。所有文献均未报告随机分配隐藏、盲法实施相关情况。纳入文献方法学质量总体中等水平,见图 2。
|
| 图 2 Cochrane协作网偏倚风险评估图 Fig. 2 Risk assessment diagram of Cochrane collaboration network |
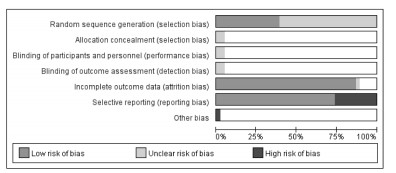
纳入的文献中,共19篇报告了完全缓解率,试验组共762例,367例出现完全缓解情况,对照组共750例,237例出现完全缓解情况。异质性检验I2=0,说明无异质性,选择固定效应模型进行Meta分析。森林图显示,效应量RR=1.51,95%CI(1.33,1.70),P < 0.000 01,研究结果有显著性差异,试验组完全缓解率优于对照组,见图 3。研究表明,基础或常规治疗加用TG可以提高治疗的完全缓解率。
|
| 图 3 完全缓解率Meta分析森林图 Fig. 3 Forest plot of complete remission rate in Meta-analysis |
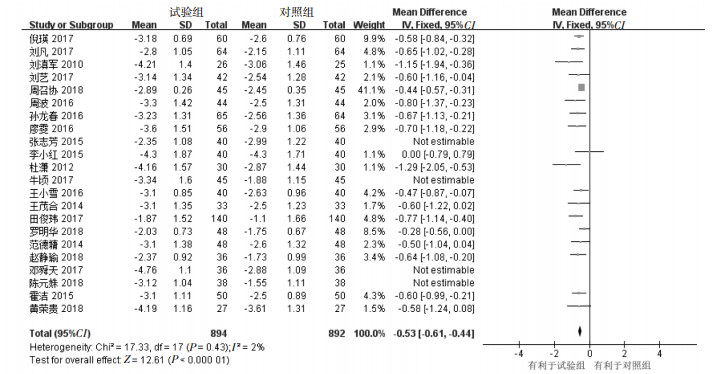
连续性变量选择原始研究的24 h尿蛋白定量进行分析。试验组共894例,对照组共892例。异质性检验I2=77%存在实质性异质性。探索异质性来源:依次单独剔除文献“张志芳2015”“牛顷2017”“邓舜天2017”“陈元姝2018”,I2分别降到71%、76%、70%、73%。而单独剔除其余文献,均会导致I2不变或升高,所以推测异质性来源于这4篇文献。把这4篇文献同时剔除,检验异质性I2=2%,异质性可忽略,验证出上述推测正确。选择固定效应模型,做森林图。效应量MD=-0.53,95%CI(-0.61,-0.44),P < 0.000 01,说明两组指标有显著性差异,试验组优于对照组。研究表明,基础或常规治疗加用TG可以降低患者24 h尿蛋白含量。见图 4。
|
| 图 4 24 h尿蛋白定量Meta分析森林图 Fig. 4 Forest plot of 24 h urine protein quantity in Meta-analysis |
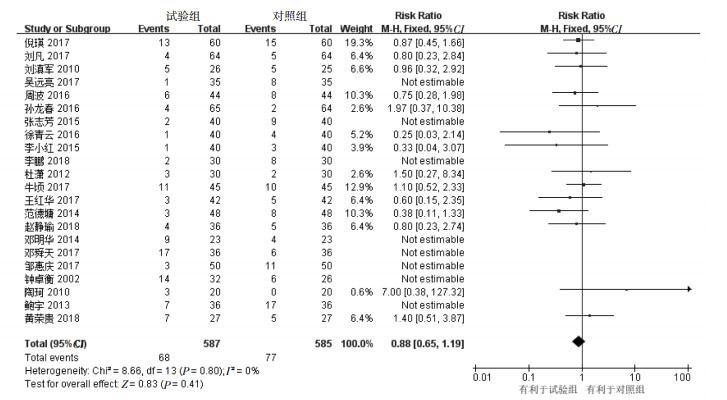
共22篇文献对不良反应进行了报道,异质性检验I2=49% 与50%接近,存在明显的异质性,应选择随机效应模型。按照上述2.3.2的方法剔除对异质性影响较大的文献8篇,重新进行异质性检验I2=0,无异质性,用固定效应模型。森林图显示,试验组共587例,共出现68例不良反应,对照组共585例,共出现77例不良反应。RR=0.88,95%CI(0.65,1.19),P > 0.05,两组结果无统计学差异,试验组不优于对照组。统计结果与未剔除前随机效应模型结果一致(P > 0.05),故排除异质性影响导致。研究尚不能证明在基础或常规治疗的基础上加用TG可以降低治疗的不良反应发生率。见图 5。
|
| 图 5 不良反应发生率Meta分析森林图 Fig. 5 Forest plot of the incidence of adverse reaction in Meta-analysis |
选择覆盖全部原始研究的指标总有效率进行漏斗图分析,漏斗图不对称,说明存在一定程度发表偏倚。推测与选择性发表、阳性结果偏多有关。见图 6。

|
| 图 6 Meta分析总有效率漏斗图 Fig. 6 Funnel plot of total efficiency in Meta-analysis |
NS为免疫性疾病的一种,目前多使用免疫抑制剂治疗和激素疗法[7]。临床上首选糖皮质激素治疗,但长期使用会发生激素依赖性和耐药性,还可能引发多种不良反应[8]。中医药的国际定位为补充替代医学,被越来越多的人肯定[9]。中医把NS归为“水肿”范畴,可由风邪袭表、外感水湿、久病劳倦等病因引起,导致肺失通调、脾失转输、肾失开阖、三焦气化不利,造成机体的水液代谢失常,发为水肿,应根据不同的病因病机辨证论治,施以利水攻逐、温肾养阴等不同治法[2]。中药雷公藤有祛风除湿、活血通络、消肿止痛、杀虫止痒的功效,长于“从肾论治”[4]。TG是从雷公藤中提取和纯化后的药物制剂,具有较强的抗炎和免疫抑制作用[10]。但是雷公藤毒性较大,不良反应主要集中在肝脏、肾脏和血液系统等[11]。而TG因其提取于中药雷公藤,也具有肝毒性[12]、血液系统毒性[13]、消化道毒性[14]等。
文章Meta分析结果显示,基础或常规治疗加用TG,可以显著增加治疗的完全缓解率,可显著降低患者的24 h尿蛋白含量,确有增效作用。但是系统评价结果显示试验组和对照组不良反应发生率并无统计学差异,甚至在纳入的22篇报告不良反应发生率的原始研究中有8篇出现试验组不良反应情况多于对照组的情况[15-22],所以尚不能证明TG减毒作用。当然阴性结果可能由Meta分析的误差和数据偏倚导致,也可能与TG本身毒性或药物间相互作用有关。需扩大样本量做进一步挖掘,并且从药理机制和中西药相互作用的角度进行进一步探索,以期探索TG与基础用药联合使用时是否能够减轻毒性、降低药物不良反应发生率。
因此,笔者认为TG在治疗NS方面具有较为广阔前景,有望成为糖皮质激素类等常规疗法的补充替代用药,在与激素或其他对症支持治疗联用时有增强疗效的作用。同时TG也具有一定毒性,有必要在其毒副作用与不良反应方面进行更深一步的研究,以达到减轻毒性作用的目的。
临床上CKD(慢性肾病分期)把慢性肾脏病分为5期,基于中医“治未病”理论基础,应在CKD的前3期进行尽早的筛查、诊断和治疗,做到未病先防、既病防变,而在CKD的后两个阶段,肾脏替代治疗或优于单纯的药物治疗。因此文章目标人群的临床定位排除CKD4期或5期人群。
此外,文献质量评价结果显示,纳入的原始文献方法学质量中等,虽评价方法有一定的主观成分,但是纳入原始文献普遍缺少随机分配隐匿、盲法实施的报道,这使得RCT研究的严谨性无法考证。漏斗图显示,本研究结果存在发表偏倚,不排除由选择性报告、阳性结果发表偏多导致。
| [1] |
郭华, 李志航, 王淑君, 等. 肾病综合征新型生物标志物研究进展[J]. 海南医学, 2018, 29(10): 1430-1433. GUO H, LI Z H, WANG S J, et al. Advances and clinical significance of biomarkers in nephrotic syndrome[J]. Hainan Medical Journal, 2018, 29(10): 1430-1433. DOI:10.3969/j.issn.1003-6350.2018.10.030 |
| [2] |
王先锋, 许勇强, 李陈雪, 等. 中医药治疗肾病综合征的研究进展[J]. 中医药导报, 2018, 24(11): 100-103, 116. WANG X F, XU Y Q, LI C X, et al. Research progress of traditional Chinese medicine in the treatment of nephrotic syndrome[J]. Guiding Journal of Traditional Chinese Medicine and Pharmacy, 2018, 24(11): 100-103, 116. |
| [3] |
赵良斌, 王燕涛, 李明权. 肾病综合征的中西医治疗研究进展[J]. 中国中西医结合肾病杂志, 2009, 10(11): 1024-1026. ZHAO L B, WANG Y T, LI M Q. Research progress in the treatment of nephrotic syndrome with traditional Chinese and Western medicine[J]. Chinese Journal of Integrated Traditional and Western Nephrology, 2009, 10(11): 1024-1026. DOI:10.3969/j.issn.1009-587X.2009.11.036 |
| [4] |
贾微, 吴晓君, 岑妍慧, 等. 雷公藤多苷治疗肾脏疾病的研究进展[J]. 中华中医药学刊, 2018, 36(4): 866-868. JIA W, WU X J, CEN Y H, et al. Progress of Tripterygium Glycosides in kidney disease clinical application[J]. Chinese Archives of Traditional Chinese Medicine, 2018, 36(4): 866-868. |
| [5] |
汪洋. Cochrane偏倚风险评估工具简介[J]. 中国全科医学, 2019, 22(11): 1322. WANG Y. Introduction to Cochrane bias risk assessment tool[J]. Chinese General Practice, 2019, 22(11): 1322. |
| [6] |
刘括, 孙殿钦, 廖星, 等. 随机对照试验偏倚风险评估工具2.0修订版解读[J]. 中国循证心血管医学杂志, 2019, 11(3): 284-291. LIU K, SUN D Q, LIAO X, et al. Bias risk review tool (2.0 revision) for randomized controlled trials[J]. Chinese Journal of Evidence-Based Cardiovascular Medicine, 2019, 11(3): 284-291. |
| [7] |
邵英媛. 肾病综合征应用糖皮质激素联合环磷酰胺治疗的效果分析与评价[J]. 中国医药指南, 2019, 17(3): 67-68. SHAO Y Y. Analysis and evaluation of the effect of glucocorticoid combined with cyclophosphamide in the treatment of nephrotic syndrome[J]. Guide of China Medicine, 2019, 17(3): 67-68. |
| [8] |
张胜志. 他克莫司联合小剂量糖皮质激素治疗合并HBsAg阳性的原发性肾病综合征的临床研究[J]. 国际医药卫生导报, 2017, 23(8): 1211-1213. ZHANG S Z. Clinical study of tacrolimus combined with low-dose glucocorticoid in the treatment of primary nephrotic syndrome with HBsAg positive[J]. International Medicine and Health Guidance News, 2017, 23(8): 1211-1213. DOI:10.3760/cma.j.issn.1007-1245.2017.08.034 |
| [9] |
周欣. 中医药国际化的发展及趋势研究[D]. 广州: 广州中医药大学, 2011. ZHOU X. Research on the development and trend of Chinese medicine internationalization[D]. Guangzhou: Guangzhou University of Chinese Medicine, 2011. |
| [10] |
郭雪红. 雷公藤多苷的药理作用及临床应用概述[J]. 中成药, 2010, 32(7): 1199-1202. GUO X H. Overview of the pharmacological effects and clinical applications of Tripterygium Wilfordii Polyglycosides[J]. Chinese Traditional Patent Medicine, 2010, 32(7): 1199-1202. DOI:10.3969/j.issn.1001-1528.2010.07.031 |
| [11] |
侯海荣, 何秋霞, 李晓彬, 等. 雷公藤的效/毒物质基础研究进展[J]. 现代医药卫生, 2018, 34(7): 1018-1020. HOU H R, HE Q X, LI X B, et al. Research progress on the effectiveness/toxic substances of Tripterygium Wilfordii[J]. Journal of Modern Medicine & Health, 2018, 34(7): 1018-1020. DOI:10.3969/j.issn.1009-5519.2018.07.017 |
| [12] |
罗岚, 江振洲, 张陆勇. 雷公藤多苷肝毒性发生机制及减毒相关研究进展[J]. 药物评价研究, 2017, 40(10): 1504-1509. LUO L, JIANG Z Z, ZHANG L Y. Research progress of hepatotoxicity mechanism and attenuation of Tripterygium wilfordii polyglycosides[J]. Drug Evaluation Research, 2017, 40(10): 1504-1509. |
| [13] |
杨威, 雷夏凌, 柳璐, 等. 雷公藤多苷对SD大鼠血液系统毒性的研究[A]. 中国毒理学会、湖北省科学技术协会. 中国毒理学会第七次全国毒理学大会暨第八届湖北科技论坛论文集[C]. 北京: 中国毒理学会, 武汉: 湖北省科学技术协会, 2015: 2. YANG W, LEI X L, LIU L, et al. Study on the toxicity of Tripterygium wilfordii polyglycosides on the blood system of SD rats[A]. Chinese Toxicology Society, Hubei Science and Technology Association. Chinese Toxicology Society seventh The Second National Conference on Toxicology and the Eighth Hubei Science and Technology Forum Proceedings[C]. Beijing: Chinese Toxicology Society, Wuhan: Hubei Science and Technology Association, 2015: 2. |
| [14] |
杨威, 黄远铿, 雷夏凌, 等. 雷公藤多苷对消化道的毒性研究[A]. 中国毒理学会、湖北省科学技术协会. 中国毒理学会第七次全国毒理学大会暨第八届湖北科技论坛论文集[C]. 北京: 中国毒理学会, 武汉: 湖北省科学技术协会, 2015: 1. YANG W, HUANG Y K, LEI X L, et al. Study on the toxicity of Tripterygium wilfordii polyglycosides to the digestive tract[A]. Chinese Toxicology Society, Hubei Science and Technology Association. The 7th National Toxicology Committee Science Conference and the 8th Hubei Science and Technology Forum Proceedings[C]. Beijing: Chinese Toxicology Society, Wuhan: Hubei Science and Technology Association, 2015: 1. |
| [15] |
孙龙春. 他克莫司联合雷公藤多苷对肾病综合征患者NF-κB与炎症细胞因子的影响[J]. 上海医药, 2016, 37(19): 38-40, 50. SUN L C. Effect of tacrolimus combined with Tripterygium glycosides on NF-κB and inflammatory cytokines in patients with nephrotic syndrome[J]. Shanghai Medical & Pharmaceutical Journal, 2016, 37(19): 38-40, 50. |
| [16] |
杜潇. 雷公藤多甙联合甲泼尼龙治疗老年肾病综合征的疗效观察[J]. 吉林医学, 2012, 33(2): 283-284. DU X. Observation on the efficacy of Tripterygium glycosides combined with methylprednisolone in the treatment of senile nephrotic syndrome[J]. Jilin Medical Journal, 2012, 33(2): 283-284. |
| [17] |
牛顷. 环磷酰胺联合雷公藤多甙治疗激素依赖型肾病综合征患者临床分析[J]. 内科, 2017, 12(3): 382-383, 315. NIU Q. Clinical analysis of cyclophosphamide combined with tripterygium glycosides in the treatment of hormone-dependent nephrotic syndrome patients[J]. Internal Medicine, 2017, 12(3): 382-383, 315. |
| [18] |
邓明华, 谢林伸. 雷公藤多甙联合糖皮质激素对肾病综合征调节性T细胞的影响和临床疗效分析[J]. 现代医药卫生, 2014, 30(20): 3051-3052, 3055. DENG M H, XIE L S. Influence and clinical efficacy of Tripterygium glycosides combined with glucocorticoid on regulatory T cells of patients with nephritic syndrome[J]. Journal of Modern Medicine & Health, 2014, 30(20): 3051-3052, 3055. DOI:10.3969/j.issn.1009-5519.2014.20.005 |
| [19] |
钟卓衡, 卢娟娟, 蔡楚丹. 激素合用雷公藤治疗30例复发性肾病综合征临床分析[J]. 中国综合临床, 2002, 18(5): 53-54. ZHONG Z H, LU J J, CAI C D. Hormone combined with Tripterygium wilfordii in the treatment of 30 cases of recurrent nephrotic syndrome[J]. Clinical Medicine of China, 2002, 18(5): 53-54. |
| [20] |
邓舜天, 杨玉仙, 戴德竟, 等. 醋酸泼尼松和环磷酰胺冲击疗法联合雷公藤多苷治疗肾病综合征的疗效观察[J]. 中国临床研究, 2017, 30(5): 631-634. DENG S T, YANG Y X, DAI D J, et al. Efficacy of pulse therapy of prednisone acetate plus cyclophosphamide combined with Tripterygium glycosides for treatment of nephrotic syndrome[J]. Chinese Journal of Clinical Research, 2017, 30(5): 631-634. |
| [21] |
黄荣贵, 牙秋艳, 蒙兰芬. 甲泼尼龙联合雷公藤多甙在老年肾病综合征治疗中的应用价值分析[J]. 右江医学, 2018, 46(2): 164-167. HUANG R G, YA Q Y, MENG L F. Analysis of the value of methylprednisolone combined with Tripterygium glycosides in the treatment of senile nephrotic syndrome[J]. Chinese Youjiang Medical Journal, 2018, 46(2): 164-167. |
| [22] |
陶珂. 雷公藤多甙联合泼尼松治疗肾病综合征(肾炎型)疗效观察[J]. 中外健康文摘, 2010, 7(36): 97-99. TAO K. Observation on the efficacy of Tripterygium glycosides combined with prednisone in the treatment of nephrotic syndrome (nephritis type)[J]. World Health Digest, 2010, 7(36): 97-99. |
2. Department of Clinical Pharmacology, The Second Affiliated Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300150, China
 2021, Vol. 38
2021, Vol. 38