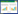文章信息
- 谷岩, 侯骊坤, 刘辉, 何菊
- GU Yan, HOU Likun, LIU Hui, HE Ju
- 丹酚乙酸镁对大鼠肢体缺血再灌注损伤炎性因子及其mRNA调控作用的探讨
- Study on the regulation effect of magnesium salvianolic acetate on inflammatory factors and mRNA limbs ischemia-reperfusion injury in rats
- 天津中医药, 2021, 38(5): 666-670
- Tianjin Journal of Traditional Chinese Medicine, 2021, 38(5): 666-670
- http://dx.doi.org/10.11656/j.issn.1672-1519.2021.05.25
-
文章历史
- 收稿日期: 2021-01-02
肢体的创伤、手术、血栓形成均可引起肢体缺血,而随着血流的恢复,在缺血后恢复血流在某些情况下导致进一步组织损伤和功能障碍,甚至出现远隔脏器的损伤[1],也就是肢体缺血再灌注损伤(LI-RI)。危重患者可导致多器官功能障碍,其通常是一个致命性的结局。因此,针对LI-RI的病理机制及其防治机制的研究,对有效防治或保护急性肢体缺血损伤,降低致残率和病死率,具有十分重要的现实意义。炎性因子在LI-RI过程中尤为重要,其中白介素(IL)-1、IL-6、肿瘤坏死因子-α(TNF-α)等多种细胞因子大量释放并导致了机体自身组织和器官的损伤,因此炎性因子水平是LI-RI程度的一个标志[2-3]本实验通过建立大鼠缺血再灌注的动物模型,观察缺血前后及用药前后大鼠体内不同组别中肢体缺血再灌注损伤期炎性细胞因子IL-6、TNF-α、IL-1β和IL-10及其mRNA的变化规律,从而探讨丹酚乙酸镁对大鼠肢体缺血再灌注的保护作用。
1 材料和方法 1.1 实验动物及分组健康雄性Sprague-Dawley大鼠32只,级别SPF级,体质量(240±10) g。(北京华阜康实验动物科技有限公司,天津放射所动物房饲养)。老鼠饲养条件:22~25 ℃,12 h明暗循环,标准食物颗粒。将大鼠随机分为4组,每组8只大鼠。第1组为空白对照组;第2组为缺血再灌注组,接受腹腔生理盐水(SP)治疗;第3组是接受低浓度治疗的缺血再灌注组(12 mg/kg)(简称低浓度处理组);第4组为接受高浓度治疗的缺血再灌注组(24 mg/kg)(简称高浓度处理组)。
1.2 主要实验试剂大鼠IL-1β酶联免疫吸附测定(ELISA)试剂盒购于索莱宝生物科技有限公司。大鼠IL-6 ELISA试剂盒购于索莱宝生物科技有限公司。大鼠IL-10 ELISA检测试剂盒购于索莱宝生物科技有限公司。大鼠TNF-α ELISA试剂盒购于索莱宝生物科技有限公司。各种动物外周血淋巴细胞分离液试剂盒购于索莱宝生物科技有限公司。
1.3 缺血再灌注模型制备及标本采集按照经典方法制备大鼠缺血再灌注模型[4]。大鼠术前12 h禁食,自由饮水。戊巴比妥钠(首剂40 mg/kg,维持剂量20 mg/kg)腹腔注射麻醉后固定于动物手术台上,右下肢股三角区剪毛,于腹股沟处沿血管走行纵行切开皮肤、皮下组织,钝性分离缝匠肌后部,游离股动、静脉和股神经。用微血管夹分别夹闭右股动脉。缺血2 h后,放松微血管夹恢复血流灌注2 h。假手术组治疗方法相同,但未阻断股动脉血流。再灌注前15 min,给第2组腹腔注射生理盐水,给第3组注射低浓度丹参多酚酸盐,给第4组注射高浓度丹参多酚酸盐。缺血2 h后。从每只大鼠下腔静脉抽取约10 mL血液进行各项指标测定。
1.4 血清TNF-α、IL-1β、IL-6和IL-10水平的测定将全血收集到含抗血凝剂的管中,混合20 min,在4 ℃条件下1 000×g,离心半径160 mm,离心10 min,然后将上清等量分装于小EP管并于-20 ℃下保存(24 h内检测可放入2~8 ℃储存),避免反复冻融。将取得的上清液用ELISA法按照检测试剂盒说明书分别检测TNF-α、IL-1β、IL-6和IL-10的含量。
1.5 实时荧光定量PCR(qRT-PCR)法测定血清TNF-α、IL-1β、IL-6和IL-10 mRNA水平首先提取外周淋巴细胞,将稀释后的血液进行离心,洗涤,弃去上清液。按TRIzol法提取RNA,用酶标仪检测RNA浓度和纯度,直接进行逆转录操作。逆转录反应:总反应体系20 μL,包括样品RNA 2 g,DEPC焦磷酸二乙酯水7 μL,OligodT 1 μL,RNA酶抑制剂1 μL,10 mmol/L dNTPs 2 μL,5×MMLV buffer 4 μL,MMLV RT 1 μL。
反应条件为:70 ℃ 5 min,42 ℃ 60 min,70 ℃ 10 min根据Gene bank数据库中参考序列设计用于Real-time PCR的引物,并采用Blast程序比对确定引物的特异性,用β-actin作为内参。IL-1β上游引物:5’-AGGTGGTGTCGGTCATCGT- 3’,下游引物:5’-GCT-CTCTGTCCTGGAGTTTGC- 3’;IL-6上游引物:5’-ATGCTTCCAATCTGGGTTC-3’,下游引物:5’- TGA-GGATAATCTTTGCGTTC-3’;TNF-α上游引物:5’-ACGGGCTTTACCTCATCTACTC-3’,下游引物:5 ’-GCTCTTGATGGCAGACAGG-3’;IL-10上游引物:5’-CAGTCAGCCAGACCCACAT-3’,下游引物:5’-GCT-CCACTGCCTTGCTTT-3’;β-actin上游引物:5’-CCAAGGCCAACCGTGAGAAGAT- 3’,下游引物:5’-CCACGTTCCGTGAGGATCTTCA-3’。
Real-time PCR扩增实验采用SYRB Green I染料法,使用荧光定量全自动PCR仪上进行基因扩增,扩增采用两步法,反应条件为:94 ℃ 5 min预变性后,94 ℃ 10 s,58 ℃ 30 s,共进行40个循环,再于72 ℃延伸7 min。反应结束后,根据实验结果记录相应的Ct值。以β-actin的Ct值为参照,计算Δt,运用公式2-Δt计算各基因的相对表达量。
1.6 统计学方法检测结果应用SPSS 24.0软件分析,实验数据以均数±标准差(x±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD法,P<0.05为差异具有统计学意义。
2 结果 2.1 各组中炎性因子水平的结果及比较与空白对照组相比,缺血再灌注组中TNF-α、IL-1B、IL-6和IL-10水平明显升高,差异具有统计学意义(P < 0.05)。与缺血再灌注组相比,低浓度处理组和高浓度处理组中TNF-α、IL-1β和IL-6的水平明显下降,差异具有统计学意义(P < 0.05);IL-10水平明显升高,差异具有统计学意义(P < 0.05)。高浓度处理组与低浓度处理组相比,TNF-α、IL-1β、IL-6水平明显降低,IL-10水平明显升高,差异具有统计学意义(P < 0.05)。见表 1。
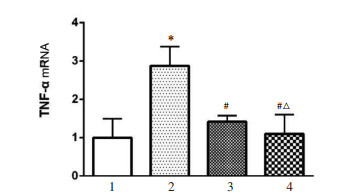
正常情况下,空白对照组血清中有少量TNF-α表达。与空白对照组相比,缺血再灌注组血清中TNF-α表达明显升高,差异具有统计学意义(P < 0.05)。与缺血再灌注组相比,高浓度处理组和低浓度处理组中TNF-α表达明细降低,差异具有统计学意义(P < 0.05)。高浓度处理组与低浓度处理组相比,血清中TNF-α表达降低,差异具有统计学意义(P < 0.05)。见图 1。
|
| 注:1.空白对照组,2.缺血再灌注组,3.低浓度处理组,4.高浓度处理组;与空白对照组比较,*P < 0.05;与缺血再灌注组比较,#P < 0.05;与低浓度处理组比较,△P < 0.05。 图 1 各组中TNF-αmRNA表达情况比较 Fig. 1 Comparison of TNF-α mRNA expression in each group |
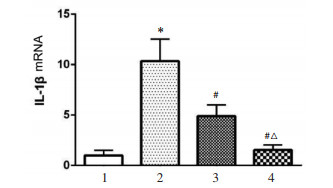
正常情况下,空白对照组血清中有少量IL-1β表达。与空白对照组相比,缺血再灌注组血清中IL-1β表达明显升高,差异具有统计学意义(P < 0.05)。与缺血再灌注组相比,高浓度处理组和低浓度处理组中IL-1β表达明细降低,差异具有统计学意义(P < 0.05)。高浓度处理组与低浓度处理组相比,血清中IL-1β表达降低,差异具有统计学意义(P < 0.05)。见图 2。
|
| 注:1.空白对照组,2.缺血再灌注组,3.低浓度处理组,4.高浓度处理组;与空白对照组比较,*P < 0.05;与缺血再灌注组比较,#P < 0.05;与低浓度处理组比较,△P < 0.05。 图 2 各组中IL-1βmRNA表达情况比较 Fig. 2 Comparison of IL-1 β mRNA expression in each group |
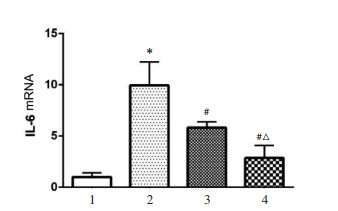
正常情况下,空白对照组血清中有少量IL-6表达。与空白对照组相比,缺血再灌注组血清中IL-6表达明显升高,差异具有统计学意义(P < 0.05)。与缺血再灌注组相比,高浓度处理组和低浓度处理组中IL-6表达明细降低,差异具有统计学意义(P < 0.05)。高浓度处理组与低浓度处理组相比,血清中IL-6表达降低,差异具有统计学意义(P < 0.05)。见图 3。
|
| 注:1.空白对照组,2.缺血再灌注组,3.低浓度处理组,4.高浓度处理组;与空白对照组比较,*P < 0.05;与缺血再灌注组比较,#P < 0.05;与低浓度处理组比较,△P < 0.05。 图 3 各组中IL-6 mRNA表达情况比较 Fig. 3 Comparison of IL-6 mRNA expression in each group |
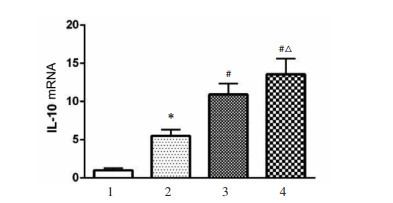
正常情况下,空白对照组血清中有少量IL-10表达。与空白对照组相比,缺血再灌注组血清中IL-10表达明显升高,差异具有统计学意义(P < 0.05)。与缺血再灌注组相比,高浓度处理组和低浓度处理组中IL-10表达明细升高,差异具有统计学意义(P < 0.05)。高浓度处理组与低浓度处理组相比,血清中IL-10表达升高,差异具有统计学意义(P < 0.05)。见图 4。
|
| 注:1.空白对照组,2.缺血再灌注组,3.低浓度处理组,4.高浓度处理组;与空白对照组比较,*P < 0.05;与缺血再灌注组比较,#P < 0.05;与低浓度处理组比较,△P < 0.05。 图 4 各组中IL-10 mRNA表达情况比较 Fig. 4 Comparison of IL-10 mRNA expression in each group |
肢体缺血再灌注在血管外科、骨科、创伤等多种情况下发生。其影响的并非单纯是出现缺血的肢体,通过一系列的炎性反应等病理过程,造成大量炎性细胞因子和有害物质的生成和释放,从而对远隔的心、肺、脑、肾等重要器官功能造成损害[5]。
炎症细胞因子在肢体缺血再灌注损伤中发挥了重要作用,在肢体发生缺血再灌注后,细胞会释放一氧化氮、TNF-α、IL-1及IL-6等炎症细胞因子,对受损的细胞组织产生二次损伤。这两种细胞因子都具有多种致炎活性,包括白细胞趋化、吞噬细胞刺激、增强下游细胞因子和趋化因子的产生。TNF-α可提高中性粒细胞的吞噬能力,也能促进内皮细胞对IL-1、IL-6的分泌,并能促进中性粒细胞和内皮细胞的黏附作用,从而刺激扩大机体局部炎症反应及组织的损伤[6]。在以往的研究实验中也证实了当缺血再灌注损伤发生时,炎性细胞因子会出现明显升高的情况[7],因此炎性因子在缺血再灌注过程中的表达水平可以反应炎症反应的剧烈程度,同时也可以反应出缺血再灌注损伤的严重程度,而同时也发现在缺血再灌注发生时,阻断这些炎性因子的表达,可以减轻缺血再灌注损伤的程度[8]。
有研究证明,IL-10具有抗炎作用,抑制其他炎性因子的产生,发挥神经保护作用[9]。另外有研究证明IL-10在通过抑制单核巨嗜细胞释放炎性介质的作用,使得血浆中TNF-α和IL-1及IL-6炎性介质水平降低[10]。而在局部炎性反应中,IL-10可以降低T淋巴细胞和巨噬细胞的活性[11],因此也成为影响缺血再灌注损伤的重要因素。
丹酚乙酸镁又称丹参乙酸镁是丹参多酚酸盐的主要有效成分,是一种丹参提取物。在多项关于抗氧化,清除自由基和缺血再灌注损伤的临床研究中,丹参多酚酸盐均显示出良好的效果[12]。在心脏和脑组织的缺血再灌注研究中也发现具有很好的治疗效果[13]。在本次实验中通过对大鼠下肢缺血再灌注实验标本的给予丹参多酚处理,观察丹参多酚盐对炎症细胞因子的影响,讨论其对于肢体缺血再灌注损伤的保护作用。
在本次实验中,通过建立大鼠下肢缺血再灌注模型,在缺血再灌注2 h后取血,在实验组中给予不同剂量的丹参多酚酸盐处理。通过检测血清中TNF-α、IL-6、IL-1β和IL-10的数值进行各组比较。缺血再灌注组中TNF-α、IL-6、IL-1β指标的数值较假手术组明显升高,说明缺血再灌注过程中,炎性细胞因子的升高,从而发生一系列炎症反应出现组织损伤,这与之前的其他研究报导结果一致。通过对经丹参多酚酸盐处理组的血中炎性指标的测定,与缺血再灌注组相对比发现,无论是高浓度处理组还是低浓度处理组,其炎性细胞因子TNF-α、IL-1β和IL-6的水平明显下降。说明丹参多酚酸盐处理后明显降低了炎性细胞因子的水平,降低炎症反应的程度,减轻了缺血再灌注损伤的程度。此外在经丹参多酚酸盐处理组和缺血再灌注组的比较当中,抗炎性细胞因子IL-10的水平显著升高,表明丹参多酚可以明显增强了IL-10的水平,从而起到抑制炎性细胞因子的释放以减轻缺血再灌注损伤的程度。同时在高低浓度处理组之间的对比发现,TNF-α、IL-1β和IL-6水平在高浓度处理组中较低浓度处理组降低,具有统计学意义,而IL-10水平是升高的,也具有统计学意义(P > 0.05)。因此可以推断丹参多酚酸盐可以降低缺血再灌注后血清中炎性因子,提高血清中抗炎因子的水平,起到减轻缺血再灌注损伤的作用,同时这种作用是与丹参多酚酸盐的浓度成正相关的。
同时,在本次实验中还同时通过实时荧光PCR法进行了TNF-α、IL-1β、IL-6和IL-10的mRNA表达水平的定量测定并进行了比较。在缺血再灌注组中各项指标的mRNA水平较空白组均显著升高,并具有统计学意义。这与之前的临床报导一致。说明缺血再灌注过程明显诱发了炎性因子mRNA表达水平的上调,从而引起一系列炎症反应,最终造成缺血再灌注损伤。通过对处理组中炎性因子表达水平的测定,与缺血再灌注组相比较,发现TNF-α、IL-1β、IL-6炎性因子水平显著降低,IL-10因子mRNA表达水平明显升高。说明在经过丹参多酚酸盐处理后,能够明显降低炎性因子的mRNA表达水平。
丹参类药物对于缺血再灌注损伤的实验研究和临床研究为数不少,但多集中于心、脑组织的缺血再灌注损伤[14],对于肢体缺血再灌注损伤的研究相对不多。比较以前的实验研究和临床观察[15-16],也证实了丹参多酚对肢体缺血再灌注的保护作用,但以往的研究多为丙二醛和超氧化物歧化酶作为缺血再灌注损伤的参照指标。本次实验中观察了丹参多酚对于炎性因子及其mRNA表达的调控作用,更进一步揭示了丹参多酚对于肢体缺血再灌注损伤的保护作用。
总之,在本次实验中,发现丹参多酚酸盐通过上调抗炎性细胞因子水平,降低血浆中炎性细胞因子的浓度,使得缺血再灌注过程中组织的损伤程度得以减轻,从而起到保护作用。
| [1] |
BARRY M C, KELLY C J, ABDIH H, et al. Differential effects of lower limb revascularisation on organ injury and the role of the amino acid taurine[J]. European Journal of Vascular and Endovascular Surgery, 1997, 13(2): 193-201. DOI:10.1016/S1078-5884(97)80018-4 |
| [2] |
张江锋, 覃晓, 李喆, 等. 大鼠肢体缺血再灌注不同时段相关炎性介质的表达[J]. 中外医学研究, 2011, 9(2): 1-3. ZHANG J F, QIN X, LI Z, et al. Expression of inflammatory mediators at different stages of limb ischemia-reperfusion in rats[J]. Chinese and Foreign Medical Research, 2011, 9(2): 1-3. DOI:10.3969/j.issn.1674-6805.2011.02.001 |
| [3] |
ESPOSITO E, CUZZOCREA S. TNF-alpha as a therapeutic target in inflammatory diseases, ischemia-reperfusion injury and trauma[J]. Current Medicinal Chemistry, 2009, 16(24): 3152-3167. DOI:10.2174/092986709788803024 |
| [4] |
DURAN A, CILOGLU S, SEHIRLI O, et al. Apocynin and dimethyl sulfoxide synergistically protect against ischemia-reperfusion injury in a rat hind limb ischemia-reperfusion model[J]. European Journal of Plastic Surgery, 2017, 40: 507-512. DOI:10.1007/s00238-017-1309-8 |
| [5] |
KALOGERIS T, BAINES C P, KRENZ M, et al. Cell biology of ischemia/reperfusion injury[J]. International Review of Cell and Molecular Biology, 2012, 298: 229-317. |
| [6] |
HASTURK A, ATALAY B, CALıSANELLER T, et al. Analaysis of serum pro-inflammatory cytokine levels after rat spinal cord ischemia/reperfusion injury and correlation with tissue damage[J]. Turk Neurosurgery, 2009, 19(4): 353-359. |
| [7] |
SHIH Y M, SHIH J M, PAI M H, et al. Glutamine administration after sublethal lower limb ischemia reduces inflammatory reaction and offers organ protection in ischemia/reperfusion injury[J]. Journal of Parenteral and Enteral Nutrition, 2016, 40(8): 1122-1130. DOI:10.1177/0148607115587949 |
| [8] |
DURAN A, CILOGLU S, SEHIRLI O, et al. Correction to: Apocynin and dimethyl sulfoxide synergistically protect against ischemia-reperfusion injury in a rat hind limb ischemia-reperfusion model[J]. European Journal of Plastic Surgery, 2017, 40: 599. DOI:10.1007/s00238-017-1372-1 |
| [9] |
VRIES D, JAN E. Immunosuppressive and anti-inflammatory properties of Interleukin 10[J]. Annals of Medicine, 1995, 27(5): 537-541. DOI:10.3109/07853899509002465 |
| [10] |
吕翠, 王翠花, 曾现伟. IL-10基因修饰的BMSCs对大鼠脑缺血再灌注损伤的保护作用[J]. 实用医学杂志, 2016, 32(21): 3520-3523. LYU C, WANG C H, ZENG X W. Protective effect of IL-10 gene modified BMSCs on cerebral ischemia-reperfusion injury in rats[J]. The Journal of Practical Medicine, 2016, 32(21): 3520-3523. DOI:10.3969/j.issn.1006-5725.2016.21.016 |
| [11] |
STRLE K, ZHOU J H, SHEN W H, et al. Interleukin-10 in the brain[J]. Critical Reviews in Immunology, 2001, 21(5): 427-449. |
| [12] |
吕林林, 安姿旖, 梁家健, 等. 丹参多酚酸盐对过氧化氢诱导人内皮细胞EA.hy926氧化应激损伤的保护作用及机制[J]. 中国病理生理杂志, 2019, 35(5): 865-872. LYU L L, AN Z Y, LIANG J J, et al. Protective effect and mechanism of salvianolate on oxidative stress injury induced by hydrogen peroxide in human endothelial cells EA.hy926[J]. Chinese Journal of Pathophysiology, 2019, 35(5): 865-872. DOI:10.3969/j.issn.1000-4718.2019.05.015 |
| [13] |
TANG H, PAN C S, MAO X W, et al. Role of NADPH oxidase in total salvianolic acid injection attenuating ischemia-reperfusion impaired cerebral microcirculation and neurons: implication of AMPK/Akt/PKC[J]. Microcirculation, 2014, 21(7): 615-627. DOI:10.1111/micc.12140 |
| [14] |
李辉. 丹参多酚酸盐对大鼠缺血再灌注损伤心脏、大脑组织中SOD、MDA的影响[J]. 中国实用神经疾病杂志, 2012, 15(17): 33-34. LI H. Effects of salvianolate on SOD and MDA in heart and brain tissue of rats with ischemia-reperfusion injury[J]. Chinese Journal of Practical Nervous Diseases, 2012, 15(17): 33-34. |
| [15] |
赵利军, 门秀丽, 孔小燕, 等. 大鼠肢体缺血/再灌注后多器官水肿及丹参的预防作用[J]. 中国应用生理学杂志, 2012(3): 281-283. ZHAO L J, MEN X L, KONG X Y, et al. Multiple organ edema after limb ischemia/reperfusion in rats and the preventive effect of Salvia Miltiorrhiza[J]. Chinese Journal of Applied Physiology, 2012(3): 281-283. |
| [16] |
卢卫忠, 贺小兵, 吴清. 缺血预处理和丹参对肢体缺血再灌注损伤影响的临床观察[J]. 实用医学杂志, 2012, 18(10): 1032-1034. LU W Z, HE X B, WU Q. Clinical observation of ischemic preconditioning and Salvia Miltiorrhiza on limb ischemia reperfusion injury[J]. Journal of Practical Medicine, 2012, 18(10): 1032-1034. |
 2021, Vol. 38
2021, Vol. 38