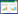文章信息
- 蔡楠, 曹宁宁, 赵利斌, 裴帅, 李晓璇, 张琬靖, 肖学凤, 刘昌孝
- CAI Nan, CAO Ningning, ZHAO Libin, PEI Shuai, LI Xiaoxuan, ZHANG Wanjing, XIAO Xuefeng, LIU Changxiao
- 基于“五原则”的血必净注射液质量标志物的预测分析
- Predictive analysis of quality marker in Xuebijing Injection based on "five principles"
- 天津中医药, 2021, 38(8): 1062-1070
- Tianjin Journal of Traditional Chinese Medicine, 2021, 38(8): 1062-1070
- http://dx.doi.org/10.11656/j.issn.1672-1519.2021.08.24
-
文章历史
- 收稿日期: 2021-05-10
2. 天士力控股集团有限公司研究院现代中药开发中心, 天津 300410;
3. 北京振东光明药物研究院, 北京 100085;
4. 天津药物研究院释药技术与药物代谢动力学国家重点实验室, 天津 300301
中药质量是中药临床安全有效的基础,是中药产业发展的生命线[1]。中药质量标准和质量控制关系到中医药科学和产业发展的国家战略问题[2]。但现行质量标准主要以成分定性鉴别和定量分析为评价方法,虽然部分品种进行了较为系统的化学成分研究,但指标成分选择往往缺乏特有性、有效性、溯源性等依据,不能充分保障中药及产品的临床疗效和安全性,质量不能有效追踪溯源。为此,2016年,刘昌孝院士提出了中药质量标志物(Q-marker)的核心概念和理论,引起了同行学者高度关注。Q-marker的研究思路着眼于全过程基础物质的特有、差异、动态变化以及质量的溯源性来建立中药全程质量控制,以提高中药质量控制的针对性和指向性[3]。概而言之,Q-marker研究应基于有效、特有、传递与溯源、可测和处方配伍的“五原则”而确定,完善现行质量标准中的诸多不足,保证临床用药的有效性和安全性。
血必净注射液是由中国危重病急救医学的奠基人和开拓者王今达教授历经30年研制成功的中药复方制剂,其由红花、赤芍、川芎、丹参和当归5味中药组成[4]。方中红花活血散瘀止痛为君药;赤芍凉血化瘀,川芎活血止痛,两者共为臣药;当归养血活血,丹参活血祛瘀,清心除烦,两者共为佐药[5]。全方配伍既可活血化瘀,又可行气养血,具有化瘀解毒之效。主治发热、喘促、心悸、烦躁等瘀毒互结症,临床多用于治疗因感染诱发的全身炎症反应综合征,或配合治疗多器官功能失常综合征的脏器功能受损期[6]。
新型冠状病毒肺炎(COVID-19)爆发后,在没有特效药和疫苗的情况下,以中医药辨证施治、多靶点干预为基础,筛选出包括血必净注射液在内的一批有效方药。血必净注射液为国家卫生健康委员会颁布《新型冠状病毒感染的肺炎诊疗方案(试行第四版)》中推荐用药,其临床应用广泛,疗效确切,改善COVID-19和重症肺炎感染患者发热、咳嗽及呼吸困难等临床症状[7-8]。血必净注射液可降低重症型COVID-19患者体温,通过降低白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)和C反应蛋白(CRP)水平以减轻炎症反应,下调血清中D-二聚体水平而抑制血小板黏附和聚集,改善微循环,显著缩短核酸转阴时间,对COVID-19有明显疗效[9]。血必净注射液能够调节重症肺炎患者血清中CD3+、CD4+和CD8+含量而增强免疫功能,促进肺部炎症的消除;升高动脉血氧分压(PaO2)和动脉血氧分压与吸入氧浓度比值(PaO2/FiO2),并降低动脉血二氧化碳分压(PaCO2)来维持动脉血气指标平衡,减轻患者肺部体征,有效治疗重症肺炎[10]。目前,血必净注射液研究主要集中在临床应用方面,其质量控制方面尚有欠缺。为保证临床用药的安全性和有效性,本文在梳理现代研究文献基础上,依据Q-marker“五原则”,对血必净注射液Q-marker的确定进行分析与论证,预测血必净注射液的Q-marker,以期为血必净注射液的后续临床及其质量控制研究提供参考依据。
1 基于质量传递与溯源的Q-marker预测分析中药化学成分是其功效表达的物质基础,是反映中药质量的客观实质。因此,中药质量控制应着眼于中药形成的全过程,建立基于质量传递与溯源的全程质量控制体系[11],保证中药临床的有效性。血必净注射液化学成分复杂,目前对其单味药材化学成分研究较多。采用质谱法从血必净注射液的5味药材中共鉴别出170余个化合物[12-33],其中从红花中辨识27个化合物,赤芍中辨识59个化合物,川芎中辨识35个化合物,丹参中辨识53个化合物,当归中辨识27个化合物。
由于各单味药材在经提取纯化等制备工艺制成中药复方制剂的过程中,既有有效性成分的获取,又有去粗取精、去伪存真的过程,因此,中药复方制剂中的化学成分是其质量控制的主要指标,其上溯药材源头,下延体内的最终效应成分。已有研究采用超高效液相色谱-四级杆/静电场轨道阱高分辨质谱方法,对血必净注射液化学成分进行表征和辨识,从血必净注射液中共辨识80余个化合物,其中从红花中辨识13个化合物,赤芍中辨识24个化合物,川芎中辨识27个化合物,丹参中辨识27个化合物,当归中辨识24个化合物[34]。
中药复方制剂的有效成分首先入血,再通过血液运输到达疾病治疗靶点发挥治疗作用,因此,入血成分才是最终的“效应成分”。从质量传递与溯源的角度,血中的效应成分是质量传递体系的最终环节,也是中药质量标志物确定的重要依据。采用液质联用方法,快速分析和辨识静脉注射血必净注射液后临床患者和大鼠的入血成分[35-41]。静脉注射血必净注射液后从临床患者和大鼠血浆中共辨识出30余种入血成分,其中从红花中辨识5个化合物,赤芍中辨识12个化合物,川芎中辨识11个化合物,丹参中辨识7个化合物,当归中辨识7个化合物。
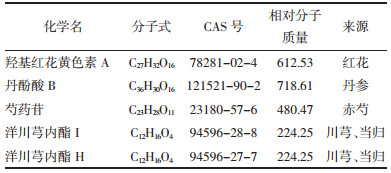
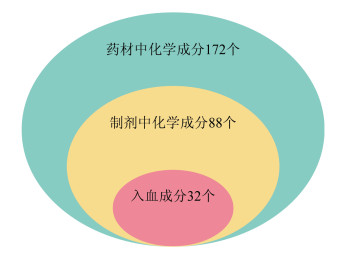
综上,通过对血必净注射液原药材、血必净注射液及其入血成分的系统辨识,进一步将血必净注射液中成分及其入血成分进行对比归类,发现血必净注射液32个入血成分均可溯源到血必净注射液及其单味药材中,结果见开放科学(资源服务)标识码(OSID),并明确其变化规律,见图 1。因此,以具有溯源性的32个入血成分可作为血必净注射液的Q-marker。
|
| 图 1 血必净注射液中化学成分变化示意图 Fig. 1 Schematic diagram of chemical components change in Xuebijing Injection |
一个好的质量评价方法应具有对特定药材的针对性和专属性,以免“以假乱真”。中药复方特有性成分大多来源于单味药材的活性成分,其特征为含量高、具有与复方临床应用相关的药理作用等。血必净注射液具有抗炎、保护血管内皮细胞、抗凝血等药理作用,临床多用于治疗因感染诱发的全身炎症反应综合征。故本研究通过分析血必净注射液各单味药材中含量高且具有抗炎、保护血管内皮细胞、抗凝血等药理作用的化学成分,预测血必净注射液具有特有性的Q-marker。
2.1 红花成分的特有性分析红花为菊科植物红花Carthamus tinctorius L.的干燥花,主要含黄酮、酚酸类、生物碱等化学成分[42]。其中以羟基红花黄色素A为主的黄酮类成分是红花主要成分,也是其他植物中较少见的成分。其不仅含量高,还具有抗炎、抗凝血等药理作用,故羟基红花黄色素A可作为红花的特有性成分。
2.2 赤芍成分的特有性分析赤芍为毛茛科植物芍药Paeonia lactiflora PalL或川赤芍Paeonia veitchii Lynch的干燥根,主要含单萜及其苷类、黄酮类和酚酸类等化学成分。其中芍药苷、苯甲酰芍药苷、芍药内酯苷等单萜及其苷类成分具有保护血管内皮细胞、抗炎等药理作用,是赤芍的特征性成分[43-44]。因此,以芍药苷、苯甲酰芍药苷、芍药内酯苷作为赤芍的特有性成分。
2.3 川芎、当归成分的特有性分析川芎为伞形科植物川芎Ligusticum chuanxiong Hort.的干燥根茎,当归为伞形科植物当归Angelica sinensis(Oliv.)Diels的干燥根。川芎和当归化学成分重叠度极高,两者均含有苯酞类、多糖类、有机酸类等成分,难以从化学成分将两者区分,故未单独分析川芎或当归的特有性成分,而是寻找当归和川芎共同区别于血必净注射液中其他药材的特有性成分。血必净注射液中川芎和当归共有成分为藁本内酯、洋川芎内酯Ⅰ、洋川芎内酯G、洋川芎内酯H、洋川芎内酯N等苯酞类成分,是区别于血必净注射液中其他药材的特有性成分[45]。因此,藁本内酯、洋川芎内酯Ⅰ、洋川芎内酯G、洋川芎内酯H、洋川芎内酯N可作为血必净注射液中当归和川芎的特有性成分。
2.4 丹参成分的特有性分析丹参为唇形科植物丹参Salvia miltiorrhiza Bge.的干燥根和根茎,主要含有酚酸类和丹参酮类成分。其中丹参酮类成分包括隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA,但由于丹参酮类成分的药理作用为抗氧化、抗肿瘤等,与血必净注射液临床治疗因感染诱发的全身炎症反应综合征无关,故其不能作为丹参的特有性成分[46-47];而酚酸类成分中90%以上是丹酚酸B,同时丹酚酸B也是丹参中含量最高的成分,其经水解等反应主要生成丹参素、原儿茶醛、丹酚酸A、迷迭香酸等,且上述成分具有与血必净注射液临床治疗因感染诱发的全身炎症反应综合征相关的抗炎、抗凝血、保护血管内皮细胞等药理作用,可作为丹参的特有性成分[48]。文献报道,李伟等[49]和杨静等[50]预测含有丹参的中成药的Q-marker为酚酸类成分丹参素、原儿茶醛、迷迭香酸、丹酚酸A和丹酚酸B。因此,丹酚酸B、丹参素、原儿茶醛、迷迭香酸、丹酚酸A可作为丹参的特有性成分。
3 基于成分与药效关联的Q-marker预测分析质量控制的根本目的是对中药有效性的控制,有效性体现中药的“物质基础”作用人体疾病主体的不同层面、不同方式的生物效应表达形式,而有效性成分是阐释中药的药效物质基础、作用原理以及配伍规律、指导临床实践的重要依据和研究路径,将有效性成分纳入中药质量评价,才能反映中药质量的完整性[51]。因此,“有效”是确定Q-marker的核心要素。现代药理学研究表明血必净注射液具有抗炎、调节免疫和保护血管内皮细胞等作用,临床多用于治疗肺炎等炎症性疾病。
研究发现,血必净注射液中的羟基红花黄色素A、丹参素、氧化芍药苷、苯甲酰芍药苷、洋川芎内酯H和洋川芎内酯Ⅰ能降低肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)-6和IL-8等炎症因子及诱导型一氧化氮合酶(iNOS)、环氧合酶2(COX-2)等炎症相关酶的含量,表明上述成分具有抗炎作用,可增强血必净注射液对机体炎症的治疗作用[42-55]。丹酚酸B可增加高脂日粮饲养小鼠外周血及脾脏CD4+、CD19+细胞数量,减少CD8+细胞数量,调节机体免疫,从而协同抗炎作用[56]。羟基红花黄色素A、丹酚酸B、芍药苷和芍药内酯苷均能够提高内皮型一氧化氮合酶(eNOS)磷酸化和一氧化氮(NO)代谢产物含量,调节内皮素-1(ET-1)、NO平衡,增强血必净注射液对血管内皮细胞保护作用,减轻炎症导致的血管内皮损伤[57-59]。
综上,羟基红花黄色素A、丹酚酸B、洋川芎内酯Ⅰ、洋川芎内酯H、芍药苷、芍药内酯苷、丹参素、氧化芍药苷和苯甲酰芍药苷是血必净注射液发挥抗炎、调节免疫及保护血管内皮细胞作用的有效成分,可作为血必净注射液Q-marker的筛选参考。
4 基于网络药理学对复方配伍环境的Q-marker预测分析复方是中药临床应用较多的形式,同一味中药在不同复方中发挥的作用及其药效物质基础不尽相同,既体现在不同作用靶点、不同信号通路协同拮抗作用,又涉及吸收、代谢等体内过程的交互作用。因此,需针对具体疾病病因病机和治法治则,基于网络药理学,从复方配伍环境出发,根据中药临床运用时最终效应成分及其功效的临床表达形式,确定复方Q-marker的配伍特点。
基于网络药理学,建立血必净注射液“药材-成分-靶点-疾病”网络,预测血必净注射液治疗新型冠状病毒肺炎(COVID-19)的Q-marker[60]。选取血必净注射液中包括黄酮类、单萜苷类、酚酸类等类型在内的36个主要活性成分,采用TCMSP、PubChem、TargetNet数据库预测447个活性成分靶点,并在Genecards数据库中挖掘259个COVID-19疾病靶点。通过STRING10、DAVID和KEGG等相关数据库,预测血必净注射液治疗COVID-19主要通过其活性成分作用于PTGS2、PTGS1、CASP3、RELA、TNF、MAPK1、IL-2、IL-6和IL-10等靶点有关的IL-17信号通路、甲型流感、乙型和丙型病毒性肝炎及炎性肠病等通路发挥作用。从网络药理学角度,阐释血必净注射液多成分、多靶点、多途径治疗COVID-19的科学内涵。此外,还发现血必净注射液36个主要活性成分中有效成分综合评分最高的10个活性成分是槲皮素、没食子酸、木犀草素、迷迭香酸、芦丁、山萘酚、绿原酸、丹参酮ⅡA、羟基红花黄色素A和芍药苷,提示其是血必净注射液治疗COVID-19的重要活性成分,可作为血必净注射液的Q-marker。
5 基于成分可测性的Q-marker预测分析Q-marker能够为建立质量标准提供依据,因此,“成分的可测性”是确定Q-marker的必要条件。由于中药化学成分复杂,质量评价不仅需要以某些成分的含量作为指标,还需对中药的整体“化学轮廓”进行研究。含量测定指标成分具有可测性,是质量评价最重要的指标,也是评价质量优劣和合格限度的“金指标”。指纹图谱作为一种综合的、可量化的色谱鉴定手段,能较为客观地反映全方的物质基础和化学成分群的整体性与复杂性,可用于评价质量的一致性[61],故本研究从含量测定和指纹图谱两个方面预测血必净注射液具有可测性的Q-marker。
首先通过含量测定预测血必净注射液中具有可测性的Q-marker,《中华人民共和国药典》“含量测定”项下绝大部分使用高效液相色谱(HPLC)法测定,未出现使用液质联用法测定含量,故本研究预测可用HPLC法测定的血必净注射液的Q-marker。2020年版《中华人民共和国药典》规定的红花、赤芍、丹参、当归、川芎的8个含量测定指标成分羟基红花黄色素A、山柰素、芍药苷、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、丹酚酸B和阿魏酸均采用HPLC法测定[62],表明其8个指标成分均具有可测性。但各指标成分含量测定色谱条件不同,不能采用《中华人民共和国药典》色谱条件同时测定血必净注射液中化学成分的含量。冀兰鑫等[63]建立同时测定血必净注射液中没食子酸、原儿茶醛、洋川芎内酯Ⅰ、洋川芎内酯H和丹酚酸B的HPLC法,李娣等[64]建立不同波长下同时测定血必净注射液中丹参素、羟基红花黄色素A、芍药苷、阿魏酸、洋川芎内酯Ⅰ的HPLC法,两种方法简便、快速、准确,能有效控制血必净注射液的质量。综上,表明上述成分羟基红花黄色素A、山柰素、芍药苷、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、丹酚酸B、阿魏酸、没食子酸、原儿茶醛、洋川芎内酯Ⅰ、洋川芎内酯H和丹参素具有可测性,可作为血必净注射液具有可测性的Q-marker。
其次根据指纹图谱预测血必净注射液中具有可测性的Q-marker。中药为多成分的复杂体系,多年来《中华人民共和国药典》一直采用1~2个指标成分控制中药质量,这与中药所含化学成分复杂、发挥药效时多成分、多靶点协同作用的特性不甚吻合。为加强中药质量的整体控制,指纹图谱在《中华人民共和国药典》中的应用逐渐增加,从整体化学轮廓的角度评价中药质量概貌,结合含量测定,使中药质量可控性明显增强。采用HPLC法建立10批血必净注射液指纹图谱,相似度均大于0.90,标定18个共有峰,经与对照品比对,共指认了6个色谱峰,分别为原儿茶醛、羟基红花黄色素A、芍药苷、阿魏酸、洋川芎内酯Ⅰ、丹酚酸B[65],增加血必净注射液质量的整体可控性。故基于Q-marker“五原则”的可测性,从含量测定和指纹图谱两个方面预测血必净注射液中具有可测性的成分有羟基红花黄色素A、丹参素、山柰素、芍药苷、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、丹酚酸B、没食子酸、阿魏酸、洋川芎内酯Ⅰ、洋川芎内酯H、原儿茶醛,可作为血必净注射液的Q-marker。
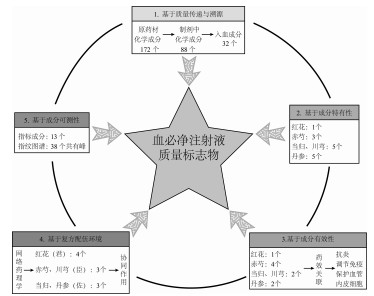
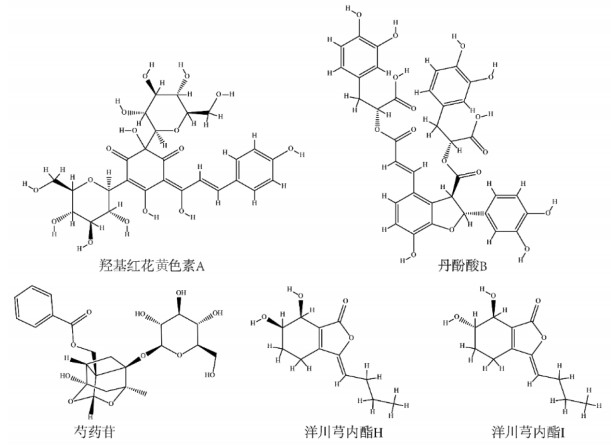
综上,基于Q-marker的传递与溯源、特有、有效、复方配伍和可测的“五原则”,建立血必净注射液Q-marker发现的研究路径,见图 2。在血必净注射液Q-marker预测分析中,发现不同原则下预测得到的血必净注射液Q-marker有所差异,故选取与血必净注射液有效性密切相关、具有溯源性、可测性强、特有性好的羟基红花黄色素A、丹酚酸B、芍药苷、洋川芎内酯Ⅰ、洋川芎内酯H作为血必净注射液的Q-marker,具体信息见表 1及图 3。
|
| 图 2 基于“五原则”的血必净注射液的Q-marker发现的研究路径 Fig. 2 Research approach of Q-marker of Xuebijing injection based on" five principles" |
|
| 图 3 血必净注射液Q-marker分子结构信息 Fig. 3 Molecular structure information of Q-markers of Xuebijing injection |
血必净注射液是中国唯一被批准治疗全身炎症反应综合征和多器官功能障碍的中药注射剂,但其未被《中华人民共和国药典》收录。2020年版《中华人民共和国药典》规定了血必净注射液中5味单药材的指标成分含量,但各单味药指标成分含量测定方法不尽相同。因此,本研究为保证血必净注射液的临床用药安全有效,基于Q-marker的“五原则”预测血必净注射液的Q-marker:1)通过对血必净注射液原药材、注射液及其入血成分的系统辨识及对比归属,预测32个入血成分作为血必净注射液中具有质量传递与溯源性的Q-marker。2)从含量测定和指纹图谱两个方面,预测13个化学成分作为血必净注射液中具有可测性的的Q-marker。3)根据化学成分的含量高低及药理作用,分别预测14个化学成分作为血必净注射液中具有特有性的Q-marker和9个化学成分作为血必净注射液中与药效关联的Q-marker。4)基于网络药理学阐释血必净注射液君臣佐使协同发挥COVID-19药效的配伍特色,并预测10个活性成分作为体现血必净注射液复方配伍环境的Q-marker。结果发现不同原则下预测血必净注射液Q-marker有所差异,但中药复方Q-marker应同时满足“五原则”。故选取与血必净注射液有效性密切相关、具有溯源性、可测性强、特有性好的羟基红花黄色素A、丹酚酸B、芍药苷、洋川芎内酯Ⅰ、洋川芎内酯H作为血必净注射液的Q-marker,后期通过建立同时测定血必净注射液中羟基红花黄色素A、丹酚酸B、芍药苷、洋川芎内酯Ⅰ、洋川芎内酯H含量的HPLC方法,评价血必净注射液的质量优劣,为血必净注射液的临床研究和质量控制研究提供依据。
| [1] |
张铁军, 白钢, 陈常青, 等. 基于"五原则"的复方中药质量标志物(Q-marker)研究路径[J]. 中草药, 2018, 49(1): 1-13. ZHANG T J, BAI G, CHEN C Q, et al. Research approaches of quality marker (Q-marker) of Chinese materia medica formula based on "five principles"[J]. Chinese Traditional and Herbal Drugs, 2018, 49(1): 1-13. |
| [2] |
唐于平, 尚尔鑫, 陈艳琰, 等. 中药质量标志物分级辨识与传递变化规律研究思路与方法[J]. 中国中药杂志, 2019, 44(14): 3116-3122. TANG Y P, SHANG E X, CHEN Y Y, et al. Research thoughts and methods on grading identification and transmission change law of traditional Chinese medicine (TCM) Q-marker[J]. China Journal of Chinese Materia Medica, 2019, 44(14): 3116-3122. |
| [3] |
刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker): 中药产品质量控制的新概念[J]. 中草药, 2016, 47(9): 1443-1457. LIU C X, CHEN S L, XIAO X H, et al. A new concept on quality marker of Chinese materia medica: Quality control for Chinese medicinal products[J]. Chinese Traditional and Herbal Drugs, 2016, 47(9): 1443-1457. |
| [4] |
ZHANG Q F, LI J, LIANG X L, et al. The preventive effect of Chinese herbal preparation Xuebijing against hyperactive inflammation after hepato-pancreato-biliary surgery[J]. Annals of Translational Medicine, 2019, 7(18): 481. DOI:10.21037/atm.2019.07.78 |
| [5] |
丁园园, 张冬华, 张荣生, 等. 基于网络药理学研究血必净注射液治疗肝脏缺血再灌注损伤的作用机制[J]. 海南医学院学报, 2021, 27(3): 212-221, 228. DING Y Y, ZHANG D H, ZHANG R S, et al. Mechanism of Xuebijing Injection on Hepatic ischemia-reperfusion injury based on network pharmacology[J]. Journal of Hainan Medical University, 2021, 27(3): 212-221, 228. |
| [6] |
梁群, 关迪新, 车思桦. 血必净注射液治疗脓毒症的研究进展[J]. 天津中医药, 2019, 36(7): 641-644. LIANG Q, GUAN D X, CHE S H. Research progress of Xuebijing Injection in the treatment of sepsis[J]. Tianjin Journal of Traditional Chinese Medicine, 2019, 36(7): 641-644. |
| [7] |
赵紫楠, 张碧华, 李可欣, 等. 血必净注射液的快速卫生技术评估[J]. 中国合理用药探索, 2020, 17(9): 6-14. ZHAO Z N, ZHANG B H, LI K X, et al. A rapid health technology assessment of Xuebijing Injection[J]. Chinese Journal of Rational Drug Use, 2020, 17(9): 6-14. |
| [8] |
靳英辉, 蔡林, 程真顺, 等. 新型冠状病毒(2019-nCoV)感染的肺炎诊疗快速建议指南(标准版)[J]. 解放军医学杂志, 2020, 45(1): 1-20. JIN Y H, CAI L, CHENG Z S, et al. A rapid advice guideline for the diagnosis and treatment of 2019 novel coronavirus (2019-nCoV) infected pneumonia(standard version)[J]. Medical Journal of Chinese People's Liberation Army, 2020, 45(1): 1-20. |
| [9] |
GUO H, ZHENG J Y, HUANG G, et al. Xuebijing injection in the treatment of COVID-19:a retrospective case-control study[J]. Annals of Translational Medicine, 2020, 9(5): 3235-3248. |
| [10] |
华远铎. 血必净注射液辅助治疗对重症肺炎患者免疫功能及血气分析的影响[J]. 齐齐哈尔医学院学报, 2020, 41(17): 2151-2152. HUA Y D. Effect of Xuebijing Injection on immune function and blood gas analysis in patients with severe pneumonia[J]. Journal of Qiqihar Medical University, 2020, 41(17): 2151-2152. DOI:10.3969/j.issn.1002-1256.2020.17.014 |
| [11] |
刘昌孝. 中药质量标志物(Q-marker): 提高中药质量标准及质量控制理论和促进中药产业科学发展[J]. 中草药, 2019, 50(19): 4517-4518. LIU C X. Quality marker(Q-marker) of Chinese materia medica: improving quality standard and quality control theory of CMM and promoting scientific development of CMM industry[J]. Chinese Traditional and Herbal Drugs, 2019, 50(19): 4517-4518. DOI:10.7501/j.issn.0253-2670.2019.19.001 |
| [12] |
康家珍, 罗兰, 冀苏龙, 等. 基于液质联用技术的脑得生中红花成分分析[J]. 广东化工, 2018, 45(7): 32-33. KANG J Z, LUO L, JI S L, et al. Analysis of the components of Carthami Flos in Naodesheng based on the technique of liquid chromatography-use[J]. Guangdong Chemical Industry, 2018, 45(7): 32-33. DOI:10.3969/j.issn.1007-1865.2018.07.016 |
| [13] |
王松松, 马艳, 张毅, 等. UHPLC-MS/MS快速鉴别红花中的化学成分[J]. 中国中药杂志, 2015, 40(7): 1347-1354. WANG S S, MA Y, ZHANG Y, et al. Rapid identification of chemical composition in Carthami Flos with UHPLC-LTQ-Orbitrap[J]. China Journal of Chinese Materia Medica, 2015, 40(7): 1347-1354. |
| [14] |
黄壮壮, 孙宇宏, 许刚, 等. 基于UPLC同测定3种成分法评价新疆主产区红花的品质[J]. 中药材, 2018, 41(9): 2150-2152. HUANG Z Z, SUN Y H, XU G, et al. Quality evaluation of Carthami Flos in Xinjiang based on UPLC simultaneous determination of three components[J]. Journal of Chinese Medicinal Materials, 2018, 41(9): 2150-2152. |
| [15] |
李石飞, 袁茂叶, 张立伟. HPLC-DAD同时测定红花中4种亚精胺成分[J]. 中国中药杂志, 2016, 41(8): 1480-1484. LI S F, YUAN M Y, ZHANG L W. Simultaneous determination of four coumaroyl spermidine constituents in Carthami Flos by HPLC-DAD[J]. China Journal of Chinese Materia Medica, 2016, 41(8): 1480-1484. |
| [16] |
余捷婧, 吴金雄, 梁亚凤, 等. HPLC同时测定赤芍和白芍中没食子酸等6种成分的量[J]. 中草药, 2015, 46(11): 1673-1677. YU J J, WU J X, LIANG Y F, et al. Simultaneous quantitative determination of six active compounds from Paeoniae Rubra Radix and Paeoniae Alba Radix by HPLC[J]. Chinese Traditional and Herbal Drugs, 2015, 46(11): 1673-1677. |
| [17] |
刘杰, 陈琳, 范彩荣, 等. 基于HPLC-DAD-Q-TOF-MS/MS的白芍和赤芍主要成分定性定量研究[J]. 中国中药杂志, 2015, 40(9): 1762-1770. LIU J, CHEN L, FAN C R, et al. Qualitative and quantitative analysis of major constituents of Paeoniae Radix Alba and Paeoniae Radix Rubra by HPLC-DAD-Q-TOF-MS/MS[J]. China Journal of Chinese Materia Medica, 2015, 40(9): 1762-1770. |
| [18] |
李瑞, 李彦程, 武玉卓, 等. 赤芍水提物化学成分的研究[J]. 中国中药杂志, 2018, 43(14): 2956-2963. LI R, LI Y C, WU Y Z, et al. Chemical constituents from water-soluble extract of dry roots of Paeonia lactiflora[J]. China Journal of Chinese Materia Medica, 2018, 43(14): 2956-2963. |
| [19] |
王彦志, 石任兵, 刘斌. 赤芍化学成分的分离与结构鉴定[J]. 北京中医药大学学报, 2006, 29(4): 267-269. WANG Y Z, SHI R B, LIU B. Isolation and structure identification of chemical principles from Paeonia Lactiflora Pall[J]. Journal of Beijing University of Traditional Chinese Medicine, 2006, 29(4): 267-269. DOI:10.3321/j.issn:1006-2157.2006.04.014 |
| [20] |
冯超. 赤芍与白芍的药动学研究与化学成分的液质联用分析[D]. 石家庄: 河北医科大学, 2010. FENG C. Studies on pharmacokinetic properties and chemical constituents of Radix Paeoniae Rubra and Radix Paeoiae Alba with HPLC-MS[D]. Shijiazhuang: Hebei Medical University, 2010. |
| [21] |
王薇. 赤芍化学成分和药理作用的研究进展[J]. 黑龙江科技信息, 2015, 19(17): 109. WANG W. Research progress on chemical constituents of Paeoniae Rubra Radix and their pharmacological effects[J]. Scientific and Technological Innovation, 2015, 19(17): 109. DOI:10.3969/j.issn.1673-1328.2015.17.104 |
| [22] |
陈嘉慧, 张雅心, 刘孟华, 等. 基于UPLC-Q-TOF-MS/MS技术的丹参水提液全成分分析[J]. 广东药科大学学报, 2020, 36(1): 1-9. CHEN J H, ZHANG Y X, LIU M H, et al. Chemical profiling of Danshen water extract by UPLC-Q-TOF-MS/MS[J]. Journal of Guangdong Pharmaceutical University, 2020, 36(1): 1-9. |
| [23] |
程沛, 韩东岐, 胡伟慧, 等. 高效液相色谱法同时测定丹参中10种水溶性和4种脂溶性成分的含量[J]. 药物分析杂志, 2015, 35(6): 991-996. CHENG P, HAN D Q, HU W H, et al. Simultaneous determination of ten hydrophilic compounds and four lipophilic compounds in Radix Salviae Miltiorrhizae by HPLC[J]. Chinese Journal of Pharmaceutical Analysis, 2015, 35(6): 991-996. |
| [24] |
霍铭, 杨子华. 不同产地丹参药材中丹参酮ⅡA与丹酚酸B的含量测定[J]. 中国处方药, 2020, 18(10): 38-39. HUO M, YANG Z H. Determination of tanshinone ⅡA and salvianolic acid B in Salvia miltiorrhiza from different habitats[J]. Journal of China Prescription Drug, 2020, 18(10): 38-39. DOI:10.3969/j.issn.1671-945X.2020.10.017 |
| [25] |
田璐, 闫海霞, 傅欣彤, 等. 一测多评法同时测定川芎、当归饮片中多种化学成分的含量[J]. 药物分析杂志, 2014, 34(5): 848-854. TIAN L, YAN H X, FU X T, et al. Simultaneous determination of multiple components in decoction pieces of Chuanxiong Rhizoma and Angelicae Sinensis Radix by quantitative analysis of multi-components by single maker[J]. Chinese Journal of Pharmaceutical Analysis, 2014, 34(5): 848-854. |
| [26] |
潘明凤. 川芎的化学成分研究与多指标成分的含量测定[D]. 成都: 西南交通大学, 2014. PAN M F. Studies on chemical constituents of Chuanxiong Rhizoma and content determination of multi-marker compounds[D]. Chengdu: Southwest Jiaotong Uninversity, 2014. |
| [27] |
李伟霞, 唐于平, 尚尔鑫, 等. 当归、川芎和归芎药对中主要芳香酸类成分在血虚大鼠体内的代谢研究[J]. 中华中医药杂志, 2013, 28(5): 1212-1218. LI W X, TANG Y P, SHANG E X, et al. Identification on the metabolites of main aromatic acids from Danggui, Chuanxiong and the Gui-Xiong herb pair in blood deficiency rats[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2013, 28(5): 1212-1218. |
| [28] |
高昕, 孙文军, 岐琳, 等. 基于超高效液相色谱-电喷雾-飞行时间质谱的川芎化学成分的快速分析[J]. 西北药学杂志, 2018, 33(6): 711-715. GAO X, SUN W J, QI L, et al. Ultra-performance liquid chromatography coupled with electrospray ionization/quadrupole time-of-flight mass spectrometry for the rapid analysis of constituents in Chuanxiong Rhizoma[J]. Northwest Pharmaceutical Journal, 2018, 33(6): 711-715. DOI:10.3969/j.issn.1004-2407.2018.06.001 |
| [29] |
鄢玉芬, 徐双美, 梁乙川, 等. HPLC法测定不同贮藏条件下川芎中10种化学成分的含量[J]. 中国药房, 2019, 30(6): 807-812. YAN Y F, XU S M, LIANG Y C, et al. Content determination of 10 kinds of chemical components in Ligusticum chuanxiong under different storage conditions by HPLC[J]. China Pharmacy, 2019, 30(6): 807-812. |
| [30] |
吴燕, 李青苗, 李彬, 等. UPLC测定川芎地上部分中的3种活性成分[J]. 华西药学杂志, 2018, 33(5): 526-528. WU Y, LI Q M, LI B, et al. Determination of three kinds of active component from the stems and leaves of Ligusticum chuanxiong by UPLC[J]. West China Journal of Pharmaceutical Sciences, 2018, 33(5): 526-528. |
| [31] |
张晓娟, 张燕丽, 左冬冬. 川芎的化学成分和药理作用研究进展[J]. 中医药信息, 2020, 37(6): 128-133. ZHANG X J, ZHANG Y L, ZUO D D. Research progress on chemical constituents and pharmacological effects of Ligusticum chuanxiong[J]. Information on Traditional Chinese Medicine, 2020, 37(6): 128-133. |
| [32] |
杨蕊菁, 赵磊, 夏鹏飞, 等. 不同产地当归药材9种成分的含量测定及主成分分析[J]. 中药新药与临床药理, 2020, 31(4): 473-477. YANG R J, ZHAO L, XIA P F, et al. Determination and principal component analysis of nine components of Angelica sinensis from different origins[J]. Traditional Chinese Drug Research and Clinical Pharmacology, 2020, 31(4): 473-477. |
| [33] |
WU Y Y, WANG L, LIU G X, et al. Characterization of principal compositions in the roots of Angelica sinensis by HPLC-ESI-MSn and chemical comparison of its different parts[J]. Journal of Chinese Pharmaceutical Sciences, 2014, 23(6): 393-402. |
| [34] |
SUN Z, ZUO L, SUN T, et al. Chemical profiling and quantification of Xuebijing Injection, a systematic quality control strategy using UHPLC-Q exactive hybrid quadrupole-orbitrap high-resolution mass spectrometry[J]. Science Report, 2017, 7(1): 16921. DOI:10.1038/s41598-017-17170-y |
| [35] |
SHENG C, PENG W, XIA Z, et al. Plasma and cerebrospinal fluid pharmacokinetics of hydroxysafflor yellow A in patients with traumatic brain injury after intravenous administration of Xuebijing using LC-MS/MS method[J]. Xenobiotica, 2020, 50(5): 545-551. DOI:10.1080/00498254.2019.1668983 |
| [36] |
ZUO L, ZHONG Q, WANG Z, et al. Simultaneous determination and pharmacokinetic study of twelve bioactive compounds in rat plasma after intravenous administration of Xuebijing Injection by UHPLC-Q-Orbitrap HRMS[J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 14(6): 347-353. |
| [37] |
欧阳慧子, 何俊. LC-MS/MS测定血必净注射液中9种有效成分在大鼠体内血药浓度及药代动力学研究[J]. 中国中药杂志, 2018, 43(17): 3553-3561. OUYANG H Z, HE J. Simultaneous determination of nine constituents of Xuebijing Injection in rat plasma and their pharmacokinetics by LC-MS/MS[J]. China Journal of Chinese Materia Medica, 2018, 43(17): 3553-3561. |
| [38] |
陈向梅, 王晓雯, 骆晶, 等. 血必净注射液大鼠体内的药动学研究[J]. 药物分析杂志, 2012, 32(5): 744-748. CHEN X M, WANG X W, LUO J, et al. Pharmacokinetic studies of Xuebijing Injection in rats[J]. Chinese Journal of Pharmaceutical Analysis, 2012, 32(5): 744-748. |
| [39] |
张纳婷. 抗脓毒症中药血必净注射液苯酞类成分药代动力学研究[D]. 上海: 中国科学院大学, 2018. ZHANG N T. Pharmacokinetics-based identification of potential therapeutic phthalides from Xuebijing, a Chinese herbal injection used in sepsis management[D]. Shanghai: University of Chinese Academy of Science, 2018. |
| [40] |
LI X, CHENG C, WANG F, et al. Pharmacokinetics of catechols in human subjects intravenously receiving Xuebijing Injection, an emerging antiseptic herbal medicine[J]. Drug Metabolism and Pharmacokinetics, 2016, 31(1): 95-98. DOI:10.1016/j.dmpk.2015.10.005 |
| [41] |
CHENG C, LIN J Z, LI L, et al. Pharmacokinetics and disposition of monoterpene glycosides derived from Paeonia lactiflora roots (Chishao) after intravenous dosing of antiseptic Xuebijing Injection in human subjects and rats[J]. Acta Pharmacologica Sinca, 2016, 37(4): 530-544. DOI:10.1038/aps.2015.103 |
| [42] |
张东博, 孙琛, 刘红波, 等. 红花叶中1个新的生物碱类化合物[J]. 中草药, 2019, 50(1): 22-24. ZHANG D B, SUN C, LIU H B, et al. A new alkaloid isolated from leaves of Carthamus tinctorius[J]. Chinese Traditional and Herbal Drugs, 2019, 50(1): 22-24. |
| [43] |
钟万超, 李瑞, 夏欢, 等. 赤芍中的1个新木脂素苷类化合物[J]. 中国中药杂志, 2020, 45(12): 2903-2906. ZHONG W C, LI R, XIA H, et al. A new lignan glucoside from root of Paeonia lactiflora[J]. China Journal of Chinese Materia Medica, 2020, 45(12): 2903-2906. |
| [44] |
陆小华, 马骁, 王建, 等. 赤芍的化学成分和药理作用研究进展[J]. 中草药, 2015, 46(4): 595-602. LU X H, MA X, WANG J, et al. Research progress on chemical constituents of Paeoniae Rubra Radix and their pharmacological effects[J]. Chinese Traditional and Herbal Drugs, 2015, 46(4): 595-602. DOI:10.7501/j.issn.0253-2670.2014.04.026 |
| [45] |
曹建华, 刘艳之, 刘海霞, 等. 基于"五原则"的脑震宁颗粒质量标志物(Q-marker)的辨识分析[J]. 中草药, 2019, 50(19): 4654-4662. CAO J H, LIU Y Z, LIU H X, et al. Analysis of quality marker in Naozhenning Granule based on "five principles"[J]. Chinese Traditional and Herbal Drugs, 2019, 50(19): 4654-4662. DOI:10.7501/j.issn.0253-2670.2019.19.018 |
| [46] |
陈凌霆, 张静宇, 赵娅敏, 等. 丹参有效成分的研究进展[J]. 山东化工, 2018, 47(20): 38-41. CHEN L T, ZHANG J Y, ZHAO Y M, et al. Research progress on active components and antitumor effects of Salvia Miltiorrhiza[J]. Shandong Chemical Industry, 2018, 47(20): 38-41. DOI:10.3969/j.issn.1008-021X.2018.20.015 |
| [47] |
姜雪, 史磊. 丹参活性成分及药理作用研究进展[J]. 药学研究, 2017, 36(3): 166-169. JIANG X, SHI L. Research progress on active constituents and pharmacological effects of Salvia miltiorrhiza[J]. Journal of Pharmaceutical Research, 2017, 36(3): 166-169. |
| [48] |
王涵, 杨娜, 谭静, 等. 丹参化学成分、药理作用及临床应用的研究进展[J]. 特产研究, 2018, 40(1): 48-53. WANG H, YANG N, TAN J, et al. Research progress on Salvia Miltiorrhiza Bge of the chemical constituents and their pharmacological effects[J]. Special Wild Economic Animal and Plant Research, 2018, 40(1): 48-53. |
| [49] |
李伟, 李淑明, 李挺洋, 等. 复方丹参滴丸中君药丹参的质量标志物研究[J]. 中草药, 2018, 49(9): 2000-2006. LI W, LI S M, LI T Y, et al. Quality marker research of monarch herb Salvia miltiorrhiza in compound Danshen dripping pills[J]. Chinese Traditional and Herbal Drugs, 2018, 49(9): 2000-2006. |
| [50] |
杨静, 江振作, 柴欣, 等. 中药注射液"Q-markers"的辨析研究——丹红注射液研究实例[J]. 世界科学技术-中医药现代化, 2016, 18(12): 2056-2061. YANG J, JIANG Z Z, CHAI X, et al. Differentiation and study on "Q-markers" of traditional Chinese medicine injection-a case study of Danhong Injection[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2016, 18(12): 2056-2061. DOI:10.11842/wst.2016.12.005 |
| [51] |
张铁军, 王杰, 陈常青, 等. 基于中药属性和作用特点的中药质量标志物研究与质量评价路径[J]. 中草药, 2017, 48(6): 1051-1060. ZHANG T J, WANG J, CHEN C Q, et al. Method of quality marker research and quality evaluation of Chinese materia medica based on drug properties and effect characteristics[J]. Chinese Traditional and Herbal Drugs, 2017, 48(6): 1051-1060. |
| [52] |
王金平, 王平, 陈润桦, 等. 羟基红花黄色素A对脓毒症小鼠外周血促炎/抗炎因子的影响[J]. 中山大学学报(医学科学版), 2017, 38(5): 665-669. WANG J P, WANG P, CHEN R H, et al. Effect of Hydroxysafflor Yellow A on pro/anti-inflammatory cytokines in peripheral blood with sepsis in mice[J]. Journal of Sun Yat-sen University(Medical Sciences), 2017, 38(5): 665-669. |
| [53] |
JIANG M, ZHOU M, HAN Y, et al. Identification of NF-κB Inhibitors in Xuebijing Injection for sepsis treatment based on bioactivity-integrated UPLC-Q/TOF[J]. J Ethnopharmacol, 2013, 147(2): 426-433. DOI:10.1016/j.jep.2013.03.032 |
| [54] |
BAE K E, CHOI Y W, KIM S T, et al. Components of rhizome extract of Cnidium officinale Makino and their in vitro biological effects[J]. Molecules, 2011, 16(10): 8833-8847. DOI:10.3390/molecules16108833 |
| [55] |
HU Y Y, WANG Y, LIANG S, et al. Senkyunolide I attenuates oxygen-glucose deprivation/reoxygenation-induced inflammation in microglial cells[J]. Brain Res, 2016, 1649(PtA): 123-131. |
| [56] |
王斌, 崔珏, 肖瀛, 等. 丹酚酸B对高脂日粮小鼠抗氧化与淋巴细胞亚群免疫功能调节的研究[J]. 天然产物研究与开发, 2010, 22(6): 965-971, 1000. WANG B, CUI J, XIAO Y, et al. Antioxidation and immunomodulatory function on lymphocyte subsets of Salvianolic Acid B in high-fat diet fed mouse[J]. Natural Product Research and Development, 2010, 22(6): 965-971, 1000. DOI:10.3969/j.issn.1001-6880.2010.06.010 |
| [57] |
JIN Z, ZHANG W, CHAI W, et al. Antibodies against AT1 receptors are associated with vascular endothelial and smooth muscle function impairment: protective effects of hydroxysafflor yellow A[J]. PLoS One, 2013, 8(6): e67020. DOI:10.1371/journal.pone.0067020 |
| [58] |
REN Y, TAO S, ZHENG S, et al. Salvianolic acid B improves vascular endothelial function in diabetic rats with blood glucose fluctuations via suppression of endothelial cell apoptosis[J]. European Journal of Pharmacology, 2016, 79(1): 308-315. |
| [59] |
乐娜, 周雪, 费文婷, 等. 赤芍、白芍及芍药苷、芍药内酯苷对急性血瘀证大鼠血液流变学及血管内皮功能的影响[J]. 环球中医药, 2019, 12(9): 1302-1307. YUE N, ZHOU X, FEI W T, et al. Effects of Radix Paeoniae Rubra, Radix Paeoniae Alba, paeoniflorin and albiflorin on hemorheology and vascular endothelial function in rats with acute blood stasis syndrome[J]. Global Traditional Chinese Medicine, 2019, 12(9): 1302-1307. DOI:10.3969/j.issn.1674-1749.2019.09.002 |
| [60] |
孔艺, 林莉莉, 陈永, 等. 基于网络药理学探讨血必净注射液治疗新型冠状病毒肺炎机制[J]. 世界科学技术-中医药现代化, 2020, 22(3): 552-560. KONG Y, LIN L L, CHEN Y, et al. Mechanism of Xuebijing Injection on treatment of coronavirus disease 2019 based on network pharmacology[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2020, 22(3): 552-560. |
| [61] |
曹宁宁, 杨文静, 林映仙, 等. 经典名方泽泻汤的HPLC指纹图谱及多指标含量测定研究[J]. 中草药, 2020, 51(10): 2773-2780. CAO N N, YANG W J, LIN Y X, et al. HPLC fingerprint and multi-components determination of classical herbal prescription Zexie decoction[J]. Chinese Traditional and Herbal Drugs, 2020, 51(10): 2773-2780. DOI:10.7501/j.issn.0253-2670.2020.10.019 |
| [62] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2020. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China[M]. Beijing: China Medical Science Press, 2020. |
| [63] |
冀兰鑫, 黄浩, 姜民, 等. HPLC测定血必净注射液内11种主要成分[J]. 中国中药杂志, 2010, 35(18): 2395-2398. JI L X, HUANG H, JIANG M, et al. Simultaneous HPLC determination of 11 essential compounds in Xuebijing Injection[J]. China Journal of Chinese Materia Medica, 2010, 35(18): 2395-2398. |
| [64] |
李娣, 曹雪晓, 蒲位凌, 等. 血必净注射液中有效成分的HPLC法定量检测[J]. 中国现代中药, 2018, 20(9): 1157-1160. LI D, CAO X X, PU W L, et al. Research on quality control method of Xuebijing Injection[J]. Modern Chinese Medicine, 2018, 20(9): 1157-1160. |
| [65] |
黄赵刚, 程钢, 汤浩, 等. 血必净注射液指纹图谱研究[J]. 中国医院药学杂志, 2018, 38(22): 2323-2327. HUANG Z G, CHENG G, TANG H, et al. Studies on HPLC fingerprint of Xuebijing Injection[J]. Chinese Journal of Hospital Pharmacy, 2018, 38(22): 2323-2327. |
2. Traditional Chinese Medicine Research Center, Tasly Holding Group Co. Ltd., Tianjin 300410, China;
3. Zhendong Guangming Pharmaceutical Research Institute, Beijing 100085, China;
4. State Key Laboratory of Drug Delivery Technology and Pharmacokinetics, Tianjin Institute of Pharmaceutical Research, Tianjin 300301, China
 2021, Vol. 38
2021, Vol. 38