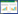文章信息
- 杨熙凯, 王耀光
- YANG Xikai, WANG Yaoguang
- “黄芪-丹参”对单侧输尿管梗阻大鼠肾间质纤维化及低氧诱导因子-1 α表达的影响
- Effect of "astragalus-salvia" on renal interstitial fibrosis and hypoxia inducible Factor-1α expression in rats with unilateral ureteral obstruction
- 天津中医药, 2022, 39(10): 1311-1317
- Tianjin Journal of Traditional Chinese Medicine, 2022, 39(10): 1311-1317
- http://dx.doi.org/10.11656/j.issn.1672-1519.2022.10.16
-
文章历史
- 收稿日期: 2022-06-10
2. 天津中医药大学第一附属医院,天津 300381
慢性肾脏病(CKD)作为一个世界性的公共卫生问题,目前仍然没有治疗疾病的特效药物或者其他根治手段,并且随着疾病的发展,2%的患者会发展为终末期肾脏病(ESRD)[1],给世界各国的卫生资源带来了沉重的压力。肾间质纤维化(RIF)是慢性肾脏疾病进展为终末期肾衰竭必经的病变过程,以肾脏间质中病理性的细胞外基质(ECM)过度沉积导致肾脏组织结构破坏和功能丧失为特征[2],是攻克慢性肾脏病的一个重要难关。其中上皮细胞-间充质细胞转分化是一个重要的细胞转化过程,肾小管上皮细胞受刺激表型转化后分泌促纤维因子并形成间质成纤维细胞[3],是形成RIF的重要途径,值得进一步探明其机制。
缺氧诱导因子(HIF)是一种在缺血或缺氧条件下适应性反应的因子[4],在缺氧状态下血管平滑肌大量分泌HIF-1α亚基,直接刺激其下游靶蛋白血管内皮生长因子(VEGF)高表达,从而参与血管再生、其次通过介导基质金属蛋白酶(MMPs)、GSK/β-catenin信号通路的表达等方式调节细胞外基质的生成与重塑[5],并且有研究表明,在HIF-1α高表达的转基因小鼠中,观察到了ECM的沉积以及间质成纤维细胞的活化,提示了RIF的发生[6]。所以研究其在RIF方面的相互作用及机制也存在较大意义,可能为RIF乃至CKD的诊断、治疗提供新的作用靶点。
“肾疏宁”为全国名中医黄文政教授根据“疏利少阳三焦”学说创立,在治疗肾系疾病方面有着不错的临床疗效[7-9],同时基于疗效的基础实验也从不同角度不同机制证明了“肾疏宁”的有效性,如肾疏宁能抑制系膜增生性肾炎大鼠模型细胞外基质的合成并促进其降解[10-12]。同时,本方蕴含了“补中寓消,消中有补”的治疗思路,结合了补气法及消瘀法。中医以“癥瘕”论述RIF,补气活血是最直接的治疗手段。其中补气、活血法代表药物“黄芪-丹参”药对则最可能为针对性药物,也是实验选择药物的理论依据。
故实验基于“肾疏宁”对RIF的有效性,对方中补气活血药对“黄芪-丹参”进行分析,利用Masson染色、免疫组化等方法对单侧输尿管梗阻(UUO)大鼠肾脏各指标进行检测,旨在研究UUO模型HIF-1α的改变以及“黄芪-丹参”药对的肾保护作用。
1 实验材料 1.1 主要仪器与试剂脱水机,武汉俊杰公司(JJ-12J)、包埋机,金华科迪公司(KD-BM)、梯度PCR仪,美国ABI ProFlex公司(4484073)、荧光定量PCR仪,瑞士Roche公司(LightCycler96)、HP Total RNA Kit,美国Omega Bio-Tek公司(R6812-01)、HiFiScript cDNA Synthesis Kit,北京康为世纪公司(CW2569)、UltraSYBR Mixture(Low ROX),北京康为世纪公司(CW2601S)、Smooth Muscle Actin Rabbit Polyclonal Antibody,武汉Proteintech公司(14395-1-AP)、GAPDH Rabbit Polyclonal antibody,武汉Proteintech公司(10494-1-AP)、Rabbit Anti-HIF-1 alpha antibody,英国abcam公司(ab179483)、辣根酶标记山羊抗兔IgG,北京中杉金桥公司(ZB-2301)。
1.2 实验动物选用大鼠为SPF级健康SD大鼠72只,雄性,体质量(190±10)g,购自北京斯贝福实验动物技术有限公司,许可证号SCXK(京)2016-0002。饲养于天津市中西医结合医院动物房,实验期间饮用水为清洁自来水、自由摄食,实验室自然光照,室温20~24 ℃左右,通风湿度良好,隔两日更换1次垫料,大鼠购回后适应性喂养1周状态良好后进行实验。
1.3 实验药物黄芪、丹参均购自天津中医药大学第一附属医院国药堂。“黄芪-丹参”药对依照肾疏宁[7]的中药配伍比例,成人每日服药用量为黄芪30 g,丹参30 g,每日总生药量为60 g。旋蒸浓缩,将药液浓度浓缩至1.8 g/mL,4 ℃保存,灌胃依照不同剂量稀释。氯沙坦钾片(科素亚)购自天津中医药大学第一附属医院西药房。参考《药理实验方法学》通过人与大鼠间体表面积换算大鼠等效剂量,将氯沙坦钾片用生理盐水溶解,配制为1 mg/mL浓度溶液,4 ℃保存,灌胃时稀释使用。
1.4 UUO模型制备选取RIF常用大鼠适应性喂养1周后开始实验,术前禁食不禁水12 h,将大鼠称质量并记录。使用生理盐水将水合氯醛配置成10%水合氯醛溶液,按照0.3 mL/100 g的剂量对大鼠进行腹腔注射麻醉,麻醉后仰卧位固定,下腹部正中偏左备皮、后进行无菌操作,于大鼠左侧肋腰点切开皮肤层、肌层至腹腔,翻开肠,找到左肾,在左肾下极钝性剥离左侧输尿管,假手术组(Sham)剥离后不作处理,缝合肌层及皮肤层,碘伏及酒精消毒;其余组大鼠使用手术缝合线在输尿管近肾盂段及输尿管远端分别结扎,缝合线间断缝合肌层及皮肤层,碘伏及乙醇消毒,术后3 d予剂量为每鼠8万单位的青霉素腹腔注射防止感染,以肾脏组织Masson染色观察肾小管萎缩、RIF、间质浸润、小管扩张的形成判定UUO模型造模成功。
2 实验方法 2.1 实验分组将72只大鼠依次编号,按照随机数字表法将大鼠分为Sham、模型组(UUO)、芪参低剂量组(UUO+TCM-L)、芪参中剂量组(UUO+TCM-M)、芪参高剂量组(UUO+TCM-H)、氯沙坦组(UUO+Losartan)共6组,每组12只。各组大鼠在手术后1 d开始灌胃,中药参考《药理实验方法学》换算药物浓度进行灌胃,具体如下:1)Sham与UUO组灌服生理盐水。2)UUO+TCM-L:依照1/2等效剂量[2.7 g/(kg·d)]灌胃。3)UUO+TCM-M:依照等效剂量[5.4 g/(kg·d)]灌胃。4)UUO+TCM-H:依照2倍等效剂量[10.8 g/(kg·d)]灌胃。5)UUO+Losartan:依照等效剂量[9 mg/(kg·d)]灌胃。大鼠于给药第13日灌胃后开始禁食不禁水,次日灌胃2 h后开始取材检测。
2.2 肾脏病理标本的制作及Masson染色使用4%多聚甲醛对肾脏组织进行固定,后经过脱水、透明、浸蜡、包埋等步骤制作病理标本,切片后进行Masson染色,之后将染色后切片置于光镜下观察肾脏组织胶原纤维形成情况。对每个样品,进行400×的显微照相,镜下随机选取5个视野进行观察,借助Image J软件,计算肾组织胶原纤维占整个肾组织面积的百分比,得出胶原容积。
2.3 免疫组织化学法将已固定的肾脏组织切片后脱蜡,使用0.01 mmol柠檬酸盐缓冲液进行抗原修复,山羊血清封闭后加入一抗体α-SMA(1∶100稀释),4 ℃过夜。使用生物素化二抗在37 ℃下孵育30 min,链霉卵白素工作液反应后。加二氨基联苯胺法(DAB)显色,后使用苏木素复染,封片后镜下观察,本实验使用免疫组化评分(IHS)对数据进行分析,该方法所得结果近似于基于图像分析软件的评分系统生成的数据[13]。通过将出现免疫反应细胞的百分比(数量得分)与染色强度的估计值(染色强度得分)相结合得出结果。如:数量得分以0~1%=0、1~10%=1、10~50%=2、50~80%=3、80~100%=4记分;细胞染色强度得分以0(阴性)、1(弱阳性)、2(阳性)、3(强阳性)计分。通过5个视野的阅片得出数量得分以及染色强度得分,两者相乘为免疫组化积分。
2.4 聚合酶链式反应(PCR)使用试剂盒提取法提取肾脏组织总RNA,运用HiFiScript cDNA Synthesis Kit进行逆转录,实时定量PCR由Roche LC96系统进行。反应程序如下进行PCR:预变性95 ℃ 10 min,然后40个循环,每个循环包括变性95 ℃ 15 s,退火/延伸60 ℃ 1 min。PCR通过计算基因的相对表达量(2-ΔΔCt)分析结果:以GAPDH为内参基因,计算方法为:ΔΔCt=ΔCt实验组(目的基因Ct值-内参基因Ct值)-ΔCt对照组(目的基因Ct值-内参基因Ct值)。引物序列通过NCBI网站查询,运用BLAST进行序列比对、检验引物特异性。所获得序列由上海生工公司代为合成。序列如下:
Col1:forwards:5'-CGGCTCCTGCTCCTCTTAG-3',reverse:5'-GCCATTGTGGCAGATACAGA-3';FN:forwards:5'-CACCGAAACCGGGAAGAG-3',reverse:5'-TTGCCTAGGTAGGTCCGTTC-3';GAPDH:forwards:5'-TGACAGTGACTTGGGACAAGG-3',reverse:5'-GGAGTTGCTGTTGAAGTCGC-3'。
2.5 蛋白免疫印迹(Western Blot)法检测UUO大鼠肾脏组织中HIF-1α蛋白的表达RIPA裂解肾脏组织,定量后制备蛋白样品后上样,通过10% SurePAGE预制胶电泳分离样品,采用湿式电转膜法将其转移到PVDF膜上。快速封闭液封闭后,将PVDF膜4 ℃下与一抗孵育过夜。一抗Rabbit Anti-HIF-1 alpha antibody(1∶500稀释)、GAPDH Rabbit Polyclonal antibody(1∶10 000稀释)。过夜后二抗孵育1 h,辣根酶标记山羊抗兔IgG(1∶10 000稀释)。之后使用特超敏ECL化学发光试剂盒在成像仪平台可视化蛋白质。应用Image J软件测定目的条带及相应内参的灰度值。结果以目的蛋白灰度值/GAPDH灰度值表示。
2.6 统计学方法利用SPSS 26.0统计分析软件进行分析,计量资料以均数±标准差(x±s)表示,各组数据比较前先进行正态性及方差齐性检验。多组间差异比较采用单因素方差分析(One-Way ANOVA),符合正态分布且方差齐时组间两两比较采用SNK检验,方差不齐时采用Dunnett’s T3检验;不符合正态分布时使用非参数检验。P < 0.05为差异具有统计学意义。
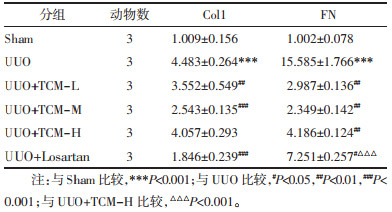
3 实验结果 3.1 Masson染色染色蓝色区域主要为胶原成分。Sham的胶原纤维主要出现在基底膜和系膜区,而与Sham比较,UUO大鼠可见大量蓝色胶原纤维沉积,充斥于肾间质区域。治疗组大鼠肾间质内的蓝色胶原较模型组减少。通过对胶原容积的计算可知,UUO与Sham比较,差异具有统计学意义(P<0.001),UUO+TCM-L较UUO有改善,差异具有统计学意义(P<0.05);UUO+TCM-M、UUO+TCM-H与UUO比较纤维化有改善,差异具有统计学意义(P<0.01);UUO+Losartan与UUO及UUO+TCM-H比较,差异具有统计学意义(P<0.001)。见图 1。
|
| 注:与Sham比较,***P<0.001;与UUO比较,#P<0.05,##P<0.01,###P<0.001;与UUO+TCM-H比较,△△△P<0.001;bar=20 μm,n=3。 图 1 Masson染色及胶原容积情况(x±s,×400) Fig. 1 Masson staining and collagen volume(x±s, ×400) |
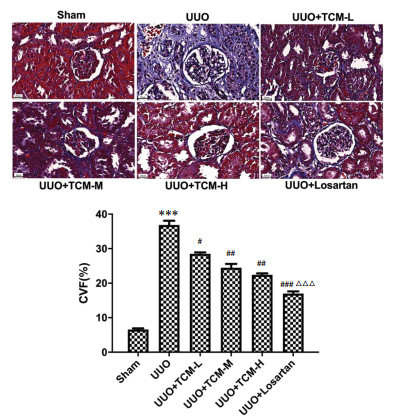
UUO手术后出现了α-SMA的高表达,蛋白的沉积主要出现在肾间质及肾小管上皮细胞。根据免疫组化积分,大鼠UUO相较Sham蛋白表达增加,差异具有统计学意义(P<0.001),在服用芪参中、高剂量以及氯沙坦后蛋白表达均有改善,差异具有统计学意义(P<0.01),UUO+TCM-L与UUO比较有改善,差异具有统计学意义(P<0.05)。见图 2。
|
| 注:与Sham比较,***P<0.001;与UUO比较,#P<0.05,##P<0.01;bar=20 μm,n=3。 图 2 α-SMA蛋白表达及免疫组化反应积分(x±s,×400) Fig. 2 Expression level of α-SMA and IHS(x±s, ×400) |
UUO大鼠对比Sham,Col1、FN mRNA表达水平升高,差异具有统计学意义(P<0.001);UUO+TCM-L与UUO比较时,差异具有统计学意义(P<0.01);对于Col1 mRNA表达的改善,UUO+TCM-M、UUO+Losartan均有较好效果,与UUO比较,有下降,差异具有统计学意义(P<0.001);在抑制FN mRNA表达方面UUO+TCM-M、UUO+TCM-H与UUO相比,均有改善,差异具有统计学意义(P<0.01);UUO+Losartan与UUO+TCM-H比较,差异具有统计学意义(P<0.001)。见表 1。
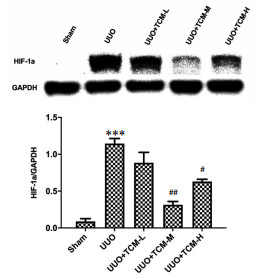
实验以观察中药在HIF-1α蛋白在肾脏组织中的表达,不涉及疗效观察,故不设置UUO+Losartan。UUO术后大鼠的HIF-1α蛋白表达水平明显升高,UUO大鼠对比Sham,差异具有统计学意义(P<0.001);同时芪参组对于HIF-1α蛋白表达水平的升高具有一定的抑制作用,UUO+TCM-M较UUO有明显改变,差异具有统计学意义(P<0.01);UUO+TCM-H较UUO有一定改善,差异具有统计学意义(P<0.05)。见图 3。
|
| 注:与Sham比较,***P<0.001;与UUO比较,#P<0.05,##P<0.01。 图 3 HIF-1α蛋白表达水平(x±s,n=3) Fig. 3 Hif-1α protein expression level(x±s, n=3) |
肾纤维化是所有CKD的发展过程,肾脏疾病的进展,本质上是肾纤维化的一步步加重,直至最终肾脏萎缩,失去其应有功能。肾纤维化过程中存在肾小球硬化、RIF、血管纤维化等方面的病理改变,RIF作为重要的一个环节存在着深入研究的价值。UUO模型,是通过结扎一侧输尿管引起尿路梗阻,造成肾脏结构的进行性破坏,出现RIF的模型。在啮齿类动物中,UUO被认为是研究非免疫性肾小管间质纤维化机制最广泛使用的模型[14]。其特点在于能够快速的形成管状萎缩和间质纤维化,出现细胞外基质沉积[15]。能迅速形成与人类疾病相似的纤维化事件[16],故本研究使用SD大鼠的UUO模型进行RIF的研究。
在中医理论研究中,RIF被归为“癥瘕”的范畴[17]。叶天士在《临证指南医案》中强调“大凡经主气,络主血,久病血瘀”。说明瘀血是形成癥瘕的主要病机,治疗时最宜补气活血治之。就如唐容川《血证论》中强调:“瘀血在经络脏腑之间,则结为癥瘕……即虚人久积,不便攻治者,亦宜攻补兼施,以求克敌。”肾疏宁虽以“疏利三焦”法立方,但肾脏疾病患者久病血瘀,虽有癥瘕不便破血行气,故应当攻补兼施,补气活血。选用黄芪、丹参作为方中臣药,黄芪益卫固表,升阳举陷,补养元气、肾气;丹参活血祛瘀,安神宁心。作为肾疏宁方中祛瘀“重臣”,“黄芪-丹参”药对长于补气活血,两药配伍,消补结合,祛除肾脏癥瘕。为“黄芪-丹参”药对治疗RIF提供了理论依据。
本研究结果显示,UUO术后的大鼠出现了明显的肾脏损伤,Masson染色提示肾脏组织中胶原纤维的产生,在Sham中可以看到少量胶原纤维出现在肾间质,用于稳定肾脏结构,是正常的生理结构。当输尿管梗阻术后大量的胶原纤维产生,出现在了肾间质以及肾小球内。通过胶原容积的计算发现,中药组在术后减轻了纤维化的沉积。长期以来,慢性缺氧一直被认为是各种类型慢性肾病的最终共同病理状态。RIF造成了对肾小管周毛细血管的包围与挤压,血流的减少使得肾间质周围各类细胞出现了缺氧,在本次UUO模型中也检测到了缺氧诱导因子的表达,UUO对比Sham HIF-1α的表达明显升高,同时越来越多的证据表明,HIF-1α是RIF的关键因素[18-20]。过表达的HIF-1α进一步加重了纤维化的进展[21],并在临床上展现了与慢性肾脏病的病情进展的相关性[22]。有证据显示,在纤维化过程中,HIF-1α可诱导纤维化标志物(Ⅰ型胶原、Ⅲ型胶原)和转分化标志蛋白(波形蛋白、平滑肌动蛋白)的改变[23-24]。实验通过免疫组化观察到,本应在肾小球系膜区少量表达的α-SMA在UUO术后高表达,并且异常出现在了肾小管上皮细胞,提示了UUO术后肾小管上皮细胞发生了表型转化。说明了肌成纤维细胞的形成。同时利用PCR技术也检测到了肾脏组织中Col1、FN出现了升高,作为细胞外基质的主要构成成分,以上两指标的升高也提示了肾脏组织细胞外基质的异常增多。
而在UUO大鼠接受“黄芪-丹参”药物治疗后,RIF情况得到改善。目前已有人对“黄芪-丹参”药对在肾间质纤维化的作用进行了研究[25],周萍等[26]同样使用大鼠UUO模型进行观察,对成模大鼠进行“黄芪-丹参”药对颗粒剂溶液灌胃治疗,治疗后大鼠肾功能水平较UUO改善,并促进了par-3蛋白表达,从而延缓肾间质纤维化。而在本次研究中,结果显示当经过“黄芪-丹参”治疗后,胶原纤维沉积减少,说明了“黄芪-丹参”药对在治疗RIF方面的作用;药物治疗可能一定程度缓解了受损肾脏组织的缺氧情况,HIF-1α的表达较UUO出现下降,且下降趋势明显;细胞外基质主要成分的过表达得到抑制、表型转化标志蛋白表达降低,证明了中药在抑制肾小管上皮细胞-间充质细胞转分化上的良好作用。综上所述,“黄芪-丹参”药对可能通过改善缺氧情况,下调HIF-1α的表达,从而抑制细胞外基质的生成及减轻肾小管上皮细胞-间充质细胞转分化,进而延缓RIF的进展。
| [1] |
张路霞, 王海燕. 中国慢性肾脏病的现状及挑战: 来自中国慢性肾脏病流行病学调查的启示[J]. 中华内科杂志, 2012, 51(7): 497-498. ZHANG L X, WANG H Y. The status quo and challenges of diseases in southern China: enlightenment from the investigation of chronic diseases in China[J]. Chinese Journal of Internal Medicine, 2012, 51(7): 497-498. DOI:10.3760/cma.j.issn.0578-1426.2012.07.001 |
| [2] |
IWANO M, NEILSON E G. Mechanisms of tubulointerstitial fibrosis[J]. Current Opinion in Nephrology and Hypertension, 2004, 13(3): 279-284. DOI:10.1097/00041552-200405000-00003 |
| [3] |
LI R, GUO Y J, ZHANG Y M, et al. Salidroside ameliorates renal interstitial fibrosis by inhibiting the TLR4/NF-κB and MAPK signaling pathways[J]. International Journal of Molecular Sciences, 2019, 20(5): E1103. DOI:10.3390/ijms20051103 |
| [4] |
HEYMAN S N, LEIBOWITZ D, MOR-YOSEF LEVI I, et al. Adaptive response to hypoxia and remote ischaemia pre-conditioning: a new hypoxia-inducible factors era in clinical medicine[J]. Acta Physiologica (Oxford, England), 2016, 216(4): 395-406. DOI:10.1111/apha.12613 |
| [5] |
LEE J W, BAE S H, JEONG J W, et al. Hypoxia-inducible factor (HIF-1) alpha: its protein stability and biological functions[J]. Experimental & Molecular Medicine, 2004, 36(1): 1-12. |
| [6] |
RYU D R, YU M R, KONG K H, et al. Sirt1-hypoxia-inducible factor-1α interaction is a key mediator of tubulointerstitial damage in the aged kidney[J]. Aging Cell, 2019, 18(2): e12904. DOI:10.1111/acel.12904 |
| [7] |
黄怀鹏, 牛联改, 陈志强, 等. 肾疏宁治疗系膜增生性肾炎30例临床研究[J]. 山东中医杂志, 2002, 21(4): 217-219. HUANG H P, NIU L G, CHEN Z Q, et al. Clinical study on treatment of 30 cases of mesangial proliferative nephritis with Shenshuning[J]. Shandong Journal of Traditional Chinese Medcine, 2002, 21(4): 217-219. DOI:10.3969/j.issn.0257-358X.2002.04.012 |
| [8] |
张件云, 李甜甜. 肾疏宁加减配合虫类药治疗慢性肾小球肾炎30例临床观察[J]. 湖南中医杂志, 2016, 32(6): 57-59. ZHANG J Y, LI T T. Clinical observation on treatment of 30 cases of chronic glomerulonephritis with modified Shenshuning and insect drugs[J]. Hunan Journal of Traditional Chinese Medicine, 2016, 32(6): 57-59. |
| [9] |
张丽芬, 黄文政. 肾疏宁的组方思路及防治肾小球硬化的机制分析[J]. 天津中医学院学报, 2005, 24(1): 1-4. ZHANG L F, HUANG W Z. Compose of formulation thought of Shenshuning and analyzing mechanism for preventing and curing glomerular sclerosis[J]. Journal of Tianjin College of Traditional Chinese Medicine, 2005, 24(1): 1-4. |
| [10] |
李国霞, 黄文政, 朱小棣. 肾疏宁对肾小管间质损害大鼠FN、ColⅢ、PAI-1 mRNA的作用[J]. 中国中西医结合肾病杂志, 2007, 8(7): 388-390. LI G X, HUANG W Z, ZHU X D. The effect of herbal medicine of shenshuning(SSN) on FN, ColⅢ, PAI-1 mRNA expression in tubulointerstitial injury rats[J]. Chinese Journal of Integrated Traditional and Western Nephrology, 2007, 8(7): 388-390. DOI:10.3969/j.issn.1009-587X.2007.07.006 |
| [11] |
徐冰, 王耀光, 周慧杰. 疏利少阳法对HBV诱导HK-2细胞转分化pSmad3蛋白表达的影响[J]. 北京中医药大学学报, 2018, 41(6): 497-501. XU B, WANG Y G, ZHOU H J. Effects of shaoyang-dredging method on HBV-induced protein expression of pSmad3 in HK-2 Cells[J]. Journal of Beijing University of Traditional Chinese Medicine, 2018, 41(6): 497-501. DOI:10.3969/j.issn.1006-2157.2018.06.010 |
| [12] |
杨洪涛, 尚懿纯, 曹式丽, 等. 肾疏宁方对腹膜纤维化大鼠腹膜组织细胞外基质积聚的影响[J]. 中国中西医结合杂志, 2013, 33(12): 1683-1689. YANG H T, SHANG Y C, CAO S L, et al. Effect of Shenshuning recipe on the extracellular matrix accumulation of the peritoneal fibrosis rats[J]. Chinese Journal of Integrated Traditional and Western Medicine, 2013, 33(12): 1683-1689. |
| [13] |
REMMELE W, SCHICKETANZ K H. Immunohistochemical determination of estrogen and progesterone receptor content in human breast cancer: computer-assisted image analysis (QIC score) vs. subjective grading(IRS)[J]. Pathology-Research and Practice, 1993, 189(8): 862-866. DOI:10.1016/S0344-0338(11)81095-2 |
| [14] |
GRANDE M T, PÉREZ-BARRIOCANAL F, LÓPEZ-NOVOA J M. Role of inflammation in túbulo-interstitial damage associated to obstructive nephropathy[J]. Journal of Inflammation (London, England), 2010, 7: 19. DOI:10.1186/1476-9255-7-19 |
| [15] |
WANG L, LIU J, XU B, et al. Reduced exosome miR-425 and miR-744 in the plasma represents the progression of fibrosis and heart failure[J]. The Kaohsiung Journal of Medical Sciences, 2018, 34(11): 626-633. DOI:10.1016/j.kjms.2018.05.008 |
| [16] |
谢盛彬, 王伟铭, 陈楠. UUO模型大鼠肾间质纤维化动态进展及α-SMA、TGF-β1和VDR表达变化[J]. 上海交通大学学报(医学版), 2010, 30(7): 752-757, 796. XIE S B, WANG W M, CHEN N. Progression of renal tubulointerstitial fibrosis and expression of α-SMA, TGF-β1 and VDR in rat UUO models[J]. Journal of Shanghai Jiao Tong University (Medical Science), 2010, 30(7): 752-757, 796. DOI:10.3969/j.issn.1674-8115.2010.07.002 |
| [17] |
王杰, 何立群. "肾络癥瘕"理论指导下的肾纤维化治疗思路辨析[J]. 中外医学研究, 2017, 15(26): 157-159. WANG J, HE L Q. Clinical treatment ideas of renal fibrosis guilded by the theoretical system of miniature mass of renal collateral[J]. Chinese and Foreign Medical Research, 2017, 15(26): 157-159. |
| [18] |
LIU M N, NING X X, LI R, et al. Signalling pathways involved in hypoxia-induced renal fibrosis[J]. Journal of Cellular and Molecular Medicine, 2017, 21(7): 1248-1259. DOI:10.1111/jcmm.13060 |
| [19] |
KABEI K, TATEISHI Y, NOZAKI M, et al. Role of hypoxia-inducible factor-1 in the development of renal fibrosis in mouse obstructed kidney: special references to HIF-1 dependent gene expression of profibrogenic molecules[J]. Journal of Pharmacological Sciences, 2018, 136(1): 31-38. DOI:10.1016/j.jphs.2017.12.004 |
| [20] |
WAKASHIMA T, TANAKA T, FUKUI, et al. JTZ-951, an HIF prolyl hydroxylase inhibitor, suppresses renal interstitial fibroblast transformation and expression of fibrosis-related factors[J]. American Journal of Physiology Renal Physiology, 2020, 318(1): F14-F24. |
| [21] |
LIU M N, NING X X, LI R, et al. Signalling pathways involved in hypoxia-induced renal fibrosis[J]. Journal of Cellular and Molecular Medicine, 2017, 21(7): 1248-1259. |
| [22] |
杨树云, 吉敏, 赵文喜, 等. 慢性肾脏病患者血清HIF-1α的表达及临床意义[J]. 昆明医科大学学报, 2021, 42(1): 64-67. YANG S Y, JI M, ZHAO W X, et al. Expression and significance of serum HIF-1α in patients with chronic kidney disease[J]. Journal of Kunming Medical University, 2021, 42(1): 64-67. |
| [23] |
LIN P L, WU M, QIN J Y, et al. Magnesium lithospermate B improves renal hemodynamics and reduces renal oxygen consumption in 5/6th renal ablation/infarction rats[J]. BMC Nephrology, 2019, 20(1): 49. |
| [24] |
WU T K, WEI C W, PAN Y R, et al. The uremic toxin p-cresyl sulfate induces proliferation and migration of clear cell renal cell carcinoma via microRNA-21/HIF-1α axis signals[J]. Scientific Reports, 2019, 9(1): 3207. |
| [25] |
吴超勇, 张佳, 高艺格, 等. 丹芪合剂对肾间质纤维化大鼠的影响研究[J]. 亚太传统医药, 2016, 12(9): 8-10. WU C Y, ZHANG J, GAO Y G, et al. Effect of combined Danshen and Huangqi injection on renal interstitial fibrosis in rats[J]. Asia-Pacific Traditional Medicine, 2016, 12(9): 8-10. |
| [26] |
周萍, 李均, 阳小敏, 等. 黄芪丹参"药对"干预肾纤维化抑制因子par-3的量效关系研究[J]. 上海中医药杂志, 2013, 47(5): 77-80. ZHOU P, LI J, YANG X M, et al. Effect of paired-herb on Par-3 of renal fibrosis: a dose-effect research[J]. Shanghai Journal of Traditional Chinese Medicine, 2013, 47(5): 77-80. |
2. First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China
 2022, Vol. 39
2022, Vol. 39