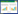文章信息
- 宋玲玲, 穆琦瑄, 王帆, 张慧, 柴欣, 王跃飞, 崔英
- SONG Lingling, MU Qixuan, WANG Fan, ZHANG Hui, CHAI Xin, WANG Yuefei, CUI Ying
- 基于顶空气相色谱质谱联用技术的紫雪散挥发性成分研究
- Study on volatile components in Zixue Powder by headspace gas chromatography mass spectrometry
- 天津中医药, 2022, 39(11): 1470-1475
- Tianjin Journal of Traditional Chinese Medicine, 2022, 39(11): 1470-1475
- http://dx.doi.org/10.11656/j.issn.1672-1519.2022.11.19
-
文章历史
- 收稿日期: 2022-08-04
2. 天津中医药大学组分中药国家重点实验室, 天津 301617;
3. 天津市中药化学与分析重点实验室, 天津 301617;
4. 天津宏仁堂药业有限公司, 天津 300385
紫雪散作为“温病三宝”之一,是凉开剂的代表方剂,源于《千金翼方》中“紫雪”,后收载于《太平惠民和剂局方》。紫雪散是由石膏、北寒水石、磁石、滑石、甘草、升麻、玄参、丁香、木香、沉香、硝石(精制)、芒硝(制)、水牛角浓缩粉、羚羊角、人工麝香、朱砂16味药组成,具有清热开窍、止痉安神之效[1]。现代药理学研究表明紫雪散具有解热、镇静、抗炎、抗惊厥等作用[2-5]。新型冠状病毒肺炎疫情爆发初期,国家印发的《新型冠状病毒感染的肺炎诊疗方案(试行第三版)》及四川、甘肃等多个省份的新型冠状病毒肺炎中医药治疗方案中紫雪散均为推荐处方[6-7]。紫雪散在多种疾病治疗中疗效确切,能有效缩短患儿发热热程[8],与参芪扶正注射液联用有效治疗感染性休克[9-10]。
基于紫雪处方,其制备工艺也在不断改革。最先制备方法为将药材煎煮后用硝石重结晶而制成,后出现将紫雪制备成散剂进行储存。目前2020年版《中国药典》收录的紫雪散制备方法为石膏、北寒水石、滑石、磁石砸成小块,加水煎煮3次,玄参、木香、沉香、升麻、甘草、丁香用石膏等煎液煎煮3次,合并煎液,滤过,滤液浓缩成膏;芒硝(制)、硝石(精制)粉碎,兑入膏中,混匀,干燥,粉碎成细粉;羚羊角锉研成细粉;朱砂水飞成极细粉;将水牛角浓缩粉、人工麝香研细,与上述粉末配研,过筛,混匀,即得[1]。宏仁堂紫雪散传统制作技艺独具代表性,2021年6月被列入第五批国家级非物质文化遗产项目。具体制备方法为石膏、北寒水石、滑石、磁石加水煎煮3次;玄参、木香、沉香、升麻、甘草、丁香用四石煎液煎煮3次,合并煎液,滤过,滤液浓缩成膏;芒硝、硝石兑入膏中,混匀,干燥,粉碎成细粉,闷圏6个月以上;过筛后的羚羊角粉、朱砂、人工麝香、水牛角浓缩粉与上述闷圏、过筛后的粉末混合、过筛,即得[11]。目前对于两种工艺的质量相关研究尚未报道。
紫雪散化学成分复杂,目前研究主要聚焦于微量元素、指标成分的质量分析等。文献报道采用微波消解和等离子发射光谱法测定了紫雪散中的钙(Ca)、镁(Mg)、锰(Mn)、铅(Pb)等微量元素[12];有学者利用薄层色谱法鉴别了方中甘草、升麻、麝香、羚羊角等药材,同时测定了紫雪散中无机盐(如硫化汞、硝酸钾)含量、水分及含氮量[13];另有报道采用气相色谱法定量分析了紫雪散中麝香酮含量[14]。紫雪散方中包含木香、丁香、麝香等芳香药材,挥发性成分为其重要成分,而目前紫雪散挥发性成分的系统研究未见报道。2020年版《中国药典》仅对紫雪散中甘草、升麻、麝香酮进行定性鉴别,因此亟需开展紫雪散中挥发性成分系统研究。
本研究运用顶空气相色谱质谱联用技术(HS GC-MS)开展紫雪散中挥发性成分的鉴定及药材来源的追溯,探讨不同批次、不同工艺间紫雪散挥发性成分种类、相对含量差异,以期阐明紫雪散挥发性化学成分物质基础,为提高紫雪散质量控制提供依据。
1 仪器与试药 1.1 仪器Agilent 7890B/5977B型GC-MS联用仪,包括7697A型顶空进样器(美国安捷伦科技有限公司);ME 204型电子天平(瑞士梅特勒–托利多公司)。
1.2 试剂与药物紫雪散(S1、S2、S3)由天津宏仁堂药业有限公司提供,为传统制作技艺(闷圈工艺)制备[11];S4、S5为中国药典收录工艺(非闷圈工艺)制备[1],由北京同仁堂股份有限公司同仁堂制药厂生产,所有样品保存于天津中医药大学中医药研究院。
玄参、升麻、甘草、沉香、丁香、木香、水牛角浓缩粉、羚羊角粉、人工麝香饮片均为天津宏仁堂药业有限公司提供,由天津宏仁堂药业有限公司质量部研究人员张慧鉴定,玄参为玄参科植物玄参Scrophularia ningpoensis Hemsl.的干燥根,升麻为毛茛科植物升麻Cimicifuga foetida L.的干燥根茎,甘草为豆科植物甘草Glycyrrhiza uralensis Fisch.的干燥根和根茎,沉香为瑞香科植物白木香Aquilaria sinensis(Lour.)Gilg含有树脂的木材,丁香为桃金娘科植物丁香Eugenia caryophyllata Thunb.的干燥花蕾,木香为菊科植物木香Aucklandia lappa Decne.的干燥根,水牛角浓缩粉为牛科动物水牛Bubalus bubalis Linnaens的角的半浓缩粉,羚羊角粉为牛科动物赛加羚羊Saiga tatarica Linnaeus的角粉碎而成。所有饮片均按照2020年版《中国药典》各药材项下要求检测,符合标准,粉碎过筛后备用。
2 实验方法 2.1 顶空进样条件加热箱温度为120 ℃;定量环温度为130 ℃;传输线温度为140 ℃;平衡时间为10 min。
2.2 色谱条件色谱柱为HP-5 MS弹性石英毛细管柱(30 m×0.25 mm×0.25 μm);柱温50 ℃,以3 ℃/min的升温速率升温至80 ℃,以8 ℃/min的升温速率升温至120 ℃,以4 ℃/min的升温速率升温至200 ℃,运行时间为35 min;进样口温度为220 ℃;载气为氦气(纯度>99.999 %);柱前压为9.8 psi,柱流量为1.0 mL/min,分流进样,分流比为10∶1;溶剂延迟时间为3.6 min。
2.3 质谱条件离子源为EI离子源;四极杆温度为150 ℃;离子源温度为230 ℃;扫描范围m/z为40~450。
2.4 样品准备各取紫雪散样品及组方药材粉末1.0 g,精密称定,分别置于20 mL顶空进样瓶中,铝盖密封,即得。
2.5 数据处理紫雪散挥发性成分总离子流图采用Qualitative Navigator B.08.00处理和NIST 17标准谱库检索分析,选择正反匹配度均≥800的化合物,运用峰面积归一化法对鉴定的挥发性成分进行归一化处理。利用Origin 2019b软件对归一化结果进行可视化分析。
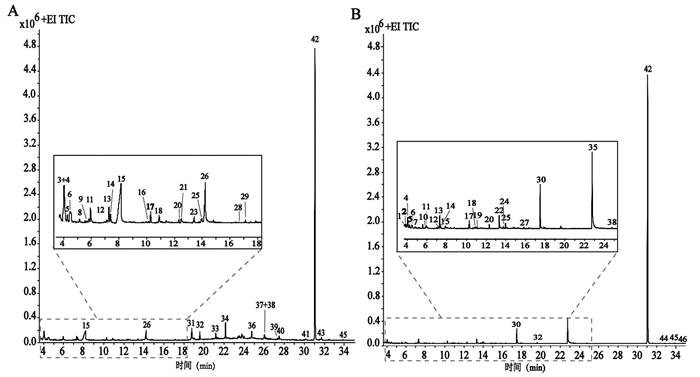
3 结果与分析 3.1 紫雪散中挥发性成分鉴定采用HS GC-MS法分析紫雪散中挥发性成分,总离子流图如图 1所示。利用Qualitative Navigator B.08.00质谱处理软件和NIST 17标准谱库鉴定紫雪散中挥发性成分,并归属各成分药材来源。从紫雪散样品中共鉴定了46个化合物,包括醇类化合物5个、酯类4个、醛类5个、酮类10个、酸类6个、烃类11个及含氮化合物等,其中12个化合物来自玄参,7个化合物来自升麻,6个化合物来自甘草,11、6、7个化合物分别来自沉香、木香、丁香,6个化合物来自羚羊角粉,4个化合物来自人工麝香,1个来自水牛角浓缩粉,具体化合物信息见表 1。
|
| 图 1 “闷圈”紫雪散(A)和“非闷圈”紫雪散(B)挥发性成分的GC-MS总离子流图 Fig. 1 GC-MS total ion chromatogram of volatile components from Zixue Powder prepared by specified process (A) and standard process (B) |
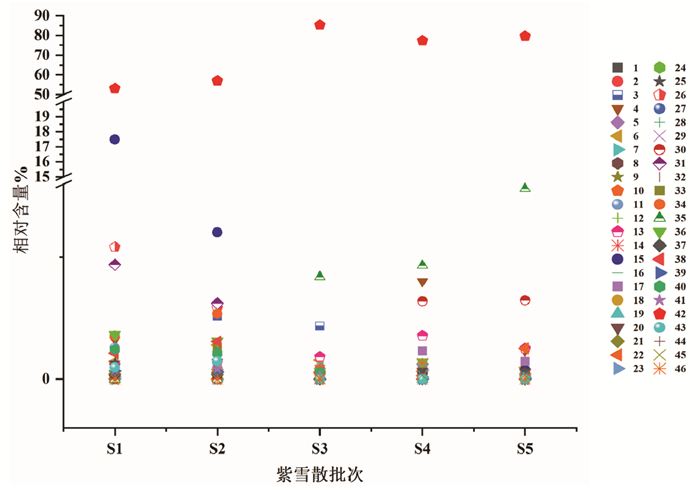
基于峰面积归一化法对5批紫雪散样品中挥发性成分进行半定量分析,成分相对含量见表 1。不同批次间紫雪散挥发性成分差异较大,其中S1批次样品中鉴定了30个化合物,S2批次样品中鉴定了34个化合物,S3批次样品中鉴定了27个化合物,S4批次样品中鉴定了26个化合物,S5批次样品中鉴定了24个化合物。结果见图 2。
|
| 图 2 不同批次紫雪散样品中46个挥发性成分相对百分含量散点图 Fig. 2 Scatter diagram of relative percent content of 46 volatile components in different batches of Zixue Powder |
在S1、S2、S3 3个批次“闷圈”工艺制备的紫雪散样品中,鉴定了21个共有成分;S4、S5两批次“非闷圈”工艺紫雪散中,也鉴定了21个共有成分。但不同工艺制备的共有成分存在区别。五批紫雪散样品中,共鉴定14个共有成分,其分别为3-甲基丁酸、2-甲基丁酸、糠醇、γ-丁内酯、苯甲醛、5-甲基-2-糠醛、己酸、苯乙醛、苯乙酮、壬醛、2-茨醇、十四烷、麝香酮、邻苯二甲酸二丁酯,其中麝香酮的相对含量最高。
3.3 “闷圈”与“非闷圈”工艺制备的紫雪散挥发性成分差异分析从“闷圈”工艺紫雪散中鉴定了36个挥发性成分,“非闷圈”工艺紫雪散中鉴定了29个挥发性成分;其中,糠醛、4-环戊烯-1,3-二酮、2-乙酰基呋喃、3,4-二甲基-2,5-呋喃二酮、2-乙酰基吡咯、甲基麦芽酚、辛酸、十三烷、正癸酸等17个化合物为闷圈工艺紫雪散所特有;1,4-丁二醇、2-甲基吡嗪、丙二酸、2,6-二甲基吡嗪、2,3-二氢-3,5二羟基-6-甲基-4(H)-吡喃-4-酮、4-苯基-2-丁酮、左旋乙酸冰片酯、2-甲氧基-4-乙烯苯酚、十七烷、十九烷10个化合物为非闷圈工艺紫雪散所特有。“闷圈”工艺中4-环戊烯-1,3-二酮具有抑制细胞增殖作用和抗癌活性[15]。4-苯基-2-丁酮被称为“止咳酮”,不仅具有良好的止咳作用,也是许多药物和香料的中间体[16]。
4 讨论 4.1 紫雪散开窍作用与芳香性药物的关系开窍药是以开窍醒神为主要作用,主治闭证神昏的药物,适用于温病热入心包、惊风、癫痫等病症[17]。紫雪散临床被用于治疗小儿高热惊厥、感染性休克等,是良好的开窍剂。紫雪散方中木香、丁香、沉香宣通解郁、行气通窍;麝香辛温香窜、芳香开窍,四者共助紫雪散开窍醒神之功。研究表明,芳香类药物以挥发性物质为主要成分,具有走窜之性、醒神开窍之效,可通过调节中枢神经递质改变中枢兴奋性神经元和抑制性神经元的活性,发挥抗惊厥、癫痫等作用[18-19]。紫雪散挥发性成分中,麝香酮相对含量最高。研究表明,麝香酮具有抗肿瘤、抗痴呆、抗脑缺血等作用,能够促进细胞增殖,缓解细胞凋亡和炎症,改善细胞活力[20]。
4.2 不同制备工艺对紫雪散挥发性成分的影响紫雪散由植物、矿物、动物3类药组成,制备过程中“闷圈”工艺与“非闷圈”工艺可能对其挥发性成分产生影响。不同制备工艺紫雪散中挥发性成分差异主要有以下原因:1)药材来源不同。2)“闷圈”工艺中产生的微生物。研究发现,不同产地药材其生长环境、加工方式、干燥及贮存时间等不同,挥发性成分会有所差异[21-22]。药材的质量差异进一步导致紫雪散中挥发性成分的差异。“闷圈”过程中其微生物菌群结构可能会发生变化,对其挥发性成分也会有所影响[23]。在对紫雪散挥发性成分药材来源归属过程中发现有19个成分未能在其组方来源药材中检出,推测其为紫雪散制备过程中新生成的成分。
目前关于紫雪散挥发性成分的研究,仅见对单一成分麝香酮的报道。本文对其挥发性成分进行系统研究,鉴定了其中46个挥发性成分,为进一步开发利用紫雪散提供了科学依据。
| [1] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2020: 1719. Chinese Pharmacopoeia Commission. Pharmacopoeia of people's republic of China[M]. Beijing: China Medical Science Press, 2020: 1719. |
| [2] |
易春媛. 中西医结合治疗小儿高热惊厥探讨[J]. 医学理论与实践, 2014, 27(22): 3039-3040. YI C Y. Study on the treatment of infantile febrile convulsion with integrated Chinese and western medicine[J]. The Journal of Medical Theory and Practice, 2014, 27(22): 3039-3040. |
| [3] |
王菊英, 刘继兰, 刘萍. 紫雪散混悬剂不同途径给药药理作用的比较[J]. 中药药理与临床, 1998, 14(3): 10-11. WANG J Y, LIU J L, LIU P. Comparison of pharmacological effects of Zixue San suspension administered in different way[J]. Pharmacology and Clinics of Chinese Materia Medica, 1998, 14(3): 10-11. |
| [4] |
李莉, 刘静, 张杰, 等. 紫雪散对大鼠胶原诱导性关节炎的治疗作用及其机制研究[J]. 现代药物与临床, 2016, 31(8): 1135-1140. LI L, LIU J, ZHANG J, et al. Therapeutic effect of Zixue Powder on collagen-induced arthritis in rats and its mechanism[J]. Drugs & Clinic, 2016, 31(8): 1135-1140. |
| [5] |
张涵彧, 胡静, 韩旭, 等. 不同工艺紫雪散抗惊厥药效特点及机制研究[J]. 药物评价研究, 2022, 45(1): 84-89. ZHANG H Y, HU J, HAN X, et al. Anticonvulsant effect of different processes of Zixue Powder in mice and its mechanism[J]. Drug Evaluation Research, 2022, 45(1): 84-89. |
| [6] |
国家卫生健康委员会办公厅, 国家中医药管理局办公室. 新型冠状病毒感染的肺炎诊疗方案(试行第三版)[J]. 天津中医药, 2020, 37(1): 1-3. National Health Commission of the People's Republic of China, National Administration of Traditional Chinese Medicine. Diagnosis and treatment plan for pneumonia caused by novel coronavirus infection (trial version 3)[J]. Tianjin Journal of Traditional Chinese Medicine, 2020, 37(1): 1-3. |
| [7] |
冯彩琴, 雍文兴, 刘永琦, 等. 甘肃省新型冠状病毒肺炎中医防治经验分析[J]. 甘肃中医药大学学报, 2020, 37(2): 10-15. FENG C Q, YONG W X, LIU Y Q, et al. TCM prevention and treatment experience of Corona virus disease 2019(COVID-19) in Gansu Province[J]. Journal of Gansu University of Chinese Medicine, 2020, 37(2): 10-15. |
| [8] |
王志兰. 紫雪散在小儿外感发热疾患中的应用[J]. 中国中药杂志, 1990, 15(3): 59. WANG Z L. Application of Zixue Powder in the treatment of exogenous fever in Children[J]. China Journal of Chinese Materia Medica, 1990, 15(3): 59. |
| [9] |
鄢家苗, 许霞. 紫雪散、参芪扶正注射液联合西医治疗急性重度感染性休克疗效观察[J]. 现代中西医结合杂志, 2017, 26(36): 4079-4082. YAN J M, XU X. Clinical observation of Zixue Powder and Shenqi-Fuzheng Injection combined with western medicine in the treatment of acute severe septic shock[J]. Modern Journal of Integrated Traditional Chinese and Western Medicine, 2017, 26(36): 4079-4082. |
| [10] |
高亮. 紫雪散联合参芪扶正注射液治疗小儿感染性休克疗效分析[J]. 中医临床研究, 2015, 7(22): 56-57. GAO L. Treating septic shock in children with the Zixue Powder plus the Shenqi Fuzheng injection[J]. Clinical Journal of Chinese Medicine, 2015, 7(22): 56-57. |
| [11] |
杨欣莹, 朱晓晶, 潘辰, 等. 紫雪散的制备方法[P]. 天津: CN105663453B, 2020-03-24. YANG X Y, ZHU X J, PAN C, et al. The preparation method of Zixue powder[P]. Tianjin: CN105663453B, 2020-03-24. |
| [12] |
陈明玉. 微波消解/等离子发射光谱法测定中成药紫雪散中的微量元素[J]. 曲阜师范大学学报(自然科学版), 2006, 32(1): 84-86. CHEN M Y. Determination of trace elements in zixuesan by microwave digestion and ICP-AES[J]. Journal of Qufu Normal University (Natural Science), 2006, 32(1): 84-86. |
| [13] |
李云谷, 董玉秀, 郭占峰, 等. 紫雪散质量标准及药理作用的研究[J]. 中成药研究, 1985(1): 12-14. LI Y G, DONG Y X, GUO Z F, et al. Study on quality standard and pharmacological action of Zixue Powder[J]. Chinese Traditional Patent Medicine, 1985(1): 12-14. |
| [14] |
欧妮, 陈少萍, 梁慧敏. 气相色谱法测定紫雪散中麝香酮的含量[J]. 中国民族民间医药, 2019, 28(5): 31-34. OU N, CHEN S P, LIANG H M. Determination of the content of muscone in Aixue Powder by gas chromatography[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy, 2019, 28(5): 31-34. |
| [15] |
孙勇, 贾文龙, 唐兴, 等. 一种4-环戊烯-1, 3-二酮的制备方法[P]. 厦门: CN111253231B, 2021-08-03. SUN Y, JIA W L, TANG X, et al. A preparation method of 4-cyclopentene-1, 3-dione[P]. Xiamen: CN111253231B, 2021-08-03. |
| [16] |
李淑玉, 党月兰. 4-苯基丁酮-2止咳作用机制的探讨[J]. 中药药理与临床, 1985, 1(10): 205-206. LI S Y, DANG Y L. Mechanism of antitussive action of 4-Phenyl-2-butanone[J]. Pharmacology and Clinics of Chinese Materia Medica, 1985, 1(10): 205-206. |
| [17] |
周祯祥, 唐德才. 临床中药学[M]. 北京: 中国中医药出版社, 2016. ZHOU Z X, TANG D C. Clinical Chinese pharmacy[M]. Beijing: China Press of Traditional Chinese Medicine, 2016. |
| [18] |
王纳, 熊磊, 吴忻晨, 等. "芳香开窍"理论探析[J]. 中国中医基础医学杂志, 2021, 27(9): 1460-1462. WANG N, XIONG L, WU X C, et al. Analysis of "resuscitation with aromatics" theory[J]. Journal of Basic Chinese Medicine, 2021, 27(9): 1460-1462. |
| [19] |
侯锡鸿, 张佩林, 王斯娴, 等. 芳香开窍中药对中枢神经系统疾病的治疗作用研究进展[J]. 药学进展, 2021, 45(5): 372-381. HOU X H, ZHANG P L, WANG S X, et al. Progress in the research on therapeutic effects of resuscitation -inducing aromatic herbs of traditional Chinese medicine on central nervous system diseases[J]. Progress in Pharmaceutical Sciences, 2021, 45(5): 372-381. |
| [20] |
WANG J, XING H, QIN X M, et al. Pharmacological effects and mechanisms of muscone[J]. Journal of Ethnopharmacology, 2020, 262: 113120. |
| [21] |
NAIK R R, SHAKYA A K, FERRI B, et al. Volatile composition and biological activity of Jordanian commercial samples of R. coriaria L. fruits[J]. Molecules, 2021, 26(18): 5691. |
| [22] |
DONG W J, TAN L H, ZHAO J P, et al. Characterization of fatty acid, amino acid and volatile compound compositions and bioactive components of seven coffee (Coffea robusta) cultivars grown in Hainan Province, China[J]. Molecules, 2015, 20(9): 16687-16708. |
| [23] |
LIU Z B, WANG Z Y, SUN J Y, et al. The dynamics of volatile compounds and their correlation with the microbial succession during the traditional solid-state fermentation of Gutian Hong Qu glutinous rice wine[J]. Food Microbiology, 2020, 86: 103347. |
2. State Key Laboratory of Component-based Chinese Medicine, Tianjin University of Traditional Medicine, Tianjin 301617, China;
3. Tianjin Key Laboratory of Traditional Chinese Medicine Chemistry and Analysis, Tianjin 301617, China;
4. Tianjin Hongrentang Pharmaceutical Co., Ltd., Tianjin 300385, China
 2022, Vol. 39
2022, Vol. 39