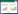文章信息
- 马漪, 谢琼
- MA Yi, XIE Qiong
- 苦参碱对结肠癌肝转移小鼠SCAP/SREBP1信号通路的调节作用研究
- Regulatory effect of matrine on SCAP/SREBP1 signal pathway in mice with liver metastasis of colon cancer
- 天津中医药, 2022, 39(3): 386-391
- Tianjin Journal of Traditional Chinese Medicine, 2022, 39(3): 386-391
- http://dx.doi.org/10.11656/j.issn.1672-1519.2022.03.23
-
文章历史
- 收稿日期: 2021-12-22
结直肠癌是最常见的消化道恶性肿瘤之一,发病率居女性第2位,男性第3位[1]。目前,结肠癌的发病率和病死率呈逐年上升趋势,其主要治疗方法是手术治疗,但对于晚期复发或转移的患者,手术治疗效果并不理想。研究表明[2]肿瘤转移是大多数癌症患者死亡和治疗失败的主要原因,而通过血液途径转移到肝脏被认为是结肠癌患者死亡的主要原因。研究证实[3]结肠癌的预后与转移尤其是肝转移密切相关,因此抑制肝转移的发生是提高结肠癌的治疗效果的手段之一。因此,结肠癌肝转移的治疗是目前临床的迫切需要。苦参碱是从中药材苦参中提取得到的生物碱类物质,近年来研究证实[4-5]其对于结肠癌的治疗表现出显著效果。本文通过研究苦参碱对结肠癌肝转移小鼠的肿瘤抑制作用及对SCAP/SREBP1通路的调节作用,为苦参碱的药理作用研究提供参考。
1 材料与方法 1.1 细胞株人结肠癌HCT116细胞购自中科院上海细胞库。
1.2 实验动物雄性Balb/c裸小鼠,SPF级,6~8周龄,22~24g,购自于长沙市天勤生物技术有限公司[实验动物许可证号SCXK(湘)2019-0014],饲养于SPF级实验动物房。
1.3 药品及试剂苦参碱(上海纯优生物科技有限公司,批号19080911,纯度 > 98%);卡培他滨(上海罗氏制药有限公司,批号20191011);SCAP、SREBP1兔多克隆抗体(艾博抗上海贸易有限公司,货号ab190103、ab28481);辣根过氧化物酶标记山羊抗兔IgG、转化生长因子β1蛋白(TGF-β1)及白介素(IL)-6酶联免疫吸附法(ELISA)试剂盒(碧云天生物科技有限公司,货号A0208、PT878、PI328);TRIzol试剂、cDNA提取试剂盒(赛默飞世尔科技有限公司,货号15596018、K1672);苏木精-伊红(HE)染色试剂盒、高效RIPA裂解液、ECL Plus超敏发光液、DMEM培养基(北京索莱宝科技有限公司,货号G1120、R0010、PE0010、11995)。
1.4 设备与仪器BX51型倒置显微镜(日本奥林巴斯公司);QuantStudio 3实时PCR系统(赛默飞世尔科技有限公司);CUT4060石蜡切片机(德国MicroTel公司);GelDoc Go凝胶成像系统(伯乐生命医学有限公司);Allegra X-15R台式冷冻离心机(贝克曼库尔特商贸有限公司);7000CO2细胞培养箱(美国Napco公司)。
1.5 分组及给药取结肠癌HCT116细胞,加入DMEM培养基,培养于5%CO2培养箱中,隔天进行传代培养,当细胞活力达到95%时,使用胰蛋白酶消化细胞,收集细胞并调整细胞密度为2×107个/mL。
72只小鼠随机分为空白对照组、肝转移模型组、苦参碱低、中、高剂量组及卡培他滨组,每组12只,参照文献方法[6]建立结肠癌肝转移小鼠模型,小鼠麻醉后称质量,取仰卧位将小鼠固定于手术台上,沿腹部正中切开,从脾下极贴近脾包膜向脾内注射0.2 mL HCT116细胞悬液,缝合,关腹,空白对照组小鼠只进行假手术,不注射细胞悬液,7 d后小鼠腹部超声显示肝脏部位可见直径为1 cm左右肿瘤生成视为造模成功。苦参碱低、中、高剂量组分别灌胃给予12.5、25、50 mg/kg[7]的苦参碱,给药21 d[8],卡培他滨组按照267 mg/kg[9]灌胃给予卡培他滨,给药14 d,停药7 d,空白对照组及肝转移模型组灌胃给予生理盐水。
1.6小鼠肝脏质量及肝转移结节数的测定小鼠处死后分离肝脏,并进行称质量,检查各组小鼠肝脏表面肝转移结节数。
1.7 肝组织TGF-β1、IL-6测定取小鼠肝组织样品在4 ℃预冷磷酸盐缓冲液中研磨匀浆,15 000 r/min,离心半径10 cm,4℃离心15 min,取上清液,用TGF-β1、IL-6 ELISA试剂盒检测肝组织上清液中TGF-β1、IL-6水平。
1.8 HE染色小鼠肝组织在4%中性甲醛固定24 h,脱水、透明处理后,石蜡包埋,石蜡切片机进行5 μm切片,经常规HE染色后,在显微镜下采用盲法进行组织病理学检查。
1.9 肿瘤组织SCAP、SREBP1 mRNA测定小鼠处死后,分离肿瘤组织,使用TRIzol试剂进行总RNA提取,用cDNA逆转录酶试剂盒将总RNA逆转录成cDNA。各基因引物如表 1所示,应用梯度实时定量聚合酶链式反应(PCR)扩增系统,PCR检测SCAP、SREBP1mRNA在肿瘤组织中的表达。结果以GAPDH为内参,采用2-ΔΔCT法计算SCAP、SREBP1 mRNA相对表达水平。
小鼠处死后取肿瘤组织,加入裂解液,研磨匀浆并离心后,测定蛋白浓度,各组取含有50 μg蛋白的上清液,进行十二烷基硫酸钠聚丙烯酰胺凝胶电泳、分离后将蛋白转移到聚偏氟乙烯膜上,用5%牛血清白蛋白室温封闭1 h,用SCAP、SREBP1(1∶1 000稀释)兔多克隆抗体和辣根过氧化物酶标记山羊抗兔二抗(1∶2 000稀释)孵育,使用ECL试剂和凝胶成像系统成像,ImageJ14.0软件定量分析SCAP、SREBP1蛋白水平。
1.11 数据处理数据所有统计分析使用SPSS 20.0软件进行,数据用均数±标准差(x±s)表示。计量资料符合正态分布且方差齐,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验,P < 0.05为差异有统计学意义。
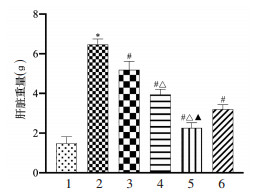
2 结果 2.1 苦参碱对结肠癌肝转移小鼠肝脏质量及肝转移结节数的影响苦参碱对结肠癌肝转移小鼠肝脏重量及肝转移结节数的影响如图 1和图 2所示,与空白对照组比较,肝转移模型组小鼠肝脏质量及肝转移结节数显著增加(P < 0.05);与肝转移模型组比较,苦参碱各剂量组及卡培他滨组肝脏质量及肝转移结节数显著减少(P < 0.05),随着苦参碱剂量的增加,肝脏质量及肝转移结节数降低更明显。
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 1 各组小鼠肝脏质量比较结果 Fig. 1 Comparison of liver weights of mice in each group |
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 2 各组小鼠肝转移结节数比较结果 Fig. 2 Comparison of the number of liver metastasis nodules in each group of mice |
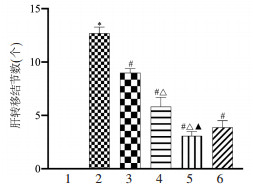
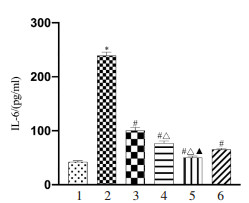
苦参碱对结肠癌肝转移小鼠肝组织TGF-β1、IL-6的影响如图 3和图 4所示,与空白对照组比较,肝转移模型组小鼠肝组织TGF-β1、IL-6水平显著升高(P < 0.05);与肝转移模型组比较,苦参碱各剂量组及卡培他滨组肝组织TGF-β1、IL-6水平显著降低(P < 0.05),随着苦参碱剂量的增加,肝组织TGF-β1、IL-6水平降低更明显。
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 3 各组小鼠肝组织TGF-β1水平比较结果 Fig. 3 Comparison of TGF-β1 levels in liver tissues of mice in each group |
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 4 各组小鼠肝组织IL-6水平比较结果 Fig. 4 Comparison of IL-6 levels in liver tissues of mice in each group |
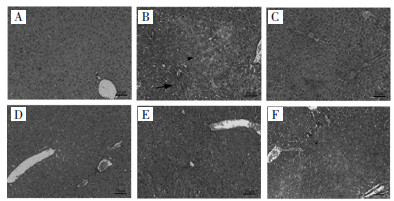
肝组织病理学检查如图 5所示,空白对照组小鼠肝组织未见明显病理学变化,与空白对照组比较,肝转移模型组小鼠肝组织肿瘤细胞聚集,伴肝组织细胞炎症浸润及坏死脱落;与肝转移模型组比较,苦参碱各剂量组及卡培他滨组肝组织肿瘤细胞聚集减轻,病理学改善。
|
| 注:A.空白对照组;B.肝转移模型组;C.苦参碱低剂量组;D.苦参碱中剂量组;E.苦参碱高剂量组;F.卡培他滨组。箭头:炎性细胞浸润;箭标:肿瘤细胞聚集。 图 5 肝组织病理学检查结果(HE染色,×400) Fig. 5 Liver histopathological examination results (HE staining, ×400) |
苦参碱对结肠癌肝转移小鼠肿瘤组织SCAP、SREBP1 mRNA的影响如图 6所示,与空白对照组比较,肝转移模型组小鼠肿瘤组织SCAP、SREBP1 mRNA水平显著升高(P < 0.05);与肝转移模型组比较,苦参碱各剂量组及卡培他滨组肿瘤组织SCAP、SREBP1 mRNA水平显著降低(P < 0.05),随着苦参碱剂量的增加,肿瘤组织SCAP、SREBP1 mRNA水平降低更明显。
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 6 小鼠肿瘤组织SCAP、SREBP1 mRNA水平比较结果 Fig. 6 Comparison of SCAP and SREBP1 mRNA levels in mouse tumor tissues |
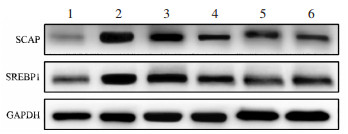
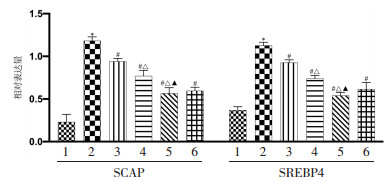
苦参碱对结肠癌肝转移小鼠肿瘤组织SCAP、SREBP1蛋白表达的影响如图 7所示,与空白对照组比较,肝转移模型组小鼠肿瘤组织SCAP、SREBP1蛋白水平显著升高(P < 0.05);与肝转移模型组比较,苦参碱各剂量组及卡培他滨组肿瘤组织SCAP、SREBP1蛋白水平显著降低(P < 0.05),随着苦参碱剂量的增加,肿瘤组织SCAP、SREBP1蛋白水平降低更明显。
|
| 注:1.空白对照组;2.肝转移模型组;3.苦参碱低剂量组;4.苦参碱中剂量组;5.苦参碱高剂量组;6.卡培他滨组。与空白对照组比较,*P < 0.05;与肝转移模型组比较,#P < 0.05;与苦参碱低剂量组比较,△P < 0.05;与苦参碱中剂量组比较,▲P < 0.05。 图 7 苦参碱对结肠癌肝转移小鼠肿瘤组织SCAP、SREBP1蛋白表达的影响 Fig. 7 The effect of matrine on the expression of SCAP and SREBP1 protein in tumor tissues of mice with liver metastases from colon cancer |
结肠癌肝转移是结肠癌进展过程中常见的远处转移现象之一,临床中表现出进行性贫血、低热、肝肿大、黄疸和腹水等多种症状,严重影响患者生存质量及预后。研究表明[10]结肠癌肝转移的发病率较高,约有50%的结肠癌患者会并发肝转移。目前临床中对于结肠癌肝转移的治疗采用全身化疗和局部手术治疗,尽管肝切除是目前最有效的局部控制治疗,但肝切除后患者5年生存率较低,且手术治疗后复发率高达70%[11]。同时目前结肠癌肝转移的临床化疗方案中卡培他滨作为一线推荐药物,但在临床使用过程中存在耐药率高、不良反应大等多种缺点,所以目前对于结肠癌肝转移的治疗药物的开发仍是临床的迫切需求。
苦参碱是从豆科植物苦参(Sophora flavescens Alt.)的干燥根、植株、果实中提取得到的生物碱,近年来研究表明[12-13],苦参碱对酒精性脂肪肝、神经病理性疼痛、萎缩性胃炎、宫颈癌等疾病具有显著的药理作用。近年来研究表明苦参碱对于结肠癌具有显著的治疗作用,缪冬映[4]研究表明苦参碱能够通过调节Akt通路显著抑制结肠癌SW480细胞增殖并促进其凋亡;王伟等[5]研究发现苦参碱能够抑制P-糖蛋白的表达,进而调控结肠癌对奥沙利铂的耐药性;常城等[14]报道了苦参碱能够诱导结肠癌HT29细胞周期阻滞,抑制HT29细胞增殖并诱导其凋亡。同时,有研究表明苦参碱对于结肠癌HT-29细胞及结肠癌肝转移均有显著的抑制作用[15-16]。
肝脏质量及肝转移结节数能够反映结肠癌肝转移的严重程度及肝组织炎症水平状态;TGF-β1及IL-6是肝组织炎症病变及病理进展的重要指标之一,近年来有学者发现其在内源性肿瘤肝转移的发生过程中起到一定的促进作用,檀谊洪等[17]研究发现小鼠结肠癌组织会释放TGF-β1进而促使肝脏Th1/Th2样细胞因子漂移,诱导结肠癌肝转移;黄晓明等[18]发现CT26细胞可诱导肝脏分泌TGF-β1,进而促进小鼠结肠癌肝转移瘤的形成;任淑萍等[19]研究发现IL-6肿瘤间质血管中表达升高,进而促进结肠癌肝转移;黄伟华等[20]报道了肝再生磷酸酶-3通过上调IL-6水平进而诱导结肠癌肝转移。本实验研究表明,与肝转移模型组比较,苦参碱各剂量组肝脏质量、肝转移结节数、肝组织TGF-β1及IL-6水平均明显降低,这提示苦参碱能够成剂量依赖性的抑制结肠癌肝转移,缓解肝组织病理进展,并降低结肠癌肝转移小鼠TGF-β1及IL-6水平,进而抑制结肠癌肝转移进一步恶化。
SCAP/SREBP1通路是维持体内糖代谢、胆固醇及脂类代谢平衡的重要信号通路。SCAP作为SREBP1蛋白激活的重要调节蛋白,SCAP在内质网中与SREBP1结合形成新的复合物,并通过囊泡被转运到高尔基体膜上,经过高尔基体膜上相应蛋白水解后转运到细胞核中被激活并发挥相应作用。近年来有学者研究发现SCAP/SREBP1通路与肿瘤疾病的发生及肿瘤转移密切相关。邓嘉成[21]研究报道了SCAP诱导的SREBP1的激活是肿瘤生长所必需的条件,同时阻断SREBP1的激活能够抑制胶质细胞瘤的增殖;Jump等[22]研究发现在结肠癌等肿瘤细胞中均发现SCAP/SREBP1过度激活;罗吉等[23]研究发现抑制SREBP1的表达则能够通过抑制PIK3R3基因进而诱导肝癌细胞周期阻滞,并诱导其凋亡;李卫华等[24]研究发现SREBP1在正常子宫细胞中低表达,而在子宫内膜癌中高表达,抑制SREBP1的表达则能够抑制子宫内膜癌的增殖和转移侵袭能力,由此可见SCAP/SREBP1的过度表达在肿瘤的发生发展中起到重要作用。本实验结果表明,与肝转移模型组比较,肿瘤组织SCAP、SREBP1 mRNA及蛋白水平显著降低,提示苦参碱成剂量依赖性的抑制SCAP/SREBP1通路的过度激活,进而抑制结肠癌肝转移进展。
综上所述,苦参碱能够显著抑制结肠癌肝转移,缓解肝组织病理学改变,其机制可能与调节SCAP/SREBP1信号通路有关。
| [1] |
DEITRICK J, PRUITT W M. Wnt/β catenin-mediated signaling commonly altered in colorectal cancer[J]. Progress in Molecular Biology and Translational Science, 2016, 144(5): 49-68. |
| [2] |
JING Y Y, HAN Z P, ZHANG S S, et al. Epithelial-mesenchymal transition in tumor microenvironment[J]. Cell & Bioscience, 2011, 12(1): 29. |
| [3] |
DU T, NIU H X. Inhibitory effect of gene combination in a mouse model of colon cancer with liver metastasis[J]. Experimental and Therapeutic Medicine, 2014, 8(3): 913-918. DOI:10.3892/etm.2014.1809 |
| [4] |
缪冬映. 苦参碱对结肠癌SW480细胞凋亡的影响[J]. 中医学报, 2018, 33(4): 517-520. MIAO D Y. Effect of matrine on apoptosis of colon cancer SW480 cells[J]. Acta Chinese Medicine, 2018, 33(4): 517-520. |
| [5] |
王伟, 郑兵, 任锐, 等. 苦参碱调控结肠癌奥沙利铂耐药性及机制研究[J]. 中国现代医学杂志, 2018, 28(30): 20-25. WANG W, ZHENG B, REN R, et al. Effect of matrine on drug resistance of human colon cells to oxaliplatin[J]. China Journal of Modern Medicine, 2018, 28(30): 20-25. |
| [6] |
李华驰, 熊治国, 谢敏, 等. 结肠癌肝转移裸鼠模型的建立[J]. 中国比较医学杂志, 2019, 29(5): 63-68. LI H C, XIONG Z G, XIE M, et al. Establishment of a nude mouse model of colon cancer liver metastasis[J]. Chinese Journal of Comparative Medicine, 2019, 29(5): 63-68. |
| [7] |
龚雪, 崔换天, 郭玮钰, 等. 苦参碱对CT26荷瘤小鼠肿瘤组织中VEGF及HIF-1α水平的影响[J]. 天津中医药大学学报, 2020, 39(6): 679-685. GONG X, CUI H T, GUO W Y, et al. Anti-tumor effects of matrine on colon tumor-bearing mice and the expression of VEGF and HIF-1α in tumor[J]. Journal of Tianjin University of Traditional Chinese Medicine, 2020, 39(6): 679-685. |
| [8] |
张蕾, 乔大伟, 毛海燕, 等. 淫羊藿苷抑制小鼠结肠癌肝转移作用及机制研究[J]. 时珍国医国药, 2019, 30(8): 1829-1832. ZHANG L, QIAO D W, MAO H Y, et al. Effect of icariin on colorectal cancer with liver metastasis in mice and its mechanism[J]. Lishizhen Medicine and Materia Medica Research, 2019, 30(8): 1829-1832. |
| [9] |
李赛花, 李心亮, 刘月平, 等. 苦参碱联合顺铂对Lewis肺癌小鼠抑制作用的研究[J]. 肿瘤药学, 2020, 10(4): 429-432, 439. LI S H, LI X L, LIU Y P, et al. Inhibitory effects of matrine combined with cisplatin on mice with lewis lung cancer[J]. Anti-Tumor Pharmacy, 2020, 10(4): 429-432, 439. DOI:10.3969/j.issn.2095-1264.2020.04.09 |
| [10] |
杨家和, 吴孟超. 结肠癌肝转移治疗方式的选择[J]. 肝胆外科杂志, 2014, 22(4): 245-248. YANG J H, WU M C. The choice of treatment modalities for liver metastases from colon cancer[J]. Journal of Hepatobiliary Surgery, 2014, 22(4): 245-248. |
| [11] |
四川大学华西医院肝癌MDT团队, 文天夫. 肝细胞癌切除术后复发转移的防治: 华西医院多学科专家共识[J]. 中国普外基础与临床杂志, 2017, 24(8): 927-939. Liver Cancer MDT Team, West China Hospital, Sichuan University, WEN T F. Prevention and treatment of recurrence and metastasis after hepatocellular carcinoma resection: a consensus of multidisciplinary experts from west China hospital[J]. Chinese Journal of Bases and Clinics in General Surgery, 2017, 24(8): 927-939. |
| [12] |
李欣, 刘稀金, 张平, 等. 苦参碱对神经病理性疼痛大鼠P2X2和P2X3受体作用的影响[J]. 中国临床药理学杂志, 2020, 36(19): 3037-3040. LI X, LIU X J, ZHANG P, et al. Effects of matrine on P2X2 and P2X3 receptors in neuropathic pain rats[J]. The Chinese Journal of Clinical Pharmacology, 2020, 36(19): 3037-3040. |
| [13] |
刘平, 陈晓杰. 苦参碱上调LncRNA BDNF-AS抑制宫颈鳞癌细胞增殖的机制研究[J]. 中草药, 2020, 51(6): 1593-1599. LIU P, CHEN X J. Mechanism of matrine inhibiting proliferation of cervical squamous carcinoma cells by up-regulating LncRNA BDNF-AS[J]. Chinese Traditional and Herbal Drugs, 2020, 51(6): 1593-1599. |
| [14] |
常城, 饶德利, 邱晓明, 等. 苦参碱对人结肠癌HT29细胞生长抑制作用的实验研究[J]. 中国中西医结合杂志, 2014, 34(1): 62-65. CHANG C, RAO D L, QIU X M, et al. The inhibitory effect of matrine on the growth of human colorectal cancer HT29 cells: an experimental observation[J]. Chinese Journal of Integrated Traditional and Western Medicine, 2014, 34(1): 62-65. |
| [15] |
朱玉森, 刘敏, 周国威, 等. 苦参碱对人结肠癌细胞株HT-29肝转移潜能的抑制作用[J]. 中国临床实用医学, 2007, 1(7): 24-27. ZHU Y S, LIU M, ZHOU G W, et al. Inhibitory effect of matrine on the liver metastasis potential of human colon cancer cell line HT-29[J]. China Clinical Practical Medicine, 2007, 1(7): 24-27. |
| [16] |
刘敏, 朱玉森, 周国威, 等. 苦参碱联合5-FU对人结肠癌裸鼠移植瘤肝转移的影响[J]. 中国临床实用医学, 2007, 1(8): 15-17. LIU M, ZHU Y S, ZHOU G W, et al. Effects of matrine combined with 5-FU on liver metastasis of transplanted human colon cancer in nude mice[J]. China Clinical Practical Medicine, 2007, 1(8): 15-17. |
| [17] |
檀谊洪, 邱万寿, 杜国能, 等. 小鼠结肠癌肝转移前肝脏Th1/Th2细胞因子的变化及与门静脉IL-10、TGF-β1的相关性[J]. 肿瘤防治研究, 2012, 39(10): 1166-1169. TAN Y H, QIU W S, DU G N, et al. Shift of hepatic Th1/Th2 cytokines and its correlation with IL-10 and TGF-β1 in portal vein of colon tumor-bearing mice previous to liver metastasis[J]. Cancer Research on Prevention and Treatment, 2012, 39(10): 1166-1169. |
| [18] |
黄晓明, 练磊, 邹一丰, 等. 白细胞介素10和转化生长因子β1与小鼠结肠癌肝转移的关系[J]. 中华普通外科学文献(电子版), 2012, 6(3): 193-199. HUANG X M, LIAN L, ZOU Y F, et al. Correlation of IL-10 and TGF-β1 expression with the liver metastasis of colon carcinoma in mice[J]. Chinese Archives of General Surgery (Electronic Edition), 2012, 6(3): 193-199. |
| [19] |
任淑萍, 张秀英, 李鹏, 等. PCNA、IL-6和IL-1β在肿瘤组织中的表达[J]. 吉林大学学报(医学版), 2006, 32(6): 953-955, 940. REN S P, ZHANG X Y, LI P, et al. Expressions of PCNA, IL-6 and IL-1β in tumor tissues[J]. Journal of Jilin University (Medicine Edition), 2006, 32(6): 953-955, 940. |
| [20] |
黄伟华, 来伟, 罗兴喜, 等. 肝再生磷酸酶-3上调白细胞介素-6和白细胞介素-8促进结肠癌侵袭的机制研究[J]. 中华实验外科杂志, 2015(7): 1637-1638. HUANG W H, LAI W, LUO X X, et al. Phosphatase of regenerating liver-3 promoted the invasion of LoVo cells through interleukin-6 and interleukin-8[J]. Chinese Journal of Experimental Surgery, 2015(7): 1637-1638. |
| [21] |
邓嘉成. 葡萄糖介导SCAP的N-糖基化为SREBP-1激活和肿瘤生长所必需[J]. 生理科学进展, 2016, 47(2): 87. DENG J C. Glucose-mediated N-glycosylation of SCAP is necessary for SREBP-1 activation and tumor growth[J]. Progress in Physiological Sciences, 2016, 47(2): 87. |
| [22] |
JUMP D B, TORRES-GONZALEZ M, OLSON L K. Soraphen A, an inhibitor of acetyl CoA carboxylase activity, interferes with fatty acid elongation[J]. Biochemical Pharmacology, 2011, 81(5): 649-660. |
| [23] |
罗吉, 苗杜凌, 程竹君, 等. 桦木脑通过SREBP1抑制靶基因PIK3R3抗肝癌[J]. 中国细胞生物学学报, 2019, 41(12): 2300-2310. LUO J, MIAO D L, CHENG Z J, et al. Betulin on anti-hepatocellular carcinoma through SREBP1 inhibits the target gene PIK3R3[J]. Chinese Journal of Cell Biology, 2019, 41(12): 2300-2310. |
| [24] |
李卫华, 周洁, 顾伟亭, 等. 子宫内膜癌SREBP1表达及SREBP1 shRNA对内膜癌细胞生物学行为的影响[J]. 现代妇产科进展, 2012, 21(6): 458-461. LI W H, ZHOU J, GU W T, et al. SREBP1 expression in endometrial cancer and the influence of SREBP1 shRNA on the biological behavior of endometrial cancer cells[J]. Progress in Obstetrics and Gynecology, 2012, 21(6): 458-461. |
 2022, Vol. 39
2022, Vol. 39