文章信息
- 晋黎, 胡思源, 郦涵, 李璇, 郭圣璇
- JIN Li, HU Siyuan, LI Han, LI Xuan, GUO Shengxuan
- 小儿手足口病随机对照试验设计要素的文献研究
- Literature research on design elements in clinical randomized controlled trials of children with hand-foot-and-mouth disease
- 天津中医药, 2022, 39(4): 450-455
- Tianjin Journal of Traditional Chinese Medicine, 2022, 39(4): 450-455
- http://dx.doi.org/10.11656/j.issn.1672-1519.2022.04.09
-
文章历史
- 收稿日期: 2021-12-06
2. 国家中医针灸临床医学研究中心, 天津 300381
手足口病(HFMD)是由肠道病毒(EV)感染引起的一种儿童常见传染病,其中以柯萨奇病毒A组16型(CV-A16)和肠道病毒71型(EV-A71)病毒最为常见。本病好发于5岁以下儿童,发病率为37.01/10万~205.06/10万,重症率约为0.5%,病死率在6.46/10万~51.00/10万之间。根据发生发展过程,本病分为1期(出疹期)、2期(神经系统受累期)、3期(心肺功能衰竭前期)、4期(心肺功能衰竭期)、5期(恢复期)。其中,1期属于手足口病普通型,部分病例仅表现为皮疹或疱疹性咽峡炎,多在1周内痊愈,预后良好。2~4期属于重症病例重型及危重型,多在发病1~5 d进展而成[1-2]。
国内关于小儿HFMD的临床研究文献较多,但试验设计差异较大,其干预措施、试验设计与评价指标,都不尽相同[3-4],给试验结果评估及二次文献研究带来了不利影响。为此,本课题组系统检索了2011—2020年发表在国内外期刊文献,总结、提炼设计与评价要素,以期为小儿手足口病药物临床试验的标准化设计提供借鉴和指导。
1 资料与方法 1.1 纳入标准1)研究适应症:手足口病(HFMD)。2)研究类型:临床随机对照试验(RCT)。3)受试人群:年龄为0.5~14岁儿童。4)干预措施:口服/静脉用药物(中药/西药)。5)发表语种:中文、英语。
1.2 排除标准1)疱疹性咽峡炎[5]患儿。2)重复发表的文献。3)非临床随机对照研究(如动物实验、综述、会议文献、个案报道或单臂临床试验等)。4)有试验设计明显错误或无法提取获取有效信息的文献。
1.3 检索策略中文数据库检索中国知网(CNKI)、万方数据库(WanFang)、维普数据库(VIP)、中国生物医学文献数据库(SinoMed),外文数据库检索Pubmed、Cochrane Library、Embase等,检索时间为2011年1月1日—2020年12月30日。检索词:“手足口病”“Hand foot and mouth disease”“hand-foot-and-mouth disease”“Hand,foot,and mouth disease”“HFMD”“幼儿”“儿童”“小儿”“婴幼儿”“青少年”“child*” “pediatric”“infant”“adolescent” “随机”“临床试验”“Random*”“clinical trial”“RCT”等。
1.4 文献筛选、质量评价和资料提取 1.4.1 文献筛选参考Cochrane协作网系统评价员手册制定文献纳入方法:1)将所有文献导入NoteExpress文献管理软件中并查重,剔除重复文献;2)阅读剩余文献题目和摘要,排除不符合要求的文献;3)下载相关文献全文并阅读,剔除不符合纳入标准的文献。
1.4.2 质量评价1)改良Jadad量表≥4分的文献视为高质量文献;2)采用Cochrane系统评价员手册[6]提供的偏倚评价量表进行质量评价,主要包括7个方面:1)随机分配方法;2)是否分配隐藏;3)实施盲法;4)评价盲法;5)结局数据的完整性;6)选择性报告研究结果;7)其他偏倚。
1.4.3 资料提取由两位研究者分别提取纳入文献的信息并整理到Excel表中,对存在有争议的文献由第3位评价者核对。提取内容包括作者、题目、试验、设计(随机、盲法、分配隐藏的使用等)、样本量、诊断标准、纳入标准、排除标准、干预措施、合并用药、疗程、有效性指标及安全性指标(观察指标、评价时点、评估工具、指标测量方法及定义)、导入期及随访等信息。
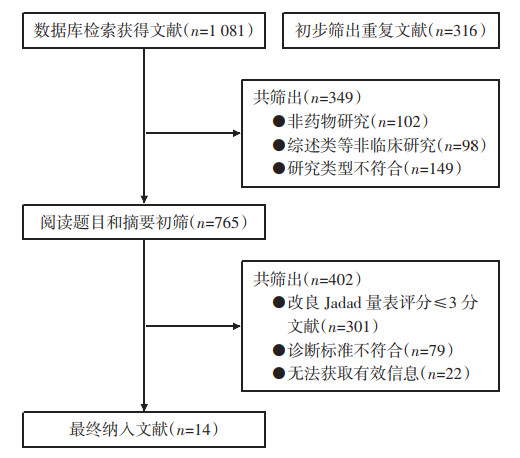
2 结果 2.1 文献检索结果共搜索文献1 081篇,中文文献共搜索909篇,其中CNKI 422篇,WanFang 138篇,VIP 204篇,SinoMed 145篇;英文文献共搜集172篇,其中Pubmed 72篇,Cochrane Liberary 57篇,Embase 43篇。筛除重复文献316篇;研究者仔细阅读题目及摘要,剔除研究类型不符合149篇、非药物研究102篇、综述类98篇等349篇;剩余的文献阅读全文,排除改良Jadad量表评分≤3分301篇,诊断标准不符合79篇,等共402篇,最终纳入文献14篇[7-20]。文献筛选流程,见图 1。
|
| 图 1 文献筛选流程 Fig. 1 Literature screening process |
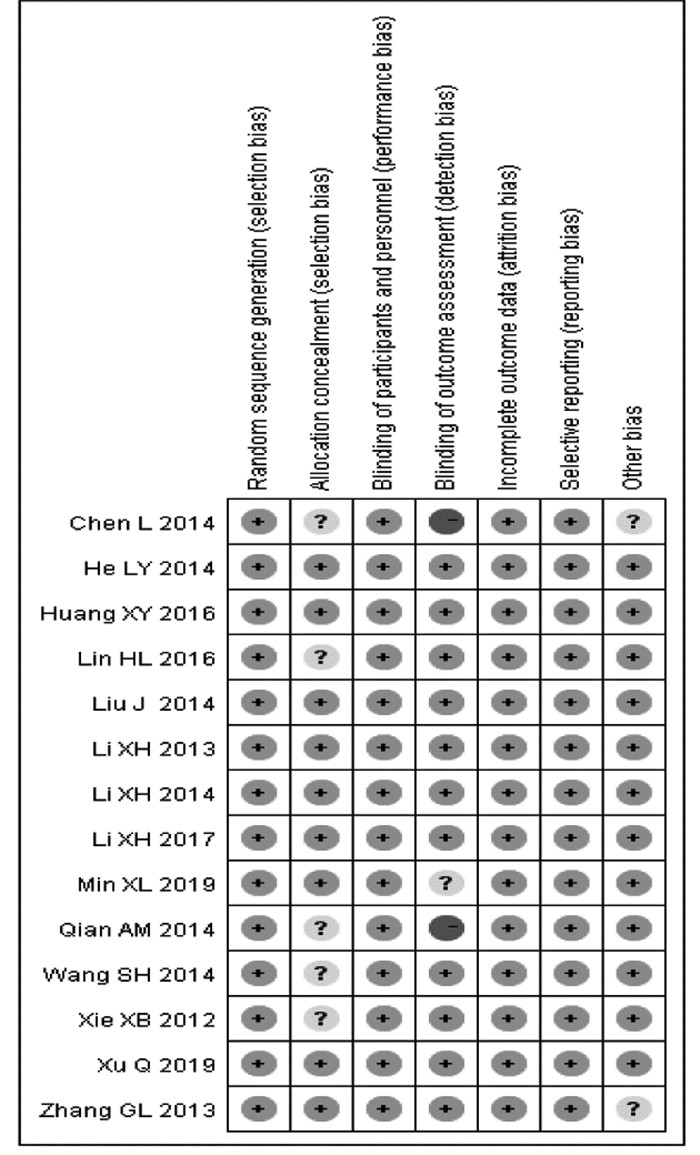
纳入研究14篇文献,其总体偏倚风险较低,文献质量较高。14篇文献详细描述了随机的产生方法,主要为电脑产生随机数字;9篇[8-9, 14-15, 16-20](64.29%)研究使用分配隐藏,主要为中心分配;5篇[8-10, 13-14](35.71%)对研究者及患者实施了双盲设计,综合考虑盲法对结局指标的影响,有2篇[11-12](14.29%)存在评价者盲法高风险;所有研究均未发现有选择性报告的风险;1篇[13](7.14%)的研究可能存在其他偏倚。见图 2。
|
| 图 2 纳入研究偏倚风险总结 Fig. 2 Summary of bias risk |
明确的研究目的是保证临床试验成功的根本。当前纳入的文献研究,均以1期/普通型及2期/重症重型HFMD病例为目标适应症,前者共9项[7-15](64.29%),试验目的均为缩短整体病程/热程;后者共5项[16-20](35.71%),其中2项[18-19](14.29%)研究目的为缩短热程,2项[16-17](14.29%)为降低危重症发生率,1项[20](7.14%)为改善总体疗效。
3.2 研究总体设计研究总体设计主要包括随机、盲法、对照、检验类型、样本量估算及参研中心等内容。全部14项研究(100%)均采用随机设计,双盲设计5项[8-10, 13-14](35.71%),1项[15](7.14%)仅提及使用盲法;对照药物选择中,安慰剂对照5项[8-10, 13-14](35.71%),阳性药对照7项[7, 11-12, 15, 17-18, 20](50%);共5项[12, 15, 17-18, 20]试验采用三臂试验设计;8项[8-9, 12-13, 16-19](57.14%)有样本量估算;10项[8-10, 13-19](71.43%)为多中心研究。
3.3 受试者的选择与退出14项研究均设计了病例纳入标准,主要包括以下几个方面:1)适应症:全部14项研究均纳入符合HFMD诊断的病例。2)年龄:全部研究纳入的患儿年龄下限为0.5~1岁,上限为5~13岁。3)病程设定:8项普通型研究[7-11, 12-15](57.14%)限定病程/热程时间,其中24 h内者2项[14-15](14.29%),48 h内5项[7-9, 11, 13](35.71%),72 h内1项[10](7.14%);5项重症重型病例研究,3项[16-17, 19](21.43%)限定神经系统症状出现24 h内者纳入。4)入组时体温限定:5项[7-9, 14, 18](35.71%)研究规定了入组时体温。4项[7-9, 14](28.57%)为普通型病例研究,2项[8-9](14.29%)设定体温 < 39.0 ℃,1项[7](7.14%)设定体温>38 ℃,1项[14](7.14%)设定体温 < 38.5 ℃;1项[18](7.14%)重症重型病例研究,设定体温>38.5 ℃者纳入。5)病原体规定:1项[18](7.14%)重症重型研究明确限定纳入EV-A71检查阳性者。6)全部研究均要求签署知情同意。
14项研究均设计了明确的病例排除标准,主要包括以下几个方面:1)全部14项研究均明确要求排除存在基础性、原发性、慢性、精神性疾患者及过敏性体质或对试验药物存在过敏者,其中1项研究[13](7.14%)要求排除癫痫或其他中枢神经系统疾病。2)影响基线的药物:6项研究[7, 10, 13, 16-17, 20](42.86%)要求排除影响药物疗效或作用机制类似的其他治疗药物,如激素(28.57%),丙种球蛋白(14.29%),抗病毒药物(21.43%)。3)实验室指标:1项[14](7.14%)研究要排除血糖增高、转氨酶增高者;1项[19](7.14%)研究要求排除胆红素轻度升高,伴血管内增高溶血(或尿胆原阳性)者。4)其他:1项研究[10](7.14%)要求排除继发细菌感染者(CRP>8 mg/L)。
3.4 干预措施纳入研究干预措施包括4项[8-9, 11, 14](28.57%)中药/中成药口服(抗病毒合剂,金莲清热泡腾片,金振口服液、中药汤剂),均针对普通型病例;5项[7, 15-17, 19](35.71%)中药注射液(喜炎平注射液、热毒宁注射液),其中3项[16-17, 19](21.43%)针对重症重型病例,2项[7, 15](14.29%)是普通型病例;4项[10, 12-13, 18](28.57%)抗病毒药(利巴韦林、干扰素),1项[18](7.14%)为重症重型病例研究,3项[10, 12-13](21.43%)为普通型病例研究;1项[20](7.14%)免疫抑制药物(丙种球蛋白),为重症重型病例。
3.5 疗程纳入的14项研究试验疗程均在3~10 d。普通型试验,疗程以3~7 d为主,其中疗程3 d[7]、5 d[14]、3~7 d[15]、5~7 d[10]、5~8 d[12]、6 d[11]各1项(7.14%),疗程7 d共3项[8-9, 13](21.43%);重症重型研究,疗程以7~10 d为主,5 d 1项[16](7.14%),7 d 1项[18](7.14%),7~10 d 3项[16-17, 19](21.43%)。
3.6 导入期与随访设立导入期的目的一般有2个,一则清洗既往治疗用药,二则收集或稳定基线数据。14项研究均没有设计导入期。14项研究中,6项[8-9, 15-17, 19](42.86%)设计了3~15 d的随访期。其中,普通型病例研究共3项(21.43%),分别为3 d[9, 15]及10 d[8];重症重型病例研究共3项[16-17, 19](21.43%),其中5 d[19]1项(7.14%),15 d 2项[16-17](14.29%)。
3.7 有效性评价全部14项研究均设1~2项主要疗效指标,主要围绕发热、皮疹/疱疹、重症/危重症病例发生率设立。其中,8项[8-9, 11-15, 18](57.14%)围绕发热设立主要疗效指标,2项[7, 9](14.29%)围绕皮疹/溃疡消退设立主要指标,2项[11, 20](14.29%)以疾病总体疗效为主要指标,3项[16-17, 19](21.43%)以危重症病例发生率为主要指标。
12项[7-9, 11-15, 16-19](85.71%)试验设立发热相关评价指标,分别为完全退热时间11项[8-9, 12-15, 16-19](78.57%)、退热起效时间1项[11](7.14%)、退热人数1项[7](7.14%),其中8项[8-9, 11-15, 18](57.14%)以完全退热时间作为主要评价指标。其次,14项试验中,有10项[7-9, 11-15, 18-19](71.43%)观察了皮疹/口腔疱疹消退情况,皮疹/疱疹完全消退时间8项[8-9, 11-15, 18](57.14%),皮疹消退比例/人数2项[7, 19](14.29%),皮疹开始消退时间1项[14](7.14%),1项[19](7.14%)以皮疹消退时间作为试验主要评价指标。最后,4项[14, 16-17, 19](28.57%)试验观察了转重症/危重症发生率,普通型病例1项[14](7.14%),重症重型3项[16-17, 19](21.43%),后者中有2项[16-17](14.29%)以此为主要评价指标。次要指标的选择,多选择肠道病毒载体量/转阴率[7, 13-14, 17](4项,28.57%),住院时间[8, 16-17](3项,21.43%),单项症状[9, 11, 13-14, 19](4项,28.57%),中医证候积分/疗效[14](1项,7.14%)等指标。重症重型病例研究中,病死率[16-17](2项,14.29%)及某特异性实验室指标,例如神经特异性烯醇化酶(NSE)、T细胞亚群水平等[20](1项,7.14%),也可以作为次要指标之一。
3.8 安全性评价14项研究中,13项[7-10, 14-20](92.86%)对不良事件/不良反应进行了详细描述,1项[11](7.14%)未提及;5项[7, 10, 13-14, 18](35.71%)设计了实验室检查指标,如肝肾功能、血常规指标;5项[10, 13-14, 16, 18](35.71%)设计了生命体征检查;1项[14](7.14%)设计了心电图检查。
3.9 试验结果的分析纳入的14项研究中,其中有12项[8-15, 16, 18-20](85.71%)获得了阳性结果。其中普通型病例8项,抗病毒合剂,金莲清热泡腾片,金振口服液、中药汤剂、喜炎平注射液、热毒宁注射液、利巴韦林、干扰素联合利巴韦林、干扰素雾化各1项。重型病例研究结果阳性者共4项,喜炎平注射液2、热毒宁1项、干扰素1项。以上结果可能会为阳性对照药的选择提供参考。
4 讨论本研究系统检索了CNKI、WanFang、VIP、SinoMed,Pubmed、Cochrane Library、Embase等国内外主要医学文献数据库从2011至2020年间小儿HMFD临床随机对照试验文献,采用Cochrane系统评价员手册,应用改良Jadad量表评分评估,最终纳入了14篇高质量文献。
归纳小儿HMFD药物临床试验设计要点,主要包括:1)HFMD主要的适应症定位,以1期/普通型或2期/重症重型为主。其临床试验目的以缩短热程为主。2期/重症重型适应症,也可以减少危重症发生。2)临床设计一般应采用随机、双盲、安慰剂平行对照、优效性检验、多中心研究的设计方法。3)西医诊断与分期分型建议参照最新版指南,国家卫生健康委员会《手足口病诊疗指南(2018年版)》。4)纳入标准中,应对年龄(一般将0.5~5岁的HFMD患儿作为受试人群)、病程(以第1期/普通型为适应症者,一般限定入选病程在24~48 h及以内)以及神经系统损害症状出现时间进行限定。5)排除标准中,首先应排除需要与HFMD相鉴别的疾病以及其他器质性、基础性、慢性疾病者;其次应注意除外入组前使用过对有效性评价有较大影响药物的患者。6)导入期设置:HFMD普通型自然病程短,重症重型病情严重,一般不设置导入期。7)疗程设置:第2期/重症重型适应症,一般设计7~10 d的治疗观察期;第1期/普通型病例一般设计5~7 d的疗程。8)随访期:若评价完全退热时间或临床痊愈时间,建议设计至少1 d的随访;重症重型病例,为随访神经系统后遗症,一般设计至少2周的随访期。9)主要评价指标选择中,定位于第1期/普通型适应症的试验,可采用完全退热时间/比例或临床痊愈时间/比例;定位于第2期/重症重型适应症的临床试验,可采用转危重症率、完全退热时间。上述结果涵盖了儿童手足口病临床研究设计的基本要素,具有一定的借鉴价值。
在文献质量评价中,课题组先用改良Jadad量表评价研究质量,一方面可以在海量筛选的过程中,将质量量化,快速筛选出符合质量要求的文献,缩短前期工作的时间。另一方面,指南的制定需要高质量的研究支撑与指导,可以通过量化粗略的分别出较高质量的文献。在入选后,通过目前公认的Cochrane偏倚风险评估工具,对所有文献的设计细节进行评价,以评估其偏倚的风险。两者的结合,一方面加快了研究进度,快速筛除低质量文献,另一方面又细致的对入选文献进行了多方位评价,满足了指南制定的需求。
另外,纳入的14篇文献中,共有6篇文献采用双盲设计。考虑到HFMD的有效性评价指标多为完全退热时间、皮疹消退时间、转重症率等为客观指标,故在进行偏倚风险分析时,将其归属于低风险,但本文仍建议采用双盲试验设计。其次,HFMD是以症状命名的疾病,同时也是一类肠道病毒性传染病,病原学检测对于疾病诊断、预后判断和疗效评价,均具有重要价值。综合考虑病原学检测的方法学局限性及其在本病有效性评价中的价值[21],故仍建议以热程/病程和重症危重症发病比例作为主要评价指标,将病毒学指标作为次要指标。此外,需要注意的是,HFMD病例的退热时间和皮疹/口腔疱疹消退时间应该是平行的。但部分HFMD病例可能存在复发性阿弗他溃疡病史,口腔疱疹破溃后易于形成溃疡,愈合时间延后(溃疡病程7~10 d甚至更长[22]),会影响皮疹/疱疹完全消退时间的评价。若以缩短病程为目的,可考虑以皮疹/疱疹消退/开始消退时间(不起新疹)为主要评价指标,而不用皮疹/疱疹完全消退时间。
| [1] |
中华人民共和国国家卫生和计划生育委员会. 手足口病诊疗指南(2018年版)[J]. 中国实用乡村医生杂志, 2018, 25(6): 8-13. The National Health Commission of the People's Republic of China. Guidelines for HFMD (2018 edition)[J]. Chinese Practical Journal of Rural Doctor, 2018, 25(6): 8-13. DOI:10.3969/j.issn.1672-7185.2018.06.004 |
| [2] |
JU Y, TAN Z, HUANG H, et al. Clinical and epidemiological characteristics of Coxsackievirus A6 and Enterovirus 71-associated clinical stage 2 and 3 severe hand, foot, and mouth disease in Guangxi, Southern China, 2017[J]. The Journal of Infection, 2020, 80(1): 121-142. |
| [3] |
李芹, 高虹, 敖雯, 等. 210例手足口病普通型患儿证候及疗效分析[J]. 中医杂志, 2013, 54(7): 584-586, 596. LI Q, GAO H, AO W, et al. A clinical analysis on symptom, syndrome and efficacy in 210 children with common type of hand-foot-and-mouth disease[J]. China Journal of Chinese Materia Medica, 2013, 54(7): 584-586, 596. |
| [4] |
常玉双. 甘露消毒丹加味联合除湿祛疹方治疗小儿手足口病肺脾湿热证50例临床观察[J]. 中医儿科杂志, 2020, 16(4): 76-79. CHANG Y S. Clinical observation on 50 cases of hand-foot-mouth disease in children with damp-heat of both lung and spleen syndrome treated by modified Ganlu Xiaodu dan combined with Chushi Quzhen fang[J]. Journal of Pediatrics of Traditional Chinese Medicine, 2020, 16(4): 76-79. |
| [5] |
中华医学会儿科学分会感染学组, 国家感染性疾病医疗质量控制中心. 疱疹性咽峡炎诊断及治疗专家共识(2019年版)[J]. 中华儿科杂志, 2019, 57(3): 177-180. Infection Group of Pediatrics Branch of the Chinese Medical Association, the National Center for Medical Quality Control of Infectious Diseases. Expert consensus on diagnosis and treatment of herpangina (version 2019)[J]. Chinese Journal of Pediatrics, 2019, 57(3): 177-180. DOI:10.3760/cma.j.issn.0578-1310.2019.03.004 |
| [6] |
HIGGINS J P T, GREEN S. Assessing risk of bias in included studies: Cochrane handbook for systematic reviews of interventions 5.1.0[EB/OL]. [2021-03-05].
|
| [7] |
谢新宝, 曾玫, 俞蕙, 等. 喜炎平注射液治疗儿童手足口病的随机对照试验[J]. 中国新药与临床杂志, 2012, 31(2): 73-76. XIE X B, ZENG M, YU H, et al. A randomized control trial of Xiyanping injection in treatment of children with hand, foot and mouth disease[J]. Chinese Journal of New Drugs and Clinical Remedies, 2012, 31(2): 73-76. |
| [8] |
HE L Y, ZHANG G L, YAN S Y, et al. A double-blind comparative study of Chinese herbal medicine Jinlianqingre Effervescent Tablets in combination with conventional therapy for the treatment of uncomplicated hand, foot, and mouth disease[J]. European Journal of Clinical Microbiology & Infectious Diseases, 2014, 33(8): 1429-1437. |
| [9] |
LIU J, ZHANG G L, HUANG G Q, et al. Therapeutic effect of Jinzhen oral liquid for hand foot and mouth disease: a randomized, multi-center, double-blind, placebo-controlled trial[J]. PLoS One, 2014, 9(4): e94466. DOI:10.1371/journal.pone.0094466 |
| [10] |
王树海, 王晓宁, 刘京. 利巴韦林气雾剂治疗儿童手足口病的随机双盲多中心临床研究[J]. 世界临床药物, 2014, 35(10): 596-600. WANG S H, WANG X N, LIU J. Clinical studies on the efficacy and safety of ribavirin aerosol in children with hand-foot-mouth disease[J]. World Clinical Drugs, 2014, 35(10): 596-600. |
| [11] |
陈鲁, 李燕宁. 手足口病2号方治疗手足口病的临床研究[J]. 中国中医基础医学杂志, 2014, 20(10): 1399-1401. CHEN L, LI Y N. Clinical study on the treatment of NO.2 prescription for HFMD[J]. Chinese Journal of Basic Medicine in Traditional Chinese Medicine, 2014, 20(10): 1399-1401. |
| [12] |
钱爱民. 重组人干扰素α-2b联合利巴韦林治疗手足口病的随机对照研究[J]. 齐齐哈尔医学院学报, 2014, 35(23): 3435-3437. QIAN A M. A randomized controlled study: the application of recombinant human interferonα-2b combined with ribavirin in the treatment of hand-foot-and-mouth disease[J]. Journal of Qiqihar Medical University, 2014, 35(23): 3435-3437. |
| [13] |
LIN H L, HUANG L T, ZHOU J, et al. Efficacy and safety of interferon-α2b spray in the treatment of hand, foot, and mouth disease: a multicenter, randomized, double-blind trial[J]. Archives of Virology, 2016, 161(11): 3073-3080. DOI:10.1007/s00705-016-3012-7 |
| [14] |
徐强, 刘虹, 胡思源, 等. 抗病毒口服液治疗小儿手足口病肺脾湿热证的随机对照、多中心临床研究[J]. 药物评价研究, 2019, 42(5): 973-978. XU Q, LIU H, HU S Y, et al. Antiviral oral liquid in treatment of lung and spleen damp-heat syndrome in children with hand-foot-mouth disease: a randomized controlled, multicenter clinical study[J]. Drug Evaluation Research, 2019, 42(5): 973-978. |
| [15] |
ZHANG G, ZHAO J, HE L, et al. Reduning injection for fever, rash, and ulcers in children with mild hand, foot, and mouth disease: a randomized controlled clinical study[J]. Journal of Traditional Chinese Medicine, 2013, 33(6): 733-742. DOI:10.1016/S0254-6272(14)60005-4 |
| [16] |
LI X, ZHANG C, SHI Q, et al. Improving the efficacy of conventional therapy by adding andrographolide sulfonate in the treatment of severe hand, foot, and mouth disease: a randomized controlled trial[J]. Evidence-Based Complementary and Alternative Medicine, 2013, 2013: 316250. |
| [17] |
LI X, ZHANG X, DING J, et al. Comparison between Chinese herbal medicines and conventional therapy in the treatment of severe hand, foot, and mouth disease: A randomized controlled trial[J]. Evidence-Based Complementary and Alternative Medicine, 2014, 2014: 140764. |
| [18] |
HUANG X, ZHANG X, WANG F, et al. Clinical efficacy of therapy with recombinant human interferon α1b in hand, foot, and mouth disease with Enterovirus 71 infection[J]. PLoS One, 2016, 11(2): e0148907. DOI:10.1371/journal.pone.0148907 |
| [19] |
LI X H, LI S J, XU Y, et al. Effect of integrated Chinese and Western medicine therapy on severe hand, foot and mouth disease: A prospective, randomized, controlled trial[J]. Chinese Journal of Integrative Medicine, 2017, 23(12): 887-892. DOI:10.1007/s11655-016-2504-3 |
| [20] |
闵晓兰, 蔡强, 卢玉容. 重组人干扰素α-1b联合大剂量丙种球蛋白治疗重症手足口病合并病毒性脑炎的疗效[J]. 安徽医学, 2019, 40(4): 392-395. MIN X L, CAI Q, LU Y R. Effects of recombinant human interferon α-1b combined with high-dose gamma globulin on serum levels of T cell subsets and insulin-like growth factor-1 in children with severe hand-foot-mouth disease and viral encephalitis[J]. Anhui Medical Journal, 2019, 40(4): 392-395. DOI:10.3969/j.issn.1000-0399.2019.04.010 |
| [21] |
张杨武. 实时荧光PCR法在手足口病病毒检测中应用分析[J]. 标记免疫分析与临床, 2019, 26(11): 1872-1875. ZHANG Y W. The application of real-time fluorometric PCR in detection of hand-foot-mouth disease virus[J]. Labeled Immunoassays and Clinical Medicine, 2019, 26(11): 1872-1875. |
| [22] |
邵彦雄, 周海文. 壳聚糖口腔贴膜治疗轻型复发性阿弗他溃疡随机对照临床研究[J]. 口腔疾病防治, 2020, 28(1): 36-40. SHAO Y X, ZHOU H W. Treating recurrent aphthous stomatitis with oral mucoadhesive films containing chitosan: a clinical random-ized controlled study[J]. Journal of Prevention and Treatment for Stomatological Diseases, 2020, 28(1): 36-40. |
2. National Clinical Research Center for Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China
 2022, Vol. 39
2022, Vol. 39