文章信息
- 孙梦晓, 丁辉, 王跃飞, 高秀梅, 李雪, 杨文志
- SUN Mengxiao, DING Hui, WANG Yuefei, GAO Xiumei, LI Xue, YANG Wenzhi
- 5种清感饮系列制剂同时多成分表征与鉴定
- Simultaneous multicomponent profiling and characterization of five Qinggan Yin series preparations
- 天津中医药, 2022, 39(6): 783-793
- Tianjin Journal of Traditional Chinese Medicine, 2022, 39(6): 783-793
- http://dx.doi.org/10.11656/j.issn.1672-1519.2022.06.22
-
文章历史
- 收稿日期: 2021-12-13
中药复方药效物质基础研究是保障其国际化的重中之重。在新型冠状病毒肺炎疫情中,中药复方也成为疫情防控的中国亮点[1]。但因其多味药叠加,具有“多成分、多靶点、多渠道”整体性协同发挥作用的特点[2],这就使得其物质基础的阐明尤为迫切。
随着分析仪器的快速发展,液质联用技术因兼有色谱的高分离性能和质谱的高灵敏度以及高选择性的特点,被广泛用于中药及复方分析,极大推动了对中药的研究探索[3]。超高效液相色谱/离子淌度-四极杆-飞行时间质谱(UHPLC/IM-QTOF-MS)是一种集快速色谱分离与维度增强高分辨测定的分析技术,通过选用亚2 μm填料色谱柱,能够极大减少溶剂消耗,增强分离度、提高分析效率;另外,数据非依赖高分辨MSE采集(HDMSE)具有离子淌度分离功能、同时最大可能覆盖所有母离子获取二级质谱信息,从而支持中药复方多成分的系统表征与鉴定[4]。
张伯礼院士团队为助力常态化疫情防控,研发了对呼吸系统感染性疾病的防治有较好疗效的清感饮(春饮、夏饮、秋饮、冬饮、童饮)制剂,具有清咽润喉,疏风解毒的功效,也有预防季节性流感的作用,目前已在天津市共400余家医疗机构调剂使用[5]。其中,清感春饮用于外感风邪、湿浊内蕴证,处方由炒草果仁、连翘、炒牛蒡子、射干、桔梗、茉莉花茶等组成;夏饮用于暑热犯表证,处方由广藿香、薄荷、牛蒡子、射干、桔梗、赤芍、紫苏叶、金银花、焦山楂、甘草、绿茶组成;秋饮用于风燥袭肺证,处方由北沙参、桑叶、炒牛蒡子、射干、桔梗、赤芍、紫苏叶、金银花、焦山楂、甘草片、菊花等组成;冬饮用于外感风寒、阳气不足证处方由黄芪、虎杖、炒牛蒡子、射干、桔梗、红茶等组成;童饮用于外感风邪、肺气失宣证,处方由薏苡仁、连翘、牛蒡子、薄荷、桔梗、赤芍、紫苏叶、焦山楂、甘草、菊花组成。
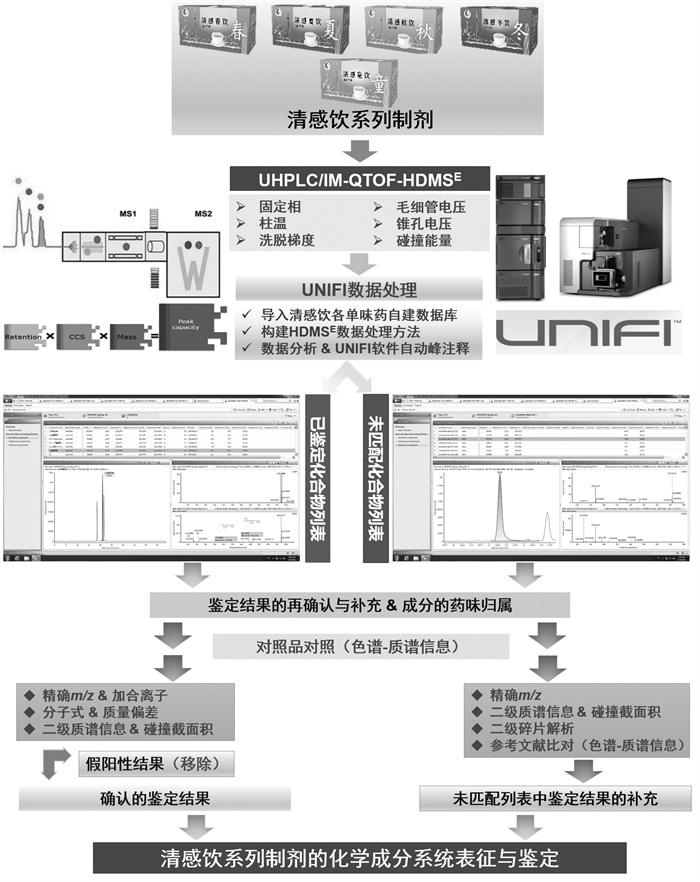
本研究从中药复方整体性出发,采用超高效液相色谱与离子淌度-四极杆-飞行时间质谱联用技术(UHPLC/IM-QTOF-HDMSE),进行色谱质谱参数优化后采集清感饮制剂样品及其单味药数据,基于UNIFI软件调用自建数据库的自动峰注解流程进行数据处理;优先对主要色谱峰进行单味药归属,根据对照品比对结果和高分辨质谱裂解信息,结合相关参考文献,全面快速地阐明清感饮(系列)制剂的化学成分,见图 1。
|
| 图 1 基于UHPLC/IM-QTOF-HDMSE结合UNIFI自动峰注释和自建数据库的清感饮系列制剂的多成分表征流程图 Fig. 1 A schematic diagram exhibiting the efficient characterization of the multiple components from Qinggan Yin series preparations based on UHPLC/IM-QTOF-HDMSE in combination with automatic peak annotation by UNIFI and searching against the in-house libraries |
Vion IMS-QTOF离子淌度高分辨液质联用仪(Waters公司,美国);Milli-Q Integral 5纯水机(Millipore公司,美国);MS105DU型十万分之一电子天平、ME104/02型万分之一电子天平(Mettler Toledo公司,瑞士),LQ-A6001型十分之一电子天平(上海瑶新电子科技有限公司);L530型台式离心机(长沙高新技术产业开发区湘仪离心机仪器有限公司);5804R型台式高速冷冻离心机(Eppendorf公司,美国);98-1-B型电子调温电热套(天津市泰斯特仪器有限公司);FSJ-A05N6型小熊粉碎机(小熊电器股份有限公司)。
甲醇、乙腈(Thermo Fisher Scientific公司,美国)、甲酸(Sigma-Aldrich公司,瑞士)均为色谱纯,超纯水由Milli-Q纯水机制备。
1.2 药品清感饮系列制剂:天津中医药大学省部共建组分中药国家重点实验室科研团队研制(清感春饮、夏饮、秋饮、冬饮、童饮);单味药药材饮片黄芪[Astragali Radix:Astragalus membranaceus(Fisch.)Bge. var. mongholicus(Bge.)Hsiao或Astragalus membranaceus(Fisch.)Bge,批号:1908045],牛蒡子(Arctii Fructus:Arctium lappa L.,批号:1909015),射干[Belamcandae Rhizoma:Belamcanda chinensis(L.)DC.,批号:2005011],桔梗[Platycodonis Radix:Platycodon grandiflorum(Jacq.)A.DC.,批号:190601],赤芍(Paeoniae Radix Rubra:Paeonia lactiflora Pall.或Paeonia veitchii Lynch,批号:2004082),紫苏叶[Perillae Folium:Perilla frutescens(L.)Britt.,批号:2001032],金银花(Lonicerae Japonicae Flos:Lonicera japonica Thunb.,批号:20200701),焦山楂(Crataegi Fructus:Crataegus pinnatifida Bge. var. major N. E. Br.或Crataegus pinnatifida Bge.,批号:200301),甘草(Glycyrrhizae Radix et Rhizoma:Glycyrrhiza uralensis Fisch.或Glycyrrhiza inflata Bat.或Glycyrrhiza glabra L.,批号:200601),连翘[Forsythiae Fructus:Forsythia suspensa(Thunb.)Vahl,批号:191201],草果(Tsaoko Fructus:Amomum tsaoko Crevost et Lemaire,批号:190801),广藿香[Pogostemonis Herba:Pogostemon cablin(Blanco)Benth.,批号:2003034],薄荷(Menthae Haplocalycis Herba:Mentha haplocalyx Briq.,批号:2003149),北沙参(Glehniae Radix:Glehnia littoralis Fr. Schmidt ex Miq.,批号:2004065),桑叶(Mori Folium:Morus alba L.,批号:1902158),虎杖(Polygoni Cuspidati Rhizoma et Radix:Polygonum cuspidatum Sieb. Et Zucc.,批号:2003018),菊花(Chrysanthemi Flos:Chrysanthemum morifolium Ramat.,批号:191101),薏苡仁[Coicis Semen:Coix lacrymajobi L. var. mayuen(Roman.)Stapf,批号:200301]均由安徽省世茂医药有限公司提供;茉莉花茶(Jasminum Tea,批号:HXJ19-0356),绿茶(Green Tea,批号:202004006),武夷红茶(Black Tea,批号:201910016)均由天津市河西区春光茶业经营部提供。饮片经检测均符合《中国药典》2020年版一部的有关规定。
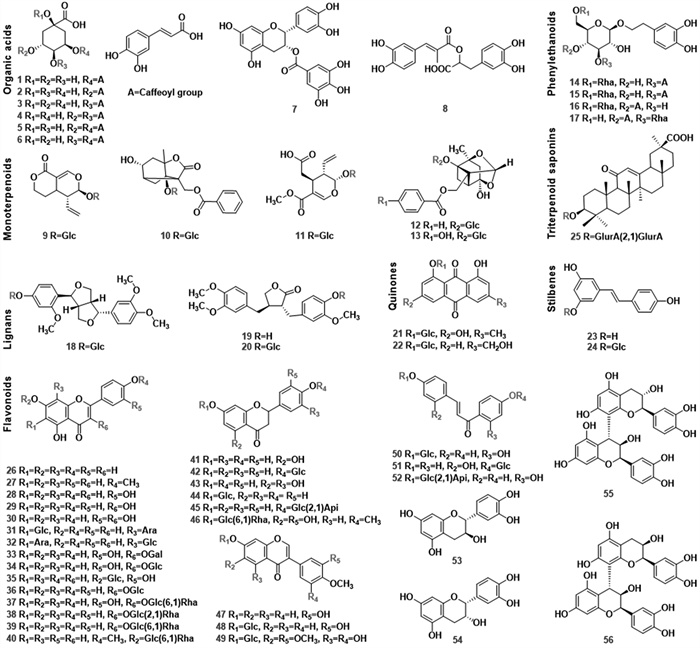
对照品新绿原酸(编号1,批号:DST191028-015)、绿原酸(编号2,批号:DST190906-021)、隐绿原酸(编号3,批号:DST190908-035)、异绿原酸B(编号4,批号:DST191008-037)、异绿原酸A(编号5,批号:DST190918-036)、异绿原酸C(编号6,批号:DST190904-038)、表儿茶素没食子酸酯(编号7,批号:DST191026-037)、迷迭香酸(编号8,批号:DST190506-027)、獐牙菜苷(编号9,批号:DST200310-014)、芍药内酯苷(编号10,批号:DST190912-071)、断氧化马钱子苷(编号11,批号:DST190803-111)、芍药苷(编号12,批号:DST191024-070)、氧化芍药苷(编号13,批号:DST191012-074)、毛蕊花糖苷(编号17,批号:DST200709-061)、白藜芦醇(编号23,批号:DST200308-045)、虎杖苷(编号24,批号:DST190821-038)、芹菜素(编号26,批号:DST190816-026)、金合欢素(编号27,批号:DST200618-037)、木犀草素(编号28,批号:DST191020-032)、山奈酚(编号29,批号:DST191020-056)、夏佛托苷(编号31,批号:DST200524-006)、异夏佛塔苷(编号32,批号:DST200416-019)、木犀草苷(编号35,批号:DST191020-016)、紫云英苷(编号36,批号:DSTDZ000101)、芦丁(编号37,批号:DSTDL001701)、柚皮素(编号41,批号:DST200109-100)、橙皮苷(编号46,批号:DST200517-038)、野鸢尾苷(编号49,批号:DST191011-247)、儿茶素(编号53,批号:DST200602-001)、表儿茶素(编号54,批号:DST200304-035)、原花青素B1(编号55,批号:DST200602-051)、原花青素B2(编号56,批号:DST200523-050)均购自成都德思特生物技术有限公司;连翘酯苷I(编号14,批号:3313)、异连翘酯苷A(编号15,批号:7894)、连翘酯苷A(编号16,批号:3639)、连翘苷(编号18,批号:3212)、牛蒡子苷元(编号19,批号:4137)、牛蒡苷(编号20,批号:5691)、大黄素-8-O-葡萄糖苷(编号21,批号:7823)、芦荟大黄素-8-O-葡萄糖苷(编号22,批号:8075)、槲皮素(编号30,批号:1116)、金丝桃苷(编号33,批号:5067)、异槲皮苷(编号34,批号:5650)、山奈酚-3-O-新橙皮糖苷(编号38,批号:7989)、山奈酚-3-O-芸香糖苷(编号39,批号:6889)、蒙花苷(编号40,批号:5515)、圣草酚(编号43,批号:3535)、新甘草苷(编号44,批号:7543)、毛蕊异黄酮(编号47,批号:6126)、毛蕊异黄酮葡萄糖苷(编号48,批号:5240)、异甘草苷(编号50,批号:6387)、新异甘草苷(编号51,批号:6971)、芹糖异甘草苷(编号52,批号:5063)均购自上海诗丹德标准技术服务有限公司;甘草酸(编号25,批号:PS010448)、甘草苷(编号42,批号:PS012028)、芹糖甘草苷(编号45,批号:PS011457)均购自成都普思生物科技股份有限公司,对照品纯度均大于98%。本研究所用56种对照品结构式及编号见图 2。
|
| 图 2 56种对照品结构图 Fig. 2 Chemical structures of the 56 reference compounds used in the current work |
参考文献[5]报道的热水浸泡服药方式,分别取清感饮(系列)制剂(清感春饮、夏饮、秋饮、饮冬、童饮)各1袋,精密称定,约3 g,分别置于圆底烧瓶中,精密加入药材20倍量的超纯水,混合均匀,称定质量,加热回流提取1 h,取出,放冷,再次称定质量,用超纯水补足失重,摇匀,离心(4 000 r/min,10 min,半径10 cm),取上清液储存备用。同时取上清液加超纯水稀释5倍,离心(14 000 r/min,10 min,半径8.8 cm),即得。
2.1.2 各单味药供试品的制备分别取21味单味药粉末(过4号筛)约1.0 g,精密称定,分别置于圆底烧瓶中,精密加入药材粉末20倍量的超纯水,混合均匀,称定质量,加热回流提取1 h,取出,放冷,再次称定质量,用超纯水补足失重,摇匀,离心(4 000 r/min,10 min,半径10 cm),取上清液储存备用。同时取上清液加超纯水稀释5倍,离心(14 000 r/min,10 min,半径8.8 cm),即得。
2.1.3 对照品溶液的制备分别精密称定各对照品1 mg,加甲醇制备为浓度1.00 mg/mL的各对照品溶液,精密吸取等量各对照品溶液,涡旋混匀后加甲醇稀释为每1 mL分别含各化合物50 μg的混合对照品储备液,离心(14 000 r/min,10 min,半径8.8 cm),即得50 μg/mL的混合对照品溶液。
2.2 色谱条件色谱柱:ACQUITY UPLC HSS T3柱(2.1 mm×100 mm,1.8 μm);流动相:0.1%甲酸水(A),乙腈(B)。梯度洗脱:0~0.5 min,1% B;0.5~6 min,1%~3% B;6~7 min,3%~10% B;7~19 min,10%~15% B;19~29 min,15%~20% B;29~31 min,20%~24% B;31~37 min,24%~40% B;37~39 min,40%~45% B;39~40 min,45%~70% B;40~41 min,70%~98% B;41~44 min,98% B;44~44.5 min,98%~1% B;44.5~49 min,1% B;流速:0.3 mL/min;柱温:40 ℃;进样量2 μL。
2.3 质谱条件离子源:电喷雾离子源(ESI);采集方法:数据非依赖HDMSE;扫描方式:正负离子同时扫描;全扫描范围(m/z):100~2 000;离子源温度:120 ℃;脱溶剂气体温度:500 ℃;锥孔气流速(N2):50 L/h;脱溶剂气体流速(N2):800 L/h;毛细管电压:1.0 kV;锥孔电压40 V;碰撞能量20~50 eV。
2.4 数据处理和分析首先,通过查阅CNKI、Web of Science、ChemSpider、PubChem等数据库,检索清感饮系列制剂中的各单味药化学成分相关文献,对其已报道NMR数据的化学成分名称、分子式、结构式、亚型等信息进行归纳总结,并将每个化合物结构式保存为.mol文件,导入UNIFI软件,构建清感饮系列制剂化学成分自建数据库。
其次,将Vion IMS-QTOF所采集的清感饮系列制剂及单味药HDMSE数据导入UNIFITM 1.9.3.0软件(Waters,美国)进行处理和分析。UNIFITM软件通过调用自建数据库进行自动峰注释,其关键参数设置如下:保留时间范围0~41 min;一级响应阈值为100.0 counts;二级响应阈值为50.0 counts;目标质量数偏差范围为10.0 ppm;选定筛选所有同位素中的一个候选者,从结构中生成预测碎片;启用在源代码中寻找碎片功能,碎片匹配偏差为10.0 ppm;Lock mass:combine width,3 scans;质量窗口0.5 m/z。负离子模式加合离子包括+HCOO,-H,+Cl,+e;参比质量数554.262 0;参比电荷-1。正离子模式加合离子包括+H,+Na,-e;参比质量数556.2766;参比电荷+1。
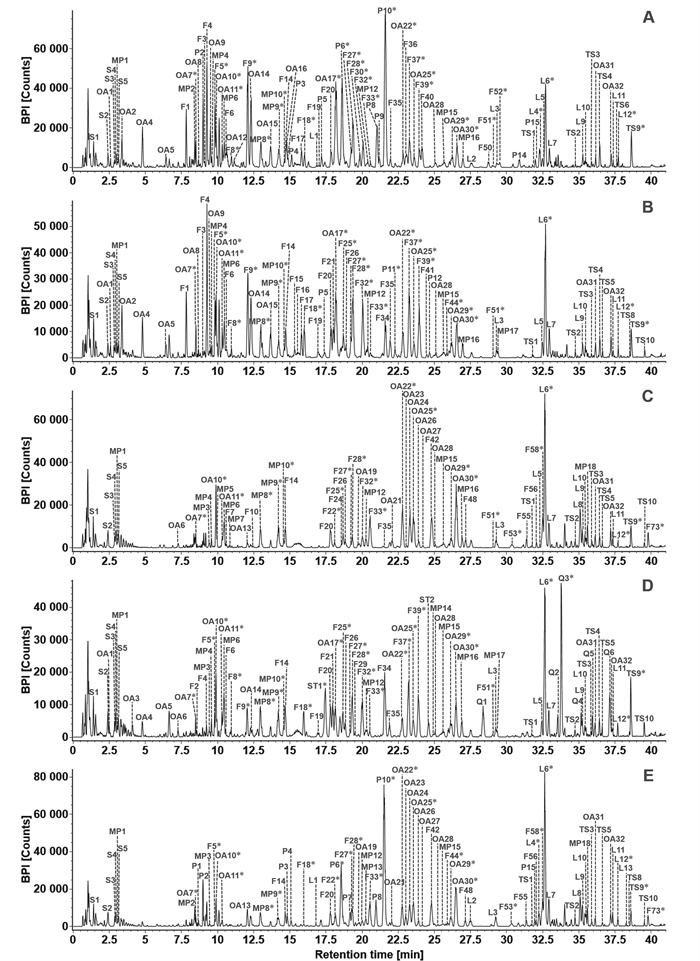
3 实验结果采用UHPLC/IM-QTOF-HDMSE在上述色谱和质谱条件下对清感饮系列制剂全方及单味药供试品溶液进行分析,由于大多数化合物在负离子模式的响应较好,因此以负离子模式为主分析清感饮系列制剂中化合物。见图 3。
|
| 注:A. 清感春饮;B. 清感夏饮;C. 清感秋饮;D. 清感冬饮;E. 清感童饮;*为通过对照品比对鉴定的成分。 图 3 清感饮系列制剂负离子模式下基峰离子图 Fig. 3 Base peak intensity chromatograms of Qinggan Yin series preparations in the negative ion mode |
图 3为负离子模式下分别测定的清感饮系列制剂(春饮、夏饮、秋饮、冬饮、童饮)基峰离子图,图中色谱峰编号与鉴定列表(基于UHPLC/IM-QTOF-HDMSE的正负离子模式下清感饮系列制剂所含化合物鉴定及归属)中化合物编号一致,具体信息见开放科学资源服务标识码(OSID)。
利用UHPLC/IM-QTOF-HDMSE正负离子模式数据非依赖HDMSE模式采集清感饮系列制剂(春饮、夏饮、秋饮、冬饮、童饮)中所含的化学成分的高分辨碰撞诱导解离二级质谱数据(CID-MS2),建立基于UNIFI软件调用自建数据库的自动峰注解流程,初步鉴定清感饮系列制剂的化学成分。在此基础上,进一步通过高分辨一级质谱识别分子式,对照品比对、二级质谱裂解行为分析、与相关文献对照等,对鉴定结果进行确证。在同条件下对清感饮系列制剂各单味药进行分析,通过色谱峰辨识归属可能的中药来源。最终共有177种化学成分被初步表征,包括73种黄酮类,32种有机酸类,18种单萜类,15种苯乙醇苷类,13种木脂素类,10种三萜皂苷类,6种醌类,5种糖类,3种生物碱类及2种二苯乙烯类。这些成分在清感春、夏、秋、冬、童饮中被表征数量分别为106、100、99、101、99种;其中清感饮系列制剂中特有单味药茉莉花茶、绿茶、红茶、菊花所占比例较多,含量较高,所含化合物易被表征;同时也有部分黄酮类及有机酸类等化合物来源于多味中药,属于处方中多种单味药来源。同时,所鉴定的化合物中有46种化合物通过与对照品的保留时间及质谱图进行比对而确认,所鉴定的化合物的误差范围均在±5 ppm以内。
清感饮系列制剂所表征的177种化合物见开放科学资源服务标识码(OSID),涉及参考文献[6-26]。
3.1 黄酮类化合物本研究从清感饮系列制剂中共鉴定出73种黄酮类化合物(F1-F73),主要来源于菊花、金银花、甘草等。黄酮类化合物,易发生糖苷键的解离,中性丢失有芸香糖残基(C12H20O9,308 Da),葡萄糖残基(C6H10O5,162 Da)等;对于黄酮苷元母核,易在C环上发生RDA裂解,产生特征碎片离子;同时还可以观察到常见的中性丢失,如CO(28 Da),CO2(44 Da),H2O(18 Da)等[27]。
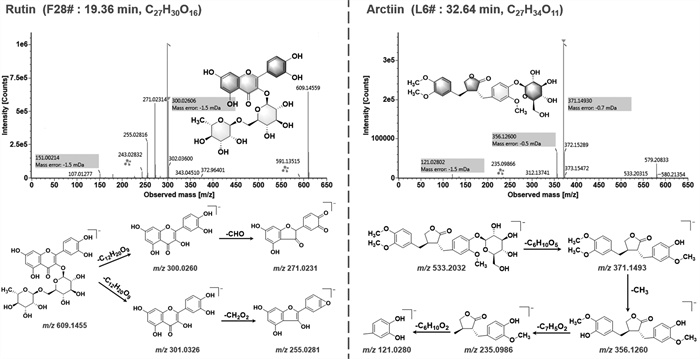
化合物F28在负离子模式下观察到准分子离子m/z 609.145 5 [M-H]-,推断分子式为C27H30O16。糖苷键断裂脱去一分子芸香糖后分别产生一个均裂碎片峰m/z 300.026 0 [M-2H-Glc-Rha]-和一个异裂碎片离子峰m/z 301.032 6 [M-H-Glc-Rha]-;且碎片离子m/z 300.026 0的丰度明显高于m/z 301.032 6,与3-O糖基取代的黄酮苷的二级质谱裂解特征(均裂碎片丰度大于异裂碎片丰度)一致[28];脱糖之后剩下的黄酮苷元产生的碎片离子主要有m/z 271.023 1 [300-CO-H]-,m/z 255.028 1 [301-CO-H2O]-;m/z 151.002 1是黄酮苷元发生RDA裂解,C环上的1键和3键断裂形成的1,3A-特征碎片,由此推测该化合物为3-O-黄酮苷。经与对照品芦丁比对,保留时间及二级质谱行为一致,故鉴定该化合物为芦丁。其二级质谱图与裂解途径见图 4。
|
| 图 4 黄酮类代表化合物(芦丁)和木脂素类代表化合物(牛蒡苷)负离子模式下的二级质谱图及裂解途径 Fig. 4 The collision-induced dissociation-MS2 spectra and proposed fragmentation pathways for the representative flavonoid (rutin) and lignan (arctiin) compounds in negative ion mode |
本研究从清感饮系列制剂中共鉴定出13种木脂素类化合物(L1-P13),主要来源于牛蒡子。木脂素因有苄基集团,易发生苄基裂解。
化合物L6在负离子模式下一级质谱图中可以观察到准分子离子m/z 579.208 3[M+COOH]-,m/z 533.203 2 [M-H]-,推断分子式为C27H34O11。二级质谱图中主要碎片离子有m/z 371.149 3[M-H-Glc]-,与牛蒡子苷元对应;m/z 356.126 0[M-H-Glc-CH3]-,进而发生苄基裂解产生碎片离子m/z 235.098 6。经与对照品比对,该化合物的保留时间、二级质谱行为与对照品牛蒡苷一致,最终鉴定该化合物为牛蒡苷。其二级质谱图和裂解途径见图 4。
3.3 有机酸类化合物本研究从清感饮系列制剂中共鉴定出32种有机酸类化合物(OA1-OA32),主要来源于金银花、菊花等。该类化合物主要产生酯键的解离或糖苷键的断裂,中性丢失有咖啡酰基(C9H6O3,162 Da)、奎宁酸残基(C7H10O5,174 Da)等。
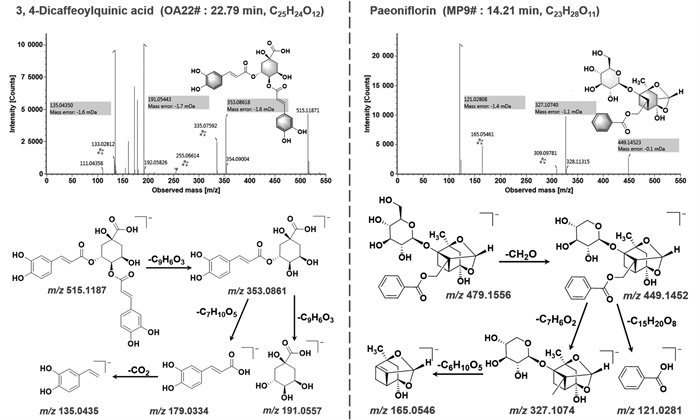
化合物OA10在负离子模式下观察到准分子离子m/z 353.086 9 [M-H]-,推断分子式为C16H18O9。其产生的主要碎片离子有m/z 191.054 6 [M-H-Caffeoyl]-,m/z 173.043 9[M-H-Caffeoyl-H2O]-,m/z 127.038 7 [173-HCOOH]-,由此推测该化合物为咖啡酸与奎宁酸的缩酚酸。通过与绿原酸对照品的色谱质谱行为进行比对,确认该化合物为绿原酸。化合物OA22、OA25、OA30准分子离子m/z 515,均比绿原酸多一份子的咖啡酰基(C9H6O3,162 Da),且具有相似的结构碎片,经与对照品色谱质谱行为比对,将化合物OA22鉴定为异绿原酸B,OA25鉴定为异绿原酸A,OA30鉴定为异绿原酸C;并以异绿原酸B(OA22)为例,其二级质谱图与裂解途径见图 5。
|
| 图 5 有机酸类代表化合物(异绿原酸B)和单萜类代表化合物(芍药苷)负离子模式下的二级质谱图及裂解途径 Fig. 5 The collision-induced dissociation-MS2 spectra and proposed fragmentation pathways for the representative organic acid (3, 4-dicaffeoylquinic acid) and monoterpenoid (paeoniflorin) compounds in negative ion mode |
本研究从清感饮系列制剂中共鉴定出18种单萜类化合物(MP1-MP18),主要来源于赤芍和金银花。萜类在负离子模式下响应较好,碎片离子以丢失糖配基较为常见。对于分子中带有羧酸基团(·COOH,45 Da)、甲氧基(·OCH3,31 Da)等基团时还可以发生自由基丢失[27]。
化合物MP9在负离子模式下一级质谱图中可以观察到准分子离子m/z 525.161 3 [M+COOH]-,m/z 479.155 7 [M-H]-,推断分子式为C23H28O11。二级质谱图中主要碎片离子有m/z 449.145 2 [M-H-CH2OH]-,再丢失一分子苯甲酸产生碎片离子m/z 327.107 4,脱去一分子葡萄糖产生碎片离子m/z 165.054 6。同时m/z 165.054 6的碎片离子源于芍药苷类化合物的蒎烷基本骨架[29],经对照品比对,该化合物的保留时间及质谱行为与对照品芍药苷一致,将该成分鉴定为芍药苷。其二级质谱图及裂解途径见图 5。
3.5 苯乙醇苷类化合物本研究从清感饮系列制剂中共鉴定出15种苯乙醇苷类化合物(P1-P15),主要来源于连翘,是连翘中药材中的特征性成分。该类化合物主要在负离子模式下形成准分子离子[M-H]-,碎片离子主要通过糖苷键的断裂形成,常见的中性丢失有葡萄糖残基(C6H10O5,162 Da)、咖啡酰基(C9H6O3,162 Da)H2O(18 Da)、CO2(44 Da)等。
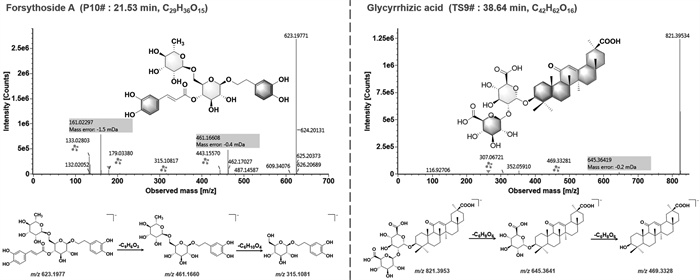
化合物P10在负离子模式下观察到准分子离子m/z 623.197 7 [M-H]-,推断分子式为C29H36O15。二级质谱图中主要碎片离子有m/z 461.166 1[M-H-Caffeoyl]-,m/z 315.108 2[M-H-Caffeoyl-Rha]-,315为二羟基苯乙醇苷母核碎片,咖啡酸碎片m/z 179.033 8,咖啡酸脱去一分子H2O的碎片m/z 161.020 9。经对照品比对,该化合物的保留时间、质谱行为与对照品连翘酯苷A一致,鉴定该化合物为连翘酯苷A。其二级质谱图及裂解途径见图 6。
|
| 图 6 苯乙醇苷类代表化合物(连翘酯苷A)和三萜皂苷类代表化合物(甘草酸)负离子模式下的二级质谱图及裂解途径 Fig. 6 The collision-induced dissociation-MS2 spectra and proposed fragmentation pathways for the representative phenylethanoid (forsythoside A) and triterpenoid saponin (glycyrrhizic acid) compounds in negative ion mode |
本研究从清感饮系列制剂中共鉴定出10种三萜皂苷类化合物(TS1-TS10),主要来源于甘草和桔梗。该类化合物常含有葡萄糖,鼠李糖,芹糖和葡萄糖醛酸等,易发生糖苷键的断裂产生碎片离子。
化合物TS9在负离子模式下可以观察到准分子离子m/z 821.395 3[M-H]-,推断分子式为C42H62O16。二级质谱图的主要碎片离子有m/z 645.364 1[M-H-Glucuronide acid]-和m/z 469.319 6[M-H-2Glucuronide acid]-,可以推测结构中含有两个葡萄糖醛酸。化合物TS10与TS9具有相同的碎片离子,裂解途径相同,证明两者互为同分异构体,经文献[13]与对照品比对,化合物TS9的保留行为与对照品甘草酸一致,鉴定该化合物为甘草酸,其二级质谱图和裂解途径见图 6;推测TS10化合物为甘草皂苷H2或其同分异构体。
3.7 其他化合物除上述6种主要类型的化合物之外,还从清感饮系列制剂中初步表征了4种其他类型的化合物,其中包括醌类化合物(Q1-Q6),主要为蒽醌类化合物,化合物Q3与对照品比对,被鉴定为大黄素-8-O-葡萄糖苷;二苯乙烯类化合物(ST1、ST2)来源于虎杖,化合物ST1与对照品比对,被确认为虎杖苷;糖类化合物(S1-S5),主要为寡糖,来源于桔梗;生物碱类化合物(A1-A3),只在正离子模式下被表征,主要来源于红茶等。
4 讨论本研究首次利用UHPLC/IM-QTOF-HDMSE方法对清感饮系列制剂(春饮、夏饮、秋饮、冬饮、童饮)的化学成分进行了较为全面、高效地解析,并对5种制剂的主要色谱峰来源进行了归属和鉴定,因5种制剂同属清感饮系列,且因色谱图中有共有峰,故最终将5种制剂鉴定结果进行整合,共有效表征该系列制剂中177种化学成分,按化学结构分类主要分为黄酮类、有机酸类、单萜类、苯乙醇苷类等,其中主要为黄酮类和有机酸类成分。
文献报道,清感饮系列制剂具有清咽润喉,疏风解毒的功效,有较好的抗氧化和抗炎活性,且对呼吸系统感染性疾病的防治均有较好的疗效[5]。本研究利用液质联用技术对清感饮系列制剂进行化学成分分析,并与所组成的各方单味药进行比对分析,初步确定各制剂的化学成分来源。其中有16种成分来源于牛蒡子,主要为牛蒡苷、牛蒡子苷元等木脂素类化合物,具有解毒利咽,止咳抑菌等作用;有17种成分来源于金银花,主要为绿原酸等咖啡酰奎宁酸类衍生物,具有抗病毒抗炎等作用,且与连翘配伍使用能增强解热抗炎功效;有33种成分来源于菊花,主要为有机酸及黄酮类成分,具有抑菌抗炎、抗氧化抗病毒抗肿瘤等活性,因其清肝明目解毒等功效除药用外也常被用于保健品。
综上所述,利用本研究所建立的UHPLC/IM-QTOF-HDMSE方法并结合UNIFI智能解析策略,快速实现了对清感饮系列制剂的定性分析,且该方法简便、高效、灵敏度高,也可进一步用于中药其他复方的定性分析,同时也为阐明该制剂的药效物质基础研究及其进一步研究开发提供参考。但在全方的BPI图中也观察到一些响应较好或单味药中没有出现的色谱峰,表明清感饮系列制剂中还有大量的未知成分,有待于进一步研究。
| [1] |
DU H Z, HOU X Y, MIAO Y H, et al. Traditional Chinese medicine: An effective treatment for 2019 novel coronavirus pneumonia (NCP)[J]. Chinese Journal of Natural Medicines, 2020, 18(3): 206-210. DOI:10.1016/S1875-5364(20)30022-4 |
| [2] |
王睿, 梁鑫淼. 中药复方的复杂性特征与方法学探讨[J]. 现代中药研究与实践, 2004, 18(S1): 98-100. WANG R, LIANG X M. Complexity of herb formula and methodology for study as well[J]. Research and Practice of Chinese Medicines, 2004, 18(S1): 98-100. |
| [3] |
苑婕, 薛媛, 贺虹. 液质联用技术在中药药效物质基础研究中的应用[J]. 国际中医中药杂志, 2019, 41(5): 548-550. YUAN J, XUE Y, HE H. Application of combined technique of liquid chromatography-mass spectrometry to pharmacodynamic material basic of traditional Chinese medicine[J]. International Journal of Traditional Chinese Medicine, 2019, 41(5): 548-550. DOI:10.3760/cma.j.issn.1673-4246.2019.05.027 |
| [4] |
ZUO T T, QIAN Y X, ZHANG C X, et al. Data-dependent acquisition and database-driven efficient peak annotation for the comprehensive profiling and characterization of the multicomponents from compound Xueshuantong capsule by UHPLC/IM-QTOF-MS[J]. Molecules, 2019, 24(19): E3431. DOI:10.3390/molecules24193431 |
| [5] |
任明, 付鲲, 周胜元, 等. "清感饮"系列制剂临床应用专家共识[J]. 天津中医药, 2020, 37(11): 1201-1204. REN M, FU K, ZHOU S Y, et al. Expert consensus on clinical application of "Qinggan yin" series pharmaceutics[J]. Tianjin Journal of Traditional Chinese Medicine, 2020, 37(11): 1201-1204. DOI:10.11656/j.issn.1672-1519.2020.11.01 |
| [6] |
SVOBODA P, VLKOVČ H, NOVÁKOVÁ L. Development and validation of UHPLC-MS/MS method for determination of eight naturally occurring catechin derivatives in various tea samples and the role of matrix effects[J]. Journal of Pharmaceutical and Biomedical Analysis, 2015, 114: 62-70. DOI:10.1016/j.jpba.2015.04.026 |
| [7] |
ZHONG J Y, CHEN N, HUANG S C, et al. Chemical profiling and discrimination of green tea and Pu-erh raw tea based on UPLC-Q-Orbitrap-MS/MS and chemometrics[J]. Food Chemistry, 2020, 326: 126760. DOI:10.1016/j.foodchem.2020.126760 |
| [8] |
刘金玲, 李文姣, 王韧, 等. 基于UPLC-Q-TOF/MS技术的桑叶化学成分快速识别分析[J]. 中国中医药信息杂志, 2018, 25(2): 69-73. LIU J L, LI W J, WANG R, et al. Fast identification analysis on chemical constituents in mori folium by using UPLC-Q-TOF/MS method[J]. Chinese Journal of Information on Traditional Chinese Medicine, 2018, 25(2): 69-73. DOI:10.3969/j.issn.1005-5304.2018.02.016 |
| [9] |
LIN L Z, HARNLY J M. Identification of the phenolic components of Chrysanthemum flower (Chrysanthemum morifolium Ramat)[J]. Food Chemistry, 2010, 120(1): 319-326. DOI:10.1016/j.foodchem.2009.09.083 |
| [10] |
LI J, LI W Z, HUANG W, et al. Quality evaluation of Rhizoma Belamcandae[Belamcanda chinensis (L.) DC.] by using high-performance liquid chromatography coupled with diode array detector and mass spectrometry[J]. Journal of Chromatography A, 2009, 1216(11): 2071-2078. DOI:10.1016/j.chroma.2008.05.082 |
| [11] |
亢倩丽, 李壮壮, 范珊珊, 等. 基于UPLC-Q-Exactive-Orbitrap-MS的紫苏叶与紫苏梗化学成分分析[J]. 中国实验方剂学杂志, 2020, 26(13): 156-162. KANG Q L, LI Z Z, FAN S S, et al. Qualitative analysis on Perilla frutescens leaves and stalks by UPLC-Q-exactive-orbitrap-MS[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2020, 26(13): 156-162. |
| [12] |
毛祈萍, 何明珍, 黄小方, 等. 基于超高效液相色谱和飞行时间质谱联用的紫苏化学成分鉴定[J]. 现代食品科技, 2021, 37(1): 282-291, 259. MAO Q P, HE M Z, HUANG X F, et al. Analysis of chemical components of Perilla frutescens based on ultra high performance liquid chromatography-quadrupole/time of flight mass spectrom (UHPLC-Q/TOF MS)[J]. Modern Food Science and Technology, 2021, 37(1): 282-291, 259. |
| [13] |
赵艳敏, 刘素香, 张晨曦, 等. 基于HPLC-Q-TOF-MS技术的甘草化学成分分析[J]. 中草药, 2016, 47(12): 2061-2068. ZHAO Y M, LIU S X, ZHANG C X, et al. Analysis on chemical constituents from Glycyrrhizae Radix et Rhizoma by HPLC-Q-TOF-MS[J]. Chinese Traditional and Herbal Drugs, 2016, 47(12): 2061-2068. DOI:10.7501/j.issn.0253-2670.2016.12.007 |
| [14] |
ZHANG Y Y, WANG Q, QI L W, et al. Characterization and determination of the major constituents in Belamcandae Rhizoma by HPLC-DAD-ESI-MSn[J]. Journal of Pharmaceutical and Biomedical Analysis, 2011, 56(2): 304-314. DOI:10.1016/j.jpba.2011.05.040 |
| [15] |
YIN Y Q, YING X H, LUAN H R, et al. UPLC-DAD/Q-TOF-MS based ingredients identification and vasorelaxant effect of ethanol extract of jasmine flower[J]. Evidence-Based Complementary and Alternative Medicine, 2014, 2014: 707908. |
| [16] |
LI S L, SONG J Z, CHOI F F, et al. Chemical profiling of Radix Paeoniae evaluated by ultra-performance liquid chromatography/photo-diode-array/quadrupole time-of-flight mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2009, 49(2): 253-266. DOI:10.1016/j.jpba.2008.11.007 |
| [17] |
沈菲, 邹立思, 文红梅, 等. HPLC-PDA指纹图谱结合UFLC-Q-TOF-MS定性鉴别评价连翘药材质量[J]. 中国中药杂志, 2019, 44(20): 4495-4503. SHEN F, ZOU L S, WEN H M, et al. Qualitative evaluation of Forsythia suspensa by HPLC-PDA fingerprint combined with UFLC-Q-TOF-MS qualitative identification[J]. China Journal of Chinese Materia Medica, 2019, 44(20): 4495-4503. |
| [18] |
KUCHARSKA A Z, FECKA I. Identification of iridoids in edible honeysuckle berries (Lonicera caerulea L. var. kamtschatica sevast.) by UPLC-ESI-qTOF-MS/MS[J]. Molecules, 2016, 21(9): 1157. DOI:10.3390/molecules21091157 |
| [19] |
李小芩, 孙晓红, 蔡爽, 等. 采用UPLC-ESI-MS/MS以及主成分聚类分析研究不同品种金银花的化学成分及其差异[J]. 药学学报, 2009, 44(8): 895-904. LI X Q, SUN X H, CAI S, et al. Investigation on the chemical constituents and variation of the flower buds of Lonicera species by UPLC-ESI-MS/MS and principle component analysis[J]. Acta Pharmaceutica Sinica, 2009, 44(8): 895-904. DOI:10.3321/j.issn:0513-4870.2009.08.013 |
| [20] |
何厚洪, 姚建标, 畅文琦, 等. 基于HPLC-LTQ-Orbitrap MS/MS技术的复方鱼腥草合剂化学物质基础表征研究[J]. 亚太传统医药, 2020, 16(8): 37-44. HE H H, YAO J B, CHANG W Q, et al. Analysis of chemical material basis of compound Yuxingcao mixture based on HPLC-LTQ-orbitrap MS/MS technology[J]. Asia-Pacific Traditional Medicine, 2020, 16(8): 37-44. |
| [21] |
胡静, 秦昆明, 祝婷婷, 等. 基于UHPLC-UV-Q-TOF-MS/MS的牛蒡子炒制前后化学成分定性定量研究[J]. 药学学报, 2017, 52(4): 603-608. HU J, QIN K M, ZHU T T, et al. Qualitative and quantitative analysis of major constituents of raw and processed Arctii Fructus by UHPLC-UV-Q-TOF-MS/MS[J]. Acta Pharmaceutica Sinica, 2017, 52(4): 603-608. |
| [22] |
QIN K M, LIU Q D, CAI H, et al. Chemical analysis of raw and processed Fructus arctii by high-performance liquid chromatography/diode array detection-electrospray ionization-mass spectrometry[J]. Pharmacognosy Magazine, 2014, 10(40): 541-546. DOI:10.4103/0973-1296.141806 |
| [23] |
LEE D Y, CHOI B R, LEE J W, et al. Simultaneous determination of various platycosides in Four Platycodon grandiflorum cultivars by UPLC-QTOF/MS[J]. Applied Biological Chemistry, 2019, 62: 47. DOI:10.1186/s13765-019-0457-x |
| [24] |
马海娟, 高简, 张亚丽, 等. 基于HPLC-MSn的甘草成分快速鉴定及质谱裂解途径研究[J]. 中华中医药杂志, 2018, 33(3): 1120-1123. MA H J, GAO J, ZHANG Y L, et al. Study on identification of compounds and their fragmentation pathways in licorice by HPLC-MSn[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2018, 33(3): 1120-1123. |
| [25] |
闫利利, 史家文, 王金芳, 等. 基于UPLC/Q-TOF-MSE方法分析半夏泻心汤的化学成分[J]. 药学学报, 2013, 48(4): 526-531. YAN L L, SHI J W, WANG J F, et al. UPLC/Q-TOF-MSE based analysis of chemical composition of Banxia Xiexin decoction[J]. Acta Pharmaceutica Sinica, 2013, 48(4): 526-531. |
| [26] |
董静, 王弘, 万乐人, 等. 高效液相色谱/电喷雾-离子阱-飞行时间质谱分析鉴定中药虎杖中的主要化学成分[J]. 色谱, 2009, 27(4): 425-430. DONG J, WANG H, WAN L R, et al. Identification and determination of major constituents in Polygonum cuspidatum Sieb. et Zucc. by high performance liquid chromatography/electrospray ionization-ion trap-time-of-flight mass spectrometry[J]. Chinese Journal of Chromatography, 2009, 27(4): 425-430. DOI:10.3321/j.issn:1000-8713.2009.04.009 |
| [27] |
龚兴成, 刘文静, 曹丽波, 等. DI-MS/MSALL法快速定性分析金银花的化学成分[J]. 中国中药杂志, 2021, 46(9): 2220-2228. GONG X C, LIU W J, CAO L B, et al. Rapid chemome profiling of chemical components of Lonicerae Japonicae Flos using DI-MS/MSALL[J]. China Journal of Chinese Materia Medica, 2021, 46(9): 2220-2228. |
| [28] |
李伟, 冯育林, 黎田儿, 等. UPLC-Q-TOF/MS技术结合诊断离子方法快速分析连钱草中黄酮类化合物[J]. 质谱学报, 2016, 37(6): 504-516. LI W, FENG Y L, LI T E, et al. Rapid analysis on flavonoids in Glechoma longituba(nakai) kupr by UPLC-Q-TOF/MS couple with diagnostic ions[J]. Journal of Chinese Mass Spectrometry Society, 2016, 37(6): 504-516. |
| [29] |
周海玲, 许舜军, 周若龙, 等. 白芍、赤芍化学成分的高效液相色谱-飞行时间串联质谱分析[J]. 中药材, 2018, 41(7): 1637-1640. ZHOU H L, XU S J, ZHOU R L, et al. Analysis of chemical constituents of Paeoniae Alba and Paeoniae Rubra by HPLC-TOF-MS[J]. Journal of Chinese Medicinal Materials, 2018, 41(7): 1637-1640. |
 2022, Vol. 39
2022, Vol. 39