文章信息
- 刘通, 李雁, 徐红日, 等.
- LIU Tong, LI Yan, XU Hongri, et al.
- 基于LC-MS/MS和靶点网络探讨扶正透邪解毒化瘀方对多重耐药铜绿假单胞菌的干预机制
- Study on the intervention mechanism against multidrug-resistant Pseudomonas aeruginosa by Fuzheng Touxie Jiedu Huayu Formula based on LC-MS/MS and target network
- 天津中医药, 2023, 40(10): 1327-1336
- Tianjin Journal of Traditional Chinese Medicine, 2023, 40(10): 1327-1336
- http://dx.doi.org/10.11656/j.issn.1672-1519.2023.10.17
-
文章历史
- 收稿日期: 2023-05-20
2. 北京中医药大学, 北京 100029;
3. 北京中医药大学第三附属医院急诊科, 北京 100029;
4. 北京中医药大学脓毒症研究所, 北京 100029
铜绿假单胞菌(PA)是院内感染最常见的条件致病菌之一,易引发医院获得性肺炎、呼吸机相关性肺炎,也是支气管扩张、慢性阻塞性肺疾病患者继发感染的常见致病菌[1]。PA耐药形势一直不容乐观,高耐药率导致了高多重耐药(MDR)检出率,中国细菌耐药监测(CARST)研究2019—2020革兰氏阴性菌监测报告显示[2],MDRPA检出率为39.7%,且来自重症监护病房的菌株耐药率还要高出近10%。这使得治疗药物的选择压力日益增加。国外研究显示,PA肺炎的病死率约为25%~39%,而MDRPA患者的病死率更是高达40%~70%[3]。国内有研究发现,PA肺炎患者治疗总体有效率为38.3%,而MDRPA治疗有效率仅为28.6%[4]。因此,亟需探索更加有效的抗菌药物,但抗菌药物研发周期长,远远赶不上细菌耐药的速度。
中药具有多成分、多靶点且不易耐药等优势,已被证实具有直接体外抑菌/逆转耐药作用,还能联合抗菌药物发挥协同作用。扶正透邪解毒化瘀方是本课题组在周平安、姜良铎和王成祥教授等呼吸热病专家指导下,根据课题组前期临床总结的耐药菌肺炎“正气亏虚、毒瘀互结”的基础病机[5],以临床疗效显著[6]的扶正解毒化瘀方为基础组方而成。课题组前期研究结果显示,该方1倍和2倍等效剂量含药血清联合亚胺培南后[7],使亚胺培南对MDRPA的最小抑菌浓度(MIC)由16 μg/mL降至8 μg/mL和4 μg/mL;对于头孢他啶[7],联合1倍和2倍等效剂量含药血清后,MIC由16 μg/mL降至8 μg/mL和4 μg/mL;对于环丙沙星[8],联合1倍等效剂量含药血清后,MIC由4 μg/mL降至2 μg/mL。然而,该方体外抑菌/逆转耐药的药效学基础和直接/协同机制尚不清楚。研究拟通过液相色谱-串联质谱联用(LC-MS/MS)结合网络药理学,从药物作用靶点层面对上述问题进行探讨,以期为进一步开发抑制/逆转细菌耐药的中药新药提供客观依据,这对减轻抗菌药物的选择压力具有重要的研究意义。
1 材料 1.1 药物与试剂扶正透邪解毒化瘀方(金银花、赤芍、瓜蒌、连翘、黄芩、漏芦、生黄芪、西洋参、当归、生甘草、薏苡仁、败酱草),采用北京康仁堂药业有限公司生产的中药全成分配方颗粒剂,购自北京中医药大学第三附属医院药学部;试剂: 甲醇(质谱级)、乙腈(质谱级)、甲酸(质谱级)均购自美国Fisher Chemical公司;超纯水由Millipore纯水系统进行纯化。
1.2 主要仪器高效液相色谱仪(美国Thermo Scientific,U3000),高分辨液相色谱-质谱联用仪(美国AB Sciex,TripleTOF5600+),真空离心浓缩仪(德国Eppendorf,Concentrator plus),分析天平(瑞士Sartorius,BP211d),低温高速离心机(美国Beckman Coulter,Microfuge 22R Centrifuge),掌上离心机(美国Scilogex,D1008),涡旋仪(美国Scilogex,MX-S)。
1.3 数据库、分析平台/软件及作图工具中药系统药理数据库和分析平台(TCMSP,https://old.tcmsp-e.com/tcmsp.php)、Cytoscape 3.9.1软件、uniprot数据库(https://www.uniprot.org/)、Stitch数据库(http://stitch.embl.de/)String数据库https://cn.string-db.org/)、DAVID数据库(https://david-d.ncifcrf.Gov)、微生信作图(http://www.bioinformatics.com.cn/)。
2 方法 2.1 定性鉴定扶正透邪解毒化瘀方样品制备将中药全方颗粒剂研磨、混匀后,准确称取50 mg中药样本于2 mL的离心管中;加入400 μL冷甲醇(含内标),涡旋振荡2 min;加入2粒钢珠,4 ℃下50 Hz研磨4 min;使用超声探头萃取30 min;涡旋振荡2 min,4 ℃静置10 min,14 000 g离心15 min(离心半径10 cm);取上清液离心浓缩后置于-20 ℃冰箱保存备用。进行上机分析前,将离心浓缩后的提取液样本,用100 μL的20%甲醇/水溶液复溶,振荡至完全溶解后离心取上清液,进行正、负离子模式分析。
2.2 色谱条件质谱正离子模式色谱条件: 色谱柱为美国Waters公司BEH C8柱(1.7 μm,2.1×100 mm);柱温: 50 ℃;流动相A: 水(含0.1%甲酸);流动相B: 乙腈(含0.1%甲酸);采用梯度洗脱(0~1 min,95% A;1~24 min,0%~95%A;24~27.5 min,0% A;27.5~30 min,0%~95% A),流速: 0.35 mL/min;进样体积5 μL。
质谱负离子模式色谱条件: 色谱柱为美国Waters公司HSS T3柱(1.8 μm,2.1×100 mm);柱温: 50 ℃;流动相A: 水(含6.5 mmol/L碳酸氢铵);流动相B: 95%甲醇水(含6.5 mmol/L碳酸氢铵);采用梯度洗脱(0~1 min,95% A;1~18 min,0%~95% A;18~22 min,0% A;22~25 min,0%~95% A),流速: 0.35 mL/min;进样体积5 μL。
2.3 质谱条件加热电喷雾(ESI)离子源,在正负离子下,采用质谱一级全扫描+ DDA二级子离子扫描模式。喷雾电压: 3.8 kV(正离子)、-3 kV(负离子);离子传输管温度: 320 ℃;辅助气加热温度: 350 ℃;鞘气流速: 35 Arb;辅助气流速: 8 Arb;离子透镜射频电压: 50 V;扫描质量范围(m/z): 70~1 050;全ms分辨率: 70 000;MS/MS分辨率: 17 500;最大响应离子: 5;碰撞能量: 20、40 eV。
2.4 LC-MS/MS数据分析和筛选将检测得到的数据导入大连达硕与中国科学院大连化学物理研究所联合开发的化合物快速鉴定分析系统OSI/SMMS对化合物进行自动鉴定。根据TCMSP提供的理化性质指标和类药性指标设定依据[9],将鉴定后的化合物中口服生物利用度(OB)≥30%、类药性(DL)≥0.18、Caco-2渗透率≥-0.4、半衰期(HL)≥4的化合物筛选出来,作为研究的候选活性分子。
2.5 TCMSP数据库中扶正透邪解毒化瘀方化学成分筛选筛选标准同上: OB≥30%、DL≥0.18、Caco-2≥-0.4、HL≥4。
2.6 扶正透邪解毒化瘀方和抗菌药物化学成分作用于铜绿假单胞菌靶点收集将2.4项与2.5项中得到的化学成分进行汇总去重,通过Stitch数据库查找上述成分以及亚胺培南、头孢他啶、环丙沙星作用于铜绿假单胞菌的蛋白靶点;使用UniProt数据库校正筛选得到靶点的名称;并通过Cytoscape 3.9.1软件构建“中药—化学成分—作用靶点网络”。
2.7 构建蛋白质-蛋白质相互作用网络(PPI)将2.6项中得到的扶正透邪解毒化瘀方作用于铜绿假单胞菌的靶点输入String数据库,以“Pseudomonas aeruginosa”,“medium confidence=0.4”为筛选条件,将获取的数据导入Cytoscape 3.9.1软件,根据度值(degree)筛选出关键作用靶点。
2.8 扶正透邪解毒化瘀方与抗菌药物的协同作用机制分析筛选出扶正透邪解毒化瘀方、亚胺培南、头孢他啶、环丙沙星联合作用于铜绿假单胞菌的蛋白靶点,通过韦恩图进行可视化分析。
2.9 扶正透邪解毒化瘀方功能富集分析通过DAVID数据库对扶正透邪解毒化瘀方作用于铜绿假单胞菌的靶点进行基因本体(GO)和京都基因与基因组百科全书(KEGG)功能富集分析;利用微生信平台将结果进行可视化操作。
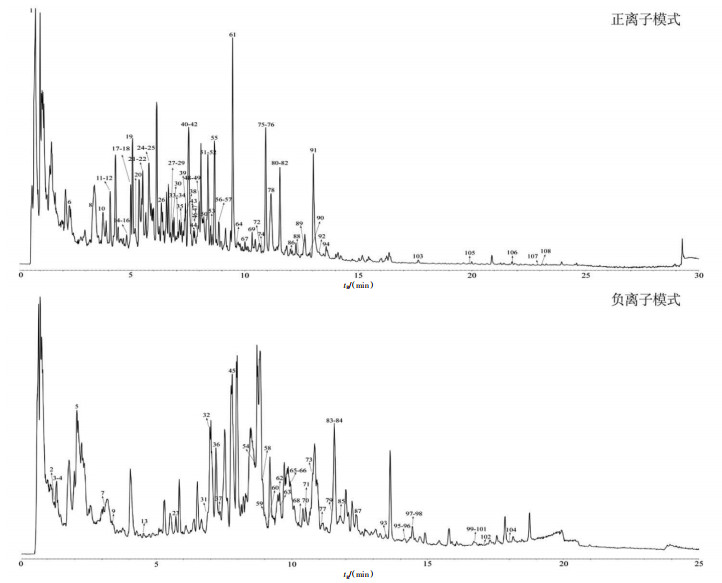
3 结果 3.1 扶正透邪解毒化瘀方化学成分分析及筛选结果将数据导入OSI/SMMS系统进行峰提取、峰匹配等质谱数据处理,根据质荷比(m/z)、保留时间,从该方中共鉴定出108个化学成分,以黄酮类、萜类、有机酸、甾醇类等为主,具体见图 1和开放科学(资源服务)标识码(OSID)。共有20个化学成分符合筛选条件(OB≥30%、DL≥0.18、Caco-2≥-0.4、HL≥4)。
|
| 图 1 扶正透邪解毒化瘀方正/负离子模式总离子流图 Fig. 1 Negative and positive total ion chromatogram of Fuzheng Touxie Jiedu Huayu Formula |
按照OB≥30%、DL≥0.18、Caco-2≥ -0.4、HL≥4条件,共筛选出155种化学成分。
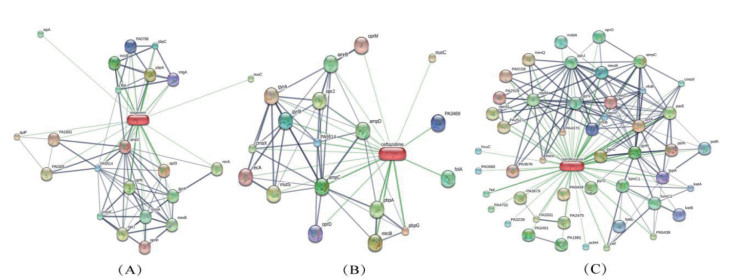
3.3 中药和抗菌药物化学成分作用于铜绿假单胞菌靶点收集结果将3.1项与3.2项中筛选得到的化学成分进行合并、去重,共得到162个化学成分,其中42个化学成分能够通过Stitch数据库找到直接作用于铜绿假单胞菌的靶蛋白240个,根据度值大小,以度值大于中位数8共筛选出17项,以黄酮类、甾醇类为主,还包括三萜类、生物碱类;其中β-谷甾醇、槲皮素、木犀草素度值显著高于其它化学成分,推测这些可能为扶正透邪解毒化瘀方作用于铜绿假单胞菌的核心化学成分,见图 2和表 1。亚胺培南、头孢他啶和环丙沙星对铜绿假单胞菌分别有22个、18个和47个直接作用靶点,见图 3。

|
| 注:该图由294个节点、1 430条边构成;绿色为中药、橙色为单味药化学成分、紫色为多味药共有化学成分、蓝色为药物作用于铜绿假单胞菌的靶点;HQ-黄芪、JYH-金银花、DG-当归、GC-甘草、HQ-黄芩、LQ-连翘、LL-漏芦、CS-赤芍、GL-瓜蒌、BJC-败酱草、YYR-薏苡仁、XYS-西洋参。 图 2 中药—化学成分—作用靶点网络图 Fig. 2 Drug-component-traget network |

|
|
| 注:A.亚胺培南;B.头孢他啶;C.环丙沙星。 图 3 抗菌药物作用于铜绿假单胞菌的靶点 Fig. 3 Targets of antibacterial drugs acting on Pseudomonas aeruginosa |
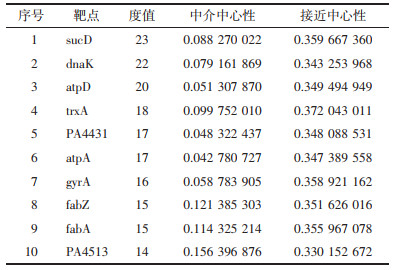
在String数据库输入240个潜在作用靶点,将结果导入Cytoscape 3.9.1,运用“Network Analysis”进行网络拓扑属性分析,依据“度值”“中介中心性”和“接近中心性”3个参数均大于平均值共筛选出10个扶正透邪解毒化瘀方干预铜绿假单胞菌的潜在核心靶点,见表 2。
|
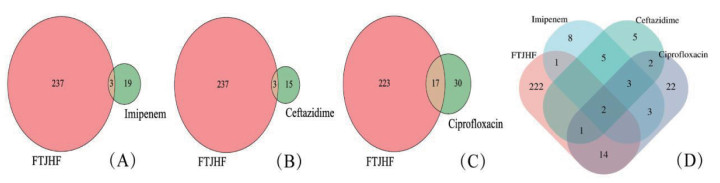
利用韦恩图对4种药物作用靶点分析发现,扶正透邪解毒化瘀方分别与亚胺培南、头孢他啶、环丙沙星有3个、3个和17个共同作用靶点;4种药物共同作用靶点2个;扶正透邪解毒化瘀方特异性作用靶点222个;共同作用靶点主要作用于细菌能量和生化代谢、DNA遗传物质复制、蛋白质功能、表面多糖形成等途径,还可以影响与细菌多重耐药性形成密切相关的AmpC(β-内酰胺酶)靶点。见图 4、表 3。
|
| 注:A~C依次为扶正透邪解毒化瘀方与亚胺培南、头孢他啶、环丙沙星共同作用靶点数目;D为4种药物共同作用靶点数目。 图 4 中药与抗菌药物共同作用靶点数目 Fig. 4 Number of targets for intervention with Chinese medicine and antibacterial drugs |
|
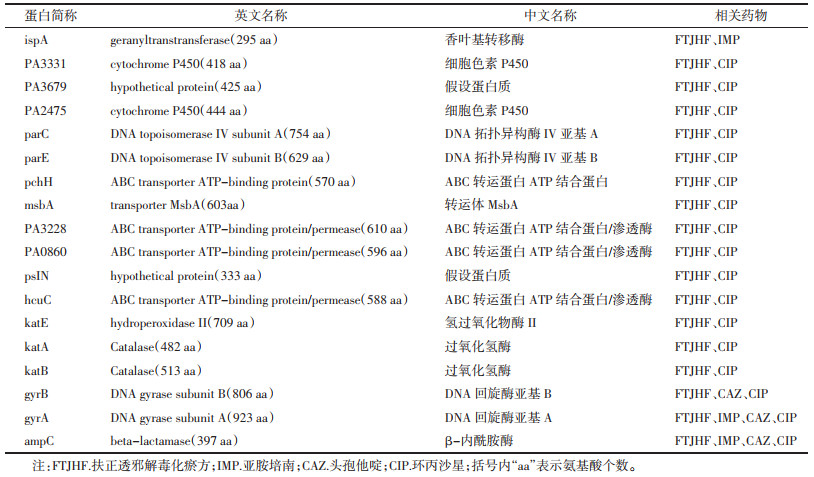
GO富集分析共得到条目24个(P<0.05),其中生物过程(BP)条目8个,细胞组成(CC)条目6个,分子功能(MF)条目10个。BP中主要涉及ATP合成耦合质子转运、DNA拓扑变化、脂质代谢过程、蛋白质折叠、dTDP-鼠李糖生物合成过程等过程;CC中主要涉及膜、染色体、质膜胞质侧的外在成分等组分;MF中主要涉及氧化还原酶活性、质子转运ATP合酶活性、ATP结合、DNA拓扑异构酶Ⅱ型(ATP水解)活性[DNA topoisomerase typeⅡ(ATP-hydrolyzing) activity]等过程,见图 5。
|
| 图 5 扶正透邪解毒化瘀方作用于铜绿假单胞菌相关靶点GO富集分析 Fig. 5 GO enrichment analysis of Pseudomonas aeruginosa-related targets by Fuzheng Touxie Jiedu Huayu Formula |
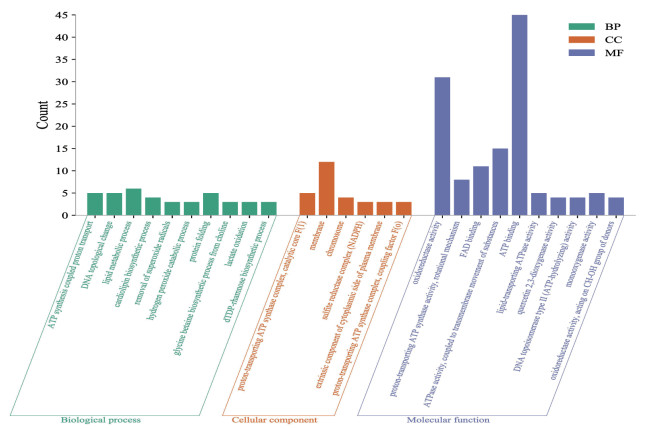
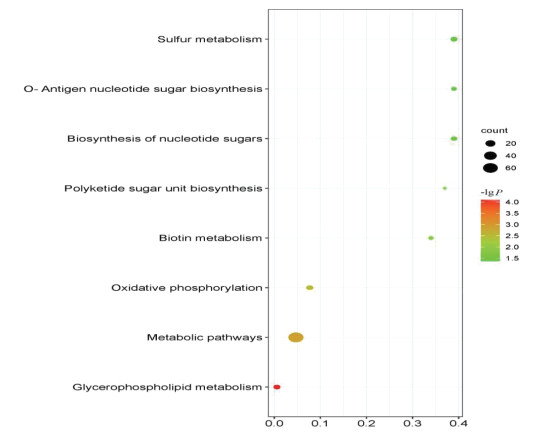
KEGG富集分析共筛选出8条信号通路(P<0.05)。主要涉及甘油磷脂代谢、代谢途径、氧化磷酸化、生物素代谢、聚酮糖生物合成、核糖生物合成、O-抗原核糖生物合成、硫代谢等通路。此外,富集结果还包括脂肪酸代谢、抗生素如链霉素生物合成等通路,见图 6。
|
| 图 6 扶正透邪解毒化瘀方作用于铜绿假单胞菌相关靶点KEGG富集分析 Fig. 6 KEGG enrichment analysis of Pseudomonas aeruginosa-related targets by Fuzheng Touxie Jiedu Huayu Formula |
铜绿假单胞菌的耐药机制分为天然耐药、获得性耐药和适应性耐药3类[10]。鉴于其较高的检出率和复杂的耐药机制带来的临床抗感染难题,世卫组织于2017年将其列入新型抗生素研发重点病原体清单[11]。目前,MDRPA的抗感染药物治疗原则主要根据药敏报告选择抗PA活性强的抗菌药物进行单独或联合用药,但MDRPA对非限制使用级和限制使用级抗菌药物往往耐药,特殊使用级抗菌药物也存在疗效上的不确定性。中药具有不良反应小、不易耐药、抑制病原体、调节宿主免疫等优势,在作为抗菌药物的补充和替代品上有重要的潜力[12]。
LC-MS/MS结果显示,扶正透邪解毒化瘀方共鉴定出108个化学成分,以黄酮类、萜类、有机酸、甾醇类等为主,而这几类化学成分对多重耐药菌均具有较好的抑菌作用。黄酮类如黄芩苷可直接抑制PA生物膜生成、减少多糖蛋白复合物产量及抑制群体感应系统的表达[13],与左氧氟沙星、头孢哌酮/舒巴坦联用可增强对生物被膜的破坏作用[14-15]。萜类如熊果酸对多种细菌具有直接抑菌作用,可与万古霉素、诺氟沙星以及β-内酰胺药物发挥协同作用[16]。有机酸类如咖啡酸、绿原酸可以干扰PA群体感应系统相关基因转录,抑制生物被膜形成[17-18]。关于甾醇类抗菌活性的研究报道较少,云杉树皮提取物对PA有直接抑菌作用[19],气质联用(GC-MS)检测发现提取物中含有较高含量的植物甾醇;麦角甾醇可以增加氨基糖苷类抗菌药物的抗真菌活性,但在细菌中尚未有类似报道,为后续研究提供了方向[20]。
网络药理学结果显示,β-谷甾醇、槲皮素、木犀草素、山奈酚、黄芩素度值较高,在扶正透邪解毒化瘀方抑制/逆转MDRPA耐药性的过程中可能发挥着关键作用。β-谷甾醇对金黄色葡萄球菌、大肠埃希菌、铜绿假单胞菌均具有直接抑制作用,是未来开发抗菌药物的潜在候选者[21]。槲皮素与阿米卡星、左氧氟沙星、庆大霉素、头孢曲松等抗菌药物联用具有协同抗MDRPA的作用,机制与抑制生物被膜形成、群体感应系统有关[22]。槲皮素和木犀草素还可以诱导TonB依赖性转运蛋白的表达,增强PA对铁载体药物的敏感性,而新型抗菌药物头孢地尔正是一种铁载体头孢菌素类药物[23]。木犀草素还可以有效抑制PA生物被膜的形成和运动性,机制与减弱群体感应系统相关信号分子和基因的表达水平有关[24]。黄槟榔青的树皮提取物可以增强诺氟沙星对PA的抗菌活性,而山奈酚和槲皮素是提取物的主要化学成分[25]。黄芩素在亚抑菌浓度下通过下调PA群体感应系统相关信号分子的表达,抑制了细菌的运动性和生物被膜形成能力[26]。说明扶正透邪解毒化瘀方中多种成分不仅可以直接抑制PA,还可以与多种抗菌药物发挥协同作用,干预生物被膜和群体感应系统可能是其主要作用机制。
通过分析扶正透邪解毒化瘀方相关化学成分和抗菌药物作用于PA的共同靶点来看,该方对抗菌药物起协同作用主要与干预细菌生化代谢、DNA复制、蛋白质功能、表面多糖形成等机制相关。IspA(香叶基转移酶)是异戊二烯的催化酶,蛋白质在异戊二烯化过程中被翻译修饰为功能蛋白,参与细胞生长、分化等活动[27]。IspA突变会导致PA对妥布霉素、庆大霉素和阿米卡星的最小抑菌浓度升高2倍[28]。细菌DNA拓扑异构酶和DNA回旋酶同属于Ⅱ型拓扑异构酶,是喹诺酮类药物抗革兰氏阴性菌的主要靶标。DNA拓扑异构酶IV在DNA复制和转录过程中负责控制DNA拓扑状态;DNA回旋酶由gyrA和gyrB亚基组成,前者负责DNA链的结合、断裂和重新连接,后者负责ATP酶的活性。DNA拓扑异构酶Ⅳ和gyrA的突变增加了PA对左氧氟沙星、环丙沙星等喹诺酮类抗菌药物的耐药性[29-30]。PA 3228/0806(ABC转运蛋白ATP结合蛋白/渗透酶)参与包括PA在内的多种革兰氏阴性菌O抗原的合成过程,而O抗原是脂多糖的主要构成部分,可保护细菌免受噬菌体、细菌素等的杀灭作用[31]。MsbA转运体属于ABC转运蛋白家族,通过利用ATP结合和水解的力量,促进脂多糖的合成和细菌活力,阻断其转运活性或许能够同时阻断ATP酶活性,在成为新型抗菌药物靶标上具有一定的吸引力[32]。
PPI蛋白互作网络结果提示,扶正透邪解毒化瘀方干预PA的核心靶点除了上述提到的gyrA外,还包括dnaK、fabZ和fabA等已知的参与PA耐药过程的关键靶点。DnaK蛋白是由ATP酶活性介导的分子伴侣,是介导PA在内的革兰氏阴性菌应激反应、保持细菌完整性的重要蛋白,诱导其突变可增强MDR菌对抗菌药物的敏感性[33]。FabZ和fabA是参与细菌Ⅱ型脂肪酸合成途径的酶,已被用作抗多种病原体的广谱药物靶点,黄酮类化合物可通过抑制fabZ活性进而对PA产生直接抑菌作用[34]。
GO和KEGG富集分析提示,扶正透邪解毒化瘀方的作用靶点主要与调节细菌能量和生化代谢、调控DNA/蛋白质稳态、影响细菌胞质胞膜以及干预对细菌起保护作用的表面多糖和生物被膜合成等密切相关。ZHOU D P等[35]通过基因编辑技术干预PA,并用高通量测序(RNA-Seq)发现,857个上调基因与氧化还原过程、跨膜转运、脂质代谢、甘油磷脂代谢、氧化还原酶活性等途径密切相关,本研究也得到了类似的结果。细胞质膜是细菌的基本结构之一,具有DNA复制、酶分泌、生物成分合成和能量生产等功能[19]。Ⅱ型DNA拓扑异构酶相关功能在上文中已经论述,以其为靶标设计的二碱四氢吡喃化合物对PA显示出直接抑制作用[36]。Rha(鼠李糖脂)是细菌多糖的常见成分,例如脂多糖、胞外多糖、荚膜多糖和细胞壁多糖。dTDP-Rha是最重要的糖前体之一,在许多生物过程中起着关键作用[37]。
综上,研究通过LC-MS/MS技术结合网络药理学探讨了扶正透邪解毒化瘀方单独及与抗菌药物联用干预铜绿假单胞菌耐药性的药效物质学基础和机制,发现该方具有多成分、多靶点、多途径的干预特点。潜在的起主要干预作用的化学成分以黄酮类、甾醇类、萜类为主,主要干预机制包括抑制生物被膜和群体感应系统以及影响铜绿假单胞菌能量和生化代谢、DNA复制、蛋白质功能、表面多糖生成等相关。目前,关于中药抗细菌耐药性的研究大多停留在宏观层面,较少细化到化学成分层面;而网络药理学既往常用于探索药物和疾病之间的潜在联系,研究综合LC-MS/MS和网络药理学来探索药物具体化学成分对病原体的直接作用,为从天然药物中开发抗菌药物提供了一定的思路和借鉴。同时,从药物作用靶点层面为日后深入研究该方做出了积极的探索。
| [1] |
KOCSIS B, GULYÁS D, SZABÓ D. Diversity and distribution of resistance markers in Pseudomonas aeruginosa international high-risk clones[J]. Microorganisms, 2021, 9(2): 359. DOI:10.3390/microorganisms9020359 |
| [2] |
李耘, 郑波, 吕媛, 等. 中国细菌耐药监测(CARST)研究2019—2020革兰氏阴性菌监测报告[J]. 中国临床药理学杂志, 2022, 38(5): 432-452. LI Y, ZHENG B, LYU Y, et al. Antimicrobial susceptibility of Gram-negative organisms: results from China antimicrobial resistance surveillance trial(CARST) program, 2019-2020[J]. The Chinese Journal of Clinical Pharmacology, 2022, 38(5): 432-452. |
| [3] |
LYNCH J P 3rd, ZHANEL G G, CLARK N M. Emergence of antimicrobial resistance among Pseudomonas aeruginosa: implications for therapy[J]. Seminars in Respiratory and Critical Care Medicine, 2017, 38(3): 326-345. DOI:10.1055/s-0037-1602583 |
| [4] |
郭咸希, 何文, 许鸣, 等. 我院133例痰培养铜绿假单胞菌阳性患者抗菌药物应用分析[J]. 中国药师, 2020, 23(12): 2426-2430. GUO X X, HE W, XU M, et al. Analysis of the application of antibiotics in 133 patients with positive sputum culture of Pseudomonas aeruginosa[J]. China Pharmacist, 2020, 23(12): 2426-2430. DOI:10.3969/j.issn.1008-049X.2020.12.025 |
| [5] |
李猛, 王成祥, 徐红日, 等. 正气亏虚、毒瘀互结是老年性肺炎的基本病机[J]. 中医药临床杂志, 2011, 23(4): 353-354. LI M, WANG C X, XU H R, et al. Deficiency of vital qi and mutual accumulation of toxin and blood stasis are the basic pathogenesis of senile pneumonia[J]. Clinical Journal of Traditional Chinese Medicine, 2011, 23(4): 353-354. |
| [6] |
XU H R, LI M, WANG C X, et al. Evaluation on clinical efficacy of Fuzheng Jiedu Huayu Decoction combined with antibiotics in the treatment of pneumonia in the elderly-a multi-center, double-blind, parallel, randomized controlled trial[J]. Complementary Therapies in Medicine, 2018, 37: 127-132. DOI:10.1016/j.ctim.2017.11.012 |
| [7] |
马洁, 刘国星, 徐红日, 等. 扶正透邪解毒化瘀方联合抗生素对多重耐药铜绿假单胞菌体外抑制作用[J]. 中华中医药杂志, 2018, 33(6): 2574-2577. MA J, LIU G X, XU H R, et al. Inhibitory effect of Fuzheng Touxie Jiedu Huayu Decoction combined with antibiotics on multiple drug-resistant Pseudomonas aeruginosa in vitro[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2018, 33(6): 2574-2577. |
| [8] |
马洁. 扶正透邪解毒化瘀方对MDRPA的抑菌作用及免疫损伤的部分干预机制研究[D]. 北京: 北京中医药大学, 2018. MA J. Study on the bacteriostatic effect of Fuzheng Touxie Jiedu Huayu recipe on MDRPA and some intervention mechanisms of immune injury[D]. Beijing: Beijing University of Chinese Medicine, 2018. |
| [9] |
顾浩, 何文静, 马群. 基于靶点网络的芪归银复方与亚胺培南和左氧氟沙星联用对铜绿假单胞菌的作用机制分析[J]. 中华中医药杂志, 2019, 34(10): 4561-4565. GU H, HE W J, MA Q. Mechanism analysis of the combination of Qiguiyin Formula and Imamipenem and Levofloxacin antibiotics on Pseudomonas aeruginosa based on target network[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2019, 34(10): 4561-4565. |
| [10] |
LEPE J A, MARTÍNEZ-MARTÍNEZ L. Resistance mechanisms in Gram-negative bacteria[J]. Medicina Intensiva, 2022, 46(7): 392-402. DOI:10.1016/j.medin.2022.02.004 |
| [11] |
Guidelines for the prevention and control of carbapenem-resistant Enterobacteriaceae, Acinetobacter baumannii and Pseudomonas aeruginosa in health care facilities[J]. Geneva: World Health Orgnization, 2017.
|
| [12] |
PANG Z, ZHU Q J. Traditional Chinese medicine is an alternative therapeutic option for treatment of Pseudomonas aeruginosa infections[J]. Frontiers in Pharmacology, 2021, 12: 737252. DOI:10.3389/fphar.2021.737252 |
| [13] |
李少滨, 方泓, 成颜琦, 等. 黄芩苷、黄芪甲苷对铜绿假单胞菌生物膜的体外干预实验研究[J]. 上海中医药杂志, 2017, 51(11): 63-67, 83. LI S B, FANG H, CHENG Y Q, et al. Experimental study on intervention of baicalin and astragaloside IV on Pseudomonas aeruginosa biofilm in vitro[J]. Shanghai Journal of Traditional Chinese Medicine, 2017, 51(11): 63-67, 83. |
| [14] |
菅凌燕, 何晓静, 于莹. 黄芩苷联合左氧氟沙星对铜绿假单胞菌生物膜的影响及相关机制[J]. 中国医院药学杂志, 2012, 32(14): 1097-1100. JIAN L Y, HE X J, YU Y. In vitro activity and related mechanisms of action of baicalin in combination with levofloxacin on Pseudomonas aeruginose biofilms[J]. Chinese Journal of Hospital Pharmacy, 2012, 32(14): 1097-1100. |
| [15] |
董必英, 陈一强, 孔晋亮, 等. 黄芩苷联合头孢哌酮/舒巴坦对铜绿假单胞菌生物膜破坏作用的体外研究[J]. 中国现代医药杂志, 2016, 18(1): 1-4. DONG B Y, CHEN Y Q, KONG J L, et al. An in vitro study on destructive effect of baicalin combined with sulbactam-cefperazone on pseudomonas aeruginose biofilm[J]. Modern Medicine Journal of China, 2016, 18(1): 1-4. |
| [16] |
张鹏, 尹向楠, 汪子姝, 等. 熊果酸抗菌作用研究进展[J]. 轻工科技, 2021, 37(6): 15-16, 18. ZHANG P, YIN X N, WANG Z S, et al. Research progress on antibacterial effect of ursolic acid[J]. Light Industry Science and Technology, 2021, 37(6): 15-16, 18. |
| [17] |
张艳, 赵淑珍, 何静, 等. 绿原酸、c-di-GMP、人杀菌肽LL-37对铜绿假单胞菌生物被膜耐药性的影响[J]. 河北医科大学学报, 2022, 43(6): 721-726. ZHANG Y, ZHAO S Z, HE J, et al. Effect of chlorogenic acid, c-di-GMP and human bactericidal peptide LL-37 on drug resistance of Pseudomonas aeruginosa biofilm[J]. Journal of Hebei Medical University, 2022, 43(6): 721-726. |
| [18] |
于福浩, 娄在祥, 王洪新, 等. 咖啡酸对铜绿假单胞菌群体感应的抑制及毒力因子降低的研究[J]. 食品与生物技术学报, 2019, 38(6): 56-63. YU F H, LOU Z X, WANG H X, et al. Effect of caffeic acid on quorum sensing and virulence factors of Pseudomonas aeruginosa[J]. Journal of Food Science and Biotechnology, 2019, 38(6): 56-63. |
| [19] |
BURČOVÁ Z, KREPS F, GREIFOVÁ M, et al. Antibacterial and antifungal activity of phytosterols and methyl dehydroabietate of Norway spruce bark extracts[J]. Journal of Biotechnology, 2018, 282: 18-24. |
| [20] |
ANDRADE J C, MORAIS BRAGA M F B, GUEDES G M M, et al. Cholecalciferol, ergosterol, and cholesterol enhance the antibiotic activity of drugs[J]. International Journal for Vitamin and Nutrition Research Internationale Zeitschrift Fur Vitamin-Und Ernahrungsforschung Journal International De Vitaminologie et De Nutrition, 2018, 88(5/6): 244-250. |
| [21] |
EDILU A, ADANE L, WOYESSA D. In vitro antibacterial activities of compounds isolated from roots of Caylusea abyssinica[J]. Annals of Clinical Microbiology and Antimicrobials, 2015, 14: 15. |
| [22] |
VIPIN C, SAPTAMI K, FIDA F, et al. Potential synergistic activity of quercetin with antibiotics against multidrug-resistant clinical strains of Pseudomonas aeruginosa[J]. PLoS One, 2020, 15(11): e0241304. |
| [23] |
LUSCHER A, GASSER V, BUMANN D, et al. Plant-derived catechols are substrates of TonB-dependent transporters and sensitize Pseudomonas aeruginosa to siderophore-drug conjugates[J]. mBio, 2022, 13(4): e0149822. |
| [24] |
GENG Y F, YANG C, ZHANG Y, et al. An innovative role for luteolin as a natural quorum sensing inhibitor in Pseudomonas aeruginosa[J]. Life Sciences, 2021, 274: 119325. |
| [25] |
DE FREITAS M A, DA CRUZ R P, DOS SANTOS A T L, et al. HPLC-DAD analysis and antimicrobial activities of Spondias mombin L. (Anacardiaceae)[J]. 3 Biotech, 2022, 12(3): 61. |
| [26] |
LUO J, KONG J L, DONG B Y, et al. Baicalein attenuates the quorum sensing-controlled virulence factors of Pseudomonas aeruginosa and relieves the inflammatory response in P. aeruginosa-infected macrophages by downregulating the MAPK and NFκB signal-transduction pathways[J]. Drug Design, Development and Therapy, 2016, 10: 183-203. |
| [27] |
WEBER L, HAGEMANN A, KALTENH?USER J, et al. Bacteria are new targets for inhibitors of human farnesyltransferase[J]. Frontiers in Microbiology, 2021, 12: 628283. |
| [28] |
PITTON M, OBERHAENSLI S, APPIAH F, et al. Mutation to ispA produces stable small-colony variants of Pseudomonas aeruginosa that have enhanced aminoglycoside resistance[J]. Antimicrobial Agents and Chemotherapy, 2022, 66(7): e0062122. |
| [29] |
AKASAKA T, ONODERA Y, TANAKA M, et al. Cloning, expression, and enzymatic characterization of Pseudomonas aeruginosa topoisomerase Ⅳ[J]. Antimicrobial Agents and Chemotherapy, 1999, 43(3): 530-536. |
| [30] |
KOLESNIKOVA E A, BRUSNIGINA N F, MAKHOVA M A, et al. The genome structure of ciprofloxacin-resistant Mycoplasma hominis clinical isolates[J]. Acta Naturae, 2020, 12(1): 56-62. |
| [31] |
HUSZCZYNSKI S M, HAO Y A, LAM J S, et al. Identification of the Pseudomonas aeruginosa O17 and O15 O-specific antigen biosynthesis loci reveals an ABC transporter-dependent synthesis pathway and mechanisms of genetic diversity[J]. Journal of Bacteriology, 2020, 202(19): e00347-e00320. |
| [32] |
ALEXANDER M K, MIU A, OH A, et al. Disrupting gram-negative bacterial outer membrane biosynthesis through inhibition of the lipopolysaccharide transporter MsbA[J]. Antimicrobial Agents and Chemotherapy, 2018, 62(11): e01142-e01118. |
| [33] |
ASGHAR A, TAN Y C, ZAHOOR M, et al. A scaffolded approach to unearth potential antibacterial components from epicarp of Malaysian Nephelium lappaceum L[J]. Scientific Reports, 2021, 11(1): 13859. |
| [34] |
MOYNIÉ L, HOPE A G, FINZEL K, et al. A substrate mimic allows high-throughput assay of the FabA protein and consequently the identification of a novel inhibitor of Pseudomonas aeruginosa FabA[J]. Journal of Molecular Biology, 2016, 428(1): 108-120. |
| [35] |
ZHOU D P, HUANG G T, XU G C, et al. CRISPRi-mediated gene suppression reveals putative reverse transcriptase gene PA0715 to be a global regulator of Pseudomonas aeruginosa[J]. Infection and Drug Resistance, 2022, 15: 7577-7599. |
| [36] |
SURIVET J P, ZUMBRUNN C, BRUYÉRE T, et al. Synthesis and characterization of tetrahydropyran-based bacterial topoisomerase inhibitors with antibacterial activity against gram-negative bacteria[J]. Journal of Medicinal Chemistry, 2017, 60(9): 3776-3794. |
| [37] |
LI S Q, CHEN F J, LI Y, et al. Rhamnose-containing compounds: biosynthesis and applications[J]. Molecules, 2022, 27(16): 5315. |
2. Beijing University of Chinese Medicine, Beijing 100029, China;
3. Department of Emergency and Intensive Care Unit, the Third Affiliated Hospital of Beijing University of Chinese Medicine, Beijing 100029, China;
4. Institute of Sepsis, Beijing University of Chinese Medicine, Beijing 100029, China
 2023, Vol. 40
2023, Vol. 40