文章信息
- 王晓雯, 张月, 胡璐瑶, 等.
- WANG Xiaowen, ZHANG Yue, HU Luyao, et al.
- UPLC-Q-TOF/MS结合网络药理学和分子对接技术探讨山豆根抗肝癌的药效物质及作用机制
- Pharmacodynamic material basis and mechanism of Sophorae Tonkinensis Radix et Rhizoma against liver cancer: an exploration based on UPLC-Q-TOF/MS, network pharmacology and molecular docking
- 天津中医药, 2023, 40(12): 1595-1608
- Tianjin Journal of Traditional Chinese Medicine, 2023, 40(12): 1595-1608
- http://dx.doi.org/10.11656/j.issn.1672-1519.2023.12.16
-
文章历史
- 收稿日期: 2023-08-20
2. 山东广通宝医药有限公司, 青州 262500;
3. 天津市医用质谱精准诊断企业重点实验室质谱应用中心, 天津 300399;
4. 中国科学院大学宁波华美医院, 宁波 315010
原发性肝癌在临床上属于常见恶性肿瘤,是中国第2位肿瘤致死病因[1]。肝癌患者缺乏特异性筛选方法且早期症状缺乏典型性,大多数患者在诊断时已经处于晚期状态,处于肝癌晚期的患者5年内的生存率下降到2%[2-3]。近几十年,治疗肝癌已采用局部消融术和经肝动脉化疗栓塞术等非根治性治疗,以及靶向治疗及免疫治疗等[4],但是还存在着远期疗效与复发风险的局限性。因此,探索有效的肝癌治疗方法和药物仍是目前首要的问题。近年来,中医药由于具有多成分、多靶点、多途径的优势,被广泛认可用于肝癌治疗,可以减少疾病的复发[5]。肝癌的病因,综合各医家的中医理论,主要包括正气亏虚、肝脾失调、癌毒、脾虚等[6]。不同病因引起的肝癌采用不同的治疗方法,正气亏虚导致的肝癌应该扶正祛邪,用活血化瘀、疏肝行气、补肾益精等中药;癌毒类导致的肝癌应用清热解毒、化瘀软坚等中药;脾虚导致的肝癌应该益气健脾,用清热利湿、疏肝理气等中药[7]。山豆根为豆科植物越南槐Sophora tonkinensis Gagnep.的干燥根和根茎,具有清热解毒,消肿利咽的功效。目前药理研究报道,山豆根不仅有抗炎、保肝等作用,还有抗氧化、抗肿瘤、保护心血管系统等药理作用。其中许多研究表明,山豆根具有很好的抗肝癌作用,研究发现山豆根提取物能够抑制人肝母细胞瘤HepG2细胞、人肝癌Hep3B细胞的增殖,山豆根生物碱能产生明确的体内抗肝肿瘤药理作用[8-12]。然而,目前山豆根抗肝癌作用的物质基础及作用机制尚不十分明确。
超高效液相色谱串联四级杆飞行时间质谱(UPLC-Q-TOF/MS)技术与传统的高效液相相比,具有小颗粒高性能微粒固定相、超高压输液泵,其具有分析速度快、质量精度高、灵敏度高和分辨率高等特点[13]。UNIFI 1.8软件配有天然产物数据库,该库中有6 000多种组分,与UPLC-Q-TOF/MS配合使用,代替了传统的人工提峰、计算分子式及分析碎片断裂情况的模式,有利于更高效率地识别中药中的复杂化学成分及其化学结构,为研究中药药效的物质基础提供了强有力的技术支持[14-16]。网络药理学利用复杂的网络模型建立药物、靶点与疾病间的相互作用网络,是多数据、多学科融合的产物,表明了中药的多成分、多靶点的作用特点,适合运用于探索中药药理作用的作用靶点以及作用机制[17-19]。
因此,本研究利用UPLC-Q-TOF/MS结合UNIFI 1.8软件快速鉴定山豆根的化学成分,通过应用网络药理学结合分子对接技术筛选出山豆根抗肝癌的活性成分及核心靶点,以及细胞活性实验验证相关成分的抗肝癌作用,从分析化学成分和网络药理学角度进而探究山豆根抗肝癌作用的药效物质基础以及其可能的作用机制。
1 材料与方法 1.1 化学成分分析部分 1.1.1 药材、试剂和仪器山豆根饮片(安国药材市场,批号:2020G10111),经天津中医药大学中药学院李天祥教授鉴定为豆科植物越南槐Sophora tonkinensis Gagnep.的干燥根和根茎;色谱级甲醇、乙醇(赛默飞世尔科技有限公司);超高效液相色谱仪(美国Waters公司);Xevo G2 Q-TOF质谱仪(美国Waters公司);ACQUITY UPLC型二元泵和样品管理器(美国Waters公司);色谱柱[美国Waters公司ACQUITY UPLC BEH C18柱(100 mm × 2.1 mm,1.7 μm)];SB-120DT超声波清洗机(宁波新芝生物科技有限公司);H1750R离心机(湘仪离心机仪器有限公司)。
1.1.2 实验方法称取山豆根饮片50 g,用4倍量的95%乙醇溶剂加热回流提取3次,滤渣用4倍量的75%乙醇溶剂加热回流提取3次,每次2 h,合并提取液,在4 ℃以12 000 r/min,离心15 min(离心机半径为8.5 cm),取上清液,旋蒸挥发至干[20-21]。取山豆根浸膏50 mg,置于50 mL的容量瓶中,加甲醇定容至刻度,超声30 min,取上清液,经0.22 μm滤膜过滤,待进样。色谱条件:ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm);流动相:乙腈(A)- 0.2%甲酸水(B);梯度洗脱(0~1 min,10% A;1~21 min,10% A~100% A;21~22 min,100% A)。流速:0.3 mL/min;柱温:40 ℃;进样量:5 μL。质谱条件:系统采用电喷雾离子源正、负离子模式采集数据,扫描范围m/z 100~1 500,锥孔电压40 V,毛细管电压3 000 V,离子源温度120 ℃,脱溶剂气体流速800 L/h,锥孔反吹气50 L/h[22]。
运用UPLC-Q-TOF/MS技术采集数据后,采用UNIFI1.8软件自动识别化学成分。首先查阅文献[23],补充原有的山豆根化合物数据库;建立山豆根正负离子模式下的分析方法;再将原始质谱数据导入UNIFI1.8软件中,进行分析,UNIFI1.8软件对数据进行自动筛查、鉴定;之后将所得数据进行过滤筛选,设定质量误差为±10×10-6;最后结合相关文献各化合物的保留时间,以及碎片离子理论质量数、保留时间和分子式,对各化合物进行人工识别和鉴定。
1.2 网络药理学研究方法[24-25] 1.2.1 山豆根化学成分作用靶点的预测与筛选鉴定所得到的化学成分在PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)下载相应的2D结构图,未查到的化学成分结构通过查阅文献用ChemDraw作图保存为SDF结构,将结构导入PharmMapper数据库(http://www.lilab-ecust.cn/pharmmapper/)、Swiss Target Prediction数据库(http://www.swisstargetprediction.ch/)预测靶点,并借助UniProt(https://www.uniprot.org/)将靶点蛋白名称转化为对应的基因名(Gene Symbol),筛选并删除重复靶点。
1.2.2 肝癌疾病靶点的预测与筛选在GeneCards数据库(https://www.genecards.org/)及DrugBank数据库(https://go.drugbank.com/)以“liver cancer”为关键词检索,合并2个数据库的结果,并借助UniProt(https://www.uniprot.org/)将靶点蛋白名称转化为对应的官方基因名(Gene Symbol),筛选并删除重复靶点,得到肝癌治疗靶点。
1.2.3 韦恩图、蛋白质相互作用(PPI)网络及活性成分-交集靶点网络构建使用韦恩作图平台绘制出肝癌疾病和山豆根化学成分靶点的韦恩图,并通过String(https://www.stringdb.org/)数据库,构建PPI分析网络。用Cytoscape3.7.2筛选出度值排名前5位的靶点为山豆根抗肝癌的核心靶点。继续用Cytoscape3.7.2构建化学成分-交集靶点网络图,其中度值排名前6位的化学成分即为核心活性成分。
1.2.4 生物信息分析将交集靶点导入DAVID数据库(https://david.ncifcrf.gov/),进行基因本体分析(GO)和京都基因和基因组百科全书(KEGG)富集通路分析,并通过微生信平台(http://www.bioinformatics.com.cn/)对其为生物过程(BP),细胞组件(CC),分子功能(MF)各自显著性前10位的结果以及KEGG显著性前20位的条目进行可视化,以柱状图和富集气泡图进行展示。最后在Cytoscape 3.7.2软件中构建“成分-靶点-通路”网络。
1.2.5 分子对接验证利用TCMSP数据库(https://old.tcmsp-e.com/tcmsp.php)下载山豆根主要活性成分的mol 2格式的分子结构。利用RCSB PDB蛋白数据库(https://www.rcsb.org/)下载PPI网络中度值前5位的靶点蛋白的PDB格式的3D晶体结构。通过运行Autodock Vina进行分子对接。采用PyMOL软件将分子对接结果可视化。
1.3 噻唑蓝(MTT)比色法检测细胞活性 1.3.1 细胞、主要试剂与仪器人肝癌细胞(HepG2,武汉普赛诺公司);三叶豆紫檀苷、氧化苦参碱、苦参碱(成都埃法生物科技有限公司);二甲基亚砜(赛默飞世尔科技有限公司);胎牛血清、青链霉素混合液(Gibco公司);DMEM培基(BI公司);磷酸缓冲液(1×,pH= 7.2~7.4)(索莱宝生物科技有限公司);AII级生物安全柜(海尔公司);倒置显微镜(Nikon TS2);酶标仪(BioTek公司)。
1.3.2 细胞培养HepG2细胞置于5% CO2,37 ℃恒温培养箱中,在添加10%胎牛血清的DMEM培养基中生长,以传代后状态较好的细胞进行实验。
1.3.3 细胞活性检测设置分组为10组,包括空白组,三叶豆紫檀苷组(0.4、0.9、1.4 mmol/L),氧化苦参碱组(4.5、6、7.5 mmol/L),苦参碱组(4.8、6.4、8 mmol/L)。取对数生长期细胞,以5×104/孔的细胞悬液100 μL接种于96孔培养板中,每组6个复孔,培养24 h。弃去培养基,各浓度药物以每孔100 μL加入预先培养的细胞中,培养24 h。弃去培养基,加入100 μL的5% MTT溶液于各孔中,于5% CO2,37 ℃恒温培养箱中继续孵育3 h。弃上清液,各孔中分别加入150 μL的DMSO,低速转动10 s,使结晶全部溶解,在酶标仪上测定490 nm的吸光度OD值,计算细胞存活率。公式如下:
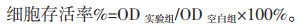 |
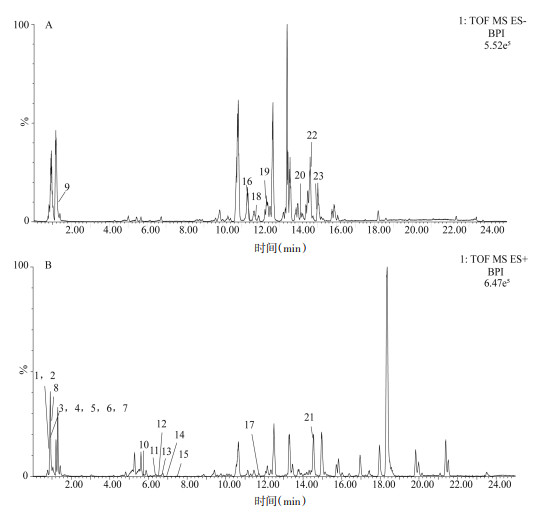
采用UPLC-Q-TOF/MS技术对山豆根提取物进行检测分析,结果分别得到正、负离子模式下的基峰图(见图 1)。采用UNIFI 1.8软件进行分析,以及与相关文献比对共鉴定出23个化合物。包括吡啶类生物碱9个,异黄酮类化合物3个,二氢黄酮类化合物4个,二氢异黄酮类化合物2个,黄酮醇类化合物1个,苯并呋喃类化合物2个,蒽醌类化合物1个,木脂素类化合物1个,并得到各化学成分的保留时间、m/z值、碎片离子等。数据见开放科学(资源服务)标识码(OSID)。
|
| 图 1 山豆根负离子模式(A)和正离子模式(B)的BPI图 Fig. 1 BPI diagram of Sophora tonkinensis in negative ion (A) and positive ion (B) mode |
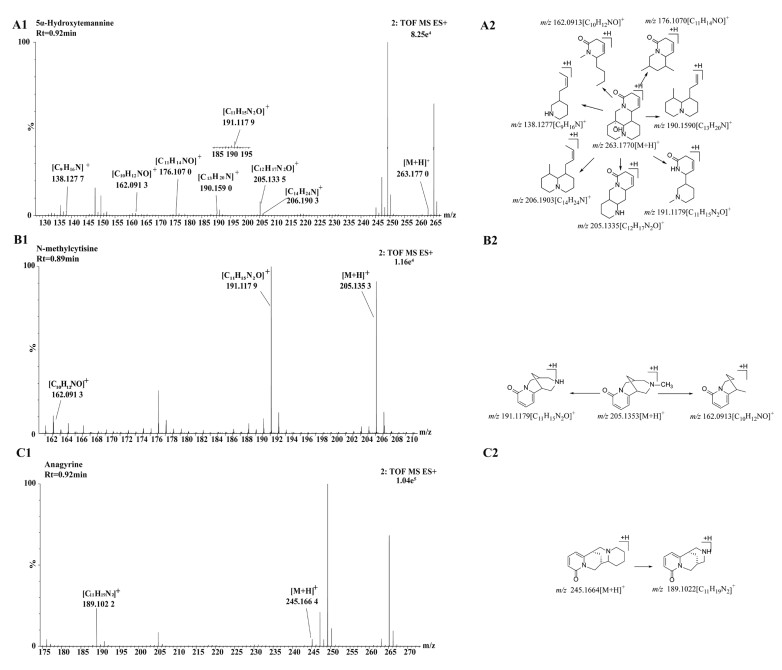
从山豆根中共鉴定出苦参碱类5个,包括5α-羟基莱曼碱、苦参碱、5α,14β-二羟基苦参碱、7,11-去氢苦参碱、氧化苦参碱。以化合物3为例,在正离子模式下,UNIFI 1.8软件预测化合物3为5α-羟基莱曼碱,在一级质谱中准分子离子峰为m/z 263.177 0[M+H]+,产生的主要碎片离子信息有138.127 7[C9H16N]+、162.091 3[C10H12NO]+、176.107 0[C11H14NO]+、190.159 0[C13H20N]+、191.117 9[C11H15N2O]+、205.133 5[C12H17N2O]+、206.190 3[C14H24N]+,推测其为5α-羟基莱曼碱,得到质谱图及其裂解途径(见图 2A)。预测所得化合物5也呈现碎片离子191.117 9[C11H15N2O]+、206.190 3[C14H24N]+,且与相关文献[26-30]进行比较,推测化合物5为苦参碱。
|
| 注:A.5α-羟基莱曼碱;B.N-甲基金雀花碱;C.臭豆碱;1.质谱图;2.裂解途径。 图 2 吡啶类生物碱类化合物质谱图及裂解途径 Fig. 2 Mass spectrogram and fragmentation pathway of pyridine alkaloid |
从山豆根中共鉴定出金雀花碱类3个,包括N-甲基金雀花碱、金雀花碱、N-己酰基金雀花碱。以化合物1为例,在正离子模式下,UNIFI 1.8软件预测化合物1为N-甲基金雀花碱,在一级质谱中准分子离子峰为m/z 205.135 3[M+H]+,产生的主要碎片离子信息有162.091 3[C10H12NO]+、191.117 9[C11H15N2O]+,与相关文献[26-29]进行比较,推测其为N-甲基金雀花碱,得到质谱图及其裂解途径(见图 2B)。预测所得化合物2、11均呈现碎片离子162.091 3[C10H12NO]+、191.117 9[C11H15N2O]+,推测化合物2、11分别为金雀花碱、N-己酰基金雀花碱。
2.1.1.3 臭豆碱类从山豆根中共鉴定出臭豆碱类1个,为臭豆碱。在正离子模式下,UNIFI 1.8软件预测化合物4为臭豆碱,在一级质谱中准分子离子峰为m/z 245.166 4[M+H]+,产生的主要碎片离子信息有189.102 2[C11H19N2]+,且与相关文献[26-28]进行比较,推测其为臭豆碱,得到质谱图及其裂解途径(见图 2C)。
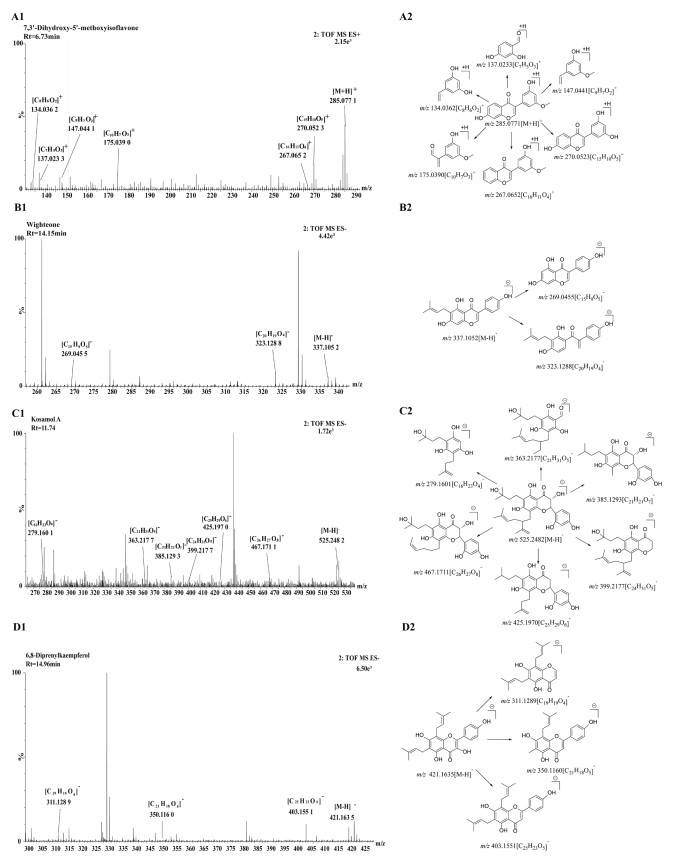
2.1.2 黄酮类化合物 2.1.2.1 异黄酮类从山豆根中共鉴定出异黄酮类化合物3个,分别为Sophoraflavone A、7,3′-二羟基-5′-甲氧基异黄酮、Wighteone。在正离子模式下,以化合物13为例,UNIFI 1.8软件预测化合物13为7,3′-二羟基-5′-甲氧基异黄酮,在一级质谱中准分子离子峰为m/z 285.077 1[M+H]+,产生的主要碎片离子信息有134.036 2[C8H6O2]+、137.023 3[C7H5O3]+、147.044 1[C9H7O2]+、175.039 0[C10H7O3]+、267.065 2[C16H11O4]+、270.052 3[C15H10O5]+,推测其为7,3′-二羟基-5′-甲氧基异黄酮,得到质谱图及其裂解途径(见图 3A)。在负离子模式下,以化合物20为例,预测化合物20为Wighteone,在一级质谱中准分子离子峰为m/z 337.105 2[M-H]-,产生的主要碎片离子信息有269.045 5[C15H9O5]-、323.128 8[C20H19O4]-,推测其为Wighteone,得到质谱图及其裂解途径(见图 3B)。
|
| 注:A.7,3′-二羟基-5′-甲氧基异黄酮;B.Wighteone;C.考萨莫A;D.6,8-二异戊烯基山柰酚;1.质谱图;2.裂解途径。 图 3 黄酮类化合物质谱图及裂解途径 Fig. 3 Mass spectrogram and fragmentation pathway of flavonoids |
从山豆根中共鉴定出二氢黄酮类化合物4个,分别为苦参醇E、考萨莫A、6,8-二异戊烯基柚皮素、山豆根黄酮K,二氢异黄酮类2个,为三叶豆紫檀苷、Sophotokin。以化合物18为例,在负离子模式下,UNIFI 1.8软件预测化合物18为考萨莫A,在一级质谱中准分子离子峰为m/z 525.248 2[M-H]-,产生的主要碎片离子信息有279.160 1[C16H23O4]-、363.217 7[C21H31O5]-、385.129 3[C21H21O7]-、399.217 7[C24H31O5]-、425.197 0[C25H29O6]-、467.171 1[C26H27O8]-,推测其为考萨莫A,得到质谱图及其裂解途径(见图 3C)。依据UNIFI 1.8软件预测化合物17为苦参醇E,化合物19为6,8-二异戊烯基柚皮素。
2.1.2.3 黄酮醇类从山豆根中共鉴定出黄酮醇类化合物1个,为6,8-二异戊烯基山柰酚。化合物23在一级质谱中准分子离子峰为m/z 421.163 5[M-H]-,产生的主要碎片离子信息有311.128 9[C19H19O4]-、350.116 0[C21H18O5]-、403.155 1[C25H23O5]-,推测其为6,8-二异戊烯基山柰酚,得到质谱图及其裂解途径(见图 3D)。
综上,黄酮类化合物在裂解电压和碰撞气体作用下,通常会发生逆-狄尔斯-阿尔德(RDA)反应,C环发生1,3键断裂或者1,4键断裂,产生1,3A、1,3B、1,4A、1,4B碎片离子;含有异戊烯基结构的黄酮化合物通常会失去异戊烯基,而黄酮C环的收缩会丢失CO、CO2,A环或B环有-OCH3的存在会丢失-CH3[31-33]。
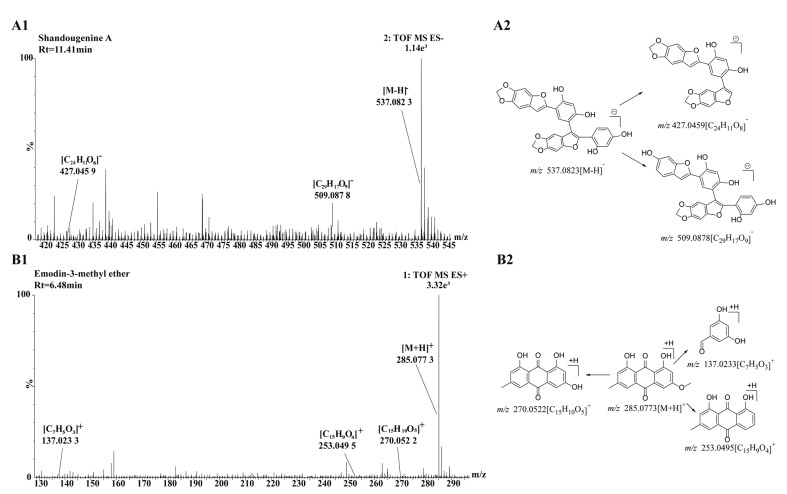
2.1.3 其他类化合物 2.1.3.1 苯并呋喃类从山豆根中共鉴定出苯并呋喃类2个,为2-(2′,4′-dihydroxyphenyl)-5,6-methylenedioxybenxofuran、Shandougenine A。以化合物16为例,在负离子模式下,UNIFI 1.8软件预测化合物16为Shandougenine A,在一级质谱中准分子离子峰为m/z 537.082 3[M-H]-,产生的主要碎片离子信息有427.045 9[C24H11O8]-、509.087 8[C29H17O9]-,推测其为Shandougenine A,得到质谱图及其裂解途径(见图 4A)。
|
| 注:A.Shandougenine A;B.大黄素甲醚;1.质谱图;2.裂解途径。 图 4 其他类化合物质谱图及裂解途径 Fig. 4 Mass spectrogram and fragmentation pathway of other compounds |
从山豆根中共鉴定出蒽醌类1个,为大黄素甲醚。在正离子模式下,UNIFI 1.8软件预测化合物12为大黄素甲醚,在一级质谱中准分子离子峰为m/z 285.077 3[M+H]+,产生的主要碎片离子信息有137.023 3[C7H5O3]+、253.049 5[C15H9O4]+、270.052 2[C15H10O5]+,推测其为大黄素甲醚,得到质谱图及其裂解途径(见图 4B)。
2.1.3.3 木脂素类从山豆根中共鉴定出木脂素类1个,为丁香脂素。在正离子模式下,UNIFI 1.8软件预测化合物14为丁香脂素,在一级质谱中准分子离子峰为m/z 419.171 0[M+H]+,产生的主要碎片离子信息有205.085 9[C12H13O3]+、217.085 9[C13H13O3]+,推测其为丁香脂素。
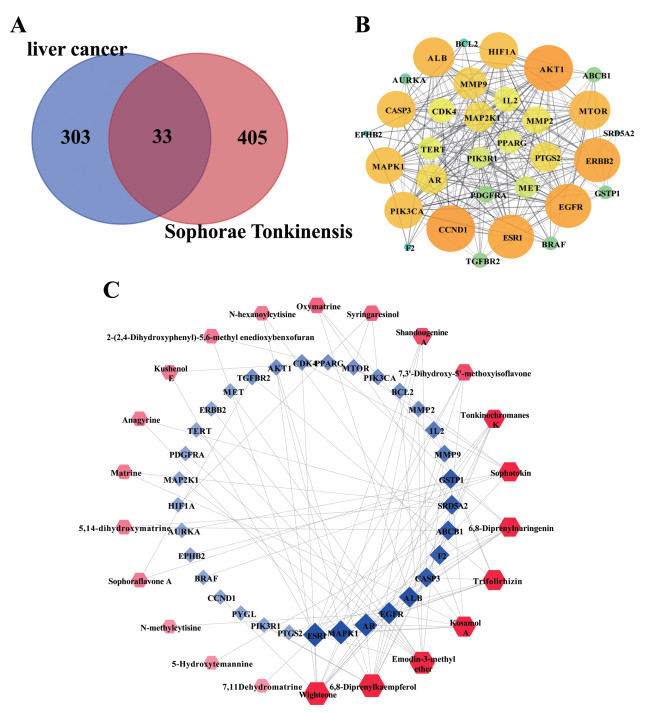
2.2 网络药理学研究部分 2.2.1 山豆根化学成分靶点和疾病靶点利用UPLC-Q-TOF/MS结合UNIFI 1.8软件鉴定得到的23种化学成分的405个靶点与肝癌的303个靶点取交集,构建韦恩图(见图 5A),结果得到33个共同靶点。
|
| 图 5 山豆根抗肝癌潜在靶点(A)、PPI网络(B)和山豆根“成分-靶点”网络图(C) Fig. 5 Potential anti-hepatoma targets of Sophora tonkinensis (A), PPI network (B) and components- targets network of Sophora tonkinensis (C) |
STRING数据库中导入33个潜在靶点,得到PPI网络关系信息,导入Cytoscape3.7.2对蛋白网络进行可视化分析(见图 5B),度值前5位的靶点为CCND1、AKT1、ERBB2、EGFR、ESR1,推测这些靶点可能是山豆根抗肝癌的核心靶点。
2.2.3 “成分-靶点”网络的构建通过Cytoscape 3.7.2软件构建“成分-靶点”网络图(见图 5C)。该网络包含55个节点和99条边,其中红色部分代表 22个山豆根化学成分(鉴定所得成分中金雀花碱潜在靶点与疾病靶点没有共同靶点),蓝色部分代表 33个共同靶点。其中6,8-二异戊烯基山柰酚、Wighteone、大黄素甲醚、考萨莫A、三叶豆紫檀苷、Sophotokin的度值较大,分别为11、11、10、8、8、7,因此,这些化合物可能是山豆根抗肝癌的关键成分。
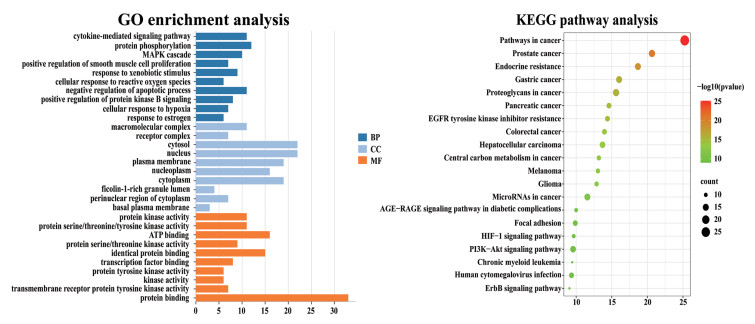
2.2.4 富集分析GO功能富集分析显示(见图 6),生物过程共获得117条注释结果,主要涉及细胞因子介导的信号通路、蛋白质磷酸化、MAPK级联、蛋白激酶B信号的正向调节、凋亡过程的负调控等;细胞成分共获得15条注释结果,主要包括细胞质、核质、核、大分子复合物等方面;分子功能共获得23条注释结果,主要涉及ATP结合、相同蛋白结合、转录因子结合等方面。
|
| 图 6 GO富集分析与KEGG通路分析 Fig. 6 GO enrichment analysis and KEGG pathway analysis |
KEGG通路富集分析共得到112个条目,删去不相关通路,选取前20条富集通路,并运用微生信平台进行可视化(见图 6)。结果显示山豆根抗肝癌主要涉及癌症的途径、HIF-1信号通路、AGE-RAGE信号通路、PI3K/AKT信号通路、ErbB信号通路等。以上结果说明山豆根可以通过调节协调多个生物过程及多个通路发挥抗肝癌的作用。
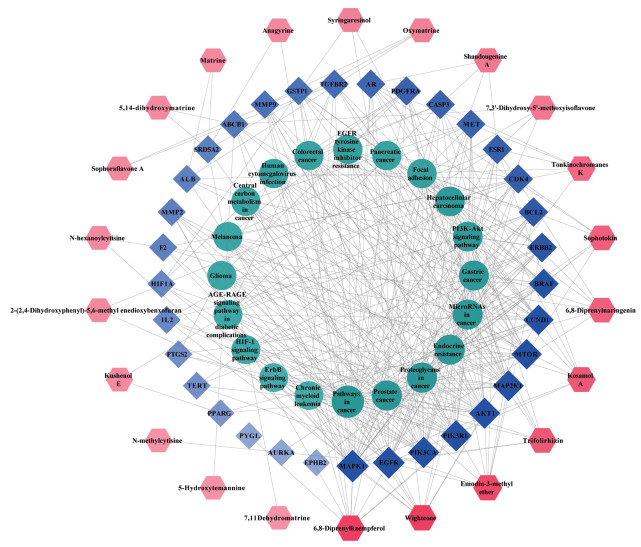
取显著性前20条的KEGG通路构建“成分-靶点-通路”网络(见图 7),网络共有75个节点和362条边。其中红色部分代表 22个山豆根化学成分,蓝色部分代表 33个共同靶点,绿色部分代表 20条信号通路。说明山豆根抗肝癌的药理过程涉及多成分、多靶点以及多途径。
|
| 图 7 山豆根“成分-靶点-通路”网络图 Fig. 7 Components- targets-pathways network of Sophora tonkinensis |
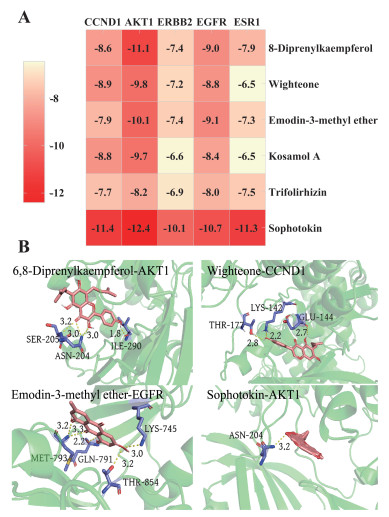
选取成分-靶点网络中度值前6位的活性成分6,8-二异戊烯基山柰酚、Wighteone、大黄素甲醚、考萨莫A、三叶豆紫檀苷、Sophotokin与PPI网络中度值排名前5位的核心靶点CCND1(PDBID:2W96)、AKT1(PDBID:7NH5)、ERBB2(PDBID:3PP0)、EGFR(PDBID:7AEM)、ESR1(PDBID:5FQV)进行对接,得到山豆根活性成分与靶点蛋白的最低结合能(见图 8A),通过pymol软件绘制分子对接(见图 8B)。结合能<0 kcal/mol表明配体化合物分子可以与受体靶点蛋白自发结合,结合能≤-5.0 kcal/mol表明配体化合物分子与受体靶点蛋白具有良好的结合活性。由图 8A可知,最低结合能均小于-5.0 kcal/mol,说明靶点蛋白和山豆根活性成分具有较好的亲和力。由图 8B可知,山豆根活性成分与靶点蛋白能通过氢键等分子间作用力结合。
|
| 图 8 分子对接最低结合能热图(A)和活性成分与靶点对接图(B) Fig. 8 Heat map of the lowest binding energy for molecular docking (A) and docking diagram of active components with targets (B) |
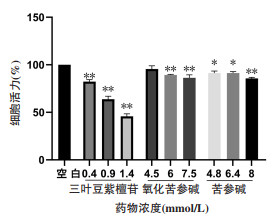
根据网络药理学分析结果以及中国药典中山豆根的指标成分,选择三叶豆紫檀苷、氧化苦参碱和苦参碱进行细胞活性验证。实验结果显示,三叶豆紫檀苷不同浓度组处理细胞的存活率较空白组明显降低,且呈现一定的剂量依赖性,差异有统计学意义(P < 0.05,P < 0.01),氧化苦参碱、苦参碱不同浓度组处理细胞的存活率比空白组降低,差异有统计学意义(P < 0.05,P < 0.01)(见图 9)。结果表明三叶豆紫檀苷、氧化苦参碱和苦参碱均有不同程度的抗肝癌作用。作用细胞相同时间下,三叶豆紫檀苷抑制HepG2细胞增殖的作用大于氧化苦参碱、苦参碱,符合网络药理学的分析结果。
|
| 注:与空白组比较,*P < 0.05,**P < 0.01。 图 9 三叶豆紫檀苷、氧化苦参碱、苦参碱对HepG2细胞活力的影响 Fig. 9 Effects of Trifolirhizin, Oxymatrine, Matrine on the viability of HepG2 cells |
据报道,在中国每年新发肝癌病例和肝癌导致的死亡病例约占全球病例的50%[34]。目前主要的肝癌治疗方法为手术切除肿瘤和进行肝脏移植,然而却存在肝源缺乏、手术困难、复发概率高、预后较差等问题[35]。因此,迫切需要继续探索和制定科学有效的抗肝癌策略。随着不断深入中药在肿瘤方面的研究,发现中医药可以通过抑制肿瘤的生长与转移、改善肿瘤微环境、调控细胞凋亡与自噬等不同机制发挥治疗作用[36]。山豆根具有清热解毒,消肿利咽的功效,而造成肝癌的病理机制大多是因为情志抑郁,气机阻滞,血行不畅,导致气滞血瘀而成;或者由于湿热邪毒或虫蛊、酒毒为害日久,瘀血毒结聚于肝脏所致[37]。许多研究表明山豆根具有很好的抗肝癌作用。山豆根生物碱通过调控血管内皮生长因子(VEGF)、磷脂酰肌醇3激酶(PI3K)及磷酸酯酶与张力蛋白同源物(PTEN)基因发挥明确的抗肝肿瘤作用[8];山豆根提取物可以明显抑制人肝癌细胞的增殖,降低线粒体的代谢活性[11];山豆根提取物不仅能抑制人肝母细胞瘤HepG2细胞、人肝癌Hep3B细胞的增殖,并且能使大部分HepG2和Hep3B细胞株产生凋亡[12];山豆根颗粒与饮片被证实可以提高荷瘤小鼠血清中白细胞介素-2、干扰素-γ及肿瘤坏死因子-α等细胞因子含量,进而抑制肿瘤生长[9];山豆根非生物碱成分也能显著保护免疫性肝损伤[38]。但是,山豆根抗肝癌的药效学及作用机制研究只涉及到山豆根提取物,对山豆根抗肝癌作用的药效物质基础及其作用靶点尚未阐明。
目前,山豆根的化学成分主要通过NMR、IR、UV、柱色谱、高效液相色谱(HPLC)、X射线单晶衍射和圆二色谱(CD)进行鉴定,分离过程复杂且耗时[39]。而中药的化学成分多样,全面了解化学成分的组成有助于阐明中药药效物质基础及作用机制。近年来,UPLC-Q-TOF/MS可以对复杂组分进行高效、快速的分析,其提供了丰富的二级质谱信息,可以实现中药化学成分的快速分离和鉴定。采用UPLC-Q-TOF/MS技术鉴定山豆根化学成分可以避免复杂、繁琐耗时的分离纯化工作,提高定性分析的效率和准确性,实现对山豆根成分的鉴定,为山豆根的进一步开发利用、质量控制和药效物质基础研究奠定了基础。
因此,本研究首先利用UPLC-Q-TOF/MS结合UNIFI软件对山豆根成分进行了快速鉴定,共鉴定出23个化合物。包括吡啶类生物碱9个,异黄酮类化合物3个,二氢黄酮类化合物4个,二氢异黄酮类化合物2个,黄酮醇类化合物1个,苯并呋喃类2个,蒽醌类1个,木脂素类1个。运用网络药理学方法进行研究,获得了包括三叶豆紫檀苷、氧化苦参碱、苦参碱在内的23个有效成分,并发现其主要作用于AKT1、ERBB2、CCND1、EGFR、ESR1等33个核心靶点,通过调节HIF-1信号通路、AGE-RAGE信号通路、PI3K/AKT信号通路、ErbB信号通路等多条通路发挥抗肝癌作用。细胞活性实验中不同浓度的三叶豆紫檀苷、氧化苦参碱、苦参碱均能抑制HepG2细胞的增殖,说明三叶豆紫檀苷、氧化苦参碱、苦参碱具有不同程度的抗肝癌作用,且三叶豆紫檀苷的抗肝癌作用更显著,与网络药理学结果一致,表明了山豆根的潜在活性成分具有抗肝癌作用。
研究发现,苦参碱作用于以诱导糖酵解调节磷酸酶(TP53)、血管内皮生长因子A(VEGFA)及CCND1等多靶点,通过体内外实验同时验证了苦参碱通过调节细胞凋亡、线粒体稳态等多条通路,从而起到抑制肝癌的作用[40];苦参碱和氧化苦参碱通过抑制蛋白激酶B(AKT)磷酸化,阻滞AKT/GSK3β/β-catenin信号通路,诱导癌细胞凋亡;或阻滞PI3K/AKT通路,上调PTEN表达,从而使p21、p27、p53细胞周期负性调控因子表达上调,下调细胞周期相关蛋白表达,进而抑制细胞增殖[41]。而Wighteone能抑制EGFR信号通路,诱导细胞凋亡,抑制细胞增殖[42];三叶豆紫檀苷能够激活EGFR-MAPK信号通路,通过体内外实验表明三叶豆紫檀苷可能在癌症治疗中有治疗应用[43]。
此外,AKT1作为一种苏氨酸蛋白激酶,能够激活PI3K/AKT信号通路,促进肝癌细胞的增殖、迁移和侵袭[44]。ERBB2基因也称HER2基因,可以调节细胞生长、增殖、分化和凋亡[45]。ERBB2基因可能激活PI3K/AKT信号通路,抑制肝癌HepG2细胞的生长。而PI3K/AKT通路与各种人类恶性肿瘤生物过程有关,具有调节肿瘤细胞的葡萄糖代谢、增殖及凋亡的作用,其中AKT还能通过调节细胞周期来调节细胞增殖[46]。相关研究表明,CCND1作为一种细胞周期调节蛋白,不仅能调节细胞周期蛋白依赖性激酶,而且能参与G1期向S期的细胞周期转化。因此CCND1可以调节肝癌细胞的细胞周期,促进肝癌细胞的侵袭转移、肝癌干细胞干性维持等[47]。抑制表皮生长因子受体(EGFR)是原癌基因C-erbB-1的表达产物,EGFR的高表达与肿瘤的发生发展密切关系[48]。ESR1是一种类固醇受体,一旦突变,ESR1在原发性恶性肿瘤转移中被激活,抑制ESR1基因活化可用于抗癌;而在人类肝癌样本中ESR1 mRNA表达上调,下调ESR1 mRNA表达对肝癌具有治疗作用[49]。HIF作为转录因子,不仅可以通过转录激活VEGF、下调ENT中的E-钙黏蛋白进而影响肿瘤细胞[50],而且HIF是抑制病毒性肝炎的重要治疗靶点,也可以被乙肝病毒(HBV)激活,是发生肝癌的主要原因之一。
综上所述,本研究在对山豆根化学成分鉴定分析的基础上,利用网络药理学方法对山豆根23种化学成分的33个潜在抗肝癌靶点进行了分析,发现山豆根可能通过HIF-1信号通路、PI3K/AKT信号通路等多条通路抑制肝癌细胞的增殖、促进肝癌细胞的凋亡来发挥抗肝癌作用,通过分子对接技术以及细胞活性实验进行了进一步验证,为进一步明确山豆根抗肝癌的作用机制及临床应用提供了理论依据和研究方向。本研究存在一定的局限性,由于流动相洗脱程序中有机相比例较高,响应较好的峰大多为极性较低的成分,如脂肪酸等,因此未能鉴定出这部分峰代表的化合物。此外,通过细胞实验对预测的活性成分进行了初步验证,后续研究中将进一步验证网络药理学推测的作用靶点,明确活性成分与关键靶点的关系,从而为山豆根抗肝癌的基础研究和临床应用提供更加充分、完善的思路。
| [1] |
中华人民共和国国家卫生健康委员会医政医管局. 原发性肝癌诊疗规范2019年版[J]. 临床肝胆病杂志, 2020, 36(2): 277-292. Bureau of Medical Administration, National Health Commission of the People's Republic of China. Guidelines for diagnosis and treatment of primary liver cancer in China (2019 edition)[J]. Journal of Clinical Hepatology, 2020, 36(2): 277-292. DOI:10.3969/j.issn.1001-5256.2020.02.007 |
| [2] |
KUMADA T, TOYODA H, TADA T, et al. High-sensitivity Lens culinaris agglutinin-reactive alpha-fetoprotein assay predicts early detection of hepatocellular carcinoma[J]. Journal of Gastroenterology, 2014, 49(3): 555-563. DOI:10.1007/s00535-013-0883-1 |
| [3] |
TANG L S, CHEN R G, XU X. Synthetic lethality: a promising therapeutic strategy for hepatocellular carcinoma[J]. Cancer Letters, 2020, 476: 120-128. DOI:10.1016/j.canlet.2020.02.016 |
| [4] |
胡泽玉, 杨清瑞, 周铖, 等. 肝癌化疗耐药机制及中药干预研究进展[J]. 中国实验方剂学杂志, 2022, 28(14): 254-261. HU Z Y, YANG Q R, ZHOU C, et al. Mechanism of chemotherapy resistance of hepatocellular carcinoma and intervention with Chinese medicine: a review[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2022, 28(14): 254-261. DOI:10.13422/j.cnki.syfjx.20220923 |
| [5] |
邱文亮, 孙倩倩, 邱冰. 中药及其活性成分在肝癌治疗中的作用机制研究进展[J]. 中医药信息, 2022, 39(5): 79-84. QIU W L, SUN Q Q, QIU B. Action mechanism progress of Chinese medicinal and its active ingredients in treatment of hepatic carcinoma[J]. Information on Traditional Chinese Medicine, 2022, 39(5): 79-84. |
| [6] |
戚益铭, 吴霜霜, 沈敏鹤, 等. 中医药治疗原发性肝癌研究述评[J]. 中医学报, 2015, 30(1): 14-16. QI Y M, WU S S, SHEN M H, et al. General situation of traditional Chinese medicine treatment of primary liver cancer[J]. China Journal of Chinese Medicine, 2015, 30(1): 14-16. DOI:10.16368/j.issn.1674-8999.2015.01.005 |
| [7] |
牛玉清, 杨冰, 王丽, 等. 抗肝癌中药作用机制研究进展[J]. 中医肿瘤学杂志, 2021, 3(6): 88-96. NIU Y Q, YANG B, WANG L, et al. Advances in the mechanism of anti-hepatoma effect of Chinese medicine[J]. Journal of Oncology in Chinese Medicine, 2021, 3(6): 88-96. DOI:10.19811/j.cnki.ISSN2096-6628.2021.06.013 |
| [8] |
曹洛云, 李天娇, 孟宪生, 等. 山豆根生物碱对DEN诱发肝癌大鼠的作用及机制研究[J]. 中国现代应用药学, 2018, 35(3): 370-374. CAO L Y, LI T J, MENG X S, et al. Study on the efficacy and mechanism of liver cancer induced by DEN in rats of alkaloids of Sophorae Tonkinensis radix et rhizoma[J]. Chinese Journal of Modern Applied Pharmacy, 2018, 35(3): 370-374. DOI:10.13748/j.cnki.issn1007-7693.2018.03.013 |
| [9] |
彭百承, 黄健, 李萍, 等. 山豆根颗粒及其饮片抗肿瘤作用及其机制[J]. 中国实验方剂学杂志, 2014, 20(23): 190-193. PENG B C, HUANG J, LI P, et al. Studies on antitumor effect and mechanisms of Sophora tonkinensis and its granules[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2014, 20(23): 190-193. DOI:10.13422/j.cnki.syfjx.2014230190 |
| [10] |
姚仲青, 朱虹, 王光凤. 山豆根总生物碱抗肿瘤作用的初步研究[J]. 南京中医药大学学报, 2005, 21(4): 253-254. YAO Z Q, ZHU H, WANG G F. Anti -tumor effect of total alkaloids of Radix sophorue tonldnensis[J]. Journal of Nanjing University of Traditional Chinese Medicine, 2005, 21(4): 253-254. DOI:10.3969/j.issn.1000-5005.2005.04.018 |
| [11] |
肖正明, 宋景贵, 徐朝晖, 等. 山豆根水提物对体外培养人肝癌细胞增殖及代谢的影响[J]. 山东中医药大学学报, 2000, 24(1): 62-64. XIAO Z M, SONG J G, XU Z H, et al. Effects of the sscc extracts on proliferation and mitochondria metabolism of human hepatoma smmc-7721 cells[J]. Journal of Shandong University of Traditional Chinese Medicine, 2000, 24(1): 62-64. |
| [12] |
CHUI C H, LAU F Y, TANG J C, et al. Activities of fresh juice of Scutellaria barbata and warmed water extract of Radix Sophorae Tonkinensis on anti-proliferation and apoptosis of human cancer cell lines[J]. International Journal of Molecular Medicine, 2005, 16(2): 337-341. |
| [13] |
张杨, 冯宝民, 卢轩. UPLC/Q-TOF-MS联用技术在药物分析中的应用进展[J]. 天然产物研究与开发, 2017, 29(11): 1992-1996. ZHANG Y, FENG B M, LU X. Research progress on application of UPLC/Q-TOF-MS in pharmaceutical analysis[J]. Natural Product Research and Development, 2017, 29(11): 1992-1996. |
| [14] |
GENG Z, LIU Y F, GOU Y, et al. Metabolomics study of cultivated Bulbus fritillariae cirrhosae at different growth stages using UHPLC-QTOF-MS coupled with multivariate data analysis[J]. Phytochemical Analysis: PCA, 2018, 29(3): 290-299. DOI:10.1002/pca.2742 |
| [15] |
YANG S S, SHAN L L, LUO H M, et al. Rapid classification and identification of chemical components of Schisandra chinensis by UPLC-Q-TOF/MS combined with data post-processing[J]. Molecules, 2017, 22(10): 1778. DOI:10.3390/molecules22101778 |
| [16] |
ZHOU Y, XU G, CHOI F F K, et al. Qualitative and quantitative analysis of diterpenoids in Salvia species by liquid chromatography coupled with electrospray ionization quadrupole time-of-flight tandem mass spectrometry[J]. Journal of Chromatography A, 2009, 1216(24): 4847-4858. DOI:10.1016/j.chroma.2009.04.017 |
| [17] |
GAO L, WANG X D, NIU Y Y, et al. Molecular targets of Chinese herbs: a clinical study of hepatoma based on network pharmacology[J]. Scientific Reports, 2016, 6: 24944. DOI:10.1038/srep24944 |
| [18] |
GUO Q Q, ZHENG K, FAN D P, et al. Wu-Tou Decoction in rheumatoid arthritis: integrating network pharmacology and in vivo pharmacological evaluation[J]. Frontiers in Pharmacology, 2017, 8: 230. |
| [19] |
MAO Y, HAO J, JIN Z Q, et al. Network pharmacology-based and clinically relevant prediction of the active ingredients and potential targets of Chinese herbs in metastatic breast cancer patients[J]. Oncotarget, 2017, 8(16): 27007-27021. |
| [20] |
WU C, HE L J, YI X, et al. Three new alkaloids from the roots of Sophora tonkinensis[J]. Journal of Natural Medicines, 2019, 73(3): 667-671. |
| [21] |
JIN X, LU Y, CHEN S X, et al. UPLC-MS identification and anticomplement activity of the metabolites of Sophora tonkinensis flavonoids treated with human intestinal bacteria[J]. Journal of Pharmaceutical and Biomedical Analysis, 2020, 184: 113176. |
| [22] |
程钱. 山豆根指纹图谱、含量测定及成分分析研究[D]. 北京: 北京中医药大学, 2017. CHENG Q. Study on fingerprint, content determination and composition analysis of Sophora Tonkinensis[D]. Beijing: Beijing University of Chinese Medicine, 2017. |
| [23] |
周思雨, 陈金鹏, 刘志东, 等. 山豆根的化学成分和药理作用的研究进展[J]. 中草药, 2021, 52(5): 1510-1521. ZHOU S Y, CHEN J P, LIU Z D, et al. Research progress on chemical constituents and pharmacological effects of Sophorae Tonkinensis radix et Rhizoma[J]. Chinese Traditional and Herbal Drugs, 2021, 52(5): 1510-1521. |
| [24] |
LI S. Network pharmacology evaluation method guidance-draft[J]. World Journal of Traditional Chinese Medicine, 2021, 7(1): 148. |
| [25] |
LI S, ZHANG B. Traditional Chinese medicine network pharmacology: theory, methodology and application[J]. Chinese Journal of Natural Medicines, 2013, 11(2): 110-120. |
| [26] |
赵凤春. 苦参不同部位化学成分及含量差异研究[D]. 北京: 中国中医科学院, 2015. ZHAO F C. Simultaneous analysis of chemical components and contents in various organs of Sophora flavescens ait[D]. Beijing: China Academy of Chinese Medical Sciences, 2015. |
| [27] |
赵琴琴, 张玉峰, 范骁辉. 高效液相色谱多级质谱联用法同时鉴定苦参中的两大类活性成分[J]. 中国中药杂志, 2011, 36(6): 762-769. ZHAO Q Q, ZHANG Y F, FAN X H. Simultaneous characterization of two types of major active components in Kushen by high performance liquid chromatography coupled to multi-stage mass spectrometry[J]. China Journal of Chinese Materia Medica, 2011, 36(6): 762-769. |
| [28] |
宿美凤, 雒晓梅, 王小明, 等. 基于UHPLC-MS/MS苦参实定性定量及其入血成分分析[J]. 中草药, 2019, 50(9): 2041-2048. SU M F, LUO X M, WANG X M, et al. Qualitative and quantitative determination of Sophora flavescens seeds and analysis of its blood components based on UHPLC-MS/MS[J]. Chinese Traditional and Herbal Drugs, 2019, 50(9): 2041-2048. |
| [29] |
李晓娜, 董馨, 包保全, 等. 基于Q-Exactive高分辨质谱的蒙中药材苦参化学成分的快速分析鉴定[J]. 中药材, 2019, 42(1): 103-109. LI X N, DONG X, BAO B Q, et al. Rapid analysis and identification of chemical constituents of Mongolian traditional Chinese medicine Sophora flavescens based on Q-Exactive high resolution mass spectrometry[J]. Journal of Chinese Medicinal Materials, 2019, 42(1): 103-109. |
| [30] |
潘其明. 山豆根化学成分及生物活性的研究[D]. 桂林: 广西师范大学, 2016. PAN Q M. Studies on the chemical constituents of the rhizomes of Sophora tonkinensis and their bioactivities[D]. Guilin: Guangxi Normal University, 2016. |
| [31] |
郭智. 基于UPLC-ESI-QTof的山豆根、苦参化学成分比较及柴胡不同提取方法柴胡皂苷a、d变化的研究[D]. 北京: 北京协和医学院, 2014. GUO Z. Studies on chemical constituents of S. Tonkinensis and S. flavescens, and transformation of saikosaponin A, D in different extracting method by using UPLC-ESI-QTof[D]. Beijing: Peking Union Medical College, 2014. |
| [32] |
WENG Z B, ZENG F, ZHU Z H, et al. Comparative analysis of sixteen flavonoids from different parts of Sophora flavescens Ait. by ultra high-performance liquid chromatography-tandem mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2018, 156: 214-220. |
| [33] |
何常明. 苦参和山豆根黄酮类成分及其生物活性的比较研究[D]. 上海: 复旦大学, 2010. HE C M. Comparative studies on flavonoids and their bioactivities of Sophora flavescens and S. Tonkinensis[D]. Shanghai: Fudan University, 2010. |
| [34] |
王学浩, 周浩明. 中国肝癌外科70年[J]. 中国肿瘤外科杂志, 2019, 11(4): 229-232. WANG X H, ZHOU H M. 70 years of hepatocellular carcinoma surgery in China[J]. Chinese Journal of Surgical Oncology, 2019, 11(4): 229-232. |
| [35] |
万赤丹, 王国斌. 原发性肝癌治疗进展[J]. 腹部外科, 2019, 32(1): 1-6, 22. WAN C D, WANG G B. Advances in treatments for primary liver cancer[J]. Journal of Abdominal Surgery, 2019, 32(1): 1-6, 22. |
| [36] |
陈勇, 覃乐, 叶晓雪, 等. 细胞焦亡与肝脏疾病的相关性及中医药研究进展[J]. 中国实验方剂学杂志, 2021, 27(21): 232-241. CHEN Y, QIN L, YE X X, et al. Correlation and traditional Chinese medicine intervention of pyroptosis and liver diseases[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2021, 27(21): 232-241. |
| [37] |
邓哲, 欧阳昭广, 龙红萍, 等. 基于UPLC-Q-TOF-MS分析下瘀血汤活性成分及其抗肝癌作用机制网络药理学研究[J]. 中国中医药信息杂志, 2022, 29(8): 9-17. DENG Z, OUYANG Z G, LONG H P, et al. Study on active components of Xiayuxue Decoction and network pharmacology of its anti-liver cancer mechanism based on UPLC-Q-TOF-MS analysis[J]. Chinese Journal of Information on Traditional Chinese Medicine, 2022, 29(8): 9-17. |
| [38] |
周明眉, 范自全, 赵爱华, 等. 山豆根非生物碱部位对免疫性肝损伤模型小鼠的影响[J]. 时珍国医国药, 2011, 22(11): 2709-2710. ZHOU M M, FAN Z Q, ZHAO A H, et al. Effect of non-alkaloid fraction of Sophora Tonkinensis on immune liver injury model mice[J]. Lishizhen Medicine and Materia Medica Research, 2011, 22(11): 2709-2710. |
| [39] |
HE L J, LIU J S, LUO D, et al. Quinolizidine alkaloids from Sophora tonkinensis and their anti-inflammatory activities[J]. Fitoterapia, 2019, 139: 104391. |
| [40] |
曹建, 朱晓燃, 杨振寰, 等. 基于网络药理学探讨清肝化瘀颗粒治疗肝癌的作用机制[J]. 中草药, 2021, 52(7): 2039-2052. CAO J, ZHU X R, YANG Z H, et al. An exploration on mechanisms of Qinggan Huayu Granule in treating liver cancer based on network pharmacology[J]. Chinese Traditional and Herbal Drugs, 2021, 52(7): 2039-2052. |
| [41] |
张明发, 沈雅琴. 苦参碱和氧化苦参碱抗大肠癌药理作用研究进展[J]. 药物评价研究, 2020, 43(6): 1189-1196. ZHANG M F, SHEN Y Q. Research advances in pharmacologic effects of matrine and oxymatrine against large intestine carcinoma[J]. Drug Evaluation Research, 2020, 43(6): 1189-1196. |
| [42] |
SUN P Y, QU Y N, WANG Y N, et al. Wighteone exhibits an antitumor effect against EGFR L858R/T790M mutation non-small cell lung cancer[J]. Journal of Cancer, 2021, 12(13): 3900-3908. |
| [43] |
LU X G, MA J X, QIU H F, et al. Anti-proliferation effects of trifolirhizin on MKN45 cells and possible mechanism[J]. Oncology Reports, 2016, 36(5): 2785-2792. |
| [44] |
邝玉慧, 徐方飚, 陈晓琦, 等. 基于计算机虚拟筛选研究菝葜抗肝癌的作用机制[J]. 中医学报, 2021, 36(8): 1751-1757. KUANG Y H, XU F B, CHEN X Q, et al. Study of anti-liver cancer mechanism of Baqia(Smilax China L.) based on computer virtual screening[J]. Acta Chinese Medicine, 2021, 36(8): 1751-1757. |
| [45] |
GROENENDIJK F H, JONG J D, FRANSEN V D P E E, et al. ERBB2 mutations characterize a subgroup of muscle-invasive bladder cancers with excellent response to neoadjuvant chemotherapy[J]. European Urology, 2016, 69(3): 384-388. |
| [46] |
吴雨蒙, 王莹, 吴琪, 等. 二仙汤对过氧化氢诱导的成骨细胞蛋白组学及PI3K信号通路的影响[J]. 中国中药杂志, 2021, 46(15): 3934-3942. WU Y M, WANG Y, WU Q, et al. Effect of Erxian Decoction on proteomics and PI3K signaling pathway of osteoblasts stimulated by H2O2[J]. China Journal of Chinese Materia Medica, 2021, 46(15): 3934-3942. |
| [47] |
GENNARO V J, STANEK T J, PECK A R, et al. Control of CCND1 ubiquitylation by the catalytic SAGA subunit USP22 is essential for cell cycle progression through G1 in cancer cells[J]. Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(40): E9298-E9307. |
| [48] |
BENKHEIL M, PAESHUYSE J, NEYTS J, et al. HCV-induced EGFR-ERK signaling promotes a pro-inflammatory and pro-angiogenic signature contributing to liver cancer pathogenesis[J]. Biochemical Pharmacology, 2018, 155: 305-315. |
| [49] |
ZHAO F L, QIN J R, LIANG Y J, et al. Exploring anti-liver cancer targets and mechanisms of oxyresveratrol: in silico and verified findings[J]. Bioengineered, 2021, 12(2): 9939-9948. |
| [50] |
JU C, COLGAN S P, ELTZSCHIG H K. Hypoxia-inducible factors as molecular targets for liver diseases[J]. Journal of Molecular Medicine, 2016, 94(6): 613-627. |
2. Shandong Guangtongbao Pharmaceuticals Co., Ltd., Qingzhou 262500, China;
3. Mass Spectrometry Application Center, Tianjin Medical Mass Spectrometry Precision Diagnosis Enterprise Key Laboratory, Tianjin 301617, China;
4. Ningbo Huamei Hospital, University of Chinese Academy of Sciences, Ningbo 315010, China
 2023, Vol. 40
2023, Vol. 40