文章信息
- 解天, 姚广哲, 晏一淇, 王益民
- XIE Tian, YAO Guangzhe, YAN Yiqi, WANG Yimin
- 气质联用检测不同提取方法对泽泻挥发性成分的影响研究
- Investigation of the effects of different extraction methods on volatile compounds of Alismatis Rhizoma using temperament combination assay
- 天津中医药, 2023, 40(3): 389-394
- Tianjin Journal of Traditional Chinese Medicine, 2023, 40(3): 389-394
- http://dx.doi.org/10.11656/j.issn.1672-1519.2023.03.18
-
文章历史
- 收稿日期: 2023-01-04
泽泻始载于《神农本草经》,乃本经上品[1],为泽泻科多年生水生或沼生草本植物,2020年版《中国药典》收载泽泻Alismatis Rhizoma来源于泽泻科植物东方泽泻Alisma orientale(Sam.)Juzep.或泽泻Alisma plantago-aquatica Linn.的干燥块茎,其性寒味甘、淡,归肾、膀胱经。具有利水渗湿,泄热,化浊降脂等功效,主治小便不利,水肿胀满,泄泻尿少,痰饮眩晕,热淋涩痛,高脂血症[2]。
目前国内多采用超高效液相色谱(UPLC)法对泽泻进行质量研究[3],且集中针对泽泻三萜类成分进行研究分析,但各种成分的相对含量会随生长环境、采收季节、贮藏及加工方法的不同而产生差异[4],因此单一的指标性成分的含量并不能全面反映出药材的质量和效价。本实验分别采用水蒸气蒸馏法和顶空进样法从泽泻中提取挥发油,并采用气相色谱-质谱(GC-MS)的分析方法对两种不同提取方法获得的泽泻挥发性成分进行定性分析与比较,为完善泽泻药材质量评价及研究和开发泽泻挥发性成分提供参考依据。
1 材料与方法 1.1 材料与仪器仪器:气质联用仪(型号:GCMS-QP2010 Ultra,日本Shimadzu公司);GCMSsolution工作站(日本Shimadzu公司);千分之一天平(型号:JA5003,天津天马衡基公司);Milli-Q超纯水制备仪(Millipore公司);旋涡混合器(型号:G3KT18273,Thermo Fisher Scientific公司);高速台式冷冻离心机(型号:TGL-16,cence公司);超声波清洗机(型号:CN6-180,宁波新芝生物科技公司)。
试剂:正己烷(色谱纯)购自上海阿拉丁生化科技股份有限公司。
药材:经天津中医药大学李天祥教授鉴定其基原为泽泻科植物泽泻Alisma plantago-aquatica Linn.的干燥块茎。药材经粉碎后,过2号筛,保存于天津中医药大学中医药研究院。
1.2 实验方法 1.2.1 挥发性成分的提取水蒸气蒸馏法:精密称取300 g粉碎的泽泻药材,置烧瓶中,加水2 400 mL与数粒玻璃珠,振摇混合后,连接挥发油测定器与回流冷凝管。自冷凝管上端加水使充满挥发油测定器的刻度部分,并溢流入烧瓶时为止。置电热套中缓缓加热至沸,并保持微沸6 h,至测定器中油量不再增加。用吸管将挥发油移至1.5 mL离心管中,以无水硫酸钠干燥,得到深绿色油状液体。取1 μL所得到的挥发油置于5 mL容量瓶,加正己烷定容至刻度,涡旋混匀即得,4 ℃冰箱储存备用。
顶空进样:精密称取2.0 g泽泻粉末(过2号筛),置于20 mL顶空瓶中密封,放入顶空进样器中按顶空进样条件进样。顶空进样条件:样品平衡温度100 ℃,平衡时间20 min,定量管温度120 ℃,传输线温度140 ℃,载气为高纯氦气,加压时间0.1 min,进样时间1 min。
1.2.2 GC-MS分析条件色谱条件:HP-5 MS毛细管色谱柱(30 m×0.25 mm×0.25 μm);载气为高纯氦气,柱体积流量为1.0 mL/min。升温程序:50~200 ℃,50 ℃保持2 min,以6 ℃/min升温至120℃;以3 ℃/min升温至160 ℃;以5 ℃/min升温至200 ℃保持2 min。进样方式:分流进样,分流比为5∶1;进样量:1 μL;进样口温度:250 ℃;总分离时间37 min。
质谱条件:电子轰击离子源(EI),采用Scan监测模式进行扫描,离子源温度:230 ℃;接口温度:250 ℃;扫描范围:30~500 m/z;溶剂延迟时间:3.0 min。
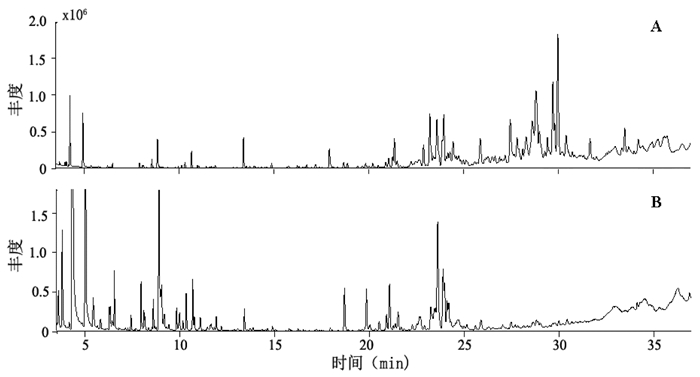
2 实验结果 2.1 泽泻挥发性成分鉴定参照实验设定的条件,对泽泻挥发油进行GC-MS分析,其GC-MS总离子流图见图 1。以峰面积归一化法计算泽泻挥发油各组分的相对含量。
|
| 注:A.水蒸气蒸馏提取;B.顶空进样提取。 图 1 泽泻挥发性成分GC-MS总离子流图 Fig. 1 GC-MS total ion chromatogram of Alismatis Rhizoma volatile components |
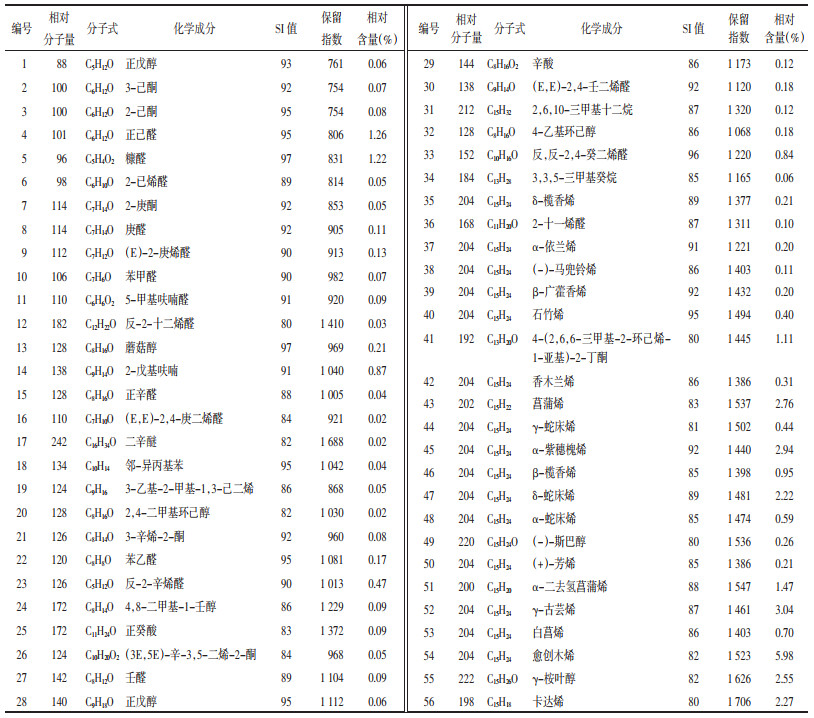
在NIST MS谱库进行检索,人工谱图解析,可知水蒸气蒸馏法从泽泻挥发油中共鉴定出56种化合物,占挥发性成分总相对含量的36.89%,其中相对含量大于2%的组分有7种,分别为愈创木烯(5.98%)、γ-古芸烯(3.04%)、α-紫穗槐烯(2.94%)、菖蒲烯(2.76%)、γ-桉叶醇(2.55%)、卡达烯(2.27%)、δ-蛇床烯(2.22%)。见表 1。
|
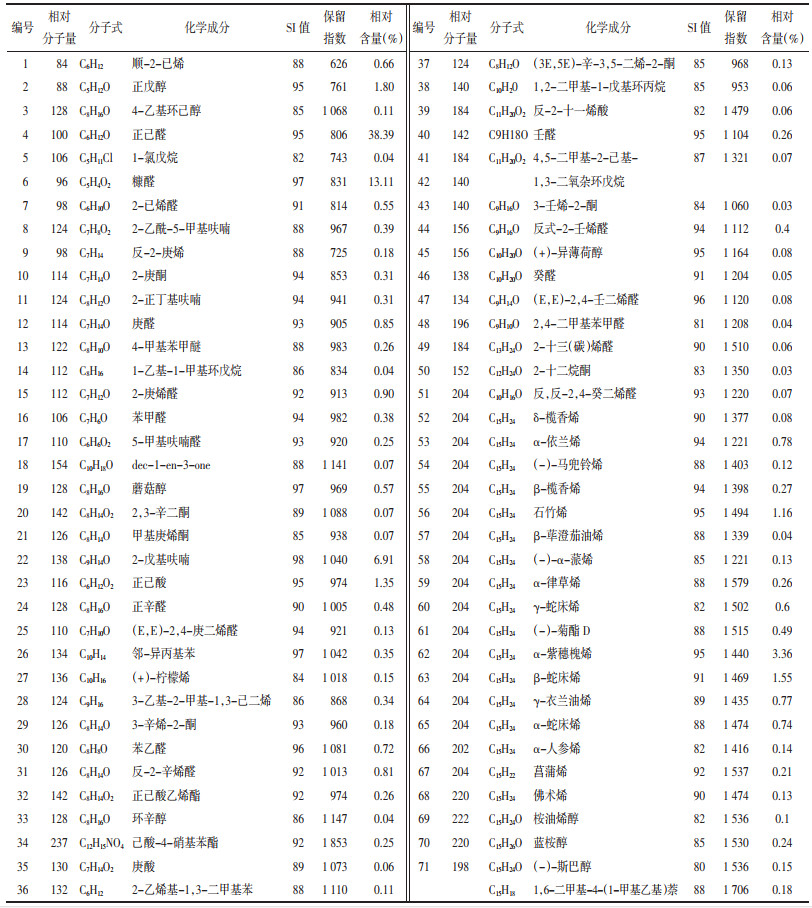
通过谱库检索,人工谱图解析,可知采用顶空进样法从泽泻挥发油中共鉴定出71种化合物,占挥发性成分总含量的84.5%,其中相对含量大于2%的组分有4种,分别为正己醛(38.39%)、糠醛(13.11%)、2-戊基呋喃(6.91%)、α-紫穗槐烯(3.36%)。见表 2。
|
泽泻中主要含有三萜类化合物,其次为倍半萜和二萜类化合物,其他还有苯丙素、糖类、黄酮、生物碱及甾体等[5-6]。三萜类成分是泽泻发挥利水渗湿、促进水代谢[7]、降血糖血脂[8-9]及保肝[10]功效的主要药效物质基础。倍半萜类化合物同样是泽泻的重要成分,存在于泽泻挥发油中[11]。β-石竹烯是一类双环倍半萜型天然物质,研究表明其具有抗凋亡、抗炎和抗氧化的药理活性及改善脑缺血再灌注损伤的作用[12-13];β-榄香烯临床常应用于人肺癌、肝癌等恶性肿瘤的辅助治疗[14],其作用机理主要是通过诱导细胞凋亡、抑制肿瘤细胞增殖迁移和调节机体免疫功能等来发挥作用[15]。泽泻的免疫调节作用可能与此类物质有关。
3.2 泽泻挥发性成分提取方式查阅文献可知泽泻挥发性成分研究的提取方法常用的有水蒸气蒸馏法[16]、超临界CO2流体萃取法[17]等。水蒸气蒸馏法是传统的挥发油提取方法,虽然操作简便且成本较低,但需要药材量较大且提取时间较长[18];超临界CO2萃取技术由于受到仪器设备条件的限制,目前尚不能推广使用[19];与这些方法相比,顶空进样可在一定时间内使挥发性成分从药材中挥发后直接进样,减少了提取挥发油所需要的萃取等步骤,具有节省药材、操作便捷且无溶剂残留等优点[20-21],但由于加热温度较低并且时间较短,可能导致挥发性成分提取不够充分。
3.3 水蒸气蒸馏法所得的泽泻挥发性化学成分水蒸气蒸馏法检测到的化合物包含倍半萜烯类、醇类、醚类、酮类、醛类和其他类化合物,其中相对含量最高的是高沸点的倍半萜烯类成分。由于水蒸气蒸馏法得到的是挥发油,且提取过程时间较长,加热温度较高,因此适用于具有挥发性,能随水蒸气蒸馏而不被破坏成分的提取,可将分子量较大、沸点高且热稳定性较好的组分提取出来[22]。
3.4 顶空进样法所得的泽泻挥发性化学成分顶空进样法检测到的化合物包含醛类、杂环类、萜烯类、烷烃类、醇类、醚类、酮类、酯类、羧酸类和其它类化合物,其中相对含量最高的是醛类成分。顶空进样法直接由药材在进样器中得到气体直接进行检测,减少了水蒸气蒸馏法中的冷藏、除水等中间步骤,没有外部环境对样品的可能作用,同时加热时间较短,提取温度较低,可以降低一些化学成分在加热过程中分解与转化的可能性,专一性收集样品中易挥发性成分[23-24]。同样由于提取温度低,富集到的物质主要是低沸点的萜类、醛酮类和弱极性的烃类。
3.5 不同提取方法所得的相同泽泻挥发性化学成分比较2种方法结合共鉴定出94种化合物,其中有33种相同的化合物(正戊醇、正己醛、糠醛、2-已烯醛、2-庚酮、庚醛、苯甲醛、5-甲基呋喃醛、蘑菇醇、2-戊基呋喃、正辛醛、(E,E)-2,4-庚二烯醛、邻-异丙基苯、3-Ethyl-2-methyl-1,3-hexadiene、3-辛烯-2-酮、苯乙醛、反-2-辛烯醛、3,5-octadienone,3,5-Octadien-2-one、壬醛、反式-2-壬烯醛、(E,E)-2,4-壬二烯醛、4-乙基环己醇、反,反-2,4-癸二烯醛、δ-榄香烯、α-依兰烯、(-)-马兜铃烯、石竹烯、菖莆烯、γ-蛇床烯、α-紫穗槐烯、β-榄香烯、α-蛇床烯、(-)-斯巴醇),这些共有化合物占水蒸气蒸馏法提取的挥发油总含量的15.9%,占顶空进样法提取的挥发油总含量的74.65%。
通过实验可知,由于泽泻挥发性成分提取方式及原理的不同,虽然顶空进样法提取到的化合物数量较水蒸气蒸馏法多,但是两者提取方法得到的化合物种类和含量均有差异,各有侧重。因此在采用GC-MS对泽泻挥发性成分进行分析时,可采用两种方法互为补充,将两种提取方法获得的GC-MS分析结果相结合,可更加全面地研究泽泻的挥发性成分。
| [1] |
许泽煌, 周楚, 阮诗玮. 泽泻古今考[J]. 中医药通报, 2021, 20(4): 36-38. XU Z H, ZHOU C, RUAN S W. Ancient and modern study of rhizoma alismatis[J]. Traditional Chinese Medicine Journal, 2021, 20(4): 36-38. |
| [2] |
国家药典委员会. 中华人民共和国药典[S]. 北京: 中国医药科技出版社, 2020: 239-240. Chinese Pharmacopoeia Commission. Pharmacopoeia of people's republic of China[S]. Beijing: China Medical Science Press, 2020: 239-240. |
| [3] |
吴双双, 孙凤灵, 秦霞, 等. UPLC-MS联用同时测定建泽泻中8种三萜类化学成分[J]. 中国民族民间医药, 2022, 31(4): 43-47. WU S S, SUN F L, QIN X, et al. Simultaneous determination of eight triterpenoids in Alisma orientalis by UPLC-MS[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy, 2022, 31(4): 43-47. |
| [4] |
李兰. 中药泽泻采收加工和贮藏养护技术研究[D]. 南京: 南京中医药大学, 2009. LI L. Studies on elaboration of collecting period and storge technique of rhizoma alismatis[D]. Nanjing: Nanjing University of Chinese Medicine, 2009. |
| [5] |
向茜, 赵文燕, 王蝉, 等. 基于UHPLC-MS/MS探究不同炮制方法对泽泻化学成分的影响[J]. 时珍国医国药, 2022, 33(9): 2154-2157. XIANG Q, ZHAO W Y, WANG C, et al. Effects of different processing methods on chemical components of Alisma orientalis based on UHPLC-MS/MS[J]. Lishizhen Medicine and Materia Medica Research, 2022, 33(9): 2154-2157. DOI:10.3969/j.issn.1008-0805.2022.09.28 |
| [6] |
刘珊珊, 郭杰, 李宗艾, 等. 泽泻化学成分及药理作用研究进展[J]. 中国中药杂志, 2020, 45(7): 1578-1595. LIU S S, GUO J, LI Z A, et al. Advances in studies on chemical compositions of Alismatis Rhizoma and their biological activities[J]. China Journal of Chinese Materia Medica, 2020, 45(7): 1578-1595. DOI:10.19540/j.cnki.cjcmm.20190616.201 |
| [7] |
TAO Y, JIANG E C, YAN J Z, et al. A biochemometrics strategy for tracing diuretic components of crude and processed Alisma orientale based on quantitative determination and pharmacological evaluation[J]. Biomedical Chromatography, 2020, 34(2): e4744. |
| [8] |
李小艳, 李雪君, 刘灿坤, 等. 泽泻三萜单体对3T3-L1脂肪细胞葡萄糖摄取活性的影响[J]. 福建中医药大学学报, 2014, 24(5): 31-33. LI X Y, LI X J, LIU C K, et al. Effects of triterpenes isolated from rhizoma alismatis on glucose uptake in 3T3-L1 cells[J]. Journal of Fujian University of Traditional Chinese Medicine, 2014, 24(5): 31-33. |
| [9] |
程志红, 萧伟, 王振中, 等. 泽泻调血脂活性成分及其药理和临床应用研究进展[J]. 中草药, 2015, 46(22): 3420-3426. CHENG Z H, XIAO W, WANG Z Z, et al. Research progress on hypolipidemic constituents in Alismatis Rhizoma and their pharmacology and clinical application[J]. Chinese Traditional and Herbal Drugs, 2015, 46(22): 3420-3426. |
| [10] |
ZHAO Z H, DENG Z T, HUANG S L, et al. Alisol B alleviates hepatocyte lipid accumulation and lipotoxicity via regulating RARα-PPARγ-CD36 cascade and attenuates non-alcoholic steatohepatitis in mice[J]. Nutrients, 2022, 14(12): 2411. DOI:10.3390/nu14122411 |
| [11] |
王雅琴, 吴伟铭, 丘志龙, 等. GC-MS分析成都产泽泻挥发油化学成分[J]. 亚太传统医药, 2022, 18(5): 52-56. WANG Y Q, WU W M, QIU Z L, et al. Analysis of chemical constituents of volatile oil from Alisma alismatis from Chengdu by GC-MS[J]. Asia-Pacific Traditional Medicine, 2022, 18(5): 52-56. |
| [12] |
左天睿. β-石竹烯通过激活HSF1/HSP70信号通路减轻大鼠脑缺血再灌注损伤研究[D]. 重庆: 重庆医科大学, 2022. ZUO T R. β-caryophyllene alleviates cerebral ischemia-reperfusion injury in rats by activating HSF1/HSP70 signaling pathway[D]. Chongqing: Chongqing Medical University, 2022. |
| [13] |
胡晴雯. β-石竹烯通过NRF2/HO-1调控铁死亡改善大鼠局灶性脑缺血再灌注损伤研究[D]. 重庆: 重庆医科大学, 2022. HU Q W. β-caryophyllene suppresses ferroptosis induced by cerebral ischemia reperfusion via activation of the NRF2/HO-1 signaling pathway in MCAO/R rats[D]. Chongqing: Chongqing Medical University, 2022. |
| [14] |
PAN Y H, WANG W, HUANG S, et al. Beta-elemene inhibits breast cancer metastasis through blocking pyruvate kinase M2 dimerization and nuclear translocation[J]. Journal of Cellular and Molecular Medicine, 2019, 23(10): 6846-6858. |
| [15] |
ZHAI B T, ZHANG N N, HAN X M, et al. Molecular targets of β-elemene, a herbal extract used in traditional Chinese medicine, and its potential role in cancer therapy: a review[J]. Biomedecine & Pharmacotherapie, 2019, 114: 108812. |
| [16] |
陈建忠, 李彧, 肖建平, 等. 药对泽泻—白术与其单味药挥发油成分的比较分析[J]. 福建中医药大学学报, 2012, 22(4): 43-46. CHEN J Z, LI Y, XIAO J P, et al. Comparative analysis of volatile oil components of Alisma orientalis-Atractylodes macrocephala and its single medicine[J]. Journal of Fujian University of Traditional Chinese Medicine, 2012, 22(4): 43-46. |
| [17] |
王雅琴, 丘志龙, 吴伟铭, 等. 成都产泽泻的超临界萃取及其GC-MS分析[J]. 海峡药学, 2022, 34(4): 31-37. WANG Y Q, QIU Z L, WU W M, et al. Supercritical extraction and GC-MS analysis of Alisma orientale from Chengdu[J]. Strait Pharmaceutical Journal, 2022, 34(4): 31-37. |
| [18] |
潘欢欢, 陈美君, 刘友平, 等. GC-MS结合保留指数分析不同方法提取的白术挥发性成分[J]. 中药与临床, 2017, 8(4): 21-23, 29. PAN H H, CHEN M J, LIU Y P, et al. Analysis of Baizhu volatile components extracted with different methods by GC-MS combing with Kovats Retention Index[J]. Pharmacy and Clinics of Chinese Materia Medica, 2017, 8(4): 21-23, 29. |
| [19] |
杨彬彬, 容蓉, 胡金芳, 等. 三种提取方法结合GC-MS分析比较草豆蔻的挥发性成分[J]. 中药材, 2014, 37(3): 443-447. YANG B B, RONG R, HU J F, et al. GC-MS analysis for volatile components from alpiniae katsumadai Semen by three extraction methods[J]. Journal of Chinese Medicinal Materials, 2014, 37(3): 443-447. |
| [20] |
王维, 贾晓华, 高梦园, 等. 水蒸气蒸馏与顶空进样GC-MS法分析细辛挥发性成分[J]. 天津中医药, 2021, 38(5): 654-658. WANG W, JIA X H, GAO M Y, et al. Analysis of volatile components in Asarum heterotropoides by steam distillation and headspace injection gas chromatography-mass spectrometry method[J]. Tianjin Journal of Traditional Chinese Medicine, 2021, 38(5): 654-658. DOI:10.11656/j.issn.1672-1519.2021.05.23 |
| [21] |
ZHANG Y, KANG L P, TENG Z Q, et al. Comparison of volatile constituents in two types of mugwort leaves (produced in Qichun and Nanyang) using the headspace GC-MS[J]. Journal of Acupuncture and Tuina Science, 2016, 14(3): 164-169. |
| [22] |
徐飞, 吴启南, 李兰, 等. 气质联用法分析泽泻中的挥发性成分的研究[J]. 南京中医药大学学报, 2011, 27(3): 277-280. XU F, WU Q N, LI L, et al. GC-MS analysis of volatile components in Alisma orientalis[J]. Journal of Nanjing University of Traditional Chinese Medicine, 2011, 27(3): 277-280. |
| [23] |
刘晓芬, 张颖, 胡明勋, 等. 川芎挥发性成分的水蒸气蒸馏提取与顶空进样GC-MS分析[J]. 中国民族民间医药, 2020, 29(1): 44-47, 51. LIU X F, ZHANG Y, HU M X, et al. Gas chromatography-mass spectrometry analysis for volatile compounds in Chuanxiong rhizoma by headspace injection and steam distillation[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy, 2020, 29(1): 44-47, 51. |
| [24] |
周严严, 巩丽丽, 孙国明, 等. 水蒸气蒸馏与顶空进样GC-MS分析北柴胡挥发性成分[J]. 食品与药品, 2013, 15(5): 332-334. ZHOU Y Y, GONG L L, SUN G M, et al. Steam distillation or headspace extraction coupled to gas chromatography-mass spectrometry for volatile composition analysis of Bupleurum chinense[J]. Food and Drug, 2013, 15(5): 332-334. |
 2023, Vol. 40
2023, Vol. 40