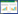文章信息
- 杨佩颖, 何佳颖, 张瑶, 等.
- YANG Peiying, HE Jiaying, ZHANG Yao, et al.
- 扶正解毒祛浊法方药联合EC化疗方案治疗广泛期小细胞肺癌患者的回顾性研究
- A retrospective study of Fuzheng Jiedu Quzhuo prescription combined with EC chemotherapy in patients with extensive-stage small cell lung cancer
- 天津中医药, 2024, 41(11): 1373-1378
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1373-1378
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.03
-
文章历史
- 收稿日期: 2024-08-10
2. 国家中医针灸临床医学研究中心, 天津 300381;
3. 天津中医药大学研究生院, 天津 301617
肺癌是世界范围内发病率第2、病死率第1的恶性肿瘤,其中约13%~15%为小细胞肺癌(SCLC),由于SCLC起病隐匿、增殖率极高、早期转移倾向强烈,约2/3的患者在首次诊断时即已属于广泛期,预后极差,5年生存率仅约2%[1-2]。过去30年间广泛期小细胞肺癌(ES-SCLC)的治疗发展缓慢,一线标准治疗方案仍以依托泊苷联合铂类为主,客观缓解率虽可达70%左右,但中位生存期仅约10个月,生存获益有限[3]。相关研究显示,肺癌患者对化疗的良好反应与患者血液中Th1细胞及其干扰素-γ(IFN-γ)含量增加和低水平的调节性T细胞(Treg)、Th2、Th17细胞相关,这表明化疗的疗效可能部分依赖于其免疫效应[4]。
近年来越来越多的证据表明中医药疗法可通过上调肿瘤微环境中的免疫应答发挥抗肿瘤作用[5]。Chen等[6]进行的1项系统评价和荟萃分析显示,中药联合EC方案化疗治疗小细胞肺癌在提高生活质量、延长生存时间和减少不良反应发生率方面优于单纯化疗组。扶正解毒祛浊法方药为贾英杰教授治疗肺癌的基础方,此方在临床应用中显示出了显著的疗效。基于此,本研究拟通过回顾性分析探究扶正解毒祛浊法方药联合化疗治疗ES-SCLC的临床疗效及可能的作用机制,为临床应用提供进一步支持。
1 资料与方法 1.1 资料来源本研究资料均来源于2022年1月1日—2023年6月30日于天津中医药大学第一附属医院肿瘤科住院治疗的ES-SCLC患者。所有患者均接受住院或电话随访,末次随访截止时间为2023年12月31日。本研究获得天津中医药大学第一附属医院伦理委员会的批准(伦理批件号TYLL2023[Z]字054)。
1.2 诊断标准1)由影像学和病理学检查确诊为SCLC。2)分期参考美国退伍军人肺癌协会(VALG)的二期分期法结合美国癌症联合委员会(AJCC)TNM分期系统分期为广泛期,广泛期定义为:AJCC(第8版)Ⅳ期,或T3~4由于肺部多发结节或肿瘤体积过大而不能被包含在一个可耐受的放疗计划中。
1.3 纳入标准1)符合上述诊断标准。2)PS 0-2,无局部症状且无脑转移,初次接受EC方案一线治疗且未接受放疗、免疫、靶向治疗的患者。3)符合实体瘤临床疗效评价标准,至少具有1处可测量病灶。
1.4 排除标准1)病历资料严重缺失者。2)合并其他恶性肿瘤、血液系统疾病、神经系统疾病、肺间质性疾病、肺部感染或其他感染性疾病。3)有影响口服药物吸收的因素(如呕吐、腹泻和肠梗阻)。
1.5 治疗方法对符合纳排标准的患者资料,根据是否联用扶正解毒祛浊法方药分为暴露组和非暴露组,第1周期治疗开始前记为治疗前,第4周期治疗结束后记为治疗后。非暴露组方案:单用EC方案化疗:依托泊苷100 mg/m2,静脉滴注,d1~3;卡铂药—时曲线下面积(AUC)=6,静脉滴注,d1,21 d为1个周期。暴露组方案:上述化疗第1天开始每周期联合扶正解毒祛浊法方药加减治疗≥14 d,扶正解毒祛浊法方药组成:瓜蒌30 g,芦根15 g,郁金10 g,姜黄10 g,猫爪草15 g,白花蛇舌草30 g,川芎15 g,黄芪30 g,枳壳15 g,半夏12 g,薏苡仁15 g,浙贝母30 g。
1.6 观察指标 1.6.1 无进展生存期观察并记录两组患者的无进展生存期(从入组开始到肿瘤出现进展或死亡之间的时间),截至随访结束时间病情未进展者或失访者记为删失数据。病情进展标准:依据实体瘤疗效评价标准(RECIST1.1)[7],基线病灶最大径之和至少增加20%或出现新发病灶。以影像学方法用来评价疗效,基线状态和随诊用同样的技术和方法进行病灶评估。
1.6.2 近期疗效评价依据实体瘤疗效评价标准(RECIST1.1)[7]评价疗效。完全缓解(CR):所有病灶消失维持4周;部分缓解(PR):病灶最大径之和减少≥30%,维持4周;稳定(SD):疗效评估在PD和PR之间;进展(PD):所有病灶半径总和增加≥20%,或出现新发病灶。疾病控制率(ORR)=(CR+PR)/总人数×100%。
1.6.3 淋巴细胞亚群和炎性细胞因子两组患者均统计第1周期治疗前1 d及第4周期化疗结束后1周内,清晨空腹肘静脉血中CD3+、CD4+T淋巴细胞、NK细胞、Treg细胞、IFN-γ、白细胞介素(IL)-4、IL-6、IL-10的血清水平。
1.6.4 中医证候评分参照《肺癌中医诊疗方案2021》[8]中的相关中医证候标准,结合ES-SCLC患者实际临床表现,制定中医证候分级量化评价标准,包括疲乏无力、食欲不振、恶心呕吐、咳嗽、咳痰、咯血、胸痛、气短、夜寐不安、便秘10个症状体征作为观察指标,根据临床观察将其分为无、轻、中、重4级,由无至重分别计为0、1、2、3分,观察治疗前和4个治疗周期后中医证候疗效指数是否存在差异。疗效指数=(治疗前证候积分-治疗后证候积分)/治疗前证候积分×100%。显著改善:症状明显改善,疗效指数≥70%;部分改善:症状部分好转,70%>疗效指数≥30%;稳定:症状无明显改善,30%>疗效指数≥0%,加重:症状加重:疗效指数<0%。
1.6.5 Karnofsky功能状态评分(KPS)治疗前后依据KPS评分标准进行评分。
1.6.6 化疗相关不良反应根据常见不良反应事件评价标准5.0版本(NCI-CTCAE v5.0)[9]观察两组患者因化疗药物所致不良反应的严重程度,统计Ⅰ~Ⅳ级不良反应程度的发生例数。不良事件发生率=Ⅰ~Ⅳ级阳性事件人数/该组总人数×100%。
1.7 统计学方法数据均采取SPSS26.0软件进行处理,计量资料符合正态分布用均数±标准差(x±s)表示,组间比较采用t检验,不符合正态分布或方差不齐时用中位数(25%四分位数,75%四分位数)[M(Q25,Q75)]表示,组间比较使用Mann-Whitney U秩和检验;计数资料用频数及百分比表示,组间比较采用卡方检验;等级资料组间比较使用Mann-Whitney U秩和检验。生存分析采用绘制Kaplan-Meier曲线对无进展生存期(PFS)进行描述,估计中位无进展生存时间,两组之间采用Log-rank检验进行比较。P<0.05为差异有统计学意义。
2 结果 2.1 两组患者基线资料比较使用电子病历系统最终筛选出暴露组(化疗联合扶正解毒祛浊法方药组,30例);非暴露组(单纯化疗组,30例)。两组患者年龄、性别、吸烟史、饮酒史、恶性肿瘤家族史、远处转移、治疗前KPS评分差异无统计学意义,具有可比性(P>0.05)。见表 1。
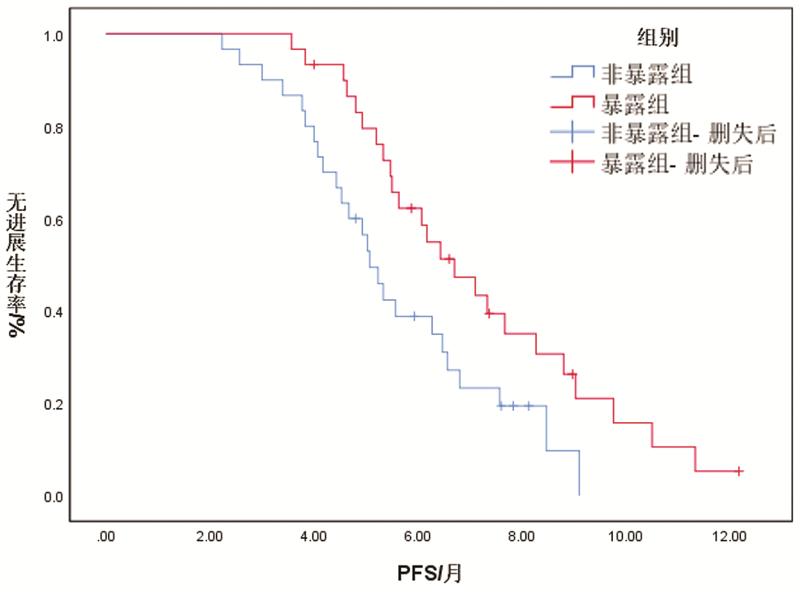
直至失访或随访结束非暴露组与暴露组,mPFS分别为5.07个月[95%CI(4.56,5.59)]和6.70个月[95%CI(5.45,7.96)],单因素Log-rank检验结果显示,两组差异有统计学意义(P=0.024)。见图 1。
|
| 图 1 两组患者PFS生存曲线 Fig. 1 PFS survival curves of patients between the two groups |
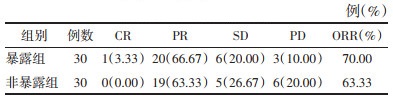
分析两组患者疾病控制情况可以得出结论,暴露组客观缓解率(70.00%)稍高于非暴露组(63.33%),但差异无统计学意义(P>0.05)。见表 2。
|
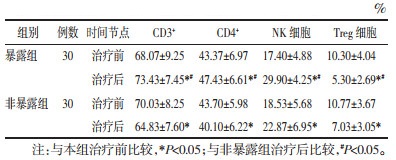
治疗前两组差异均无统计学意义,治疗后暴露组较非暴露组CD3+、CD4+T淋巴细胞、NK细胞指标升高,Treg细胞下降,差异均有统计学意义(P<0.05)。见表 3。
|
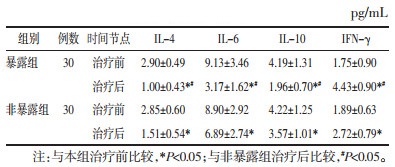
两组治疗后IL-4、IL-6、IL-10血清水平均较治疗前明显降低,暴露组治疗后低于非暴露组,IFN-γ均升高,暴露组较非暴露组明显升高,差异均有统计学意义(P<0.05)。见表 4。
|
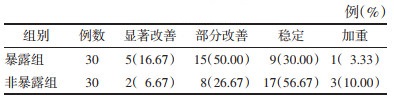
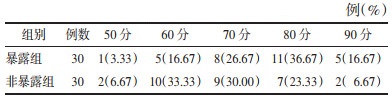
治疗后,暴露组患者中显著改善5例,部分改善15例,稳定9例,加重1例,总有效率66.67%。非暴露组患者中显著改善2例,部分改善8例,稳定17例,加重3例,总有效率33.33%。结果显示,治疗组在改善中医证候疗效上优于非暴露组(P<0.05)。见表 5。
|
治疗后,暴露组患者KPS评分显著高于非暴露组,差异具有统计学意义(P<0.05),提示联合使用扶正解毒化浊方加减可显著改善患者生活质量。见表 6。
|
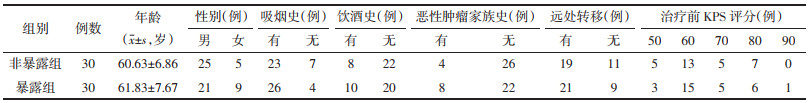
两组均有白细胞减少、血小板减少、贫血、恶心呕吐等不良反应发生,多为Ⅰ~Ⅱ度,均可耐受。暴露组白细胞减少、胃肠道反应发生率明显低于非暴露组(P<0.05),血小板减少、贫血方面两者差异不显著(P>0.05)。见表 7。
SCLC是一种高级别神经内分泌癌,与接触烟草致癌物密切相关,多数患者在首次诊断时已发生远处转移,临床症状常以呼吸道症状为主,包括咳嗽、呼吸困难、咯血等。SCLC最初对细胞毒性药物治疗尤其敏感,即使ES-SCLC的患者同步放化疗的缓解率仍可超过60%,然而其迅速出现耐药的特点,常使得原化疗方案无效导致疾病进展[1]。中医药作为中国传统医学的重要组成部分,在ES-SCLC标准一线治疗过程中尽早介入可发挥增效减毒、延长生存期、改善中医证候、提高免疫等治疗优势[10]。中医根据SCLC不同临床主症将其归为“肺积”“息贲”“咳嗽”等病范畴,《圣济总录》云:“肺积息贲气胀满咳嗽,涕唾脓血”。现代医家多认为其病机多与正气虚损、邪毒侵肺、痰瘀内聚相关[11]。贾英杰教授凭借多年临床经验认为“正气内虚,浊毒瘀并存”是肺癌发生的内在病机。如《外证医案汇编》云:“正气虚则成岩。”正气虚损,肺失宣降,脾失健运,气机不利,痰浊内生,贮于肺中,此浊环境胶结日久,而为积聚。久病入络,瘀血裹结,郁而成毒。化疗药物属“药毒”,在杀伤癌肿之邪的同时,亦损伤人体正气,致气血阴阳失调,短期或可收效,终致机体难以耐受。
扶正解毒祛浊法方药是贾英杰教授治疗肺癌的基础方,由千金苇茎汤合小陷胸汤根据围化疗期特点加减化裁而成,在三焦辨证基础上参以卫气营血辨证,清气分药用黄芩、金银花、连翘、鱼腥草、白花蛇舌草、半边莲、半枝莲等,清营血分热用赤芍、牡丹皮、生地黄等。对改善患者生活质量、提高化疗疗效具有较好的临床效果。基本处方中用重剂黄芪,补气不恋邪,鼓舞气血,培育本源;川芎、郁金、姜黄3味药合用,行气活血,使体内瘀滞之浊血得祛,避免有形浊邪积聚而生内热。若扶正祛瘀而不解毒则毒根深藏,持续消耗人体气血津液,使正气难复,故使用猫爪草、白花蛇舌草两药解毒。针对肺癌病位特点,肺苦气上逆,枳壳能泄肺之浊气,畅达三焦气机,使气行则水行,改善胶结的浊环境;以瓜蒌配伍半夏、薏苡仁、芦根、浙贝母,宽胸散结,荡涤胸中痰浊。“脾为生痰之源,肺为贮痰之器”,断痰之源,当顾及脾胃,临证常加用健脾祛湿药以助脾散精,上输于肺,如陈皮、半夏、厚朴、莱菔子、佩兰等。全方紧扣肺癌病机,以培植本元,罢黜癌浊为治则,共奏解毒祛浊、扶正抗癌之功。方中黄芪、郁金、姜黄、白花蛇舌草亦是贾英杰教授自拟消岩汤的核心药物,前期相关基础研究证明了以上部分药物可通过阻断不同信号通路而改善肺癌患者免疫功能及逆转耐药[12-14]。
T淋巴细胞及NK细胞介导的细胞免疫是人体抗肿瘤免疫的重要机制,CD3+、CD4+淋巴细胞亚群血清水平反映了人体细胞免疫状态,其较高的浸润水平与SCLC患者的长期生存相关[15],而NK细胞作为人体对抗肿瘤的第一道防线,可通过释放穿孔素和颗粒酶、诱导细胞凋亡、合成分泌多种细胞因子、抗体依赖性的细胞介导的细胞毒作用途径杀伤肿瘤细胞[16]。Treg细胞是CD4+T细胞的一类特殊分支,在机体免疫系统中发挥负向调节作用,可以避免免疫炎症反应的扩大和减轻免疫机体损伤。现已充分证实,大量的Treg细胞浸润到各种癌症的肿瘤组织中通常与不良的临床预后有关,去除Treg细胞能够唤起有效的抗肿瘤免疫[17]。有研究显示,对于体能状态差的ES-SCLC患者,双药化疗可降低其CD4水平,可能是导致6个月生存率下降的重要因素[18]。另有研究发现益气活血中药能显著改善非小细胞肺癌化疗患者CD3+、CD4+水平,与本研究结果相近[19]。本研究数据显示,治疗后暴露组较非暴露组CD3+、CD4+、NK细胞等血清水平明显升高,Treg细胞降低,免疫细胞水平较前改善,说明扶正解毒祛浊法方药可改善ES-SCLC患者化疗后细胞免疫功能受损情况,增强抗肿瘤免疫。
Th1、Th2细胞是人体辅助性T细胞的重要亚群,Th1细胞主要分泌IFN-γ、肿瘤坏死因子-α(TNF-α)、IL-2等因子,具有抗肿瘤和免疫调节作用;Th2细胞主要分泌IL-4、IL-6、IL-10等因子,可抑制肿瘤细胞免疫应答过程[20]。肿瘤患者体内Th2细胞因子普遍占优势,导致Th1/Th2比例失衡,Th1/Th2偏移越大,机体的免疫抑制也越严重,肺癌患者预后也越差[21]。IL-6还与下游IL-6/STAT3信号通路结合,构成化疗反应的中枢调节分子,参与化疗耐药[22]。相关研究发现,晚期肺癌患者相对于健康体检者IL-4、IL-6、IL-10水平较高,IFN-γ水平较低,出现Th1向Th2偏移,化疗2周期后肺癌患者血清IL-4、IL-6、IL-10水平显著降低,IFN-γ水平显著升高。此外,IL-4、IL-6、IL-10、IFN-γ预测疗效均具有较高AUC值,尤以联合预测最高[23]。本研究中,扶正解毒祛浊法方药方可进一步提高化疗组IFN-γ水平,降低IL-4、IL-6、IL-10水平,提示扶正解毒祛浊法方药联合化疗可协助化疗逆转Th1/Th2偏移状态,恢复有效抗肿瘤免疫。
中药有效成分可通过多种机制调节免疫细胞及细胞因子,如抑制免疫抑制因子[IL-10、转化生长因子-β(TGF-β)、前列腺素E2(PGE2)等]的分泌,促进抗肿瘤免疫因子(IFN-γ、TNF-α、IL-1β等)的分泌、免疫抑制细胞数量下调[Tregs、骨髓来源抑制细胞(MDSC)、M1巨噬细胞等]以及增加Teffs的活性和数量,逆转肿瘤介导的免疫抑制,重塑肿瘤微环境[24-26]。Zou等[27]研究发现姜黄素通过抑制叉头盒蛋白-3的基因转录和增加IFN-γ的表达,将肺癌患者分离的Tregs转化为Th1细胞,发挥抗肿瘤作用。1项Meta分析显示,与单纯化疗相比,联合中药能提高ES-SCLC的客观缓解率[RR=1.29,95%CI(1.10,1.52),P=0.002]、生活质量[RR=3.41,95%CI(1.45,6.80),P=0.004],与本研究结论相符[28]。本研究结果表明,暴露组PFS、ORR获益明显高于非暴露组,中医证候、KPS评分也明显改善,不良反应减少,机制可能与中医药通过多途径多靶点改善患者化疗耐药及免疫功能有关。
总之,扶正解毒祛浊法方药用于治疗ES-SCLC,在一线化疗方案基础上可减少患者免疫功能损伤,提高化疗疗效,降低化疗相关不良反应,改善患者临床症状,有一定的临床应用价值。但本研究纳入样本量小,且随访时间较短,后续有待进一步增加样本量,开展多中心大样本临床研究,并延长随访时间,其具体作用机制也有待进一步研究验证。
| [1] |
RUDIN CM, BRAMBILLA E, FAIVRE-FINN C, et al. Small-cell lung cancer[J]. Nature Reviews Disease Primers, 2021, 7(1): 3. DOI:10.1038/s41572-020-00235-0 |
| [2] |
MEGYESFALVI Z, GAY C M, POPPER H, et al. Clinical insights into small cell lung cancer: tumor heterogeneity, diagnosis, therapy, and future directions[J]. CA: A Cancer Journal for Clinicians, 2023, 73(6): 620-652. DOI:10.3322/caac.21785 |
| [3] |
ZUGAZAGOITIA J, PAZ-ARES L. Extensive-stage small-cell lung cancer: first-line and second-line treatment options[J]. Journal of Clinical Oncology, 2022, 40(6): 671-680. DOI:10.1200/JCO.21.01881 |
| [4] |
ALDAROUISH M, SU X Y, QIAO J B, et al. Immunomodulatory effects of chemotherapy on blood lymphocytes and survival of patients with advanced non-small cell lung cancer[J]. International Journal of Immunopathology and Pharmacology, 2019, 33: 1-9. |
| [5] |
WANG Y S, ZHANG Q F, CHEN Y C, et al. Antitumor effects of immunity-enhancing traditional Chinese medicine[J]. Biomedecine & Pharmacotherapie, 2020, 121: 109570. |
| [6] |
CHEN S T, BAO Y J, XU J, et al. Efficacy and safety of TCM combined with chemotherapy for SCLC: a systematic review and meta-analysis[J]. Journal of Cancer Research and Clinical Oncology, 2020, 146(11): 2913-2935. DOI:10.1007/s00432-020-03353-0 |
| [7] |
EISENHAUER E A, THERASSE P, BOGAERTS J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline(version 1.1)[J]. European Journal of Cancer, 2009, 45(2): 228-247. DOI:10.1016/j.ejca.2008.10.026 |
| [8] |
肺癌中医诊疗方案[S]. 北京: 国家中医药管理局, 2021: 1-10.
|
| [9] |
U.S. Department of Health and Human Services. Common Terminology Criteria for Adverse Events(CTCAE) v5.0[EB/OL]. (2017-11-27)[2024-07-12]. https://ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/CTCAE_v5_Quick_Reference_8.5x11.pdf.
|
| [10] |
李姝蒙, 陈芋屹, 吴桐桐, 等. 西医一线、中医药联合西医一线治疗广泛期小细胞肺癌的研究进展[J]. 中国医药导报, 2023, 20(30): 43-46. DOI:10.20047/j.issn1673-7210.2023.30.07 |
| [11] |
张星星, 李泽庚. 肺癌中医病因病机探讨[J]. 中华中医药杂志, 2015, 30(10): 3447-3449. |
| [12] |
杨佩颖, 刘宏根, 贾英杰. 消岩汤干预Beclin1-YAP1环路逆转肺癌顺铂耐药研究[J]. 中草药, 2023, 54(4): 1184-1189. DOI:10.7501/j.issn.0253-2670.2023.04.018 |
| [13] |
赵林林, 王艳亭, 王晓群, 等. 消岩汤治疗非小细胞肺癌临床及基础研究进展[J]. 中草药, 2022, 53(2): 627-634. |
| [14] |
刘筱迪. 消岩颗粒联合化疗对晚期非小细胞肺癌患者MDSC-NKT免疫调控的研究及机制探讨[D]. 天津: 天津中医药大学, 2020.
|
| [15] |
MUPPA P, PARRILHA TERRA S B S, SHARMA A, et al. Immune cell infiltration may be a key determinant of long-term survival in small cell lung cancer[J]. Journal of Thoracic Oncology, 2019, 14(7): 1286-1295. |
| [16] |
SIVORI S, PENDE D, QUATRINI L, et al. NK cells and ILCs in tumor immunotherapy[J]. Molecular Aspects of Medicine, 2021, 80: 100870. |
| [17] |
TANAKA A, SAKAGUCHI S. Regulatory T cells in cancer immunotherapy[J]. Cell Research, 2017, 27(1): 109-118. |
| [18] |
邱野, 江玉兰, 张霞, 等. 双药联合化疗对不同体能状态广泛期小细胞肺癌患者T淋巴细胞亚群及预后的影响[J]. 实用癌症杂志, 2020, 35(3): 410-413. |
| [19] |
陈启庭, 李际强, 蔡俊媛, 等. 益气活血中药联合化疗对非小细胞肺癌患者免疫功能的影响[J]. 中医肿瘤学杂志, 2023, 5(3): 70-78. DOI:10.19811/j.cnki.ISSN2096-6628.2023.05.011 |
| [20] |
BASU A, RAMAMOORTHI G, ALBERT G, et al. Differentiation and regulation of TH cells: a balancing act for cancer immunotherapy[J]. Frontiers in Immunology, 2021, 12: 669474. |
| [21] |
孔琦, 朱家胜, 芮景. Th1/Th2偏移与肿瘤免疫研究进展[J]. 现代肿瘤医学, 2010, 18(8): 1653-1655. |
| [22] |
LI J, HE K, LIU P, et al. Iron participated in breast cancer chemoresistance by reinforcing IL-6 paracrine loop[J]. Biochemical and Biophysical Research Communications, 2016, 475(2): 154-160. |
| [23] |
韦安猛, 张伟华, 张春玲, 等. 肺癌患者化疗前后Th1/Th2细胞因子免疫反应状态变化及对预后的影响[J]. 实用癌症杂志, 2022, 37(5): 746-751. DOI:10.3969/j.issn.1001-5930.2022.05.013 |
| [24] |
ZHANG W L, LI S B, LI C T, et al. Remodeling tumor microenvironment with natural products to overcome drug resistance[J]. Frontiers in Immunology, 2022, 13: 1051998. |
| [25] |
HUO J L, FU W J, LIU Z H, et al. Research advance of natural products in tumor immunotherapy[J]. Frontiers in Immunology, 2022, 13: 972345. |
| [26] |
DONG S T, GUO X N, HAN F, et al. Emerging role of natural products in cancer immunotherapy[J]. Acta Pharmaceutica Sinica B, 2022, 12(3): 1163-1185. |
| [27] |
ZOU J Y, SU C H, LUO H H, et al. Curcumin converts regulatory T cells to T helper 1 cells in patients with lung cancer[J]. Journal of Cellular Biochemistry, 2018, 119(2): 1420-1428. |
| [28] |
余慧, 刘庆, 周溢鑫, 等. 中医药一线联合化疗治疗广泛期小细胞肺癌的Meta分析[J]. 中国处方药, 2021, 19(5): 133-136. |
2. National Clinical Research Center for Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China;
3. Graduate School, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
 2024, Vol. 41
2024, Vol. 41