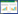文章信息
- 吴勇俊, 蒋凌, 蒋婉柔, 等.
- WU Yongjun, JIANG Ling, JIANG Wanrou, et al.
- 托里消毒散调控TLR4/Myd88/NF-κB通路和NLRP3炎性小体抑制对5-Fu所致的CID小鼠肠道损伤研究
- Tuoli Xiaodu Powder inhibited 5-fluorouracil-induced CID mice intestinal injury by regulating TLR4/Myd88/NF-κB pathway and inhibiting NLRP3 inflammasome
- 天津中医药, 2024, 41(11): 1431-1437
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1431-1437
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.13
-
文章历史
- 收稿日期: 2024-08-08
2. 成都中医药大学, 成都 610075
据国家癌症中心公布的最新数据显示,结直肠癌(CRC)的发病率和病死率分别位于恶性肿瘤第2位和第4位,且其发病率呈持续上升趋势[1-2]。化疗是CRC治疗的重要手段,其中5-氟尿嘧啶(5-Fu)是CRC治疗的关键化疗药物,5-Fu是一种抗代谢药物,通过抑制DNA和RNA的合成来抑制肿瘤细胞的增殖,从而延长无瘤生存期,提高患者的总生存率[3-5]。然而,研究表明,约50%~80%的肿瘤患者接受5-Fu化疗后会出现肠黏膜炎症,表现为严重溃疡、炎症细胞浸润,并可能出现黏膜出血[6-7]。肠黏膜损伤导致化疗相关性腹泻(CID)的发生,严重影响癌症患者的管理和健康,增加了患者的感染易感性和病死率[8-9]。目前,缺乏有效和安全的药物干预措施来减轻肿瘤化疗对肠黏膜的有害影响。
托里消毒散出自明代陈实功所著《外科正宗》一书,由生晒参、黄芪、当归、川芎、白芍、炒白术、茯苓、白芷、皂角刺、金银花、炙甘草、桔梗组成,“治痈疽已成不得内消者,宜服此药以托之”[10],该方能补益气血,托毒外出,原治痈疽已成,体虚气血不足,不能及时外溃,现代主要将其治疗各种溃疡性疾病[11]。CID的肠道表现为黏膜损伤、糜烂,恰似在肠道表面形成“疮疡”,取象比类,认为CID可参考疮疡论治。化疗药物味苦性寒,药毒伤脾,气机升降失司,津液代谢失常,下注成泻,脾虚湿盛为其全身病机;湿热下注,瘀阻肠络,导致肠黏膜充血、水肿、损伤、糜烂,湿热瘀阻为其局部病机,治疗上当扶正与祛邪兼顾,不可妄用苦寒攻邪之品,以防伤正、邪留不去,临证当以“补法”为主,“托、透”法相结合。在临床中应用托里消毒散治疗CID可取得较好的临床疗效,但尚未对其分子机制进行研究。
TLR4/MyD88/NF-κB通路是机体在应对外源病原体感染时的一种免疫应答途径[12]。研究发现,化疗药物导致的基因毒性应激反应可导致不同的Toll样受体(TLR)表达,进而导致细胞系特异性和损伤特异性[13]。选择性化疗药物可能通过Toll样受体4(TLR4)驱动脂多糖(LPS)高反应性,通过异常的细胞因子风暴加剧黏膜损伤[14]。TLR4会识别细菌的LPS,激活骨髓分化主要反应蛋白88(Myd88),进而激活核因子κB(NF-κB),激活的NF-κB促进炎症相关基因的表达,导致炎症介质的释放,炎症反应的发生[15]。在肠道炎症的发生过程中,TLR4/MyD88/NF-κB通路发挥着重要作用。因此,本研究旨在通过构建CID小鼠模型,并给予托里消毒散治疗,观察其对肠道损伤、肠黏膜炎症和TLR4/MyD88/NF-κB通路活性的调节作用。
1 材料与方法 1.1 动物、细胞、材料与试剂CT-26小鼠结肠腺癌细胞购自中国科学院(中国上海)的细胞库。雌性BALB/c小鼠(4周龄)购自成都荣盛药业有限公司[SYXK(四川)2023-0265]。小鼠在控制的环境条件下自由获取食物和水,温度范围为20~25 ℃,相对湿度为50%±1%,光照/黑暗循环12 h。
PRMI-1640培养基(Procell,#PM150110)、10%胎牛血清(FBS,Vivacell,#C04001-500)、0.25%胰蛋白酶-四乙酸乙二胺(EDTA,Gibco,#17892)、青霉素链霉素(上海源培生物科技股份有限公司,#S110JV)、BCA蛋白浓度测定试剂盒(上海碧云天生物技术有限公司,#P0009)、放射免疫沉淀实验缓冲液(RIPA,Santa Cruz Biotechnology,#sc-24948)、Immobilon-PSQ PVDF膜(Sigmaaldrich,#ISEQ00010)、山羊抗兔免疫球蛋白(Ig)G(H+L) 辣根过氧化物酶(HRP,affbiotech,#S0001)、一抗β-actin(abclonal,#AC026)、一抗Myd88(abclonal,#A0980)、一抗p65(abclonal,#A2547)、一抗TLR4(abclonal,#A5258)、牛血清白蛋白(BSA,赛维尔,#GC305010)、一抗NLRP3(ThermoFisher,#PA5-79740)、HRP标记山羊抗兔(赛维尔,#GB23303)、Molpure Cell/Tissue Total RNA Kit(YEASEN,#19221ES50)、PrimeScript RT reagent Kit(宝日医生物技术有限公司,#RR047A)、TB GreenTM Premix Ex TaqTM Ⅱ(Tli RNaseH Plus,宝日医生物技术有限公司,#RR820A)。
1.2 仪器与设备数显水平摇床(Servicebio)、JY-SCZ4+型垂直电泳槽(北京君意东方电泳设备有限公司)、数字切片扫描仪(济南丹吉尔电子有限公司)、荧光图像分析系统(Tanon)、掌上离心机(SCILOGEX)、脱水机(常州市中威电子仪器有限公司);包埋机(常州郊区中威电子仪器厂)、切片机(上海徕卡仪器有限公司)、实时荧光定量聚合酶链反应(PCR)仪(ThermoFisher)、高速低温组织研磨仪(武汉塞维尔科技有限公司)、数码三目摄像显微摄像系统(麦克奥迪实业集团有限公司)。
1.3 方法 1.3.1 托里消毒散的制备托里消毒散(生晒参30 g,黄芪30 g,当归15 g,川芎15 g,白芍15 g,炒白术15 g,茯苓15 g,白芷15 g,皂角刺15 g,金银花15 g,炙甘草10 g,桔梗10 g)。所购药材均符合《中华人民共和国药典》标准。按组方称取药材,加倍水煎煮1 h,过滤,药加5倍水煎煮1 h,过滤混合,旋转蒸发浓缩至1 g/mL。
1.3.2 细胞培养CT-26细胞在PRMI-1640培养基中培养,添加10% FBS和1%青霉素-链霉素溶液,在37 ℃加5% CO2的加湿培养箱中培养。当细胞达到80%~90%的合流度时,用0.25% EDTA溶液传代。
1.3.3 CRC异种移植模型的建立与分组参照文献制备CID模型[16]。对数生长期的CT-26细胞用0.25% EDTA收集单细胞悬液,室温下1 500 r/min离心5 min(离心半径8 cm)。将Matrigel与无血清RPMI-1640培养基按1:1比例充分混合。细胞重悬于无血清RPMI-1640培养基中,浓度为1.0×107个细胞/mL。接种前对小鼠进行常规皮肤消毒,每只小鼠0.25 mL(2.5×106个细胞/小鼠)接种于BALB/c小鼠右前肢腋窝。7 d肿瘤形成后,将小鼠随机分为对照组、空白组、CID模型组、阳性药物(洛哌丁胺)组、托里消毒散-散低剂量组、托里消毒中剂量组和托里消毒散-高剂量组。空白组和CID组小鼠灌胃蒸馏水0.2 mL/d,连续14 d。洛哌丁胺组小鼠给予洛哌丁胺混悬液0.7 mg/(kg·d)灌胃14 d,托里消毒散组小鼠给予不同剂量的托里消毒散[0.2、0.4、0.8 g/(10 g·d)]灌胃14 d。空白组小鼠自给药第5 d起连续5 d腹腔注射0.1 mL/10 g生理盐水,其余各组小鼠连续5 d腹腔注射100 mg/kg 5-Fu。另以未接种细胞的BALB/c小鼠为对照组,同时灌胃等量蒸馏水并注射生理盐水。灌胃给药14 d后,参照Akinobu Kurita[17]的方法,进行腹泻严重程度评分。正常(0分):大便正常或没有;轻度腹泻(1分):大便可见轻微湿软;中度腹泻(2分):大便较湿且不成形,并且有中度肛周着色;重度腹泻(3分):水样大便,伴有重度肛周着色。第22天,各组小鼠均安乐死,取肿瘤组织用于后续实验。用尺子测量计算肿瘤体积(1/2 ×长×宽×高)。实验流程详见图 1。动物实验所有程序均由四川大学华西医院伦理委员会批准(20240422013)。
|
| 图 1 实验流程图 Fig. 1 Experimental flow chart |
使用RIPA缓冲液(Biosharp,#BL509A)收集直肠裂解液中的总蛋白,随后使用BCA蛋白测定试剂盒测定蛋白浓度。然后在蛋白样品中加入十二烷基苯磺酸钠凝胶电泳(SDS-PAGE),转膜完毕后,用含5% 脱脂牛奶的三硼酸钠色氨酸缓冲液(TBST)溶液室温封闭2 h;一抗孵育:将聚偏二氟乙烯膜(PVDF)膜放入一抗中(一抗浓度:MyD88 1:500;p65 1:2 000;TLR4 1:5 000;β-actin 1:50 000),摇床上轻摇,4 ℃孵育过夜;用TBST将PVDF膜洗3次,每次5 min;然后将PVDF膜放入二抗(稀释浓度:1:5 000)中,摇床上轻摇,室温孵育2 h;用TBST将PVDF膜洗3次,每次10 min。加入ECL进行显色,用Tanon荧光图像分析系统软件V2.0对条带进行曝光,结果以Gel-Pro analyzer4软件扫描曝光结果,并以目的蛋白积分光密度(IOD)表示。
1.3.5 苏木精-伊红染色(HE)收集小鼠直肠组织,在4%多聚甲醛溶液中固定过夜。随后,将组织处理并包埋于石蜡中。然后将厚度为5 μm的组织切片置于49 ℃的水浴中,贴于涂有聚赖氨酸的载玻片上。载玻片经甲苯脱蜡,乙醇脱水,蒸馏水洗涤。随后,用苏木精染色,洗涤,并用1%盐酸乙醇处理以分离切片。涂上伊红染料,用蒸馏水洗涤10 min。最后用二甲苯脱水,用中性黏合剂密封。使用数码三目摄像显微摄像系统观察组织切片。
1.3.6 免疫组织化学染色(IHC)使用二甲苯、无水乙醇和梯度乙醇对石蜡切片进行脱蜡至水;抗原修复后阻断内源性过氧化物酶,将切片浸泡于3%双氧水中,在室温避光孵育25 min,然后将玻片置于pH 7.4的磷酸缓冲盐溶液(PBS)中,在脱色摇床上晃动洗涤3次,每次5 min;血清封闭切片,滴加一抗,湿盒中4 ℃冰箱过夜,37 ℃复苏35 min,PBS洗3次;滴加生物素化的二抗,37 ℃孵育30 min,PBS洗5 min×3次;二氨基联苯胺(DAB)显色(1 ℃20)8 min,木素复染切片后,自来水冲洗;梯度乙醇脱水,二甲苯透明,封片;使用数码三目摄像显微摄像系统对切片进行图像采集。
1.3.7 反转录-定量PCR(RT-qPCR)RT-qPCR检测IL-1β、IL-8、IL-6以及TNF-α的mRNA表达水平。使用Molpure?誖Cell/Tissue Total RNA Kit分离直肠组织总RNA,使用PrimeScript RT reagent Kit反转录试剂盒合成cDNA。使用TB GreenTM Premix Ex TaqTM Ⅱ(Tli RNaseH Plus)试剂盒,采用RT-qPCR检测蛋白RNA相对水平。逆转录反应条件为:95 ℃初始变性30 s,95 ℃变性5 s,55 ℃退火30 s,72 ℃延伸30 s。采用2-△△Ct法计算相对基因表达量。RT-qPCR所用引物见表 1。
所有数据均采用SPSS 20.0软件进行统计分析,各实验数据以均值±标准差(x±s)表示。两组间比较采用独立样本Student’s t检验,多组间比较采用单因素方差分析和均数事后检验。P<0.05表示差异具有统计学意义。
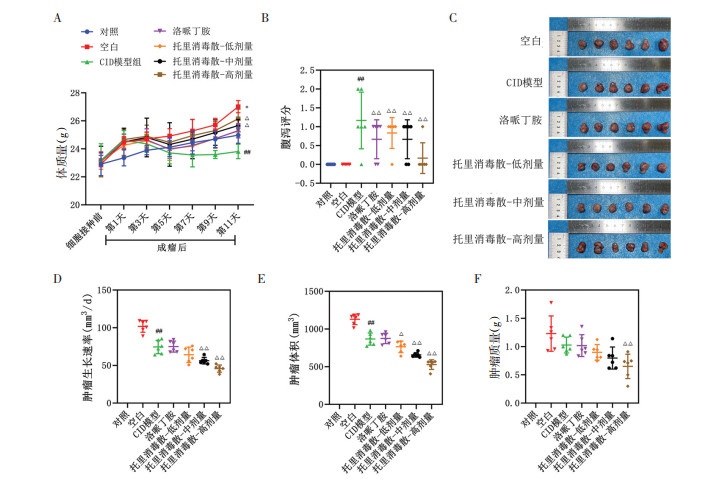
2 结果 2.1 托里消毒散对5-Fu诱导的CID小鼠腹泻和肿瘤生长的抑制作用如图 1A所示,与对照组相比,空白组小鼠体质量增加,CID模型小鼠体质量显著减轻。中、高剂量托里消毒散显著增加CID模型小鼠体质量。与空白组相比,CID模型组的腹泻严重程度明显更高(见图 2B)。此外,与CID小鼠相比,洛哌丁胺和托里消毒散低、中、高剂量组的腹泻严重程度均显著降低(见图 2B)。其次,5-Fu干预显著降低了CID小鼠的肿瘤生长速度、肿瘤体积和体重,这些都被中、高剂量托里消毒散进一步降低(见图 2C-1F)。托里消毒散对肿瘤生长的抑制作用呈剂量依赖性(见图 2C-2F)。
|
| 注:A,监测小鼠体质量;B,腹泻评分用于评价腹泻的严重程度;C,肿瘤拍照;D,通过测量肿瘤直径监测肿瘤生长速度;E,肿瘤体积;F,肿瘤质量。n=6。与对照组比较,*P<0.05;与空白组比较,##P<0.01;与CID模型组比较,△P<0.05,△△P<0.01。 图 2 托里消毒散对5-FU诱导的CID小鼠腹泻和肿瘤生长的抑制作用 Fig. 2 Inhibition of Tuoli Xiaodu Powder on diarrhea and tumor growth in 5-FU-induced CID mice |
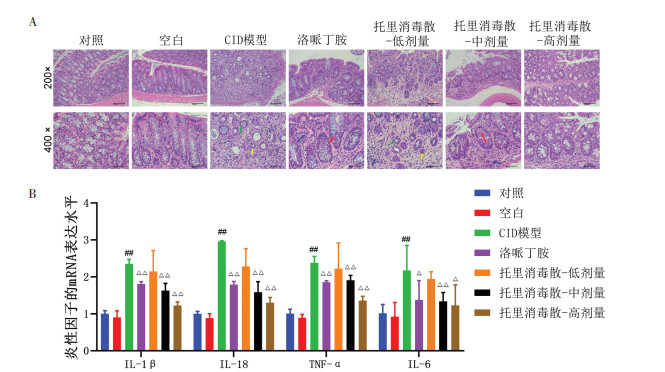
如图 3A所示,对照组和空白组HE染色显示肠道结构正常,CID模型组小鼠结肠黏膜变性坏死,肠腺萎缩,炎症细胞浸润。经洛哌丁胺、中、高剂量托里消毒散处理的CID小鼠,与未处理组相比,HE染色显示的病理改变有所减轻,肠腺萎缩、肥大和炎症反应有所改善(见图 3A)。RT-qPCR检测结果显示,5-Fu诱导的CID小鼠肠道中炎症因子白细胞介素(IL)-1β、肿瘤坏死因子-α(TNF-α)、IL-18和IL-6水平升高(见图 3B)。托里消毒散通过减轻促炎因子IL-1β、TNF-α、IL-18和IL-6的表达(见图 3B)。此外,托里消毒散对CID模型小鼠肠道炎症的抑制作用呈剂量依赖性(见图 3B)。
|
| 注:A,对直肠组织进行HE染色,放大倍数为200倍和400倍。绿色箭头表示黏膜变性坏死,黄色箭头表示肠腺萎缩,红色箭头表示肠腺肥大,蓝色箭头表示炎症细胞浸润。B,RT-qPCR分析炎性细胞因子(IL-1β、TNF-α、IL-18和IL-6)。n=3。与空白组比较,##P<0.01;与CID模型组比较,△P<0.05,△△P<0.01。 图 3 托里消毒散对5-Fu诱导的CID小鼠肠黏膜损伤和炎症的抑制作用 Fig. 3 Inhibitory effect of Tuoli Xiaodu Powder on intestinal mucosal injury and inflammation in 5-FU-induced CID mice |
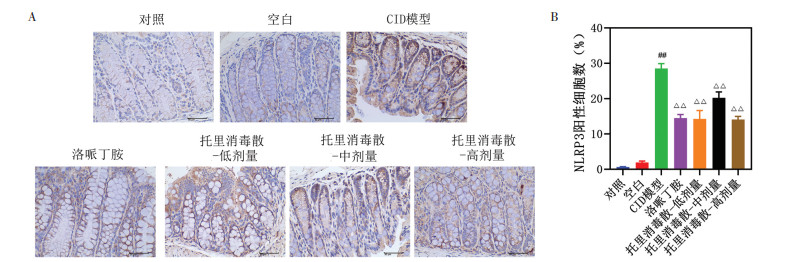
如图 4A和4B所示,5-Fu诱导的CID小鼠肠道NLRP3水平显著升高,洛哌丁胺和托里消毒散处理后肠道NLRP3水平呈依赖性降低。其中,托里消毒散高剂量组小鼠肠道中NLRP3水平降低的程度最低。
|
| 注:对直肠组织进行IHC染色,检测NLRP33炎性小体表达。放大倍数400倍。n=3。与空白组比较,##P<0.01;与CID模型组比较,△△P<0.01。 图 4 托里消毒散对5-Fu诱导的CID小鼠肠道NLRP3炎性小体的抑制作用 Fig. 4 Inhibitory effect of Tuoli Xiaodu Powder intestinal NLRP 3 inflammasome in 5-FU-induced CID mice |
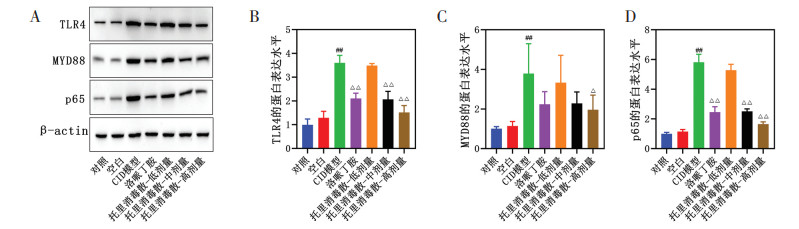
5-Fu诱导下,CID小鼠直肠TLR4,MyD88和p65水平显著上升。托里消毒散剂量依赖性地降低了5-Fu诱导的CID小鼠直肠TLR4,MyD88和p65蛋白的表达水平(见图 5A-5D)。
|
| 注:Western blot检测TLR4,MyD88和p65的蛋白表达。β-actin为内参蛋白。n=3。与空白组比较,##P<0.01;与CID模型组比较,△P<0.05,△△P<0.01。 图 5 托里消毒散对5-Fu诱导的CID小鼠肠道TLR4/MyD88/NF-κB通路活性的抑制作用 Fig. 5 Inhibitory effect of Tuoli Xiaodu Powder on TLR4/MyD88/NF-κB pathway activity in 5-FU-induced CID mice |
中药在治疗CID方面具有综合手段、多成分利用、靶向多因素、多效、毒性可忽略、不良反应有限等诸多优势[18]。既往研究表明葛根芩连汤可降低癌症患者总腹泻率[19]。黄连解毒汤可减轻CRC治疗期间腹泻的发生、减少肠道内细胞凋亡、促进上皮再生[19-20]。托里清毒散对疮疡、溃疡性结肠炎和消化道溃疡具有较好的治疗作用,可以改善溃疡性结肠炎模型大鼠的肠黏膜损伤,减轻肠道炎症[21-23]。本研究进一步表明了托里消毒散可以减轻5-Fu诱导的CID小鼠腹泻程度,并抑制肿瘤生长。托里消毒散协同抑制肿瘤的作用可能原因是托里消毒散和5-Fu的药理学特性可能相互增强,导致其在抑制肿瘤生长方面产生协同作用。此外,托里消毒散可能还具有调节肠道微生物组成、减轻肠道炎症反应等作用,进一步影响肿瘤生长的环境,从而对肿瘤产生积极影响。
CID的发生与化疗药物对肠黏膜细胞的损伤和炎症密切相关。肠黏膜作为一个重要的机械屏障,有效地阻止外来有害物质,包括抗原、细菌和内毒素进入机体[24-25]。化疗药物作用于肠上皮细胞,导致结构和功能损伤,最终导致细胞凋亡和坏死,这些影响共同损害肠黏膜结构的完整性,最终导致肠黏膜屏障功能受损[26-27]。值得注意的是,在以前的文章中已经报道了托里消毒散的多种成分可以改善肠黏膜损伤。其中人参和白芍总苷可上调紧密连接蛋白表达,进而改善肠道上皮屏障损伤[28-29]。本研究进一步证实了托里消毒散的这些成分对5-Fu诱导的CID小鼠肠道损伤的保护作用。
药物引起肠黏膜损伤后,肠道内病原体和细菌发生易位,从而激活免疫细胞,诱发炎症反应。既往研究表明,芍药总苷通过抑制结肠炎小鼠的Lyn/Snail信号通路,降低结肠组织和血清中TNF-α、IL-17A、IL-23和干扰素-γ(IFN-γ)的水平[30]。当归油通过抑制S100钙结合蛋白A8 /A9的表达,抑制其下游TLR4/NF-κB信号通路的激活,有效改善溃疡性结肠炎模型肠黏膜屏障损伤[31]。此外,黄芪提取物通过激活NF-κB和诱导Nrf2反应来减轻肠上皮细胞的炎症和氧化应激[32]。同样,本研究发现给药托里消毒散导致CID小鼠肠道内炎症因子IL-1β、TNF-α、IL-18和IL-6的表达下降,同时降低TLR4/MyD88/NF-κB通路活性。
NLRP3炎性小体是一种细胞内多聚体结构,参与调节炎症反应。在结肠炎模型中,研究表明NLRP3炎性小体的过度激活可以加重炎症反应,损害肠黏膜屏障,参与结肠炎的发生发展[33-34]。本研究发现托里消毒散可以降低致CID小鼠肠道内NLRP3炎性小体的表达。
综上所述,本研究初步探讨了托里消毒散在治疗CID小鼠肠道损伤和炎症反应中的作用机制,通过抑制TLR4/MyD88/NF-κB通路活性和NLRP3炎性小体抑制肠道炎症,进而缓解肠黏膜损伤。托里消毒散有望为5-Fu诱导的CID提供新的治疗策略。
| [1] |
郑荣寿, 张思维, 孙可欣, 等. 2016年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2023, 45(3): 212-220. |
| [2] |
ZHENG R S, CHEN R, HAN B F, et al. Cancer incidence and mortality in China, 2022[J]. Zhonghua Zhong Liu Za Zhi[Chinese Journal of Oncology], 2024, 46(3): 221-231. |
| [3] |
VODENKOVA S, BUCHLER T, CERVENA K, et al. 5-fluorouracil and other fluoropyrimidines in colorectal cancer: past, present and future[J]. Pharmacology & Therapeutics, 2020, 206: 107447. |
| [4] |
BLONDY S, DAVID V, VERDIER M, et al. 5-fluorouracil resistance mechanisms in colorectal cancer: from classical pathways to promising processes[J]. Cancer Science, 2020, 111(9): 3142-3154. DOI:10.1111/cas.14532 |
| [5] |
谷华伟, 刘孟兴, 林明珠, 等. 基于药代动力学参数AUC调整5-FU用量的化疗对晚期结直肠癌患者的影响[J]. 中国肛肠病杂志, 2023, 43(8): 6-9. |
| [6] |
HUANG J H, HWANG A Y M, JIA Y T, et al. Experimental chemotherapy-induced mucositis: a scoping review guiding the design of suitable preclinical models[J]. International Journal of Molecular Sciences, 2022, 23(23): 15434. DOI:10.3390/ijms232315434 |
| [7] |
RIBEIRO R A, WANDERLEY C W, WONG D V, et al. Irinotecan- and 5-fluorouracil-induced intestinal mucositis: insights into pathogenesis and therapeutic perspectives[J]. Cancer Chemotherapy and Pharmacology, 2016, 78(5): 881-893. DOI:10.1007/s00280-016-3139-y |
| [8] |
AKBARALI H I, MUCHHALA K H, JESSUP D K, et al. Chemotherapy induced gastrointestinal toxicities[J]. Advances in Cancer Research, 2022, 155: 131-166. |
| [9] |
BOSSI P, ANTONUZZO A, CHERNY N I, et al. Diarrhoea in adult cancer patients: ESMO clinical practice guidelines[J]. Annals of Oncology, 2018, 29(Suppl 4): iv126-iv142. |
| [10] |
陈实功. 外科正宗[M]. 北京: 中医古籍出版社, 1999: 33-34.
|
| [11] |
杜楠楠, 冯佳梅, 吴雪卿. 简述托里消毒散的现代研究进展[J]. 内蒙古中医药, 2023, 42(2): 108-111. |
| [12] |
宋远瑛, 阚竞, 李悦, 等. 基于TLR4/MyD88/NF-κB信号通路探讨复方银翘合剂缓解哮喘小鼠炎症反应的作用研究[J]. 中医药学报, 2024, 52(1): 14-19. |
| [13] |
SHATZ M, MENENDEZ D, RESNICK M A. The human TLR innate immune gene family is differentially influenced by DNA stress and p53 status in cancer cells[J]. Cancer Research, 2012, 72(16): 3948-3957. |
| [14] |
CARIO E. Toll-like receptors in the pathogenesis of chemotherapy-induced gastrointestinal toxicity[J]. Current Opinion in Supportive and Palliative Care, 2016, 10(2): 157-164. |
| [15] |
周松林, 黄俊卿, 李科, 等. 基于SIRT1/NF-κB通路探究秦艽醇提物对脂多糖诱导大鼠背根神经节神经元炎性损伤的保护作用及机制[J]. 中国老年学杂志, 2024, 44(1): 179-183. |
| [16] |
林梦娴. 基于MAPK/NF-κB信号通路研究竹叶花椒对化疗相关性腹泻小鼠肠粘膜屏障的影响[D]. 成都: 成都中医药大学, 2021.
|
| [17] |
KURITA A, KADO S, KANEDA N, et al. Modified irinotecan hydrochloride(CPT-11) administration schedule improves induction of delayed-onset diarrhea in rats[J]. Cancer Chemotherapy and Pharmacology, 2000, 46(3): 211-220. |
| [18] |
ZHENG Z C, SRINUAL S, CHEN J, et al. Herbal medicines as adjuvants for the treatment of chemotherapy-induced diarrhea[J]. Current Drug Metabolism, 2023, 24(6): 422-433. |
| [19] |
LI M, YANG X Q, CHENG Y F, et al. Equivalence of combined decoction and mixed single decoctions of Gegen Qinlian Decoction in alleviating chemotherapy-associated diarrhea[J]. China Journal of Chinese Materia Medica, 2023, 48(11): 2968-2980. |
| [20] |
CHAN Y T, CHEUNG F, ZHANG C, et al. Ancient Chinese medicine herbal formula Huanglian Jiedu Decoction as a neoadjuvant treatment of chemotherapy by improving diarrhea and tumor response[J]. Frontiers in Pharmacology, 2020, 11: 252. |
| [21] |
郝福明. 托里消毒散研究述评[J]. 中华中医药学刊, 2008, 26(3): 598-599. |
| [22] |
朱卫东. 托里消毒散加味治疗消化性溃疡52例[J]. 时珍国医国药, 2001, 12(3): 240. |
| [23] |
葛艳辉, 叶俏波, 邓豪, 等. 托里消毒散促进溃疡性结肠炎修复作用的研究[A]. //中华中医药学会第十七次中医方剂学术年会论文集[C], 2017: 313-319.
|
| [24] |
ALLAIRE J M, CROWLEY S M, LAW H T, et al. The intestinal epithelium: Central coordinator of mucosal immunity[J]. Trends in Immunology, 2018, 39(9): 677-696. |
| [25] |
VANCAMELBEKE M, VERMEIRE S. The intestinal barrier: a fundamental role in health and disease[J]. Expert Review of Gastroenterology & Hepatology, 2017, 11(9): 821-834. |
| [26] |
SOUGIANNIS A T, VANDERVEEN B N, DAVIS J M, et al. Understanding chemotherapy-induced intestinal mucositis and strategies to improve gut resilience[J]. American Journal of Physiology Gastrointestinal and Liver Physiology, 2021, 320(5): G712-G719. |
| [27] |
DAHLGREN D, SJÖBLOM M, HELLSTRM P M, et al. Chemotherapeutics-induced intestinal mucositis: pathophysiology and potential treatment strategies[J]. Frontiers in Pharmacology, 2021, 12: 681417. |
| [28] |
SANDNER G, MUELLER A S, ZHOU X D, et al. Ginseng extract ameliorates the negative physiological effects of heat stress by supporting heat shock response and improving intestinal barrier integrity: Evidence from studies with heat-stressed caco-2 cells, C. elegans and growing broilers[J]. Molecules, 2020, 25(4): 835. |
| [29] |
XU R, PENG J E, MA Z, et al. Prolonged administration of total glucosides of paeony improves intestinal immune imbalance and epithelial barrier damage in collagen-induced arthritis rats based on metabolomics-network pharmacology integrated analysis[J]. Frontiers in Pharmacology, 2023, 14: 1187797. |
| [30] |
CAO X Y, NI J H, WANG X, et al. Total glucosides of Paeony restores intestinal barrier function through inhibiting Lyn/Snail signaling pathway in colitis mice[J]. Phytomedicine, 2021, 87: 153590. |
| [31] |
LIU C, HE Y X, ZHANG J N, et al. Angelica oil restores the intestinal barrier function by suppressing S100A8/A9 signalling in mice with ulcerative colitis[J]. Phytomedicine, 2023, 108: 154490. |
| [32] |
ADESSO S, RUSSO R, QUARONI A, et al. Astragalus membranaceus extract attenuates inflammation and oxidative stress in intestinal epithelial cells via NF-κB activation and Nrf2 response[J]. International Journal of Molecular Sciences, 2018, 19(3): 800. |
| [33] |
魏祺, 程晓曙. NLRP3炎性小体研究进展[J]. 基础医学与临床, 2015, 35(1): 117-121. |
| [34] |
张坦. NLRP3炎症小体活化机制研究进展[J]. 生命科学, 2023, 35(7): 903-909. |
2. Chengdu University of Traditional Chinese Medicine, Chengdu 610075, China
 2024, Vol. 41
2024, Vol. 41