文章信息
- 范晓旭, 姜斯佳, 冯颖童, 等.
- FAN Xiaoxu, JIANG Sijia, FENG Yingtong, et al.
- 基于NF-κB和STAT3探讨白芍总苷对化学性肝损伤肝阴虚证大鼠的作用机制
- Mechanism of total glucosides of paeony on chemical liver injury rats with liver yin deficiency syndrome based on NF-κB and STAT3
- 天津中医药, 2024, 41(11): 1445-1451
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1445-1451
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.15
-
文章历史
- 收稿日期: 2024-07-05
化学性肝损伤是指包括乙醇、药物、有毒气体、有毒物质等的化学物质引起的肝损伤,常见的临床表现有胁肋胀痛、黄疸、乏力、腹水等症状[1]。“化学性肝损伤”这一疾病名称在中医中没有记载,现代临床医家将化学性肝损伤归为“胁痛”“黄疸”“虚劳”“鼓胀”等范畴。在肝损伤疾病的不同时期表现为不同证型,其中肝阴虚证常见于疾病的中后期,对于肝损伤疾病的转归预后有着重要意义[2]。肝阴虚证的治疗以养阴柔肝,平补肝肾为主,而白芍具有滋养肝阴、平抑肝阳之功。现代临床研究表明白芍能够改善肝功能,治疗肝脏疾病肝阴虚证[3]。白芍总苷(TGP)作为白芍主要的活性成分之一,具有抗炎、镇痛、抗氧化应激、保护肝脏、抗肿瘤等药理作用,对于肝损伤、肝炎、肿瘤疾病有一定治疗作用[4]。
根据中医“阴阳平衡”理论提出化学性肝损伤肝阴虚证的基本病机是邪毒内侵,耗损肝阴,肝阴不足,阴阳失衡,则白芍“滋养肝阴”的特点是“扶阴抑阳”。此外,炎症反应是肝病进程的主要病理学基础,核因子-κB(NF-κB)和信号转导和转录激活因子3(STAT3)在调节促炎细胞因子和抗炎细胞因子释放中发挥重要作用。前期研究发现,TGP对温热中药和四氯化碳(CCL4)诱导的肝阴虚证大鼠的保护作用机制可能与抑制磷脂酰肌醇3激酶(PI3K)/蛋白激酶B(AKT)通路调节炎症反应有关[5]。本研究在此基础上,采用CCL4和甲状腺片建立化学性肝损伤肝阴虚病证结合模型,从NF-κB、STAT3角度深入探究TGP抗肝损伤的机制,揭示肝阴虚证的证候本质和白芍养肝阴的科学内涵。
1 材料 1.1 实验动物雄性SD大鼠,SPF级,共32只,体质量(200 ± 20) g,自北京维通利华有限公司购买,许可证号:SCXK(京)2021-0011。所有大鼠在标准实验室条件下适应性喂养1周,实验室环境为恒温20~24℃,湿度50%~55%和标准通风系统。涉及动物的实验获得北京中医药大学动物伦理委员会批准(编号:BUCM-4-2022092904-3120)。
1.2 药物与试剂白芍饮片,自安国市广盛有限公司购买,批号为20220915;一贯煎原方饮片,从亳州亳草中药材有限公司获得,批号为20221018。甲状腺片,购于上海中华药业有限公司,生产批号为211101,国药准字为H31022151。
CCL4和橄榄油,北京百诺威科技有限公司(批号分别为C11554349、A331D011)。总胆红素(TBIL)试剂盒,北京永泰兴成科技有限公司(批号为CV114D6N3036)。白细胞介素-1受体拮抗剂(IL-1Ra)试剂盒,江苏酶免有限公司(批号为MM-0225R1)。环磷酸腺苷(cAMP)、环磷酸鸟苷(cGMP)、白细胞介素-1(IL-1)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、白细胞介素-10(IL-10)试剂盒,北京华英生物技术研究所(批号分别为20230314、20230314、20230313、20230313、20230313、20230313)。Hipure total RNA Mini Kit,北京欧北科技有限公司(批号为obr4111-02);反转录试剂盒,Thermo Scientific(批号为K1622);SYBR PCR master Mix,Invitrogen(批号为4367659);p-NF-κB p65抗体、β-actin抗体、山羊抗兔二抗、山羊抗小鼠二抗,Proteintech(货号分别为82335-1-RR、66009-1-Ig、SA00001-2、SA00001-1);NF-κB p65抗体,Immunoway(货号为YT3108);p-STAT3抗体,Cell Signaling Technology(货号为9145T);STAT3抗体,Abcam(货号为ab68153)。
1.3 主要仪器冻台,武汉俊杰电子有限公司;烘箱,上海一恒仪器有限公司;酶标检测仪,BioTeK;光学显微镜,日本Olympus;低温高速离心机,Heal Force;紫外分光光度计,Unico;PCR反转录仪,Bio-Rad;实时荧光定量PCR仪,美国ABI公司;电泳仪、扫描仪,CAVOY;化学发光仪,培清科技。
2 方法 2.1 药品制备 2.1.1 白芍总苷制备白芍饮片用水浸泡1 h后煎煮1.5 h,加水量分别为12、10倍,提取2次合并水煎液,通过D-101型大孔吸附树脂柱(饮片与大孔树脂比值为1:1),用70%乙醇洗脱,收集洗脱液,回收乙醇。减压浓缩、干燥,即白芍总苷提取物(出膏率3.45%,芍药苷质量分数44.2%)。
2.1.2 一贯煎制备北沙参、当归、麦冬、生地黄、枸杞子、川楝子饮片分别取9、9、9、20、12、4.5 g,加入药材量6倍水浸泡2 h,随后煎煮30 min。再用3倍水煎煮20 min。将两次滤液合并,浓缩或增加蒸馏水,使一贯煎生药质量浓度达到0.635 g生药/mL。
2.2 分组、模型制备与给药将SD大鼠随机分为空白组、模型组、一贯煎组和白芍总苷组,每组8只。采用腹腔注射20%CCL4橄榄油溶液联合灌胃30 mg/kg甲状腺片造模。除空白组外,其余组给予1.5 mL/kg 20%CCL4橄榄油溶液,每周2次;同时每天给予1次30 mg/kg甲状腺片。造模周期为6周,通过检测大鼠体征、肝功能指标、环核苷酸水平以及肝脏病理变化判断模型是否构建成功。本实验边造模边给药,连续6周。造模期间,空白组、模型组每天灌胃等容量蒸馏水,一贯煎组、白芍总苷组分别灌胃6.35 g/kg一贯煎水煎液和50 mg/kg白芍总苷混悬液(临床上白芍饮片成人用量15 g/d,一贯煎成人用量63.5 g/d)。
2.3 样本收集采用1%戊巴比妥钠麻醉大鼠,随后腹主动脉取血。室温静置4 h,上机4 ℃,3500 r/min离心10 min(离心半径20 cm),收集上清备用。此外,取肝大叶进行分装,一部分放入冻存管,一部分用于固定。
2.4 指标测定 2.4.1 大鼠体征实验过程中记录大鼠体质量和肛温变化;取材前1 d检测大鼠摄水量、饮食量及舌面干湿度。大鼠舌面干湿度检测[6]:将大鼠麻醉,用镊子轻轻拉出大鼠舌头,取pH试纸停留在舌面上20 s,随后使用精密电子天平称体质量并记录。
2.4.2 大鼠血清ALT、AST、γ-GT、ALP、TBIL、TBA、cAMP、cGMP水平采用比色法检测大鼠血清中ALT、AST、γ-GT、ALP、TBIL、TBA的含量变化。采用酶联免疫法,按照试剂盒说明检测大鼠血清cAMP、cGMP含量,计算cAMP/cGMP比值。
2.4.3 Masson染色取部分肝组织,进行常规Masson染色观察肝纤维化程度。
2.4.4 大鼠血清IL-1、IL-6、TNF-α、IL-10、IL-1Ra水平采用酶联免疫吸附测定法,按照试剂盒说明检测大鼠血清IL-1、IL-6、TNF-α、IL-10、IL-1Ra水平。
2.4.5 大鼠肝脏组织NF-κB、STAT3 mRNA表达水平按照Hipure total RNA Mini Kit说明书提取肝脏总RNA,随后反转录试剂盒合成cDNA。采用SYBR PCR master Mix进行扩增,反应条件为95 ℃、10 min;95 ℃、15 s→60 ℃、60 s,40次循环。引物由上海生工生物科技有限公司合成,引物见表 1。
用RIPA裂解液提取肝脏组织总蛋白,并采用BCA试剂盒测蛋白浓度。制备蛋白上样样品,随后进行电泳、电转、封闭,4 ℃一抗孵育过夜。一抗稀释比例为p-NF-κB p65(1:1 000)、p-STAT3(1:2 000)、NF-κB p65(1:2 000)、STAT3(1:2 000)。TBST洗膜3次,每次5 min。加入二抗(1:5 000)室温孵育1 h,同样步骤洗膜。在目的条带上均匀滴加ECL发光液,采用化学发光成像仪显色。最后,Image J软件以β-actin作为内参分析蛋白水平。
2.5 统计学方法计数资料用均数±标准差(x±s)表示,多组间比较采用单因素方差分析(ANOVA),组间比较采用LSD法。数据经SPSS 20.0软件统计分析,P < 0.05为差异有统计学意义。
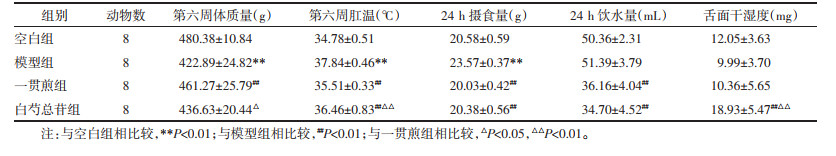
3 结果 3.1 白芍总苷对化学性肝损伤肝阴虚证大鼠体征的影响与空白组相比,化学性肝损伤模型组体质量降低,肛温升高,24 h摄食量升高(P < 0.01),饮水量增加,舌面干湿度降低(P > 0.05)。与模型组相比,给药白芍总苷后体质量升高(P > 0.05),一贯煎给药后体质量明显上升(P < 0.01),给予一贯煎和白芍总苷时肛温均显著下降(P < 0.01),24 h摄食量和24 h饮水量均显著减少(P < 0.01)。白芍总苷组舌面干湿度显著上升(P < 0.01),一贯煎组上升但差异无统计学意义(P > 0.05)。与一贯煎组相比,白芍总苷组体质量降低,肛温升高,舌面干湿度升高(P < 0.05,P < 0.01),而24 h摄食量和饮水量无显著差异(P > 0.05)。见表 2。
|
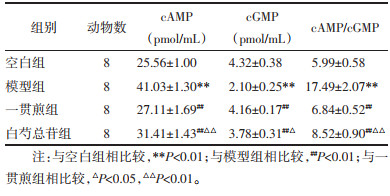
与空白组相比,化学性肝损伤模型组cAMP升高,cGMP下降,cAMP/cGMP上升(P < 0.01);与模型组比较,给予一贯煎和白芍总苷后cAMP降低,cGMP升高,cAMP/cGMP下降(P < 0.01)。与一贯煎组相比较,白芍总苷组cAMP上升,cGMP下降,cAMP/cGMP上升(P < 0.05,P < 0.01)。见表 3。
|
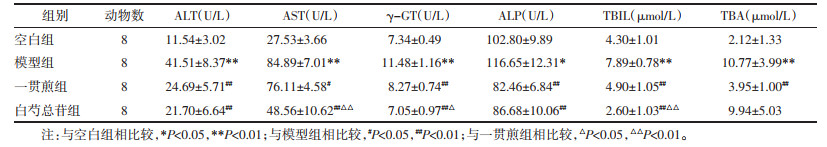
与空白组相比较,化学性肝损伤模型组ALT、AST、γ-GT、ALP、TBIL、TBA含量均显著升高(P < 0.05或P < 0.01);与模型组相比,给药一贯煎和白芍总苷后ALT、AST、γ-GT、ALP、TBIL均下降(P < 0.05或P < 0.01),一贯煎组TBA含量下降(P < 0.01),白芍总苷组TBA含量无明显差别(P > 0.05)。与一贯煎组相比,白芍总苷组AST、γ-GT、TBIL下降(P < 0.05或P < 0.01),而ALT、ALP和TBA差异无统计学意义(P > 0.05)。结果见表 4。
|
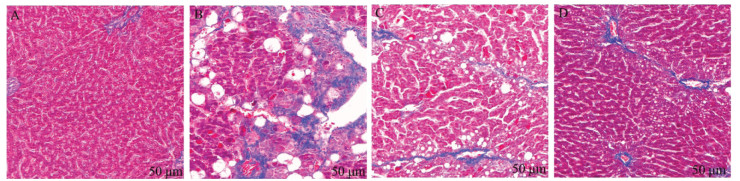
空白组肝组织小叶结构完整、清晰,被染色胶原纤维很少,而化学性肝损伤模型组小叶破坏,汇管区域扩大,胶原纤维含量明显增多,CCL4联合甲状腺片造模导致肝纤维化的形成,当给药一贯煎及白芍总苷后肝组织纤维化程度均改善,延缓了肝纤维化病理进程。此外,一贯煎组与白芍总苷组肝纤维化程度未见明显差异。见图 1。
|
| 注:A,空白组;B,模型组;C,一贯煎组;D,白芍总苷组。 图 1 各组大鼠肝脏Masson染色病理切片(×200) Fig. 1 Masson staining pathological section of liver tissue of rats in each group(× 200) |
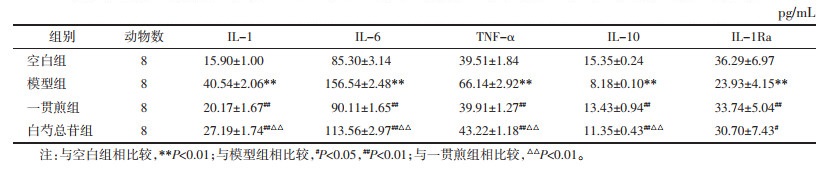
与空白组比较,化学性肝损伤模型组IL-1、IL-6、TNF-α均上升(P < 0.01),IL-10、IL-1Ra水平均降低(P < 0.01);与模型组相比较,一贯煎组及白芍总苷组IL-1、IL-6、TNF-α均下降(P < 0.01),IL-10、IL-1Ra水平上升(P < 0.05或P < 0.01)。与一贯煎组相比,白芍总苷组IL-1、IL-6、TNF-α升高(P < 0.01),IL-10下降(P < 0.01),而IL-1Ra差异无统计学意义(P > 0.05)。见表 5。
|
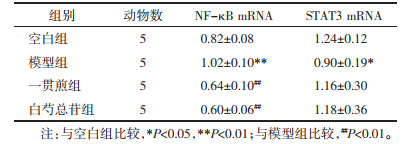
与空白组比较,化学性肝损伤模型组NF-κB mRNA水平上升,STAT3 mRNA水平下降(P < 0.05或P < 0.01);与模型组相比,各用药组NF-κB mRNA表达量均显著降低(P < 0.01),STAT3表达量升高但差异无统计学意义(P > 0.05);与一贯煎组相比,白芍总苷组NF-κB、STAT3 mRNA差异无统计学意义(P > 0.05)。见表 6。
|
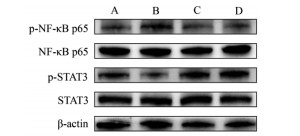
与空白组比较,化学性肝损伤模型组p-NF-κB p65蛋白表达水平显著升高,p-STAT3蛋白表达水平显著降低(P < 0.05)。与模型组相比较,一贯煎组和白芍总苷组p-NF-κB p65蛋白表达量均显著降低(P < 0.05或P < 0.01),而一贯煎组和白芍总苷组p-STAT3蛋白表达量均显著升高(P < 0.05或P < 0.01);与一贯煎组相比,白芍总苷组p-NF-κB p65、p-STAT3蛋白表达差异无统计学意义(P > 0.05)。见表 7,图 2。

|
|
| 注:A,空白组;B,模型组;C,一贯煎组;D,白芍总苷组。 图 2 各组大鼠肝脏p-NF-κB p65、NF-κB p65、p-STAT3、STAT3蛋白印迹图 Fig. 2 Western blot of p-NF-κB p65、NF-κB p65、p-STAT3 and STAT3 in livers of rats in each group |
化学性肝损伤以肝细胞损伤、脂肪变性、脂质过氧化和炎症反应为特征。当肝脏受到炎症损伤时,肝星状细胞过度增殖分泌细胞外基质,可发展为肝纤维化、肝硬化甚至肝癌[7]。肝阴虚证是肝病中后期较为常见的一种证型,采取积极有效的诊疗措施能够抑制肝损伤向肝硬化和肝癌等疾病转变[8]。前期研究采用温热中药结合CCL4构建肝阴虚证模型,发现TGP保护化学性肝损伤肝阴虚证的作用机制可能与抑制PI3K/AKT通路来调节促炎-抗炎因子平衡有关[5],而本研究通过构建CCL4联合甲状腺片模型从NF-κB、STAT3角度继续深入探究TGP对肝阴虚证模型大鼠的作用及机制。
本实验采用20% CCL4橄榄油溶液联合甲状腺片造模,其中甲状腺片灌胃造模易操作,技术成熟,时间较短,成功率较高,已经成为目前研究阴虚证模型最常用的造模方式[9]。当大鼠摄入大量甲状腺素后,造成下丘脑-垂体-甲状腺轴功能紊乱,出现发热、汗出、喜饮、大便干、小便黄、烦躁易怒、基础代谢加快等类似于临床上阴虚证患者的症状表现[10]。此外,CCL4具有肝毒性,常用于诱导动物肝损伤模型,其导致的化学性肝损伤中存在肝阴虚证的可能,该模型常见于保护肝脏与降低酶的新药药理学研究中。所以采用此模型来研究化学性肝损伤肝阴虚证的疾病特点及治疗措施。此外,一贯煎具有滋养肝肾、疏肝理气的功效,临床常应用于具有肝肾阴虚证表现的肝胆疾病。有临床研究显示,一贯煎能够改善肝脏病理结构、炎症反应、促进腹水消退,对肝肾阴虚证候表现的肝硬化有显著临床疗效[11]。此外,药理实验发现,一贯煎通过抗氧化应激、抑制肝星状细胞活化、促进肝细胞再生等治疗肝硬化[12]。从历代医家治疗经验、证候表征的改变以及肝损伤病理状态的改善来看,一贯煎可以从证候表征和理化检测等方面较好地反映复合模型是否建立成功,故选择其作为阳性对照药。
本研究采用环核苷酸水平来量化肝阴虚证候的变化。环核苷酸cAMP、cGMP与中医上的阴阳属性相似,研究表明在细胞反应中cAMP与cGMP的拮抗性调节作用能够用“阴”和“阳”来概括[13]。研究结果表示,肝阴虚证大鼠体质量下降,肛温上升,24 h摄食量和饮水量上升,舌面干湿度下降,cAMP上升,cGMP下降,cAMP/cGMP升高,以上指标变化与肝阴虚证的证候表现一致[13]。肝阴虚证大鼠肝功能指标ALT、AST、ALP、γ-GT、TBIL、TBA等均显著升高,肝脏病理Masson染色显示肝纤维化程度明显增加,这些表明肝损伤肝阴虚证造模成功。同时,给予阳性药一贯煎后大鼠的证候表征改善,而一贯煎是临床常用肝阴虚对证方剂,这也表明该模型构建成功。此外,白芍总苷组这些指标也不同程度地改善,说明白芍总苷对肝阴虚型化学性肝损伤具有较好的保护作用。
细胞因子是通过结合相应受体调节细胞生长分化并调控免疫、炎症反应的一类小分子可溶性多肽。前期申维玺等[14-16]发现细胞因子与中医证有密切关系,阴虚证的本质是细胞因子网络失衡。细胞因子包括促炎因子和抗炎因子两种,其中IL-1、IL-6、TNF-α是促炎因子,IL-10、IL-1Ra是抗炎细胞因子,而促炎因子和抗炎因子又有阴阳属性之分,促进炎症反应的细胞因子属“阳”,抑制炎症反应的细胞因子属“阴”[16]。因此,细胞因子失衡可能是肝阴虚证机体阴阳失衡的具体表现。本实验结果也证实,肝阴虚证化学性肝损伤模型大鼠阴阳失衡,IL-1、IL-6、TNF-α升高,IL-10、IL-1Ra水平下降。给予白芍总苷后,促炎因子IL-1、IL-6、TNF-α下降,抗炎因子IL-10、IL-1Ra上升,这体现了白芍调节促炎细胞因子-抗炎细胞因子平衡的特点。
炎症能引起肝纤维化,并最终导致肝硬化,是慢性肝病发生发展过程中的重要因素[17]。NF-κB是一种核转录因子,在炎症、免疫反应、血管新生、细胞凋亡的调控中发挥重要作用[18]。研究表明,NF-κB与肝纤维化的形成与发展、肝脏慢性炎症密切相关[19]。STAT3是位于胞质中的一种重要的核转录因子,研究发现,激活STAT3能够促进肝细胞增殖,加快肝损伤修复过程[20]。STAT3还能通过激活肝保护性急性期蛋白的表达,增强肝脏对抗化学物质、细菌以及药物等导致的肝损伤能力[21]。此外,研究发现,激活核因子NF-κB能促进促炎因子活化,抑制STAT3表达能降低抗炎因子的释放,从而调节炎症反应[22-23]。由此可见,NF-κB和STAT3在调节促炎细胞因子和抗炎细胞因子释放中发挥重要作用。结果显示,肝阴虚证大鼠促炎因子IL-1、IL-6和TNF-α升高,抗炎因子IL-1Ra和IL-10含量降低,肝脏中NF-κB水平显著上调,STAT3显著下调,从而导致促炎-抗炎失衡。与模型组相比较,白芍总苷组NF-κB的表达显著下调,STAT3表达升高,从而促炎因子IL-1、IL-6、TNF-α均下降,抗炎因子IL-1Ra、IL-10水平上升。促炎因子的减少可能与NF-κB的表达被抑制相关,抗炎因子的释放可能与STAT3的表达被激活相关。
此外,白芍总苷与一贯煎均不同程度逆转模型组体征、环核苷酸水平、肝功能指标、肝脏病理变化、炎性因子、NF-κB和STAT3 mRNA及蛋白的表达,说明一贯煎和白芍总苷均对肝阴虚型化学性肝损伤具有较好的保护作用。不同的是,一贯煎组在升高体质量、降低肛温、改善舌面干湿度、环核苷酸水平、降低促炎因子(IL-1、IL-6、TNF-α)及升高抗炎因子(IL-10)方面略优于白芍总苷组,但白芍总苷组在改善部分肝功能指标(AST、γ-GT、TBIL)优于一贯煎组,其余24 h摄食量、24 h饮水量、肝功能指标(ALT、ALP、TBA),IL-1Ra以及NF-κB和STAT3 mRNA蛋白表达方面,白芍总苷组与一贯煎组无显著差异。
综上所述,白芍总苷能够改善肝阴虚型化学性肝损伤,可能是通过抑制NF-κB信号的激活,升高STAT3的表达从而降低促炎细胞因子分泌,升高抗炎细胞因子释放,有助于恢复肝脏正常生理功能从而达到治疗肝阴虚证的目的,但其具体的调节机制还需进一步深入研究。
| [1] |
王雨欣, 王倩, 田颖. 不同化学物质建立肝损伤动物模型的作用机制[J]. 中国比较医学杂志, 2022, 32(10): 109-114. |
| [2] |
章晨怡. 107例药物性肝损伤患者的临床特点及中医证型研究[D]. 杭州: 浙江中医药大学, 2020.
|
| [3] |
贾岚, 王蕾蕾, 孟靓, 等. 肝阴虚证证候特点及辨证用药规律的文献研究[J]. 世界中医药, 2020, 15(18): 2704-2708. DOI:10.3969/j.issn.1673-7202.2020.18.007 |
| [4] |
杨山景, 封安杰, 孙越, 等. 白芍总苷的药理作用及机制研究进展[J]. 中国现代应用药学, 2021, 38(13): 1627-1633. |
| [5] |
贾岚, 王蕾蕾, 孟靓, 等. 白芍总苷对大鼠化学性肝损伤与肝阴虚证结合模型的影响和机制研究[J]. 中草药, 2020, 51(7): 1885-1892. |
| [6] |
刘文兰, 油红捷, 赵青舟, 等. 肝纤维化大鼠阴虚证表征的观察及一贯煎的干预作用[J]. 中国医药导报, 2015, 12(7): 7-10, 18. |
| [7] |
段小群. 玉郎伞多糖(YLS)抗肝纤维化作用及机制的研究[D]. 南宁: 广西医科大学, 2006.
|
| [8] |
李慧勇, 傅晓晴. 浅析肝阴虚之证治[J]. 吉林中医药, 2006, 26(12): 6-7. |
| [9] |
史莹, 过建春, 荀运浩. 阴虚证动物模型的建立方法及造模思路评析[J]. 中华中医药学刊, 2017, 35(3): 725-727. |
| [10] |
温玉莹, 江涛, 陈艳芬, 等. 蒿甲虚热清颗粒对利血平和甲状腺素致阴虚模型小鼠的影响[J]. 广东药科大学学报, 2018, 34(3): 320-324. |
| [11] |
陈龙, 慕永平, 张华, 等. 一贯煎干预肝硬化作用机制研究进展[J]. 中国实验方剂学杂志, 2020, 26(24): 186-192. |
| [12] |
陈佳美, 慕永平, 刘平. "病-方(效)-证" 的研究实践与创新发展(二): 一贯煎治疗肝硬化的方证病理学基础探析[J]. 上海中医药大学学报, 2023, 37(2): 1-6, 21. |
| [13] |
马露, 王俊峰. 基于cAMP、cGMP分布和比值探析六经辨证阴阳量化指标[J]. 中医临床研究, 2017, 9(27): 4-6. |
| [14] |
申维玺, 孙燕, 刘晓燕, 等. 用现代医学理论阐明阴虚证的本质和发病学机理[J]. 医学与哲学, 2005, 26(13): 67-69. |
| [15] |
申维玺, 孙燕, 张叔人. 肺癌细胞IL-1β、IL-6、TNFα、IFN-γ与肺癌阴虚证相关的免疫组化研究[J]. 中国中医基础医学杂志, 2000, 6(12): 28-31. |
| [16] |
申维玺, 孙燕, 张叔人, 等. 白细胞介素-1等细胞因子与肺阴虚证本质的相关性研究[J]. 中医杂志, 2000, 41(7): 423-425, 8. |
| [17] |
范海燕. 慢性肝病肝胆湿热证患者肝纤维化与炎症因子的关系研究[D]. 石家庄: 河北医科大学, 2004.
|
| [18] |
ZINATIZADEH M R, SCHOCK B, CHALBATANI G M, et al. The Nuclear Factor Kappa B(NF-kB) signaling in cancer development and immune diseases[J]. Genes & Diseases, 2021, 8(3): 287-297. |
| [19] |
HE S L, WANG Y R, LIU J Y, et al. Activating SIRT1 deacetylates NF-κB p65 to alleviate liver inflammation and fibrosis via inhibiting NLRP3 pathway in macrophages[J]. International Journal of Medical Sciences, 2023, 20(4): 505-519. |
| [20] |
KHALIQ M, KO S, LIU Y Z, et al. Stat3 regulates liver progenitor cell-driven liver regeneration in zebrafish[J]. Gene Expression, 2018, 18(3): 157-170. |
| [21] |
QUINTON L J, BLAHNA M T, JONES M R, et al. Hepatocyte-specific mutation of both NF-κB RelA and STAT3 abrogates the acute phase response in mice[J]. The Journal of Clinical Investigation, 2012, 122(5): 1758-1763. |
| [22] |
KALININA E V, SH HASAN A A S, TATARSKIY V V, et al. Suppression of PI3K/Akt/mTOR signaling pathway and antioxidant system and reversal of cancer cells resistance to cisplatin under the effect of curcumin[J]. Bulletin of Experimental Biology and Medicine, 2022, 173(3): 371-375. |
| [23] |
FAN Y H, MAO R F, YANG J H. NF-κB and STAT3 signaling pathways collaboratively link inflammation to cancer[J]. Protein & Cell, 2013, 4(3): 176-185. |
 2024, Vol. 41
2024, Vol. 41