文章信息
- 宋学姣, 林文涵, 庄朋伟, 等.
- SONG Xuejiao, LIN Wenhan, ZHUANG Pengwei, et al.
- 磁石煅制调节肠道菌群-神经递质/炎症因子抗抑郁作用及机制研究
- Research on antidepressant effect and mechanism of magnet processed regulating intestinal microbiota-neurotransmitter/inflammatory factors
- 天津中医药, 2024, 41(11): 1452-1458
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1452-1458
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.16
-
文章历史
- 收稿日期: 2024-08-03
2. 天津中医药大学第一附属医院, 天津 300381;
3. 国家中医针灸临床医学研究中心, 天津 300381
抑郁症是一种具有高发病率、高复发率、高自杀率的精神障碍性疾病,临床主要表现为长时间情绪低落、快感缺失、身倦乏力、对社会活动失去参与感等,严重者可伴随幻觉,甚者有自残、自杀行为,严重影响患者生活质量及生命安全。目前常用的抗抑郁药为第二代抗抑郁药,如氟西汀、西酞普兰、舍曲林、帕罗西汀等[1],其主要机制为增加脑部单胺类神经递质,普遍存在有效率低、成瘾性大、患者依从性差等问题。
抑郁症在中医归属“郁证”“脏躁”等范畴,初期多以气滞为主,气机不畅则肝气郁结而成气郁,气郁可导致痰湿内阻,血行不畅,演变为以肝气郁结为基础的火热证候,疾病经久不愈,由实转虚,日久则有心脾两虚、肾虚肝郁等证。治法当以疏肝解郁、清热化痰、宁心安神、镇惊安神为主[2]。中药磁石是重镇安神常用药,性寒,具有镇惊安神、平肝潜阳等功效[3],多用于心神不宁、惊悸失眠、肾虚气喘等。临床上多用煅磁石组方以治疗产后抑郁、应激焦虑等[4-5],但其抗抑郁作用机制仍未阐明。磁石作为一种矿物药,口服吸收入血成分有限,难以直接发挥抗抑郁样作用。近期研究显示肠道菌群和焦虑、抑郁样行为密切相关,因此本研究重点从肠道菌群、神经递质和炎症角度探讨磁石煅制抗抑郁的作用机制,为煅磁石的临床应用提供理论依据。
1 仪器与材料 1.1 实验动物7周龄Wistar雄性大鼠,体质量(250±10)g,购买于北京维通利华实验动物技术有限公司,许可证号SCXK(京)2021-0006。随机分组以每笼4只密度饲养于天津中医药大学实验动物中心,温度23 ℃,湿度40%~50%,12/12 h昼夜周期,自由进食饮水适应性喂养1周。此动物实验通过天津中医药大学实验动物伦理委员会审批(伦理编号:TCM-LAEC2022221)。
1.2 药品与试剂实验所用药物为天津中医药大学第一附属医院提供的生、煅磁石煎煮浓缩液,该加工品每包10 mL相当于原药材5 g。艾司唑仑片(规格1 mg,山东信谊制药有限公司,批号220604),蔗糖(Solarbio,批号713M0512),多巴胺(DA)标准品(aladdin,批号B2317337),5-羟色胺(5-HT)标准品(aladdin,批号D2327038),去甲肾上腺素(NE)标准品(Solarbio,批号A1110F021),5-羟基吲哚乙酸(5-HIAA)标准品(Solarbio,批号0925A021);普洛麦格总RNA提取试剂盒(LS1040,批号0000546524),天根一步法除基因组cDNA第一链合成预混试剂(KR118,批号X0320)、天根荧光定量试剂盒(FP205,批号Y1710)。
1.3 仪器电子天平(深圳市美孚电子有限公司,MTS1200D),闪光灯(广州捷创舞台灯光设备有限公司,PS108BDY),温度计(瑞斯特电子科技有限公司,RTS-1902),旷场、高架十字迷宫、TopScan Lite动物行为识别分析系统(北京吉安得尔科技有限公司,Topscan lite2.0),组织研磨机(宁波新芝生物科技股份有限公司,Scientz-48L),离心机(eppendorf,Centrifuge 5424 R),核酸分析仪(基因有限公司,NanoDrop One);聚合酶链反应(PCR)扩增仪(Bio-rad T100 Thermal Cycler);实时荧光定量PCR仪(Bio-rad CFX96 Real-time System)。
2 实验方法 2.1 慢性不可预知温和性应激(CUMS)模型建立除空白组外,对其余组大鼠每日进行以下刺激:彻夜光照、拥挤8 h、禁食12 h、禁水12 h、闪光刺激12 h、束缚6 h、湿笼8 h、昼夜颠倒、摇笼5 min、冷水游泳10 min。连续3 d内刺激不重复,造模持续5周。
2.2 动物分组和给药将40只大鼠随机分为空白组(NC)、模型组(MOD)、生磁石组(SCS)、煅磁石组(DCS)、阳性对照组(EZ),每组8只,每笼4只。以人60 kg计,参照《中华人民共和国药典(2020版)》,每日磁石剂量为0.5 g/kg,等效换算为大鼠每日用药剂量为3.15 g/kg;阳性药艾司唑仑每日用药剂量为0.63 mg/kg;灌胃体积1 mL/100 g,空白组和模型组灌胃等体积蒸馏水。造模两周后开始给药,每日光周期结束时给药,连续给药3周。
2.3 行为学检测 2.3.1 糖水偏好实验药物治疗结束后,将大鼠单笼饲养1 d后进行糖水偏好实验。配制2%蔗糖水溶液,第1天给予每只大鼠两瓶糖水,正常进食,第2天将其中1瓶糖水换成饮用水,期间调换两水瓶位置避免位置偏爱。测试前禁水12 h,称量记录每瓶糖水和饮用水质量并标记,测试时给予大鼠1瓶糖水1瓶饮用水,6 h后称质量并记录。糖水偏好率=糖水饮用量/(饮用水饮用量+糖水饮用量)×100%。
2.3.2 旷场实验造模后进行旷场实验,旷场规格50 cm×50 cm×40 cm。测试前使每只大鼠在敞箱中自由活动5 min,测试时将大鼠头朝旷场箱1角放入旷场使其在旷场中活动5 min,应用行为视频分析软件检测大鼠5 min内的行为变化,记录大鼠在旷场中的总路程、中央区域活动路程及停留时间、直立次数等。每只鼠测试完毕用75% 乙醇擦拭旷场擦除异物异味。
2.3.3 高架十字迷宫实验造模结束后暗光环境进行高架十字迷宫实验,迷宫单臂长50 cm,臂宽15 cm,闭臂高30 cm,将大鼠头朝一侧开臂,背对实验者放入迷宫,用行为视频分析软件检测大鼠5 min内的行为,记录大鼠进入开臂的次数和停留时间。每只鼠测试完毕用75% 乙醇擦拭旷场擦除异物异味。
2.4 样品采集与处理行为学检测后,禁食不禁水用代谢笼收集动物8 h内尿液和粪便;禁食12 h后,10%水合氯醛麻醉大鼠后腹主动脉取血,离心后取上清分装;取血后大鼠用生理盐水灌流冲洗至肝脏呈黄白色,冰上取脑,分离海马组织、皮层分别置于无菌微型离心管,保存在-80 ℃以便后续检测。
2.5 脑内神经递质含量检测应用高效液相色谱-电化学系统(HPLC-ECD)检测大鼠皮质单胺类神经递质DA、5-HT、NE、5-HIAA含量。称取100 mg大鼠皮质组织,加入200 μL苯甲酸、800 μL甲醇,用组织研磨机70 Hz,30 s研磨3次,14 000×g离心10 min,取800 μL上清,氮气吹干,-20 ℃保存备用。
HPLC条件:C18反相色谱柱,流动相10%乙腈-90%缓冲盐溶液(辛烷磺酸钠1 mmol/L,乙二胺四乙酸二钠0.01 mmol/L,柠檬酸25 mmol/L,乙酸钠25 mmol/L,冰乙酸40 μL/L),流速1 mL/min,柱温35 ℃,进样量10 μL。
精密称取标准品用甲醇溶解,得14 μg/mL单标溶液,用甲醇稀释至1 400、700、350、175、87.5、43.5、21.875 ng/mL,分别取单标溶液300 μL,得含量为3.5 μg/mL的混标溶液,用甲醇稀释至1 500、1 000、500、250、125、62.5、31.25 ng/mL;氮吹后的组织样品加200 μL甲醇复溶,将标品溶液、组织溶液涡旋2 min,13 000 r/min(离心半径为8.5 cm)离心10 min,取上清到进样小瓶。
2.6 脑内炎性细胞因子含量检测按照RNA提取试剂盒的说明步骤进行操作提取大鼠海马组织RNA,测定RNA浓度,将RNA逆转录为cDNA,对样本cDNA进行扩增,检测海马组织中白介素-18(IL-18)、白介素-6(IL-6)和白细胞介素-1β(IL-1β) mRNA水平。
2.7 肠道微生物检测将2.4中收集的粪便委托上海美吉生物医药科技有限公司进行16S rRNA测序。提取基因组DNA,根据指定测序区域合成特异性引物338F-806R进行PCR扩增,PCR产物用2%琼脂糖凝胶电泳检测,回收PCR产物进行荧光定量检测、Illumina文库构建,Illumina测序序列合格后进行OTU聚类分析和物种分类学分析。相关分析参数有聚类方式:SEARCH11-uparse算法,OTU序列相似度:0.97,物种分类数据库:silva138.1/16s_bacteria,分类置信度:0.7。
2.8 统计学方法使用GraphPad Prism 8.0软件对使用数据进行统计分析并作图,以均数±标准误(Mean ± SEM)表示计量资料,方差齐用单因素方差分析,方差不齐用秩和检验,P < 0.05表示差异有统计学意义。
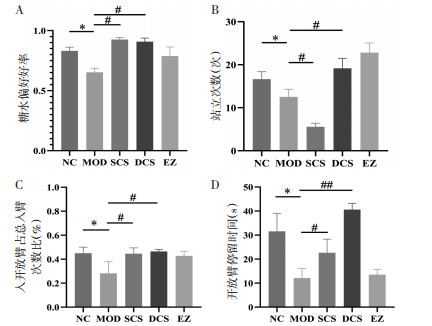
3 结果 3.1 CUMS大鼠焦虑和抑郁样行为比较 3.1.1 糖水偏好率快感缺失是抑郁症的重要表现之一,大鼠对糖水的偏好程度可反映其快感缺失症状及抑郁程度。如图 1A所示,经过5周慢性应激刺激后,与空白组相比,模型组大鼠对糖水的偏好率明显降低(P < 0.05),提示慢性应激导致大鼠快感缺失,出现抑郁症状。给药治疗3周后,与模型组相比,生、煅磁石组大鼠糖水偏好率明显升高(P < 0.05),提示生、煅磁石能改善抑郁大鼠的快感缺失。
|
| 注:A,糖水偏好实验;B,旷场垂直得分;C,高架迷宫开放臂次数比;D,高架迷宫开放臂时间。NC,空白组;MOD,模型组;SCS,生磁石组;DCS,煅磁石组;EZ,艾司唑仑组;n=8。与空白组比较,*P < 0.05;与模型组比较,#P < 0.05,##P < 0.01。 图 1 各组CUMS大鼠焦虑和抑郁样行为比较 Fig. 1 Comparison of anxiety and depression-like behavior of CUMS rats in each group |
抑郁焦虑大鼠因对新环境探索欲望降低,在旷场中表现为活动减少、探究次数减少、修饰行为增加。如图 1B所示,经过5周慢性应激刺激后,与空白组相比,模型组大鼠在旷场中直立次数显著减少(P < 0.05),提示慢性应激导致大鼠出现焦虑抑郁状态;药物治疗3周后,煅磁石组大鼠在旷场中直立次数明显增加(P < 0.05),而生磁组大鼠直立次数显著减少(P < 0.05),提示煅磁石具有改善抑郁大鼠探索行为的作用。
3.1.3 高架十字迷宫对新环境的好奇探索心理和对高悬开放臂恐惧心理的矛盾冲突反映大鼠的焦虑状态。经过5周慢性应激刺激后,与空白组相比,模型组大鼠开放臂的进入次数和停留时间显著减少(P < 0.05),提示慢性应激大鼠探索欲望降低,呈现焦虑状态。给药治疗3周后,生、煅磁石及阳性药组大鼠在高架十字迷宫开放臂的进入次数明显增加(P < 0.05),生、煅磁石组大鼠在开放臂的停留时间明显增长(P < 0.01),提示生、煅磁石均可增加抑郁大鼠的探索欲望。见图 1C和1D。
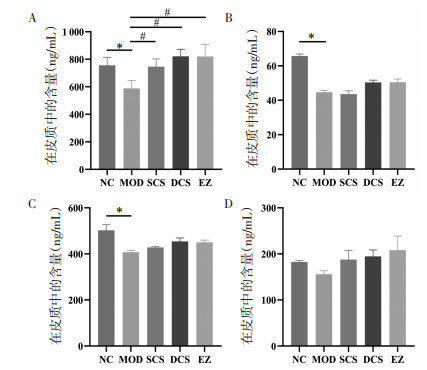
3.2 CUMS大鼠脑内神经递质水平抑郁症的神经递质假说提出5-HT、NE、DA等水平下降会引发神经元间相关神经递质含量减少,引发抑郁。模型组大鼠脑内神经递质NE、5-HT以5-HIAA含量明显降低(P < 0.05),DA含量有降低的趋势,但无显著性差异(P>0.05),提示CUMS大鼠脑内神经递质含量降低;与模型组相比,生、煅磁石及阳性药组大鼠脑内NE含量显著增高升高(P < 0.05),煅磁石及阳性药组大鼠5-HT、5-HIAA以及DA有升高的趋势但无显著性差异(P > 0.05),生磁石组大鼠脑内NE、5-HIAA、DA含量相较模型组有所提高,但较煅磁石和艾司唑仑效果较差,提示煅磁石可增加抑郁大鼠脑内单胺类神经递质含量。见图 2。
|
| 注:A,NE;B,5-HT;C,5-HIAA;D,DA。NC,空白组;MOD,模型组;SCS,生磁石组;DCS,煅磁石组;EZ,艾司唑仑组;n=8。与空白组比较,*P < 0.05;与模型组比较,#P < 0.05。 图 2 各组CUMS大鼠脑内神经递质水平比较 Fig. 2 Comparison of level of neurotransmitters in the brain of CUMS rats in each group |
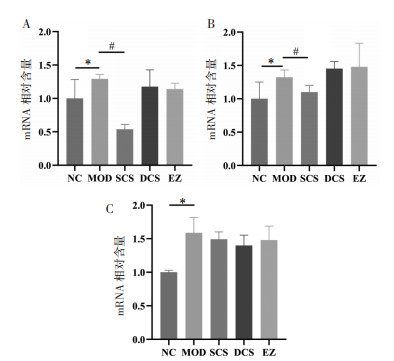
抑郁症患者常伴促炎细胞因子表达升高,一些抗抑郁药在改善抑郁症患者临床症状的同时能调节炎症因子水平。与空白组比较,模型组大鼠海马组织炎症因子IL-18、IL-6、IL-1β mRNA水平显著升高(P < 0.05),提示抑郁大鼠脑内炎症水平增加;与模型组相比,生磁石组大鼠海马组织IL-18、IL-6 mRNA水平显著降低(P < 0.05),而煅磁石和阳性药组大鼠海马组织IL-18、IL-6、IL-1β mRNA水平无明显变化(P>0.05),提示生磁石具有减轻抑郁大鼠脑内炎症的作用。大鼠海马促炎因子实时荧光定量聚合酶链反应(qPCR)结果见图 3。
|
| 注:A,IL-1β;B,IL-6;C,IL-18;NC,空白组;MOD,模型组;SCS,生磁石组;DCS,煅磁石组;EZ,艾司唑仑组;n=8。与空白组比较,*P < 0.05;与模型组比较,#P < 0.05。 图 3 各组CUMS大鼠脑内炎症水平比较 Fig. 3 Comparison of level of inflammation in the brain of CUMS rats in each group |
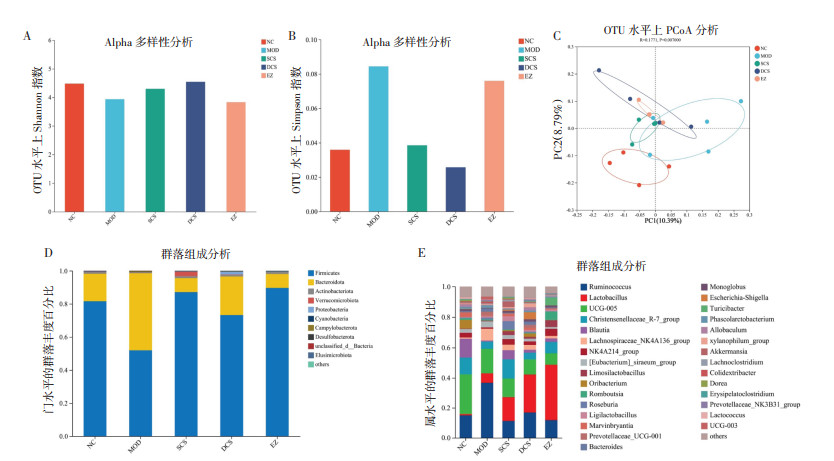
与空白组相比,模型组Shannon指数降低(P < 0.05),Simpson指数升高(P < 0.05),表明CUMS大鼠肠道菌群物种多样性降低;与模型组相比,生、煅磁石给药组大鼠Shannon指数升高(P < 0.05),Simpson指数降低(P < 0.05)(图 4A、B),初步提示生、煅磁石均可增加CUMS大鼠肠道菌群物种多样性。PCoA结果显示(图 4C),各组间样本分离明显,尤其是空白组与模型组大鼠,提示CUMS大鼠肠道菌群紊乱,而生、煅磁石组样本位于空白组与模型组之间,提示生、煅磁石均可部分恢复CUMS大鼠肠道菌群结构。
|
| 注:NC,空白组;MOD,模型组;SCS,生磁石组;DCS,煅磁石组;EZ,艾司唑仑组;n=4。 图 4 CUMS大鼠肠道菌群稳态情况 Fig. 4 Homeostasis of intestinal flora in CUMS rats |
门(Phylum)水平相对丰度分析显示(图 4D),与空白组相比,模型组厚壁菌门丰度显著降低(P < 0.05),拟杆菌门丰度显著升高(P < 0.05);与模型组相比,各给药组大鼠厚壁菌门丰度增加且拟杆菌门丰度降低,提示生、煅磁石均具有调节CUMS大鼠肠道菌群结构的作用。
属(Genus)水平相对丰度分析显示(图 4G),与空白组相比,模型组大鼠肠道菌群中瘤胃球菌属(Ruminococcus)丰度增加,克里斯滕森菌科的Christensenellaceae_R-7_group、毛螺菌科的经黏液真杆菌属(Blautia)、瘤胃球菌科的NK4A214_group、罗伊氏乳杆菌(Limosilactobacillus)等菌属相对丰度减少;与模型组相比,各给药组大鼠肠道菌群向空白组大鼠肠道菌群回调,其中,生磁石组大鼠肠菌中Christensenellaceae_R-7_group、NK4A214_group、罗氏菌属(Roseburia)等相对丰度显著升高,煅磁石组大鼠肠菌中乳杆菌(Lactobacillus)、罗伊氏乳杆菌(Limosilactobacillus)、拟杆菌属(Bacteroides)等相对丰度显著升高,提示生、煅磁石均具有维持CUMS大鼠肠道菌群失调的作用,其中生磁石对NK4A214_ group、罗氏菌等调节作用显著,煅磁石对调节乳杆菌、拟杆菌等调节作用显著。
4 讨论本研究采用CUMS诱导抑郁模型探讨了磁石的煅制对抑郁大鼠行为学指标、神经递质及炎症因子的影响,并通过16S rRNA测序检测生、煅磁石对抑郁大鼠肠道菌群稳态的影响。结果表明CUMS造模使动物长期处于压力状态,造成大鼠焦虑抑郁样行为发生,脑部神经递质水平下降,炎症因子水平上升,肠道菌群的组织和结构发生改变,抑郁大鼠肠菌中有益菌比例减少、有害菌比例升高。生、煅磁石给药治疗后改善了大鼠焦虑和抑郁样行为,其中煅磁石增加乳酸杆菌、罗氏菌等菌的相对丰度,提高了抑郁大鼠脑内神经递质水平,生磁石增加了克里斯滕森菌科等的相对丰度,降低了抑郁大鼠脑部促炎因子水平。
据世界卫生组织报告,抑郁症已成为威胁人类健康的第4大疾病,新型冠状病毒疫情导致全球抑郁症发病率大幅上升了28%。《2022国民抑郁症蓝皮书》数据显示,中国成人抑郁障碍终生患病率为6.8%,其中抑郁症为3.4%,抑郁症发病群体呈年轻化趋势,其中压力成为引发抑郁症的主要社会环境因素,每年自杀身亡人数中40%人群患有抑郁症。然而抑郁症的治疗存在诸多困难,疗效显著、使用方便、不良反应小的抗抑郁药物是当前关注的热点之一。
磁石是重镇安神的常用药,主要药效成分为四氧化三铁,磁石块去除杂质敲碎后直接使用为生磁石,醋煅淬后为煅磁石,是临床上常用药物。研究表明,磁石煅淬后铁元素的溶出增加,而镉、砷、铅等重金属溶出明显降低[6],而生磁石中锌、锰、钴、钙元素含量较高[7]。磁石古今用药多有生、煅之分,王丕明等[8]探究煅淬对磁石药理作用的研究发现,煅磁石在镇静、镇痛和中枢抑制等方面优于生磁石,王汝娟等[9]通过灌胃磁石混悬液发现生磁石在注射角叉菜胶导致足部肿胀中具有较好的抗炎作用。
研究对生、煅磁石灌胃给药后的CUMS大鼠进行了粪便微生物检测,16S rRNA测序表明,磁石在通过影响肠道菌群改善抑郁症状方面与阳性药艾司唑仑影响的肠道菌群组成不同,其作用机制也可能不相同。研究表明,抑郁症患者的菌群丰度和多样性都有所下降[10],研究者采用不同分类标准、算法等均表明抑郁症患者与健康个体的肠道菌群存在差异,总体上以抑郁患者肠道内有益菌的减少和有害菌的增加为主[11-12]。对各组大鼠粪便的16S rRNA测序结果显示,CUMS造模导致大鼠肠道菌群比例失调,拟杆菌门/厚壁菌门比值增加,这与对抑郁症患者肠道菌群的检测结果是一致的[13]。
抑郁症的单胺假说认为,中枢神经系统中5-HT、NE、DA水平下降会引发神经元间相关神经递质含量减少,引发抑郁。肠道菌群可以合成并释放多种神经递质和神经肽,同时分泌细菌素和支链氨基酸或短链脂肪酸等物质,以调节机体神经递质、细胞因子水平等。煅磁石干预升高了乳酸杆菌、瘤胃球菌、罗氏菌、拟杆菌等菌群的相对丰度,这些肠道菌群能够产生乙酸、丙酸、丁酸等短链脂肪酸(SCFA),SCFA能够透过血脑屏障入脑,是连接肠道菌群-肠-脑轴的重要信号分子[14],SCFA能够提高5-HT等神经递质的合成[15-16],缓解抑郁样行为。有研究对比健康小鼠和灌胃抑郁症小鼠粪便菌群的小鼠海马神经递质含量,抑郁菌群组小鼠海马处5-HT、DA和NE水平显著降低[17],表明抑郁患者肠道的微生物群能够降低海马内神经递质的水平,引发抑郁焦虑行为。同时,SCFA特别是乙酸,能够影响结肠运动,减少TNF-α、IL-6和IL-1β等炎症因子的产生[18]。抑郁症的细胞因子假说表明,免疫系统的过度激活以及细胞因子的分泌失衡与抑郁症的病理机制密切相关。已有研究表明,长期压力状态会大量减少肠道乳酸菌含量,促进肠道γδT细胞的增殖/分化,并迁移至大脑,进而导致抑郁神经行为学的发生[19],本实验结果表明,长期的慢性不可预知温和刺激可使大鼠表现出快感缺失、探索行为减少、绝望无助水平增加的抑郁样行为,同时肠道菌群中乳酸杆菌占比下降。克里斯滕森菌科(Christensenellaceae)在克罗恩病和结肠炎中比例下降甚至耗尽[20-21],肠道菌群物种差异分析显示,生磁石组大鼠肠道菌群中克里斯滕森菌科(Christensenellaceae)比例高于煅磁石组,可能与生磁石组抗炎效果优于煅磁石相关。
综上所述,CUMS造模引起大鼠脑部炎症因子升高、神经递质降低,导致大鼠抑郁,而给与生、煅磁石干预后能够作用于肠道菌群进而降低大鼠炎症因子水平,回调神经递质含量,改善抑郁行为。然而本研究并未对肠道菌群-脑轴的作用机制进行进一步的研究验证,磁石等矿物药的生、煅应用在治疗神经精神疾病的药效研究及其作用机制仍需更全面地研究总结。
| [1] |
王琳, 张兴军, 金黎明, 等. 抗抑郁药物的研究进展[J]. 化学世界, 2022, 63(2): 83-93. |
| [2] |
过伟峰, 曹晓岚, 盛蕾, 等. 抑郁症中西医结合诊疗专家共识[J]. 中国中西医结合杂志, 2020, 40(2): 141-148. |
| [3] |
国家药典委员会. 中华人民共和国药典-一部: 2020年版[M]. 北京: 中国医药科技出版社, 2020.
|
| [4] |
高艳敏, 周晶晶, 金涛. 金涛从心肝论治产后抑郁经验[J]. 黑龙江中医药, 2014, 43(4): 31-32. |
| [5] |
陈慧, 汪受传. 汪受传教授辨治儿童焦虑障碍经验[J]. 浙江中医药大学学报, 2022, 46(11): 1241-1243. |
| [6] |
傅兴圣, 刘训红, 田金改, 等. 磁石炮制前后的理化分析[J]. 药物分析杂志, 2012, 32(3): 483-487. |
| [7] |
朱武成, 黄寅墨, 王汝娟, 等. 生煅磁石微量元素含量与药理作用比较[J]. 微量元素与健康研究, 1998, 15(1): 40-49. |
| [8] |
王丕明, 高丽新, 张府君, 等. 煅淬对磁石药理药效的影响[J]. 中国处方药, 2018, 16(12): 35-36. |
| [9] |
王汝娟, 黄寅墨, 朱武成, 等. 生、煅磁石药理作用比较[J]. 中草药, 1997, 28(4): 223-225. |
| [10] |
ZHANG M, LI A Q, YANG Q F, et al. Beneficial effect of alkaloids from Sophora alopecuroides L. on CUMS-induced depression model mice via modulating gut microbiota[J]. Frontiers in Cellular and Infection Microbiology, 2021, 11: 665159. DOI:10.3389/fcimb.2021.665159 |
| [11] |
王艳, 卢静, 龙小花, 等. 基于高通量测序研究大学生抑郁人群肠道菌群的多样性[J]. 生物技术, 2023, 33(4): 458-465. |
| [12] |
JIANG R Y, WANG Y Y, LIU J B, et al. Gut microbiota is involved in the antidepressant effects of adipose-derived mesenchymal stem cells in chronic social defeat stress mouse model[J]. Psychopharmacology, 2022, 239(2): 533-549. |
| [13] |
LIU L X, WANG H Y, CHEN X Y, et al. Gut microbiota and its metabolites in depression: From pathogenesis to treatment[J]. eBio Medicine, 2023, 90: 104527. |
| [14] |
黄梦丽, 张亭亭, 薛瑞, 等. 肠道菌群调节神经递质影响抑郁症的研究进展[J]. 军事医学, 2021, 45(3): 229-233. |
| [15] |
朱慧越, 邹仁英, 许梦舒, 等. 短链脂肪酸-酰化淀粉对小鼠抑郁样行为的缓解及机制[J]. 食品与发酵工业, 2021, 47(6): 26-33. |
| [16] |
HORVATH T D, IHEKWEAZU F D, HAIDACHER S J, et al. Bacteroides ovatus colonization influences the abundance of intestinal short chain fatty acids and neurotransmitters[J]. iScience, 2022, 25(5): 104158. |
| [17] |
谢雅静. 肠道菌群在抑郁症发生与治疗中的作用及机制研究[D]. 济南: 齐鲁工业大学, 2023.
|
| [18] |
ZHAO C J, BAO L J, QIU M, et al. Commensal cow Roseburia reduces gut-dysbiosis-induced mastitis through inhibiting bacterial translocation by producing butyrate in mice[J]. Cell Reports, 2022, 41(8): 111681. |
| [19] |
ZHU X L, SAKAMOTO S, ISHⅡ C, et al. Dectin-1 signaling on colonic γδ T cells promotes psychosocial stress responses[J]. Nature Immunology, 2023, 24(4): 625-636. |
| [20] |
KENNEDY N A, LAMB C A, BERRY S H, et al. The impact of NOD2 variants on fecal microbiota in Crohn's disease and controls without gastrointestinal disease[J]. Inflammatory Bowel Diseases, 2018, 24(3): 583-592. |
| [21] |
LEE T, CLAVEL T, SMIRNOV K, et al. Oral versus intravenous iron replacement therapy distinctly alters the gut microbiota and metabolome in patients with IBD[J]. Gut, 2017, 66(5): 863-871. |
2. First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China;
3. National Clinical Research Center for Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China
 2024, Vol. 41
2024, Vol. 41