文章信息
- 王平, 孙文娟, 潘保朝, 等.
- WANG Ping, SUN Wenjuan, PAN Baochao, et al.
- 基于NLRP3通路研究金樱子抑制肾小管上皮细胞间质化治疗糖尿病肾病的作用机制
- Study on the mechanism of Rosa laevigata Michx inhibiting epithelial mesenchymal transformation in the treatment of diabetes nephropathy based on NLRP3 Pathway
- 天津中医药, 2024, 41(11): 1468-1474
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1468-1474
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.18
-
文章历史
- 收稿日期: 2024-08-12
糖尿病肾病(DN)是糖尿病(DM) 最常见的微血管并发症之一。在中国,DM病变的发病率在过去10年中急剧增加,而20% ~ 40%的DM患者会发展为DN[1]。因此,寻找安全可靠的药物来进行早期干预以阻断或延缓DN病变进展已成为该领域的研究热点之一。
DN的发病机制目前尚未明确,既往研究认为与遗传、高血压病、高血糖、血流动力学、氧化应激、炎症反应、血管活性物质代谢紊乱等有关[2]。临床上以水肿、血压升高和蛋白尿为主要表现[3]。目前治疗DN的方法主要包括控制血糖、降血压、改善微循环等方面[4]。然而这些治疗方法并不能阻止DN的进展,降压药等一系列西药还会对患者产生不良反应[5]。近年来,中医药在改善DN临床症状和延缓疾病进展中有明显的优势[6]。因此,研究中药对DN的保护机制成为了目前研究的新方向。
金樱子性平,味酸涩,归肾经、膀胱经和大肠经。具有固精缩尿止带、涩肠止泻、补虚固涩的功效[7]。金樱子作为一种传统药食两用植物,含有丰富的营养成分,如维生素C、花青素、黄酮类化合物等。通过研究金樱子单药,可以为开发具有特定健康功效的天然食品提供科学依据,同时有助于更准确地评估金樱子的药理学特性,避免了复方制剂中多种成分可能引起的作用机制混淆,为后续的复方制剂或提取物的开发提供基础数据[8]。临床研究表明,金樱子对DN疗效显著[9],然而其作用机制未明。本研究以高脂饲料喂养联合腹腔注射链脲佐菌素(STZ)诱导的DN模型小鼠为研究对象,首先评估金樱子的治疗作用;其次研究金樱子对小鼠肾小管上皮细胞间质化(EMT)和核苷酸结合寡聚化结构域样受体蛋白3(NLRP3)信号通路的影响,初步揭示其机制。
1 材料 1.1 动物选用雄性C57/BL小鼠60只,体质量(20±2) g,饲养环境保持在相对湿度50%~70%,温度25 ℃,自然昼夜节律。小鼠购自北京华阜康生物科技股份有限公司[生产许可证号:SCXK(京)2019-0008]。动物经河北省沧州中西医结合医院伦理委员会批准(伦理编号:CZX2023-KY-090)
1.2 药品与试剂金樱子购自沧州中西医结合医院;STZ(货号S8050);尿素氮(BUN,批号C013-2-1);肌酐(Cr,批号C011-2-1);成熟的白细胞介素-1β(mature IL-1β,货号ab283818)购于abcam;活化的半胱氨酸天冬氨酸蛋白酶1(cleaved Caspase-1,货号22915-1-AP);凋亡相关斑点样蛋白(ASC,货号bs-1185R);NLRP3(货号bs-10021R);成熟的白细胞介素-18(mature IL-18,货号bs-4986R);上皮性钙黏附蛋白(E-CDH,货号bs-10009P)波形蛋白(VIM,货号bs-23063R);α-平滑肌肌动蛋白(α-SMΑ,货号bsm-52392R);转化生长因子β(TGF-β,货号bsm-33345M)均购于博奥森生物有限公司;β-肌动蛋白(β-actin,货号20536-1-1AP)购于proteintech公司。
1.3 金樱子水提物制备由实验室将金樱子药材制备为1 g/mL的水提物备用。
2 方法 2.1 DN模型的制备在将小鼠进行1周的适应性喂养后,选取50只小鼠用于制备DN模型。给予高糖高脂饲料(10%猪油、20%蔗糖、2.5%胆固醇、67.5%常规饲料)8周。于第8周末,禁食不禁水12 h后,腹腔注射STZ 120 mg/kg(溶于0.1 mol/L柠檬酸钠缓冲液,pH=4.5)。在正常组中腹腔注射等体积的1%柠檬酸钠缓冲液。在注射后的72 h,通过尾静脉采血测定小鼠的随机血糖水平。以血糖≥16.7 mmol/L为2型糖尿病(T2DM)成模标准。之后继续喂养,每周检测小鼠24 h尿蛋白含量。以血糖水平≥16.7 mmol/L、尿糖呈阳性、尿蛋白阳性,作为DN模型建立标准。
2.2 分组及给药根据随机数表法,将造模后的小鼠分为模型组、MCC950组[10](腹腔注射10 mg/kg)和金樱子低、中、高剂量组(灌胃2.5、5、10 g/kg),每组10只。在正常组和模型组中,给予等体积的生理盐水灌胃,每日1次。各组均连续干预8周。
2.3 生化指标检测金樱子干预8周后,使用代谢笼收集各组小鼠24 h尿液,4 000 r/min离心10 min,离心半径为10 cm(下同)。按照试剂盒说明书检测24 h尿蛋白的含量。
目内眦取血,将收集到的血液以3 000r/min离心15 min,收集血清,按照试剂盒说明书检测各组小鼠血清中Cr、BUN水平。
2.4 肾组织苏木精-伊红(HE)病理学染色金樱子干预8周后,使用4%多聚甲醛固定液对取出的新鲜小鼠肾脏组织进行固定,固定不少于48 h然后经乙醇脱水、二甲苯透明化、石蜡包埋后,制成5 μm厚的冠状切片,再经二甲苯与乙醇脱水,然后进行苏木素染色,氨水返蓝,伊红染色,最后风干封片,光学显微镜下观察组织结构。
2.5 肾组织过碘酸-Schiff(PAS)病理学染色将小鼠肾组织石蜡切片,二甲苯脱蜡至水。阿利新蓝染色液染色15 min,入过碘酸溶液氧化5 min,Schiff Reagent浸染15 min,Leagene苏木素染色液染核1 min,酸性分化液分化3 s,Scott蓝化液返蓝。每个步骤后均蒸馏水洗,然后逐级常规乙醇脱水,二甲苯透明,中性树胶封片,显微镜下观察。
2.6 实时定量聚合酶链反应(qPCR)通过qPCR,从肾脏组织中提取总RNA后,确定Cdh1、Vim、Acta、Tgfb的mRNA的肾脏表达。引物序列见表 1。mRNA的表达相对于Actb。以2-ΔΔCT法计算相对表达量。
采用Western blot法检测肾组织中NLRP3炎症小体以及小鼠肾小管上皮细胞EMT相关蛋白NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18、E-CDH、VIM、α-SMA、TGF-β的水平。取20 mg冻存的小鼠肾脏组织,加入250 μL的高效组织RIPA裂解缓冲液,使用超声破碎仪在冰上对裂解的组织进行破碎匀浆。之后低温离心收集上清,并用BCA蛋白测定试剂盒测定总蛋白浓度。应用电泳对蛋白进行分离,将其转移至PVDF膜上,在室温下用5%脱脂奶粉封闭2 h并取出。取出后,将不同的一抗NLRP3(稀释比例1:2 000)、ASC(稀释比例1:2 000)、cleaved Caspase-1(稀释比例1:2 000)、mature IL-1β(稀释比例1:1 000)、mature IL-18(稀释比例1:2 000)、E-CDH(稀释比例1:4 000)、VIM(稀释比例1:10 000)、α-SMA(稀释比例1:5 000)、TGF-β(稀释比例1:500)、β-actin(稀释比例1:10 000)加入其中,4 ℃孵育过夜。洗膜后加入对应的二抗(稀释比例按1:20 000),在室温下孵育2 h,TBST洗膜后,加入ECL化学发光法显影检测,扫描电泳条带图像,以β-actin为内参检测蛋白表达。应用Image J软件进行量化后,计算目的蛋白相对表达量。
2.8 统计学方法数据统计分析使用SPSS Statistics 19.0软件,对符合正态分布的计量资料采用t检验,并以均数±标准差(x±s)表示,组间资料比较使用t检验,P<0.05为差异具有统计学意义。
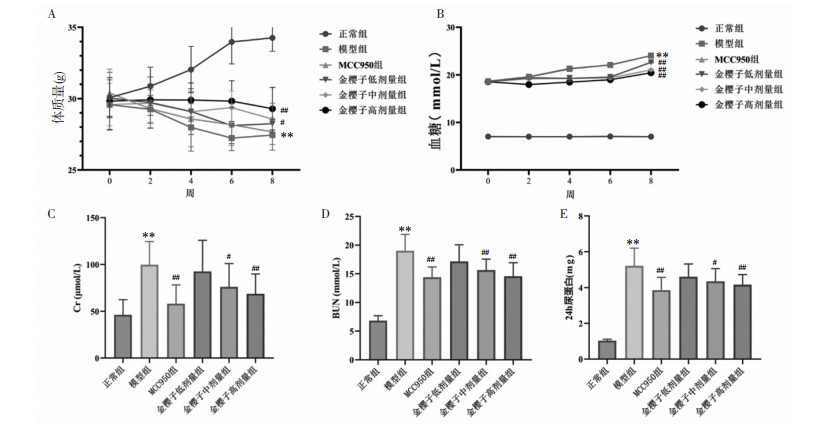
3 结果 3.1 体质量、血糖及肾功能从给药开始,每周动态观察各组小鼠体质量和血糖的变化。给药结束后,与正常组相比,模型组体质量明显下降;与模型组相比,金樱子中、高剂量组小鼠体质量显著增加(P<0.05或P<0.01)。与正常组相比,模型组空腹血糖显著升高;与模型组相比金樱子低、中、高剂量组小鼠空腹血糖显著降低(P<0.01)。见图 1A、1B。肾功能检测结果显示,与正常组相比,模型组小鼠血清中Cr、BUN水平以及24 h尿蛋白定量显著升高(P<0.01);与模型组相比,MCC950及金樱子中、高剂量干预可显著降低DN小鼠血清Cr(P<0.05或P<0.01)、BUN(P<0.01)水平以及24 h尿蛋白定量(P<0.05或P<0.01)。见图 1C、1D、1E。
|
| 注:与正常组相比,**P<0.01;与模型组相比,#P<0.05,##P<0.01。 图 1 造模给药后各组小鼠体质量、血糖、肾功能指标变化 Fig. 1 Changes in body weight, blood sugar and renal function indexes of mice in each group after modeling and drug administration |
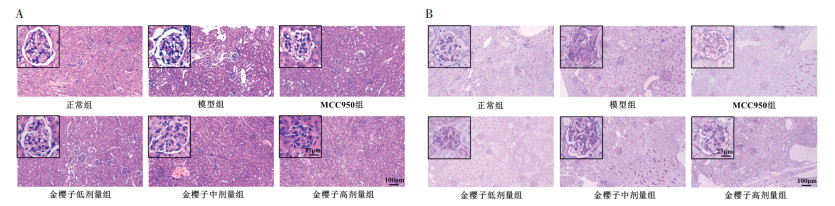
根据HE染色结果显示,正常组小鼠肾组织细胞大小平均,形态规则,肾小球结构显示正常。与正常组相比,模型组小鼠的肾组织结构明显异常,肾组织细胞大小、形态均不规则,肾小球结构受损,且细胞排列较为杂乱,肾小管严重扩张,胞质显示不完整,间质中有炎症细胞浸润。与模型组相比,各给药组的肾组织受损程度较轻。肾组织细胞结构较为完整,细胞大小、形态较规则,细胞排列较为整齐,炎症细胞浸润减少。见图 2A。
|
| 注:A,各组小鼠病理学变化(×100);B,各组小鼠病理学变化(×400)。 图 2 造模给药后各组小鼠病理学的变化 Fig. 2 Pathological changes of mice in each group after modeling and drug administration |
根据PAS染色结果显示,正常组小鼠的肾脏结构无明显病理变化;模型组肾小叶中央可见PAS染色阳性物质,基底膜增厚,系膜基质增多,肾小球呈现弥漫性病变;与模型组相比,各给药组肾脏的PAS染色呈弱阳性,可见弥漫性肾小球硬化,无基底膜增厚及肾小管病变。见图 2B。
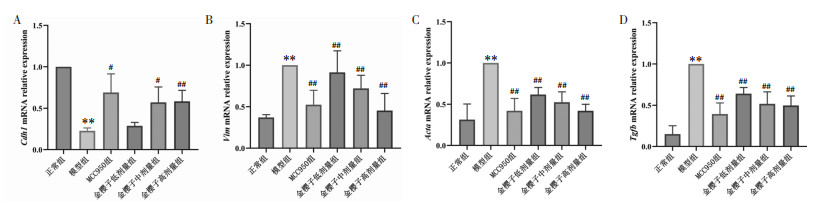
3.3 肾组织中EMT相关基因表达及蛋白水平运用qPCR检测了小鼠肾组织中EMT相关基因的表达,结果显示,与正常组相比,模型组小鼠肾组织中Cdh1的mRNA相对表达量降低,Vim、Acta、Tgfb的mRNA相对表达量增加(P < 0.01)。与模型组相比,MCC950组Cdh1的mRNA相对表达量升高(P < 0.05),Vim、Acta、Tgfb的mRNA相对表达量均有所降低(P < 0.01);金樱子低剂量组Vim、Acta、Tgfb的mRNA相对表达量均有所降低(P < 0.01);金樱子中剂量组Cdh1的mRNA相对表达量升高(P < 0.05),Vim、Acta、Tgfb的mRNA相对表达量均有所降低(P < 0.01);金樱子高剂量组Cdh1的mRNA相对表达量升高(P < 0.01),Vim、Acta、Tgfb的mRNA相对表达量均有所降低(P < 0.01)。见图 3。
|
| 注:与正常组相比,**P<0.01;与模型组相比,#P<0.05,##P<0.01。 图 3 肾组织中EMT相关基因表达 Fig. 3 Expression of EMT-related genes in renal tissue |
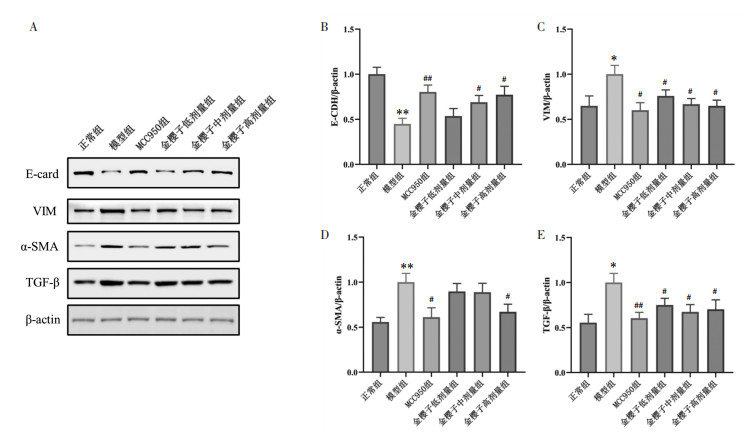
此外,运用Western-blot检测了小鼠肾组织中EMT相关蛋白的水平。结果显示,与正常组相比,模型组小鼠肾脏中E-CDH显著降低(P < 0.01),VIM、α-SMA、TGF-β水平显著升高(P < 0.01或P < 0.05);与模型组相比,MCC950组E-CDH显著升高(P < 0.01),VIM、α-SMA、TGF-β水平显著降低(P < 0.05或P < 0.01);金樱子低剂量组VIM、TGF-β水平显著降低(P < 0.05);金樱子中剂量组E-CDH显著升高(P < 0.05),VIM、TGF-β水平显著降低(P < 0.05);金樱子高剂量组E-CDH显著升高(P < 0.05),VIM、α-SMA、TGF-β水平显著降低(P < 0.05)。见图 4。
|
| 注:与正常组相比,*P < 0.05,**P<0.01;与模型组相比,#P<0.05;与模型组相比,##P<0.01。 图 4 肾组织中EMT相关蛋白表达 Fig. 4 Expression of EMT-related proteins in renal tissue |
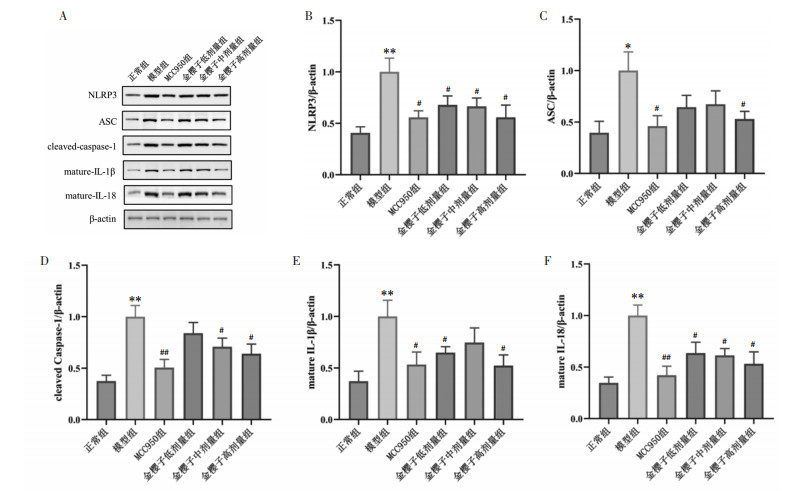
通过检测小鼠肾脏中NLRP3信号通路关键因子NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18蛋白水平。结果显示,与正常组相比,模型组小鼠肾脏中NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18水平显著升高(P < 0.05或P < 0.01),与模型组相比,MCC950组小鼠肾脏NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18水平显著降低(P < 0.05或P < 0.01);金樱子低剂量组小鼠肾脏mature IL-1β、mature IL-18水平显著降低(P < 0.05)、金樱子中剂量组小鼠小鼠肾脏NLRP3、cleaved Caspase-1、mature IL-18水平显著降低(P < 0.05);金樱子高剂量组小鼠肾脏NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18水平显著降低(P < 0.05)。见图 5。
|
| 注:与正常组相比,*P < 0.05,**P<0.01;与模型组相比,#P<0.05,##P<0.01。 图 5 肾组织NLRP3通路相关蛋白表达 Fig. 5 Expression of NLRP3 pathway-related proteins in renal tissue |
EMT与DN的发生发展密切相关[11],是指上皮细胞受到各种病理生理刺激,失去上皮表型,获得新的间质表型,转分化后的细胞侵袭迁移至间质区域,分泌细胞外基质,促进纤维化发生的过程[12]。上皮细胞经过形态和功能变化,上皮标志物如E-CDH下调,获得间充质表型,间充质标志物如α-SMA和VIM上调,增加迁移和侵袭能力,增加细胞外基质成分产生,促进组织纤维化发生[13]。而TGF-β是肾纤维化发生过程中的必需因子,长期高糖环境会导致TGF-β基因、蛋白表达上调,诱导肾小管EMT发生,且通过多种途径调控EMT过程[14]。
研究发现,NLRP3炎症小体参与DN的发生发展 [15-17]。NLRP3炎症小体是NLRP3、ASC和Caspase-1组成的大分子蛋白复合物。NLRP3在细胞内作为受体蛋白,与接头蛋白ASC组装,从而招募Caspase-1,使其自剪成cleaved Caspase-1。cleaved Caspase-1会对IL-1β和IL-18的前体pro IL-1β和pro IL-18进行切割,使其成熟并释放到胞外,介导炎症的级联反应。同时cleaved Caspase-1通过切割介导细胞焦亡的成孔蛋白(GSDMD),生成肽段GSDMD-N,并使后者发生多聚化并在细胞膜上形成孔道,大量成熟的炎性因子IL-1β和IL-18可经此通道释放至细胞外,扩大炎症反应[18-20]。在DN发生发展过程中,持续高血糖诱导肾脏慢性炎症反应,其释放的炎症因子作为启动信号被细胞表面的TLR识别并激活NF-κB,促进NLRP3炎症小体的组装,导致IL-1β、IL-18等炎性因子释放至胞外促进炎症反应和肾小管间质纤维化进一步加重疾病发展[21-22]。研究发现,在基因敲除NLRP3和ASC的小鼠肾小管上皮细胞模型中,通过TGF-β干预后,细胞中Smad2和Smad3的磷酸化水平较正常组显著降低,提示NLRP3具有放大TGF-β信号的作用[23]从而加速诱导EMT。MCC950是一种明确的NLRP3炎性小体抑制剂,多项研究表明MCC950可以通过抑制NLRP3炎症小体减轻炎症反应,缓解DN小鼠肾组织损伤 [24]。
本研究在明确金樱子治疗作用的基础上,进一步通过检测EMT及NLRP3炎症小体相关表达发现,金樱子干预后E-CDH表达升高,α-SMA、VIM和TGF-β表达降低,这提示金樱子可以延缓DN小鼠肾组织EMT过程。同时,金樱子降低了肾组织中IL-1β和IL-18的水平,NLRP3、ASC、cleaved Caspase-1、mature IL-1β、mature IL-18表达。综上所述,金樱子可以通过减轻肾组织中EMT过程以及抑制NLRP3炎症小体活化达到延缓DN的目的。
| [1] |
俞烨晨, 王旭, 杨帆, 等. 益肾健脾通络方调节Th17/Treg失衡改善DKD小鼠肾损伤的作用机制研究[J]. 中药材, 2024, 47(3): 713-718. |
| [2] |
田冬琴, 刘开翔, 谢席胜. 糖尿病肾病发病机制、诊断与治疗的研究新进展[J]. 中国中西医结合肾病杂志, 2018, 19(10): 931-934. DOI:10.3969/j.issn.1009-587X.2018.10.033 |
| [3] |
AFKARIAN M, ZELNICK L R, HALL Y N, et al. Clinical manifestations of kidney disease among US adults with diabetes, 1988-2014[J]. JAMA, 2016, 316(6): 602-610. DOI:10.1001/jama.2016.10924 |
| [4] |
RODRIGUEZ F, LEE D J, GAD S S, et al. Real-world diagnosis and treatment of diabetic kidney disease[J]. Advances in Therapy, 2021, 38(8): 4425-4441. DOI:10.1007/s12325-021-01777-9 |
| [5] |
VERDECCHIA P, ANGELI F. Progress in the treatment of hypertension[J]. Giornale Italiano Di Cardiologia(2006), 2021, 22(4): 253-266. |
| [6] |
NIE Q X, CHEN H H, HU J L, et al. Dietary compounds and traditional Chinese medicine ameliorate type 2 diabetes by modulating gut microbiota[J]. Critical Reviews in Food Science and Nutrition, 2019, 59(6): 848-863. DOI:10.1080/10408398.2018.1536646 |
| [7] |
LIANG M Z, LIN J, XU R M. Value of qidi Shenkang Decoction combined with alprostadil in treatment of diabetic nephropathy and its effect on serum s ICAM-1 and urinary CTGF levels[J]. Chinese Archives of Traditional Chinese Medicine, 2022, 40(4): 203-206. |
| [8] |
黄海婷. 中药金樱子的研究现状及综合利用[J]. 中国医药指南, 2014, 12(28): 76-77, 78. |
| [9] |
刘盼英, 杨康, 杨洪涛. 金樱子在肾脏疾病治疗中的作用[J]. 中医学报, 2020, 35(6): 1196-1201. |
| [10] |
刘皎, 刘彦, 张彬, 等. NLRP3炎症小体抑制剂MCC950改善非酒精性脂肪性肝炎形成的机制研究[J]. 中国现代普通外科进展, 2022, 25(6): 421-425. |
| [11] |
HIGGINS S P, TANG Y, HIGGINS C E, et al. TGF-β1/p53 signaling in renal fibrogenesis[J]. Cellular Signalling, 2018, 43: 1-10. DOI:10.1016/j.cellsig.2017.11.005 |
| [12] |
STONE R C, PASTAR I, OJEH N, et al. Epithelial-mesenchymal transition in tissue repair and fibrosis[J]. Cell and Tissue Research, 2016, 365(3): 495-506. DOI:10.1007/s00441-016-2464-0 |
| [13] |
LAMOUILLE S, XU J, DERYNCK R. Molecular mechanisms of epithelial-mesenchymal transition[J]. Nature Reviews Molecular Cell Biology, 2014, 15(3): 178-196. DOI:10.1038/nrm3758 |
| [14] |
CHENG F, SHEN Y, MOHANASUNDARAM P, et al. Vimentin coordinates fibroblast proliferation and keratinocyte differentiation in wound healing via TGF-β-Slug signaling[J]. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(30): E4320-E4327. |
| [15] |
CRUZ-SOLBES A S, YOUKER K. Epithelial to mesenchymal transition(EMT) and endothelial to mesenchymal transition(EndMT): Role and implications in kidney fibrosis[J]. Results and Problems in Cell Differentiation, 2017, 60: 345-372. |
| [16] |
AN X, ZHANG Y H, CAO Y, et al. Punicalagin protects diabetic nephropathy by inhibiting pyroptosis based on TXNIP/NLRP3 pathway[J]. Nutrients, 2020, 12(5): 1516. DOI:10.3390/nu12051516 |
| [17] |
ZHANG K M, FAN C, CAI D P, et al. Contribution of TGF-beta-mediated NLRP3-HMGB1 activation to tubulointerstitial fibrosis in rat with angiotensin Ⅱ-induced chronic kidney disease[J]. Frontiers in Cell and Developmental Biology, 2020, 8: 1. DOI:10.3389/fcell.2020.00001 |
| [18] |
WU M, YANG Z F, ZHANG C Y, et al. Inhibition of NLRP3 inflammasome ameliorates podocyte damage by suppressing lipid accumulation in diabetic nephropathy[J]. Metabolism, 2021, 118: 154748. DOI:10.1016/j.metabol.2021.154748 |
| [19] |
LI Y J, SONG W, TONG Y, et al. Isoliquiritin ameliorates depression by suppressing NLRP3-mediated pyroptosis via miRNA-27a/SYK/NF-κB axis[J]. Journal of Neuroinflammation, 2021, 18(1): 1. DOI:10.1186/s12974-020-02040-8 |
| [20] |
YAN H L, LUO B, WU X Y, et al. Cisplatin induces pyroptosis via activation of MEG3/NLRP3/caspase-1/GSDMD pathway in triple-negative breast cancer[J]. International Journal of Biological Sciences, 2021, 17(10): 2606-2621. DOI:10.7150/ijbs.60292 |
| [21] |
赵婷, 王亚东, 章康, 等. 白头翁汤正丁醇提取物对外阴阴道念珠菌病小鼠阴道黏膜上皮屏障的影响[J]. 中国中药杂志, 2020, 45(20): 4991-4996. |
| [22] |
乔琳, 金艳, 郭兆安. 中医药调控NLRP3炎症小体缓解糖尿病肾病肾间质纤维化的机制研究进展[J]. 中国中药杂志, 2024, 49(5): 1164-1171. |
| [23] |
OTTO G. IL-1β switches on kidney fibrosis[J]. Nature Reviews Nephrology, 2018, 14(8): 475. DOI:10.1038/s41581-018-0026-2 |
| [24] |
WU M, YANG Z F, ZHANG C Y, et al. Inhibition of NLRP3 inflammasome ameliorates podocyte damage by suppressing lipid accumulation in diabetic nephropathy[J]. Metabolism, 2021, 118: 154748. |
 2024, Vol. 41
2024, Vol. 41