文章信息
- 刘玺元, 曾天, 李昀晏, 等.
- LIU Xiyuan, ZENG Tian, LI Yunyan, et al.
- 药食同源中草药通过肠道菌群调控代谢性疾病研究进展
- Research progress on regulation of metabolic diseases by intestinal flora of homologous Chinese herbs in medicine and herbs
- 天津中医药, 2024, 41(11): 1482-1490
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1482-1490
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.20
-
文章历史
- 收稿日期: 2024-08-30
2. 天津中医药大学中医药研究院, 天津 301617
全球范围内,代谢性疾病的患病率持续上升,主要包括高血压病、2型糖尿病、高脂血症、肥胖等[1]。传统药物治疗虽然是当前主要的干预手段,但随着患者数量的增加,其不良反应较多、易产生耐药性、潜在的依赖性等问题也日益凸显。在这一挑战下,越来越多的人开始注意到“药食同源”和“食疗”等非药物干预方法的重要性。例如,枸杞、山药、苦瓜等食材被广泛应用于食疗中,具有调节血压、降血糖、调脂等功效。这些食物既可作为日常饮食的一部分,又可辅助传统药物治疗,提高治疗效果,同时减少了对药物的依赖性和不良反应。
“药食同源”是指某些食物具有既能作为食品食用,又具有一定药用价值的特性。食物与药物的相互作用在中医中有着悠久的历史,而现代科学也逐渐证实了这种理念的合理性。“药食同源”中草药作为天然传统药物,富含多种生物活性物质,如多糖、生物碱、皂苷、黄酮等。它们具有纯天然、毒副作用小等优点,广泛应用于疾病预防和医疗保健等日常生活中[2]。在国家卫生健康委员会公布的110种药食同源中药中,部分中草药可通过多种方式改善代谢综合征,具有安全、依从性高、可长期服用等特点[3]。
近年来,药食同源中草药调理肠道菌群治疗代谢性疾病已成为研究热点。肠道菌群在人体健康中扮演着重要角色,其功能涵盖参与营养物质代谢、形成肠道屏障等。肠道菌群的紊乱将对人体健康产生不利影响,代谢性疾病与肠道菌群失衡密切相关。中草药富含的多种生物活性物质可通过调节肠道菌群的结构和功能,从而发挥治疗代谢性疾病的作用[4]。近年来,基因组学、代谢组学等新技术的发展,为深入探究中草药调节肠道菌群的作用机制提供了有力支撑,有利于推动中药现代化研究,为疾病预防和治疗提供新思路[5]。在调理肠道菌群、治疗代谢性疾病方面,中草药展现出巨大的潜力和应用前景。未来,进一步探索中草药调节肠道菌群的作用机制,将为代谢性疾病的预防和治疗提供新的思路和方法。本文以具有药食同源特性的部分中草药提取物对肠道菌群的影响为切入点,探讨它们在治疗代谢性疾病(肥胖、糖尿病、高血压病、高尿酸血症等)方面的潜在机制。
1 药食同源中草药活性物质许多药食同源的中草药含有丰富的活性物质,对代谢性疾病具有良好的调节作用,相较于人工合成药物而言,这些天然物质具有更长远的效益。以黄酮类、酚酸类、生物碱类、多糖类、皂苷类为代表的活性成分广泛存在于药食同源中草药中,并对代谢性疾病疗效良好。
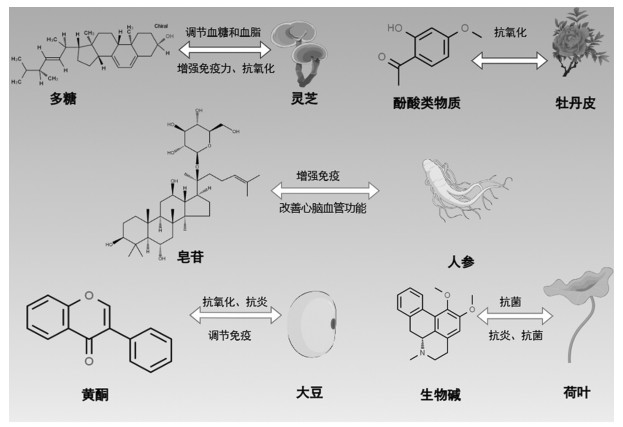
药食同源中草药中所含的活性物质可发挥多方面的保健功能。人参中的人参皂苷可增强免疫力,改善心脑血管功能。灵芝等草药含有活性多糖,具有增强免疫、抗氧化、调节血糖和血脂等效果。大豆富含黄酮类物质,可发挥抗氧化、抗炎、调节免疫等作用,对人体健康有积极影响。荷叶等草药富含生物碱,在抗炎和抗菌方面表现突出。此外,牡丹皮含有丰富的酚酸类物质如丹皮酚,也具有优良的抗氧化功能。见图 1。
|
| 图 1 部分药食同源中草药活性物质的保健功能 Fig. 1 Health care function of certain medicinal and edible homologous herbal active substances |
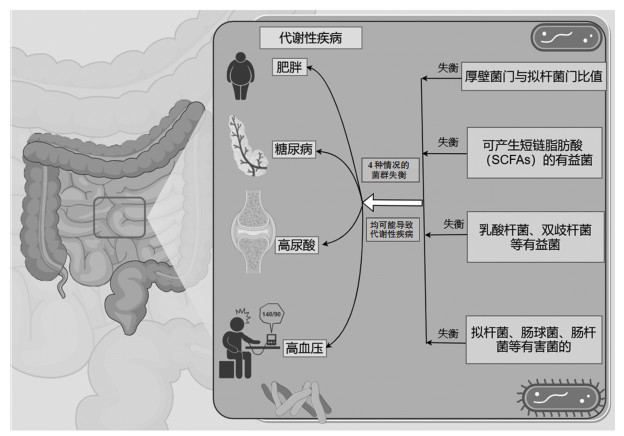
肠道菌群在肥胖、高血压病、2型糖尿病、癌症等代谢性疾病中发挥重要作用。肠道菌群及其代谢产物失衡会导致肥胖等相关代谢性疾病的发生;正常状态的肠道菌群可通过调节慢性炎症、改善肠通透性、糖稳态和免疫系统等机制调节代谢性疾病[6]。见图 2。
|
| 图 2 部分代谢性疾病与肠道菌群的联系 Fig. 2 Association between intestinal flora and some metabolic diseases |
肠道菌群与代谢性疾病之间存在密切的双向调控关系,主要体现在:肠道菌群失衡会导致能量代谢紊乱和炎症反应增强,从而增加代谢性疾病的发病风险。肠道菌群能参与宿主营养物质代谢,影响机体能量平衡,同时肠道菌群代谢产物可调节宿主代谢过程,影响代谢性疾病的发生。近些年研究表明,肠道菌群失衡引发的慢性炎症是导致代谢性疾病的重要机制之一。因此,研究肠道菌群及其代谢产物与健康关系,可为代谢性疾病治疗提供重要方向。
3 药食同源中活性物质调节肠道菌群黄酮类物质主要在胃肠道中完成吸收代谢,一部分在胃肠道中经过葡萄糖醛酸转移酶(UDPGT)的作用,生成其结合物、硫酸化物、甲基化物质等,从而进入体循环系统;另一部分与糖类物质结合,形成糖苷物质,到达肠道中被微生物代谢利用,从而改变其内在菌群组成[7]。同时,黄酮类物质可以通过破坏其细胞膜或改变膜通透性来抑制潜在致病分类群(例如大肠杆菌和金黄色葡萄球菌)的生长,还可作为双歧杆菌和乳酸菌等有益细菌的代谢底物,促进其生长和增殖[8]。Pan等[9]利用体外模拟发酵技术,研究橙皮苷、柚皮素、芦丁、异槲皮素和槲皮素等对健康受试者肠道菌群结构和代谢差异的影响,发现黄酮类物质可显著增强双歧杆菌丰度(P < 0.05)。另外,黄酮的健康有益作用主要是通过它们调节多个基因/蛋白质信号网络的能力来介导的[10]。研究表明,槲皮素、山柰酚、芹菜素等黄酮类成分对葡萄糖醛酸转移酶家族和有机阴离子转运体、有机阳离子转运体具有一定的抑制作用,还可以提高主要由细胞色素P450代谢和P-糖蛋白等相关蛋白转运的药物最大血药浓度[11]。
酚酸类物质口服后,单酚酸可经胃肠道直接吸收,而多酚酸或多酚酸酯的生物利用度较低,主要在胃肠道中被肠道菌、酯酶、pH等降解为单酚酸后,以单体形式入血。在血浆中主要以甲基化、葡萄醛酸化、硫酸化、硫酸化-葡萄糖醛酸化形式存在[12]。在改善肠道菌群方面,参与酚酸类生物转化的细菌主要有拟杆菌属、双歧杆菌属、乳杆菌属、艾克曼菌等,酚酸类化合物能促进艾克曼菌属、粪杆菌属、罗斯氏菌属等特定肠道菌群的增殖,与此同时,短链脂肪酸(SCFAs)、氧化三甲胺(TMAO)等菌群代谢物也得到相应调节[13]。酚酸类物质在抗氧化方面也有积极作用,研究表明没食子酸通过抑制活性氧(ROS)生成和脂质过氧化来减轻乙二醛诱导的肾细胞死亡,同时也具有缓解与氧化应激相关的神经系统疾病的潜力,增强内源性抗氧化防御系统和减少脂质过氧化来抵抗大脑中的氧化损伤[14]。
生物碱类成分的化学结构多呈平面状,含有较多的共轭双键,溶解度较差。有研究表示,灌胃给予黄连提取物,这些生物碱类成分的血液暴露水平和绝对生物利用度极低。被吸收的一部分广泛地分布在各组织中,其中肝脏的浓度最高,在肝脏中,生物碱可在一相代谢酶(CYP3A4等)作用下发生去甲基化、羟化,而在二相代谢酶的作用下可生成葡萄糖醛酸化或硫酸化结合物[15]。在调整肠道菌群方面,以小檗碱为代表的黄连生物碱活性成分,可通过抗菌、抗炎、调控肠道菌群构成来恢复疾病引起的肠道菌群紊乱,进而治疗胃肠道疾病;另一方面,还可通过肠-脑轴、肠-心轴、肠-肝轴或其他途径对2型糖尿病、高脂血症发挥治疗作用[16]。此外,生物碱在抗炎作用中发挥显著,研究表明小檗碱可抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠核因子κB(NF-κB)的活化和炎性细胞因子的转录,还能抑制肿瘤坏死因子-α(TNF-α)激活的多形核白细胞与血管内皮细胞的黏附,从而减少炎性细胞浸润和结肠黏膜病变[17]。
多糖类物质摄入后,未被唾液及胃液中酶消化的部分进入肠道,被肠道微生物降解,从而促进机体对多糖的消化和吸收,其在肠道中通过细胞旁路通道转运、跨细胞途径和M细胞介导的转运来吸收[18]。在维持肠道菌群方面,研究表明,山楂多糖能降低埃希氏杆菌属-志贺氏杆菌、梭形杆菌属等有害菌群的丰度,上调肠道氨基酸球菌属、巨球形菌属等有益菌的比例;枸杞多糖的干预增加了大鼠肠道内乳酸杆菌、杜氏菌和粪杆菌的丰度,降低了毛螺菌和瘤胃球菌的丰度[19]。多糖类物质同样也能够调整肠道代谢衍生物,中药多糖通过肠道微生物发酵、降解调节SCFAs与脂多糖(LPS)提高宿主肠道免疫功能,在治疗溃疡性结肠炎、肠癌等疾病方面效果明显[20]。有学者发现,黄芪多糖(APS)通过调节KKAy糖尿病模型小鼠骨骼肌中的蛋白激酶B(PKB)/葡萄糖转运蛋白4(GLUT 4)信号通路改善胰岛素敏感性,从而改善糖尿病;桑葚叶多糖(MLPII)可抑制2型糖尿病(T2DM)大鼠体内蛋白质酪氨酸磷酸酶的表达,激活磷酸肌醇3-激酶(PI3K)/蛋白激酶B(AKT)通路,减轻肝脏氧化应激,改善肝脏葡萄糖代谢[21]。
皂苷类物质极性强且生物利用度低,不易被肠道吸收。而在肠道菌群作用下,大多数皂苷可以被代谢成次生糖苷和苷元,增加脂溶性,进而促进皂苷类物质的吸收和利用[22]。研究发现主要是肠道菌群中的双歧杆菌属Bifidobacterium、乳杆菌属Lactobacillus、拟杆菌属Bacteroides和普雷沃氏菌属Prevotella参与中药皂苷的代谢转化,发生脱糖、脱氢、氧化、脱水、羟基化等反应,改变皂苷类化合物的结构,生成低极性的次级苷、苷元或其他代谢产物[23]。Zeng等[24]采用大鼠血压和颅内动脉模型,观察黄芪总苷对血压和颅内动脉的影响,发现黄芪皂苷Rb1对于降低大鼠血压有着积极意义。同时,皂苷可抑制炎性体核苷酸结合寡聚化结构域样受体(NLR)P3(NLRP 3)的活化来改善炎症[25]。具体作用机制见表 1。
4 活性物质对相关代谢性疾病的调控作用 4.1 肥胖肥胖是一种普遍存在的健康问题,过多的脂肪组织会增加心脏和血管系统的负担。此外,肥胖也会干扰身体对胰岛素的正常反应,导致糖尿病的发生和发展。肥胖还与许多其他健康问题,如关节炎、呼吸困难和睡眠呼吸暂停综合征等联系紧密。近年来,肠道菌群的研究备受关注,在肠道微生态中,厚壁菌门(Firmicutes)和拟杆菌门(Bacteroides)的相对丰度(F/B)值增加以及特定菌群的变化可能会促进肥胖的发生和发展,同时部分益生菌被认为可以通过调节肠道菌群来改善肥胖[26]。有研究表示,部分活性多糖有助于改善高脂饮食引起的肥胖和高脂血症[27]。刘伟等[28]发现枸杞、灵芝中含有的多糖成分具有促进脂肪分解并抑制脂肪合成的作用,其可以降低F/B值,增加肠道菌群的丰富度和多样性,降低总胆固醇(TC)、三酰甘油(TG)等。
黄酮类化合物存在于多种中草药中,其不仅可以降低肠道菌群中的有害菌,也可以增加有益菌的相对丰度[29]。陈斌等[30]以黄芩等中草药提取物作为研究,探索出黄酮类化合物能够通过促进产生SCFAs的菌群生长以及菌群对膳食纤维等多糖的发酵,从而产生丙酸、乙酸和丁酸等SCFAs,这些SCFAs表现出抗炎、抗肥胖和保护肠道等生物学活性。熊万涛等[31]在对肥胖小鼠进行荷叶碱治疗后,发现厚壁菌门/拟杆菌门比值降低,Alloprevotella等菌的相对丰度明显升高,而Helicobacter的相对丰度降低。多酚具有改变肠道菌群种类和数量的作用,不同的多酚及其代谢产物可以抑制有害菌生长。肖俊松等[32]发现苦丁茶多酚物质可以提高Akkermansia菌群的相对丰度,降低Oscillibacter菌群的相对丰度,进而影响机体能量的储存,能够促进亚油酸的吸收、促进胆固醇向类固醇的转变以及胆汁酸的去饱和等功能[33]。吴振宁等[34]通过茯苓提取物研究小鼠肠道以及菌群的变化,发现茯苓提取物能够修复小肠绒毛、调节肠道菌群,改善高脂饮食引起的肠道菌群失调。彭喜春等[35]通过肉桂精油对小鼠肠道内梭菌属Ⅳ簇细菌和拟杆菌属细菌的影响,发现肥胖患者的肠道中拟杆菌与厚壁菌的比例减少,而肉桂精油可以增加拟杆菌的数量、减少Ⅳ簇梭菌的数量,改变菌群的多样性和组成,从而达到减肥的效果。白荣钰等[36]经过毛冬青三萜皂苷干预后,探索出大鼠肠道菌群结构得到改善,益生菌如拟杆菌以及布劳特氏菌属的相对丰度增加,而致病菌如大肠杆菌的相对丰度降低。青钱柳中的黄酮和三萜对拟杆菌等菌种的生长有抑制作用。有益菌数量的增加可以有效抑制氨、粪臭素的形成,增加有机酸产生,降低结肠和粪便的pH值,抑制病原菌的生长[37]。
4.2 糖尿病根据国际糖尿病联盟的数据,20~79岁的糖尿病患者数量已达0.98亿,预计到2035年将增至1.43亿。随着糖尿病患病率逐年攀升,研究治疗该疾病的工作成为热点。在治疗方面,传统药物如阿卡波糖可能会引起患者肠胃不适、腹胀、腹泻等,甚至长期大量服用还可能会引起肝功能异常。而天然中草药提取物具有不良反应小的特点,因此通过天然中草药提取物辅助治疗糖尿病已成为研究热点。与此同时,肠道菌群在糖尿病治疗中的应用也备受关注。
生物碱是常见中草药的提取物,可通过影响肠道菌群预防和改善糖尿病。张立雯等[38]以2型糖尿病模型db/db小鼠为研究对象,通过16SrDNA测序研究桑叶生物碱等成分对糖尿病小鼠的生物效应及其对肠道菌群的调节作用,发现在桑叶提取物(生物碱)的调节后拟杆菌与厚壁菌门比例有所改善,罗斯氏菌属有所下降。罗斯氏菌属具有从亚油酸中形成共轭亚油酸(CLA)的能力,而CLA有助于治疗糖尿病[39-40]。小檗碱可以降低厚壁菌门菌群,而厚壁菌门菌群会增加人体肠道对脂肪和碳水化合物的吸收。双歧杆菌作为一类益生菌,可以抑制致病菌群的生长,改善肠道微生态,保护机体健康。双歧杆菌的减少可能导致肠道微环境失衡,引发多种代谢性疾病[41]。周强等[42]研究发现黄连提取物小檗碱在低丰度双歧杆菌的患者中具有降糖效果。这可能与小檗碱抑制双糖酶活性、阻断葡萄糖在肠道吸收的作用相关。人参中的人参皂苷作为其最独特成分,被认为是其降血糖作用的物质基础。孙美等[43]研究发现,人参皂苷在体内需经过胃酸降解或肠道菌群发酵去糖基化后转化为次生皂苷或苷元,其可以改善胰岛素抵抗、保护胰岛细胞等。杨芸艺等[44]研究发现,黄芪皂苷在肠道菌液中经过共同孵育后,主要代谢途径包括去糖基化、去乙酰化和脱氢。黄芪甲苷显示出降低糖尿病大鼠血糖和血脂水平、增加抗氧化酶生物活性、减少氧化应激引起的病理性损伤的能力,为临床改善和治疗糖尿病提供积极意义。戴新新等[45]通过研究地黄叶总苷提取物对糖尿病肾病大鼠肠道菌群的调节作用,发现地黄总苷能够使拟杆菌门、厚壁菌门比例趋于正常,增加乳酸杆菌的相对丰度,改善糖尿病肾病的肠道菌群失调。
柳婷等[46]采用高糖高脂饮食诱导小鼠,探究发现玉竹多糖与肠道菌群的相互作用产物SCFAs(乙酸、丙酸)在治疗糖尿病中扮演重要角色。玉竹多糖通过厚壁菌降解聚糖生成SCFAs,这些SCFAs对糖尿病具有一定的改善作用[47]。而黄芪多糖不仅对肠道菌群紊乱具有正面调节作用,还能改善体内代谢、调节肠道微环境,在抑制肝脏脂肪变性、抗炎和抗糖尿病等方面发挥关键作用。苑慧敏等[48]发现大豆异黄酮能够增加乳酸杆菌比例,减少拟杆菌与异种菌比例,对2型糖尿病患者的脂质代谢有改善作用。刘万等[49]研究发现肉桂多酚能够降低厚壁菌门的相对丰度,增加拟杆菌门、普雷沃氏菌和乳酸杆菌的数量,改善2型糖尿病大鼠的胰岛β细胞功能,进而更好地调节葡萄糖代谢,治疗糖尿病。
4.3 高血压病高血压病是常见的心血管疾病,根据《中国心血管健康与疾病报告2022》要点解读,高血压病患病率呈上升趋势,加权率为23.2%,估计中国成人高血压病患病人数为2.45亿[50]。随着西医及基因组学的不断发展,高血压病与肠道菌群之间的关系引起广泛关注。厚壁菌(F)与拟杆菌(B)之间的比值关系是衡量肠道菌群是否健康的重要标志。高血压病患者肠道中厚壁菌明显增多,拟杆菌明显减少[51],部分肠道乳酸菌属还与膳食钠摄入量和血压成强烈的负相关[52]。肠道菌群主要代谢产物有SCFAs、氧化三甲胺(TMAO)等,与高血压病有着密切的联系[53]。
药食同源中活性物质对于调节高血压有着显著作用,是当下研究热点之一。有学者采用高血压大鼠模型补充乙酸盐后,肠道菌群紊乱得到改善,F/B比例降低,拟杆菌门增加,血压下降。对此推测酚酸类物质代谢可通过增加SCFAs生成来改善高血压状态[13]。陈蕾[54]以山西苦荞粉为原料,通过建立小鼠肠道菌群发酵体外模型,对肠道菌群的影响以及群落结构进行了初步分析,表明苦荞组均对有益菌(双歧杆菌、乳杆菌和柔嫩梭菌)具有一定增殖作用,同时对有害菌(拟杆菌、肠球菌和肠杆菌)的生长具有一定抑制作用。蔡光泽等[55]研究苦荞饮食对自发性高血压大鼠(SHR)肠道菌群的影响,苦荞饮食干预后,SHR肠道菌群4大菌在门水平上的丰度发生了变化,随时间改变SHR肠道菌群结构变化较为明显的部分菌属依次为普氏菌属、拟杆菌属、甲烷粒菌属、毛螺菌属等。刘靖[56]以苦荞为原料提取苦荞蛋白,对其进行模拟体外消化及建立高血脂大鼠模型,发现灌胃苦荞蛋白,可降低高脂饮食大鼠血清低密度脂蛋白胆固醇水平、增加高脂饮食大鼠总SCFAs、乙酸和丙酸的含量及肠道菌群多样性的趋势。韩聪等[57]利用黄芪丹参对自发性高血压大鼠进行干预,结果发现其相对于对照组F/B比值降低、乳酸杆菌属、双歧杆菌属、阿克曼菌属和克里斯汀菌科丰度增加,其降压作用可能与产生血管紧张素转换酶抑制肽、SCFAs、共轭亚油酸及γ-氨基丁酸等有关。孙伟等[58]用人参皂苷对高脂模型小鼠进行诱导,结果显示人参皂苷可逆转肠道菌群差异,保护肠上皮屏障功能,降低代谢内毒素的产生,从而降低血压。郭丽娜等[59]利用葛根、夏枯草、杜仲叶、菊花、山楂、芹菜形成复合中药诱导高血压大鼠研究其肠道菌群调控作用,与模型组比较,药食同源中药复方组乳酸杆菌属、布劳特氏菌属和罗姆布茨菌属的相对丰度显著增加,肠球菌属Enterococuus的相对丰度显著降低,表明该药食同源复合物质能够改善肠道菌群丰度、血清代谢物,从而达到干预治疗高血压病的效果。
目前,大量药食同源物质已被证实可以通过调节肠道菌群组成、丰度等对高血压病等心脑血管疾病有一定的缓解作用,但由于肠道菌群复杂繁多、对于测定菌属没有统一标准,具体发挥作用的靶点及机制尚不明确有待进一步探究[60]。
4.4 高尿酸高尿酸血症是机体尿酸生成增加或排泄减少导致血尿酸水平异常升高的代谢性疾病,已成为中国仅次于糖尿病的第二大代谢性疾病[61]。现在研究表明,许多植物性活性物质如黄酮类、酚酸类、皂苷类、多糖类等对于治疗高尿酸血症有着显著作用[62]。对于肠道菌群而言,高尿酸会破坏内环境稳态,而为延缓症状发生,肠道菌群会改变其内在组成,通过离子偶联转运体促进尿酸的代谢[63]。这种现象说明可以通过外界介入改变肠道菌群的组成,进而影响菌群代谢产物来达到减轻高尿酸症和加快代谢的目的。
吴美音等[64]利用桑叶探究其降尿酸的机制,与模型组相比,小鼠的炎症因子IL-1β显著降低(P < 0.05),黄嘌呤氧化酶水平极显著降低(P < 0.01),URAT1蛋白水平显著下降(P < 0.05),推测其作用机制可能与该蛋白表达有联系。有学者[63]将桑叶制成超细粉抹茶给予SD大鼠灌胃处理,检测肠道菌群种属发现普氏菌属、乳杆菌属、CF231菌属、颤螺旋菌、拟杆菌等丰度发生变化,提示桑叶可能通过调节肠道菌群结构变化缓解高尿酸症状。张淑丽[65]对高尿酸血症血清脂质进行分析,发现银杏提取物通过调节甘油磷脂代谢来改善高尿酸血症。田萌[66]发现银杏叶提取物能够有效改善高浓度尿酸状态下腺苷酸活化蛋白激酶(AMPK)、AKT表达水平,调控信号通路途径,减少高尿酸对肾小球内皮细胞的损害。陈华海等[67]研究银杏双黄酮与银杏内酯对肠道菌群的互作现象,其发现对细菌总量和细菌SCFAs的产生没有显著影响,但可以显著增加Coriobacteriaceae科和Cupriavidus属细菌的比例,显著降低Gemella属细菌的丰度。朱春胜等[68]探讨菊苣降尿酸的有效成分,并对其降尿酸机制、安全性进行初探,发现菊苣降尿酸活性成分可能为绿原酸、秦皮甲素、菊苣酸,机制可能与抑制黄嘌呤氧化酶(XOD)、腺苷脱氨酶(ADA)活性有关。康金森等[69]探究毛菊苣醇提物对小鼠肠道菌群影响,结果说明其可以上调双歧杆菌属(Bifidobacterium)、Romboutsia、普雷沃氏菌属(Prevotella)菌群相对丰度。在多酚方面,有学者[70]研究绿茶多酚对于高尿酸血症小鼠的作用机制,发现绿茶多酚能够抑制外源酶(XO)活性,增加阴离子转运蛋白(OAT1)、OAT3及降低尿酸盐转运体(URAT1)表达,从而实现降低血清和肝脏中尿酸的作用。薛俊敏[71]研究茶多酚对小鼠肠道菌群、肠道酶活性及肠道SCFAs的影响,与模型对照组相比,灌胃茶多酚后,小肠内菌群的多样性和丰富度均提高,变形杆菌门相对丰度显著降低(P < 0.05),拟杆菌门与厚壁菌门相对丰度均提高,大肠杆菌/志贺菌属相对丰度显著降低(P < 0.05)。
根据已有的研究,药食同源植物通过抑制白细胞介素(IL)-1β和IL-8、TNF-α等促炎因子,抑制血管细胞黏附分子1(VCAM-1)蛋白表达,提升IL-4等抗炎因子,抑制炎症细胞趋化、激活,降低中性粒细胞聚集,减轻炎症反应[72]。在更深层次上,通过下调促进尿酸重吸收蛋白质[葡萄糖转运体9(GLUT9)、尿酸盐轻运蛋白1(URAT1)]的表达,上调促进尿酸排泄的蛋白质[ATP结合盒转运蛋白G2(ABCG2)、有机阴离子转运蛋白(OAT1)、OAT2和OAT3]的表达来减少高尿酸的发生[73]。值得注意的一点,尿酸在人体中代谢和啮齿类动物中代谢的途径有差异,因此临床实验部分活性物质对尿酸代谢的作用具有重要意义。
5 小结与展望代谢性疾病在全球的发生率不断增加,通过肠道菌群治疗和缓解代谢性疾病的研究已成为热点。肠道微生态失衡可能导致能量代谢失调和炎症反应加剧,从而增加代谢性疾病的发病风险。肠道菌群参与宿主营养物质代谢,影响机体能量平衡,其代谢产物也可以调节宿主代谢过程,进而影响代谢性疾病的发生。
通过药食同源中草药及其提取物的治疗,可以丰富肠道菌群的多样性,降低厚壁菌门与拟杆菌门的比例,促进厚壁菌门产生有益的SCFAs,增加乳酸杆菌、双歧杆菌、柔嫩梭菌、巨球形菌属等有益菌的相对丰度,降低拟杆菌、肠球菌、肠杆菌、志贺氏杆菌、梭形杆菌等有害菌的相对丰度,从而改善肠道健康,治疗和预防代谢性疾病。黄酮类物质在调节肠道菌群、促进SCFAs生成以及抑制潜在致病菌群生长等方面的作用,对于改善代谢性疾病确实具有一定效果。这些作用有助于维持肠道健康,调节代谢功能,从而对肥胖、糖尿病、高血压病等疾病产生积极影响。黄芩、芦丁、大豆异黄酮等含有丰富的黄酮类物质。绿原酸、咖啡酸、没食子酸中富含的酚酸类物质,酚酸类物质在改善肠道菌群方面发挥重要作用,参与生物转化的细菌主要有拟杆菌属、双歧杆菌属、乳杆菌属、艾克曼菌等。这些化合物能促进特定肠道菌群的增殖,调节SCFAs和氧化三甲胺等菌群代谢物,对改善和治疗高血压病具有显著效果。荷叶和桑叶等富含生物碱,这些生物碱能改善肠道菌群,降低厚壁菌门菌群,增加双歧杆菌和乳酸杆菌比例,对改善肥胖、调节血糖、治疗糖尿病、降低血压有显著效果。枸杞多糖干预增加了大鼠肠道内乳酸杆菌、杜氏菌和粪杆菌的丰度,降低了毛螺菌和瘤胃球菌的丰度。山楂多糖降低了有害菌群的丰度,提高了有益菌比例。灵芝多糖有助于脂肪分解和抑制脂肪合成,降低F/B值,改善肠道菌群丰富度和多样性,降低TC和TG水平,对治疗代谢性疾病有显著效果。人参和黄芪中的皂苷类物质在肠道中易被代谢成次生糖苷和苷元,主要通过肠道菌群中的双歧杆菌、乳杆菌、拟杆菌和普雷沃氏菌参与代谢转化。人参皂苷在体内需经过降解或发酵后转化为次生化合物,有助于改善胰岛素抵抗和保护胰岛细胞,治疗和预防糖尿病。
在深入探讨药食同源中草药提取物的作用机制时,研究可以发现中草药及其提取物可以显著改善肠道微生态及代谢性疾病。这些天然产品的研究展示了其通过多途径和多靶点的作用机制,多方位调节人体健康。除了广泛研究的黄酮类和多糖类成分外,诸如萜类、挥发油、氨基酸和矿物质等活性物质在促进肠道健康和调节代谢平衡方面也展现出巨大潜力。萜类化合物具有抗炎和抗菌的功能,这类物质能够通过调节肠道激素胰高血糖素样肽-1(GLP-1)的分泌,影响食欲及能量代谢,从而有效改善肥胖。挥发油则是姜黄、肉桂等植物的重要成分,能显著增强肠道屏障功能,防止有害物质进入血液循环,保护机体免受内毒素和炎症因子的侵害,同时促进肠道蠕动,有助于改善便秘问题,进一步维护肠道健康。此外,中草药中富含的氨基酸和矿物质,如韭菜籽和猪苓中富含的功能性氨基酸精氨酸,前者具有消肿、止血的效果,后者则展现出良好的抗菌特性。锌作为体内重要的微量元素,在生理功能方面的研究已经非常丰富,证实具备清热、凉血及消炎功效[74]。这些物质通过参与多种酶促反应,调节肠道菌群,优化微生物的生存环境,促进有益菌的生长,同时抑制有害菌的繁殖,对于维持肠道稳态及提升免疫力具有重要意义。
药食同源理念在中草药应用中源远流长,强调食物与药物相通性,不仅提供营养,也具有调节身体功能和治疗疾病的特性。随着肠道菌群与健康关系的深入研究,药食同源中草药活性物质通过调控肠道菌群在代谢性疾病治疗中的作用受到关注。研究发现,中草药活性物质被肠道菌群代谢吸收,发挥对代谢性疾病的调控作用,既能为有益菌提供营养,又能抑制有害菌,维持肠道菌群平衡。此外,它们还能通过调节肠道菌群代谢活动,影响营养物质吸收和代谢,改善代谢性疾病症状。然而,对这些活性物质与肠道菌群互动的机制以及如何利用这些互动来治疗代谢性疾病还需要更深入地研究。未来的研究可以更深入地探讨中草药活性物质对肠道菌群的影响,开发出个性化治疗方案,提高中草药在治疗代谢性疾病中的效果,推动中医药在医学中的发展与应用。
| [1] |
CHEW N W S, NG C H, TAN D J H, et al. The global burden of metabolic disease: data from 2000 to 2019[J]. Cell Metabolism, 2023, 35(3): 414-428. DOI:10.1016/j.cmet.2023.02.003 |
| [2] |
李秋月, 林连兵, 杨雪娇, 等. 微生物发酵中草药的研究现状[J]. 微生物学通报, 2021, 48(6): 2232-2244. |
| [3] |
毛志勇, 林子嫄, 段志伟, 等. 药食同源中药干预代谢综合征的研究进展[J]. 中华中医药杂志, 2023, 38(9): 4271-4277. |
| [4] |
田也, 麦旭东, 马凯, 等. 肠道菌群调控代谢性疾病发生和发展[J]. 科学通报, 2021, 66(13): 1602-1613. |
| [5] |
王鑫楠, 王维维, 辛贵忠, 等. 中草药调控肠道微生态组成与代谢的研究进展[J]. 中医药学报, 2019, 47(4): 117-124. |
| [6] |
苏黑艳·帕尔哈提, 张姣姣, 马壮, 等. 肠道微生物菌群与肥胖相关代谢性疾病的研究进展[J]. 中国比较医学杂志, 2023, 33(10): 146-154. DOI:10.3969/j.issn.1671-7856.2023.10.019 |
| [7] |
常化松, 袁雯雯, 玄红专, 等. 黄酮类化合物吸收代谢及其对胃肠道功能影响的研究进展[J]. 食品工业科技, 2019, 40(18): 340-347. |
| [8] |
WANG H R, ZHAO T T, LIU Z J, et al. The neuromodulatory effects of flavonoids and gut Microbiota through the gut-brain axis[J]. Frontiers in Cellular and Infection Microbiology, 2023, 13: 1197646. DOI:10.3389/fcimb.2023.1197646 |
| [9] |
PAN L X, YE H Y, PI X E, et al. Effects of several flavonoids on human gut microbiota and its metabolism by in vitro simulated fermentation[J]. Frontiers in Microbiology, 2023, 14: 1092729. DOI:10.3389/fmicb.2023.1092729 |
| [10] |
SUDHAKARAN M, DOSEFF A I. The targeted impact of flavones on obesity-induced inflammation and the potential synergistic role in cancer and the gut microbiota[J]. Molecules, 2020, 25(11): 2477. DOI:10.3390/molecules25112477 |
| [11] |
凌霄, 陈玉欢, 王盼盼, 等. 代谢酶和转运体介导的药食同源中药中黄酮类成分对其他药物的影响[J]. 中国药房, 2021, 32(18): 2287-2293. DOI:10.6039/j.issn.1001-0408.2021.18.18 |
| [12] |
斯日古楞, 刘洪涛. 中药酚酸的体内代谢研究进展[J]. 亚太传统医药, 2008, 4(6): 49-51. |
| [13] |
杨钦钦, 陈民利. 中药酚酸类物质通过调节肠道菌群防治心血管疾病的研究进展[J]. 中成药, 2022, 44(12): 3920-3926. DOI:10.3969/j.issn.1001-1528.2022.12.029 |
| [14] |
XIANG Z D, GUAN H D, ZHAO X, et al. Dietary Gallic acid as an antioxidant: a review of its food industry applications, health benefits, bioavailability, nano-delivery systems, and drug interactions[J]. Food Research International, 2024, 180: 114068. DOI:10.1016/j.foodres.2024.114068 |
| [15] |
陈阳, 马嘉仪, 张健榕, 等. 黄连中生物碱类成分抗溃疡性结肠炎的作用机制研究进展[J]. 南京中医药大学学报, 2023, 39(12): 1260-1266. |
| [16] |
王鑫喆, 沈梦婷, 闫鹏举, 等. 黄连生物碱类活性成分与肠道菌群相互作用的研究进展[J]. 中国药房, 2021, 32(1): 109-115. |
| [17] |
LI S C, LIU X, CHEN X R, et al. Research progress on anti-inflammatory effects and mechanisms of alkaloids from Chinese medical herbs[J]. Evidence-Based Complementary and Alternative Medicine, 2020, 2020: 1303524. DOI:10.1155/2020/1303524 |
| [18] |
朱赤云, 肖平, 方悦悦, 等. 多糖体内过程与免疫调节机制研究方法和技术进展[J]. 药学学报, 2024, 59(2): 322-335. |
| [19] |
李焱, 林泳峰, 刘文美, 等. 食药同源植物多糖调控肠道稳态的研究进展[J]. 食品安全质量检测学报, 2023, 14(2): 25-33. |
| [20] |
段晨晨, 赵文晓, 吕琴, 等. 药食同源类中药多糖在功能性保健食品方面的药理作用研究进展[J]. 世界科学技术-中医药现代化, 2022, 24(10): 3844-3850. DOI:10.11842/wst.20211006005 |
| [21] |
LI L, XIE J C, ZHANG Z M, et al. Recent advances in medicinal and edible homologous plant polysaccharides: preparation, structure and prevention and treatment of diabetes[J]. International Journal of Biological Macromolecules, 2024, 258. |
| [22] |
丁劲文, 林媛, 蒋建东. 肠道菌群与天然产物的相互作用研究进展[J]. 中国医药生物技术, 2024, 19(1): 52-56. DOI:10.3969/j.issn.1673-713X.2024.01.009 |
| [23] |
韩冰, 李静娜, 吕西雨, 等. 肠道菌群代谢转化中药皂苷类成分研究进展[J]. 中草药, 2023, 54(20): 6922-6932. |
| [24] |
ZENG Z B, WANG H B, YI R H, et al. Gut microbiome and metabolome in aneurysm rat with hypertension after ginsenoside Rb1 treatment[J]. Frontiers in Pharmacology, 2023, 14: 1287711. DOI:10.3389/fphar.2023.1287711 |
| [25] |
DE OLIVEIRA ZANUSO B, DE OLIVEIRA DOS SANTOS A R, MIOLA V F B, et al. Panax ginseng and aging related disorders: a systematic review[J]. Experimental Gerontology, 2022, 161: 111731. DOI:10.1016/j.exger.2022.111731 |
| [26] |
CHO K Y. Association of gut microbiota with obesity in children and adolescents[J]. Clinical and Experimental Pediatrics, 2023, 66(4): 148-154. DOI:10.3345/cep.2021.01837 |
| [27] |
NIE S Q, GE Y. The link between the gut microbiome, inflammation, and Parkinson's disease[J]. Applied Microbiology and Biotech- nology, 2023, 107(22): 6737-6749. DOI:10.1007/s00253-023-12789-6 |
| [28] |
刘伟, 吴江平, 袁平川, 等. 中药多糖对非酒精性脂肪性肝病改善作用及机制研究进展[J]. 中草药, 2022, 53(23): 7566-7574. |
| [29] |
XUAN H Z, OU A Q, HAO S Y, et al. Galangin protects against symptoms of dextran sodium sulfate-induced acute colitis by activating autophagy and modulating the gut microbiota[J]. Nutrients, 2020, 12(2): 347. DOI:10.3390/nu12020347 |
| [30] |
陈斌, 刘洁, 詹敏敏, 等. 黄酮类化合物与肠道菌群互作研究进展[J]. 中国食品学报, 2022, 22(6): 369-381. |
| [31] |
熊万涛, 廖加抱, 杨智霞, 等. 荷叶碱对肥胖模型小鼠肠道菌群及慢性炎症的影响[J]. 中国中药杂志, 2021, 46(8): 2104-2111. |
| [32] |
肖俊松, 单静敏, 曹雁平, 等. 多酚通过肠道菌群调节能量代谢研究进展[J]. 食品科学, 2012, 33(3): 300-303. |
| [33] |
储思远, 钱利生, 陈海敏. 茶成分对肠道菌群的调控作用及其健康效应的研究进展[J]. 天然产物研究与开发, 2024, 36(2): 357-367. |
| [34] |
吴振宁, 祁龙凯, 陈地灵. 茯苓提取物对高脂饮食致肠道菌群失调小鼠的影响[J]. 中国现代中药, 2020, 22(11): 1822-1829. |
| [35] |
彭喜春, 张志超, 黄丽珠, 等. 肉桂精油对大鼠肠道梭菌属Ⅳ簇菌群和拟杆菌群的影响[J]. 中草药, 2013, 44(4): 437-442. |
| [36] |
白荣钰, 易欢, 陈丰连, 等. 毛冬青三萜皂苷对动脉粥样硬化大鼠肠道菌群的影响[J]. 中草药, 2021, 52(20): 6245-6253. DOI:10.7501/j.issn.0253-2670.2021.20.014 |
| [37] |
陈玉慧, 郭彤彤, 张鑫, 等. 青钱柳黄酮及三萜调节人体肠道菌群作用研究[J]. 中国野生植物资源, 2019, 38(2): 6-10, 15. |
| [38] |
张立雯, 宿树兰, 戴新新, 等. 桑叶有效组分对db/db小鼠肠道菌群的调节作用[J]. 药学学报, 2019, 54(5): 867-876. |
| [39] |
BENJAMIN S, SPENER F. Conjugated linoleic acids as functional food: an insight into their health benefits[J]. Nutrition & Metabolism, 2009, 6: 36. |
| [40] |
DEVILLARD E, MCINTOSH F M, DUNCAN S H, et al. Metabolism of linoleic acid by human gut bacteria: different routes for biosynthesis of conjugated linoleic acid[J]. Journal of Bacteriology, 2007, 189(6): 2566-2570. DOI:10.1128/JB.01359-06 |
| [41] |
郑礼胜, 邰文, 兰新新, 等. 基于肠道菌群新靶点的中药防治糖尿病研究进展[J]. 药物评价研究, 2017, 40(8): 1173-1181. |
| [42] |
周强, 徐静, 熊红萍. 肠道菌群对小檗碱降糖效果的影响[J]. 临床合理用药杂志, 2021, 14(34): 16-19. |
| [43] |
孙美, 李继文, 马金颖, 等. 稀有人参皂苷的生物转化及其降血糖活性研究进展[J]. 吉林农业大学学报, 2023, 45(6): 674-684. |
| [44] |
杨芸艺, 沙雯君, 雷涛, 等. 黄芪基于肠道菌群调节治疗2型糖尿病的研究进展[J]. 医学综述, 2021, 27(22): 4506-4511. DOI:10.3969/j.issn.1006-2084.2021.22.025 |
| [45] |
戴新新, 蔡红蝶, 宿树兰, 等. 地黄叶对糖尿病肾病大鼠肠道菌群的调节作用[J]. 药学学报, 2017, 52(11): 1683-1691. |
| [46] |
柳婷, 邓碧莲, 李婷, 等. 以玉竹为例探讨含多糖中药网络药理学研究[J]. 世界科学技术-中医药现代化, 2022, 24(7): 2658-2668. |
| [47] |
MAHOWALD M A, REY F E, SEEDORF H, et al. Characterizing a model human gut microbiota composed of members of its two dominant bacterial Phyla[J]. Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(14): 5859-5864. |
| [48] |
苑慧敏, 李小琼, 朱立颖, 等. 大豆异黄酮对2型糖尿病小鼠脂代谢及肠道菌群结构的影响[J]. 营养学报, 2021, 43(6): 556-565. DOI:10.3969/j.issn.0512-7955.2021.06.009 |
| [49] |
刘万, 梁菲, 蔡铁全, 等. 小檗碱和肉桂多酚联合使用可通过Bas-TGR5-GLP-1改善T2DM大鼠的葡萄糖代谢[J]. 药学学报, 2024, 59(1): 135-142. |
| [50] |
《中国心血管健康与疾病报告2022》要点解读[J]. 中国心血管杂志, 2023, 28(4): 297-312.
|
| [51] |
HILLS R D Jr, PONTEFRACT B A, MISHCON H R, et al. Gut microbiome: Profound implications for diet and disease[J]. Nutrients, 2019, 11(7): 1613. |
| [52] |
PALMU J, SALOSENSAARI A, HAVULINNA A S, et al. Association between the gut microbiota and blood pressure in a population cohort of 6953 individuals[J]. Journal of the American Heart Association, 2020, 9(15): e016641. |
| [53] |
朱文, 谢凤群, 程洁, 等. 基于"心与小肠相表里"理论探讨肠道菌群与高血压的关系[J]. 上海中医药杂志, 2023, 57(8): 57-62. |
| [54] |
陈蕾. 苦荞对肠道菌群影响的研究[D]. 上海: 上海师范大学, 2016.
|
| [55] |
蔡光泽, 蔡兴勇, 王安虎, 等. 苦荞饮食对自发性高血压大鼠肠道菌群的影响[J]. 西昌学院学报(自然科学版), 2018, 32(3): 11-14, 34, 2. |
| [56] |
刘靖. 苦荞蛋白对脂质代谢的调控作用及其作用机制研究[D]. 成都: 成都大学, 2022.
|
| [57] |
韩聪, 姜月华, 李伟, 等. 基于16S rDNA测序技术探索黄芪-丹参药对干预自发性高血压大鼠肠道菌群的机制[J]. 中华中医药杂志, 2019, 34(5): 2233-2237. |
| [58] |
孙伟, 许桂凤, 唐小杭, 等. 人参总皂苷对高脂模型小鼠的降血脂作用[J]. 中成药, 2020, 42(7): 1726-1731. |
| [59] |
郭丽娜, 盛雯, 何盈犀, 等. 药食同源中药复方改善肠道菌群结构和调节血清代谢物对高血压大鼠治疗作用[J]. 中草药, 2023, 54(20): 6743-6752. |
| [60] |
魏乐乐, 顾永哲, 罗云, 等. 中药调节肠道菌群治疗心脑血管疾病的研究进展[J]. 中草药, 2023, 54(18): 6185-6196. |
| [61] |
王雨, 林志健, 张冰. 尿酸代谢紊乱相关疾病的现代认知及中医药防治进展[J]. 中国中药杂志, 2024, 49(12): 3160-3167. |
| [62] |
JIANG L L, GONG X, JI M Y, et al. Bioactive compounds from plant-based functional foods: a promising choice for the prevention and management of hyperuricemia[J]. Foods, 2020, 9(8): 973. |
| [63] |
文馨月, 唐雪阳, 何丹, 等. 中药调节肠道菌群与代谢产物改善高尿酸血症研究进展[J]. 中国中药杂志, 2021, 46(24): 6387-6394. |
| [64] |
吴美音, 陈淑宁, 高洁, 等. 菊苣、葛根、桑叶配方对高尿酸合并关节炎小鼠的降尿酸和痛风性关节炎的干预效果[J]. 食品工业科技, 2020, 41(16): 308-313. |
| [65] |
张淑丽. 银杏叶干预高尿酸血症血清脂质组学研究[D]. 北京: 北京中医药大学, 2016.
|
| [66] |
田萌. 银杏叶提取物对不同尿酸浓度的肾小球内皮细胞AMPK、AKT、eNOS信号通路及炎性因子的影响[D]. 天津: 天津医科大学, 2020.
|
| [67] |
陈华海, 赵昌会, 朱家良, 等. 银杏双黄酮和银杏内酯B与人体肠道菌群体外互作研究[J]. 微生物学报, 2021, 61(8): 2413-2426. |
| [68] |
朱春胜, 张冰, 林志健, 等. 菊苣降尿酸有效成分及机制研究[J]. 中草药, 2017, 48(5): 957-961. |
| [69] |
康金森, 闫俊林, 张芮, 等. 基于高通量测序分析毛菊苣醇提物对db/db小鼠肠道菌群的影响[J]. 现代食品科技, 2024, 40(5): 1-7. |
| [70] |
宋向飞, 雷雅坤, 刘宁, 等. 药食同源植物活性物质对尿酸代谢调控及作用机理研究进展[J]. 华北农学报, 2021, 36(S1): 188-194. |
| [71] |
薛俊敏. 茶多酚对小鼠肠道菌群、肠道酶活性及短链脂肪酸的影响[D]. 济南: 山东中医药大学, 2018.
|
| [72] |
宋向飞, 雷雅坤, 刘宁, 等. 药食同源花叶类植物对高尿酸血症的功效及机理研究进展[J]. 华北农学报, 2021, 36(S1): 195-201. |
| [73] |
WANG C Y, DAI J G. Research progress on the prevention and treatment of hyperuricemia by medicinal and edible plants and its bioactive components[J]. Frontiers in Nutrition, 2023, 10: 1186161. |
| [74] |
汤文杰, 孔祥峰, 杨峰, 等. 16种中草药的营养价值[J]. 天然产物研究与开发, 2010, 22(5): 867-872. |
2. Institute of Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
 2024, Vol. 41
2024, Vol. 41