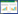文章信息
- 杜雪晨, 庞稳泰, 宋歌亮, 等.
- DU Xuechen, PANG Wentai, SONG Geliang, et al.
- 血必净注射液治疗病毒性肺炎的临床证据评价
- Clinical evidence evaluation of Xuebijing Injection in the treatment of viral pneumonia
- 天津中医药, 2024, 41(12): 1546-1552
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(12): 1546-1552
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.12.11
-
文章历史
- 收稿日期: 2024-06-08
2. 现代中医药海河实验室, 天津 301617
病毒性肺炎多由上呼吸道感染,并向下蔓延至肺部引起的炎症,常见症状包括发热、头痛、全身酸痛、咳嗽和肺部浸润性病变,全球每年约有1亿人感染。治疗不及时将转化为重症,引发多器官衰竭、脓毒症休克、急性呼吸窘迫综合征(ARDS)等一系列并发症,是其致死的主要原因[1-2]。病毒性肺炎轻症患者的治疗以支持治疗、抗病毒和抗感染为主,重症患者则需要进行有创或者无创的呼吸支持治疗[3]。但这一治疗措施的预后效果不佳,且治疗过程较为痛苦,费用昂贵,会对患者的心理、生理以及经济造成较大的负担[4-5]。相对而言,中药注射剂可减轻患者临床症状表现,提高治疗预后效果。同时,中医药临床治疗手段也较为温和,可减少患者二次创伤[6]。
血必净注射液主要成分为赤芍、川芎、丹参、红花和当归等活血化瘀药的提取物,主要用于临床急危重症的救治,如病毒性肺炎感染引起的多器官功能障碍综合征、脓毒血症、急性肺损伤及呼吸窘迫综合征等[7-9]。由此,该药在国家卫生健康委发布的《新型冠状病毒肺炎诊疗方案(试行)》第五版中,被选用作为重型与危重型用药[10],并于同月被纳入到“三药三方”当中进行推荐[11-12]。
当前,血必净注射液治疗病毒性肺炎已开展了一系列临床研究,但研究结果及质量缺乏整体评价。本研究拟通过系统文献综述,对血必净注射液治疗病毒性肺炎的临床证据进行汇总评价。
1 资料与方法 1.1 文献检索检索PubMed、EMbase、Cochrane Library、Web of Science、中国知网(CNKI)、万方知识服务平台(Wanfang Data)、维普数据库和中国生物医学文献数据库等主要中英文数据库,同时追踪纳入研究的参考文献检索。检索词包括病毒性肺炎,新型冠状病毒,新冠肺炎,冠状病毒肺炎,viral pneumonia,novel coronavirus,new coronavirus,coronavirus disease 2019,severe acute respiratory syndrome coronavirus 2和血必净注射液等关键词。检索采用主题词与自由词结合的方式,根据各数据库形式不同略作调整。检索时限为建库至2024年7月31日。
1.2 纳入排除标准 1.2.1 纳入标准1)研究类型:临床研究,包括随机对照试验(RCT)、队列研究(CS)。2)研究对象:病毒性肺炎的确诊患者,不限定病毒类型,症状表现包括呼吸困难、发热、气短等。参与者的年龄、性别不作限制。3)干预措施:试验组采用血必净注射液或西医常规联合血必净注射液治疗,应用方法不作限制。对照组采用西医常规治疗。4)结局指标:结局指标不限。
1.2.2 排除标准1)病例报告、流行病学调查、会议摘要、消息、书信。2)病毒性肺炎疑似病例的研究。3)无法获取全文或测量指标数据的研究。4)重复发表的文献仅保留第一篇。
1.3 文献筛选及资料提取文献筛选步骤:1)将数据库检索的到的文献以题录形式导入文献管理软件Note Express 3.4.0。2)通过软件结合人工的方式对文献进行剔重。3)阅读题目及摘要,根据纳排标准对剔重后的文献进行初筛。4)对初筛得到的文献进行全文下载,通过阅读全文对其复筛。
使用Excel软件根据预先设计好的资料提取表进行数据提取。提取内容包括题目、作者、发表年份、干预措施、样本量、年龄、结局指标等。数据不全的文献通过电子邮件联系作者获取,若无法联系到作者则将该文献剔除。文献筛选及资料提取均由两位研究者分别独立进行,随后交叉核对,如遇分歧交由第3位研究者裁定。
1.4 质量评价RCT根据Cochrane协作组推荐的“偏倚风险评估工具(ROB)”进行质量评价[13];CS采用Methodological index for non-randomized studies(MINORS)进行质量评估。上述内容均由两位研究者分别独立进行,随后交叉核对,如遇分歧交由第3位研究者裁定。
1.5 统计方法使用R软件进行数据统计分析。双臂研究中,计数资料采用比值比(OR)及其95%可信区间(CI)表示;计量资料采用标准化均数差(SMD)及其95%CI来表示,以P < 0.05为差异有统计学意义。纳入各研究间的统计学异质性采用Chi2检验分析,并结合I2来判断异质性的大小,若I2<50%则认为研究间异质性较小,使用固定效应模型进行合并,若I2≥50%则认为研究间异质性较大,使用随机效应模型进行合并。
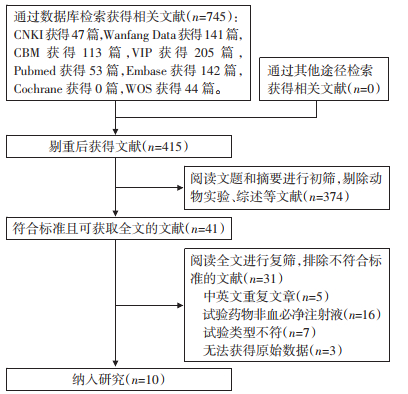
2 结果 2.1 文献筛选共检索到中文文献392篇,英文文献354篇。剔除重复后得到文献415篇,通过阅读文献题目及摘要对文献进行初筛得到41篇文献,阅读全文进行复筛选后最终得到10篇符合纳入、排除标准的文献。文献筛选流程见图 1。
|
| 图 1 文献筛选流程 Fig. 1 Document screening process |
共纳入10篇文献[6-9, 12-17],其中4篇为随机对照试验(RCT)[6-9],6篇为队列研究(CS)[12-17]。共涉及病例575例,其中轻型20例,普通型44例,重型及危重型共305例,文中未明确分型206例。相关研究详细基本信息见表 1。
RCT中1篇为英文文献[9],3篇为中文文献[6-8]。患者病情分型涉及重型(2篇)[7, 9],轻型(1篇)[8],未报告疾病分型(1篇)[6]。各研究对照方案可归纳为血必净注射液+常规治疗vs. 常规治疗。各研究样本量为20~60例。
CS中1篇为英文文献[13],4篇为中文文献[12, 14-17]。患者病情分型涉及重型及危重型(3篇)[14, 16-17],普通型(1篇)[15],未报告疾病分型(2篇)[12-13]。其中4个研究的对照方案可归纳为血必净注射液+常规治疗vs. 常规治疗[13-15, 17],1个研究报告高剂量血必净注射液+常规治疗vs. 低剂量血必净注射液+常规治疗[16]。各研究纳入患者的样本量为23~144例。
2.3 质量评价使用ROB对纳入的RCT进行质量评价。其中1篇除“其他偏倚”被评为“Unclear risk”外,其余项均被评为“Low risk”[9]。3篇均未报告盲法的实施、分配隐藏及方案注册情况,除“随机方法”被评为“Low risk”,其余项均被评为“Unclear risk”[6-8]。见表 2。
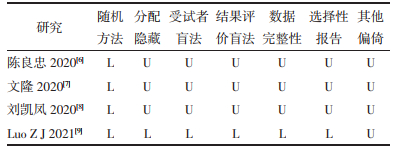
使用MINORS量表对纳入的CS进行质量评价,其中4篇被评为12分[12-14, 17],2篇被评为11分[15-16]。在“预期数据的收集”“终点指标评价的客观性”“随访时间是否充足”“失访率低于5%”“是否估算了样本量”5个条目方面各研究均未得分。见表 3。
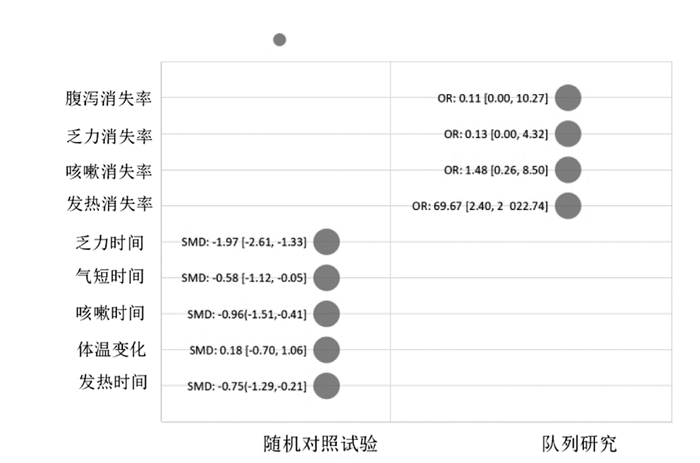
血必净注射液联用常规治疗[9, 13]在提升发热消失率(OR:69.67,95%CI:2.40~2 022.74[13])、缩短乏力(SMD:-1.97,95%CI:-2.61~-1.33[9])、气短(SMD:-0.58,95%CI:-1.12~-0.05[9])、咳嗽(SMD:-0.96,95%CI:-1.51~-0.41[9])、发热(SMD:-0.75,95%CI:-1.29~-0.21[9])等症状持续时间较单用常规治疗具有优势,组间比较差异有统计学意义(P < 0.05)。在体温变化、咳嗽、乏力、腹泻等症状消失率方面,组间比较差异无统计学意义(P≥0.05)[8, 13]。各临床症状指标见图 2。
|
| 图 2 临床症状 Fig. 2 Clinical symptoms |
血必净注射液联用常规治疗相较于单用常规治疗[7-9, 13-14],在肺部CT异常改善率(OR:9.80,95%CI:1.09~88.23[13])、白细胞计数(SMD:1.01[0.74,1.28][7-8, 17])、淋巴细胞计数(SMD:0.87,95%CI:0.48~1.25[7-9])、中性粒细胞百分比(SMD:-0.40[-0.70,-0.11][12, 15])、C反应蛋白(SMD:-0.45[-0.73,-0.18][6, 8, 17])、白细胞介素(IL)-6(SMD:-0.99,95%CI:-1.54,-0.43[9])、肿瘤坏死因子-α(SMD:-1.32,95%CI:-1.90~-0.74[9])、血沉(SMD:-1.38,95%CI:-1.98~ -0.77[7-8])等方面具有优势,组间差异有统计学意义(P < 0.05)。在CT改善率、淋巴细胞百分比、中性粒细胞计数、IL-4、IL-8、IL-10、D-二聚体、凝血酶时间、血小板计数、凝血酶原时间、纤维蛋白原、乳酸、动脉血氧分压、吸入氧浓度、氧合指数、T淋巴细胞计数、CD4+T淋巴细胞、CD8+T淋巴细胞、乳酸脱氢酶、肌酐、总胆红素、铁蛋白等指标方面,组间比较差异不具有统计学意义(P≥0.05)[9, 13-15, 17]。各理化检查指标见图 3。

|
| 图 3 理化检测 Fig. 3 Physical and chemical test results |
血必净注射液联用常规治疗相较于单用常规治疗[9, 12],在ICU住院时间(SMD:-075,95%CI:-1.29~-0.21[9])、机械通气使用率(OR:0.13,95%CI:0.03~0.54[9])、无创机械通气使用率(OR:0.13,95%CI:0.03~0.68[9])、14 d转重率(OR:0.21,95%CI:0.05~0.86[9]),ARDS发生率(OR:0.21,95%CI:0.06~0.78[9]),脓毒性休克发生率(OR:0.19,95%CI:0.04~0.97[9]),28 d病死率(OR:0.11,95%CI:0.01~0.94[9]、OR:0.41,95%CI:0.15~1.15[12])、降低PSI评分(SMD:-20.60,95%CI:-29.69~-11.51[12])方面、PSI风险评级(改善率)(OR:5.03,95%CI:2.41~10.49[12])方面具有优势,组间有统计学差异(P < 0.05)。在核酸转阴时间、7 d核酸转阴率、住院时间、有创机械通气使用率、14 d转轻率、7 d转重率、7 d转轻率及总有效率等指标方面,组间无统计学差异(P≥0.05)[7, 9, 13, 15-16]。各疾病转归及重点事件指标见图 4。

|
| 图 4 各疾病转归及重点事件指标 Fig. 4 Disease outcome and key event indicators |
血必净注射液联用常规治疗相较于单用常规治疗[7, 12, 14],在APACHEⅡ评分(SMD:-2.68,95%CI:-3.56~-1.80[7, 14])、氧合指数评分(SMD:85.00,95%CI:53.13~116.87[12])方面具有优势,组间有统计学差异(P < 0.05)。在SOFA评分方面,组间无统计学差异[12, 14](P≥0.05)。各生活质量指标见图 5。

|
| 图 5 生活质量指标 Fig. 5 Quality of life indicators |
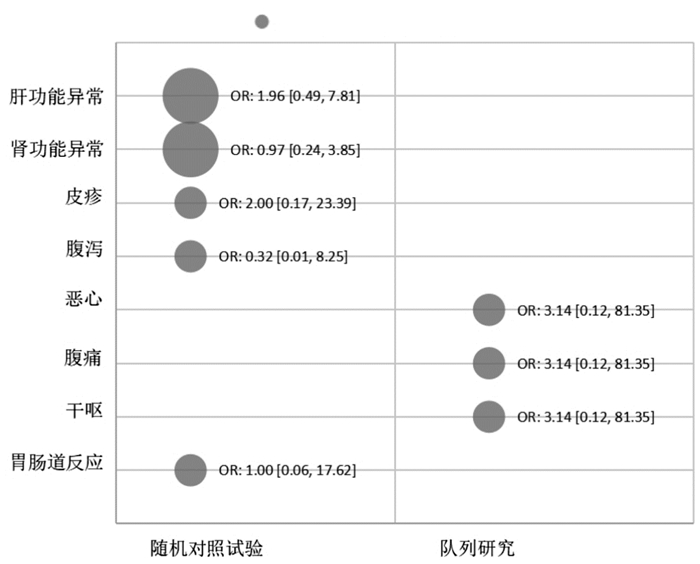
纳入研究中报告了肝功能异常、肾功能异常、皮疹、腹泻、恶心、腹痛、干呕、胃肠道反应等不良事件。血必净注射液联合常规治疗对比常规治疗,各不良事件发生率组间比较差异均无统计学意义[6, 8-9, 15](P≥0.05),见图 6。
|
| 图 6 不良事件 Fig. 6 Adverse events |
本研究对血必净注射液治疗病毒性肺炎的临床证据进行了系统评价,共检索得到4篇RCT,6篇CS,共纳入患者575例。
纳入研究除Luo[9]外,其余研究质量均不高。纳入的另外8篇研究[6-8, 12-17]均未报告研究方案的注册情况,这降低了研究的透明度。同时,纳入的3篇RCT[6-8]均未使用盲法,这导致了测量性偏倚风险的增加可能性。纳入的CS[12-13, 15-17]在“预期数据的收集”“终点指标评价的客观性”“随访时间是否充足”“失访率低于5%”“是否估算了样本量”5个条目方面各研究均未得分,这可能影响了结果测量的准确性。
疗效分析结果表明:1)血必净注射液能够缓解各分型患者的发热、乏力、气短及咳嗽等病毒性肺炎主要症状,并可以明显缩短重症患者的病死率及住院时间。2)血必净注射液组的肺部CT改善率高于对照组,白细胞及淋巴细胞计数指标方面亦优于对照组,这表明该药能够控制机体的炎症反应,促进肺部炎性渗出物的吸收。3)血必净注射液组在C反应蛋白、IL-6及TNF等炎症因子指标方面优于对照组,这表明该药具有调控炎症因子水平的作用,能够抑制炎症因子风暴的发生,降低病情转重的可能。4)在ICU住院时间、氧合指数评分、14 d转重率、28 d病死率等指标方面血必净组亦表现出优势,这些指标被核心指标集认定为重症、危重症患者病情判断的重要指标,证明血必净注射液能够截断临床病势发展,防止转重或死亡[18]。5)在安全性方面在常规治疗基础上联用血必净注射液,未发现不良事件发生率的上升,表明血必净安全性良好。目前中成药在治疗病毒性肺炎方面的RCTs数量不断增加,但缺乏整体汇总与分析,导致不同中成药的疗效差异不明确,临床应用受限[19]。病毒性肺炎作为突发性大规模传染病,临床需求迫切,本研究基于“可得最优证据”,对血必净注射液治疗病毒性肺炎的有效性和安全性进行了评价,探索了多级别、多种类证据整合的新方法,为提高中医药疗效评价的效率和准确性提供了新思路。
本研究仍存在一些局限性:1)纳入研究的整体质量不高,高级别证据数量较少,这影响了结果的证据强度。2)不同类型研究的合并或比较方法尚不完善,导致无法进行进一步的整合评价。3)未找到设置长时间随访的研究,故而无法对血必净治疗病毒性肺炎的远期疗效进行评价。
综合来看,血必净注射液在病毒性肺炎重症及危重症患者的治疗中安全有效,能够缓解症状、控制炎症反应、抑制炎症因子风暴、降低转重及死亡的发生。但是纳入研究质量较低,有可能影响该结论的可信度。
| [1] |
乔璇, 翟慧婷, 李南熹, 等. 病毒性肺炎中医病证结合动物模型研究进展[J]. 中草药, 2024, 55(12): 4248-4255. |
| [2] |
郑民洁, 张博. 中西医结合治疗病毒性肺炎机制的研究进展[J]. 医学理论与实践, 2022, 35(17): 2909-2911. |
| [3] |
田静, 杨爽, 宋丹丹, 韩晓红. 血必净在治疗重症肺炎中的临床疗效研究进展[J]. 临床肺科杂志, 2019, 24(5): 865-868, 873. |
| [4] |
余英荪, 罗丹. 新冠肺炎危重症治疗的探讨[J]. 基层医学论坛, 2021, 25(5): 593-595. |
| [5] |
刘华, 马玉侠, 冯蓓蓓, 等. 中医药防治新型冠状病毒肺炎的研究进展[J]. 中国合理用药探索, 2021, 18(8): 10-12. |
| [6] |
陈良忠, 刘辉, 肖国龙. 血必净注射液在新冠肺炎治疗中的疗效及对CRP的影响[J]. 中国处方药, 2020, 18(10): 110-111. |
| [7] |
文隆, 周志国, 姜迪譞, 等. 血必净注射液对重型新型冠状病毒肺炎患者炎症指标及病情转归的疗效观察[J]. 中华危重病急救医学, 2020, 32(4): 426-429. |
| [8] |
刘凯凤, 付敏, 张郑平, 等. 血必净对2019新型冠状肺炎患者的临床疗效[C]//. 全国科研理论学术研究成果汇编(四), 2020: 395-398.
|
| [9] |
LUO Z J, CHEN W, XIANG M, et al. The preventive effect of Xuebijing Injection against cytokine storm for severe patients with COVID-19:a prospective randomized controlled trial[J]. European Journal of Integrative Medcine, 2021, 42: 101305. DOI:10.1016/j.eujim.2021.101305 |
| [10] |
中华人民共和国国家卫生健康委员会, 关于印发新型冠状病毒肺炎诊疗方案(试行第九版)的通知[EB/OL]. (2022-03-15)[2024-03-10]. http://www.nhc.gov.cn/yzygj/s7653p/202203/b74ade1ba4494583805a3d2e40093d88.shtml.
|
| [11] |
中华人民共和国国务院新闻办公室. 新冠肺炎治疗筛选出"三药三方". [EB/OL]. (2020-03-24)[2021-08-21]. http://www.scio.gov.cn/34473/34474/Document/1675853/1675853.html.
|
| [12] |
刘学松, 宋元林, 关伟杰, 等. 血必净注射液治疗重症新型冠状病毒肺炎的多中心前瞻性队列研究[J]. 中华危重病急救医学, 2021, 33(7): 774-778. |
| [13] |
GUO H, ZHENG J, HUANG G, et al. Xuebijing injection in the treatment of COVID-19: a retrospective case-control study[J]. Ann Palliat Med, 2020, 9(5): 3235-3248. DOI:10.21037/apm-20-1478 |
| [14] |
陈丽, 张安, 李群堂, 等. 血必净联合人免疫球蛋白在重型及危重型新型冠状病毒肺炎中的应用价值[J]. 中华危重病急救医学, 2021, 33(4): 399-404. |
| [15] |
张从玉, 李志浩, 张帅, 等. 血必净治疗新型冠状病毒肺炎的临床疗效观察[J]. 中国医院药学杂志, 2020, 40(9): 964-967. |
| [16] |
李硕, 陆伟, 赵学群, 等. 不同剂量血必净注射液治疗重型新型冠状病毒肺炎的疗效观察[J]. 中国中西医结合急救杂志, 2020, 27(3): 267-270. |
| [17] |
李丹华, 韩甜甜, 张战锋. 联合血必净注射液治疗重症病毒性肺炎的回顾性研究[J]. 时珍国医国药, 2023, 34(5): 1161-1163. |
| [18] |
金鑫瑶, 庞博, 张俊华, 等. 新冠病毒肺炎临床试验核心指标集[J]. Engineering, 2020, 6(10): 196-208. |
| [19] |
强晓钰. 中成药治疗病毒性肺炎的临床证据评价[D]. 天津: 天津中医药大学, 2023.
|
2. Haihe Laboratory of Modern Traditional Chinese Medicine, Tianjin 301617, China
 2024, Vol. 41
2024, Vol. 41