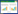文章信息
- 闫赛强, 王朝, 张珣, 等.
- YAN Saiqiang, WANG Chao, ZHANG Xun, et al.
- 疏肝健脾中药联合益生菌治疗失眠的临床疗效及对血清5-羟色胺、褪黑素、血管活性肠肽水平的影响
- Clinical efficacy of herbal medicine for soothing liver and strengthening spleen combined with probiotics in the treatment of insomnia and its influence on serum levels of 5-hydroxytryptamine, melatonin and vasoactive intestinal peptide
- 天津中医药, 2024, 41(3): 287-293
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(3): 287-293
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.03.04
-
文章历史
- 收稿日期: 2023-08-15
2. 河北中医药大学第一附属医院睡眠中心, 石家庄 050010
失眠,主要表现为入睡困难、睡眠维持障碍、早醒,伴有疲劳、情绪低落或激惹等方面的一种主观体验[1]。长期失眠,不仅对患者的心理及社会功能构成威胁,且易共病消化系统、内分泌系统及免疫系统等多系统疾病[2]。目前西医治疗失眠大多采用苯二氮类药物及抗精神类药物,虽可快速缓解失眠症状,但不良反应较多,同时还易出现耐药性、成瘾性、戒断综合征等。中医药治疗失眠症历史悠久,疗效显著,能够降低与其相关的心理障碍、精神障碍、亚健康状态以及其他内科疾病的发病率[3]。近来研究证实,肠道菌群可通过脑肠轴系统的免疫、神经内分泌及迷走神经等途径来调节睡眠,与失眠关系密切[4-5]。成立教授结合长期的临床经验,发现失眠中医辨证属肝郁脾虚型较常见。本研究旨在观察疏肝健脾中药联合益生菌治疗失眠的临床疗效及安全性,并进一步探讨失眠的发生机制,研究结果总结如下。
1 资料与方法 1.1 样本量估算及临床资料 1.1.1 样本量估算本研究为随机对照研究,以临床疗效为观测结局指标,通过查阅相关临床文献[6-7],对照组临床有效率约为70%,治疗组临床有效率预估为93%,设双侧α=0.05,把握度为90%,2组样本量比值1∶1,根据样本量计算公式,n=2p(1-p)(Zα+Zβ)2/(p1-p2)2,计算得出样本量需每组60例,共计120例,考虑到10%左右的脱落率,则至少共需入组130例。
1.1.2 临床资料选取2021年10月—2022年10月于河北中医药大学第一附属医院睡眠中心门诊就诊的130例中医辨证属于肝郁脾虚型失眠患者作为研究对象,按随机数字表法随机分为观察组65例和对照组65例。治疗期间,由于各种原因而导致脱落的病例有6例,两组均脱落3例。最终以124例患者符合规定纳入统计分析。其中观察组62例中,男30例,女32例;年龄19~64岁,平均(41.48±13.66)岁;病程5~48个月,平均(29.29±13.79)个月。对照组62例中,男29例,女33例;年龄18~65岁,平均(40.82±13.24)岁;病程3~45个月,平均(28.73±12.61)个月。两组患者的性别、年龄、病程等资料比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 1.2.1 西医诊断标准参照《睡眠障碍国际分类》第3版(ICSD-3)[8]中失眠的诊断标准拟定:1)入睡难,多梦,早醒、易醒、醒后不易入睡。2)每周至少发生3次,并连续发生30 d以上。3)伴有学习、工作、人际交往等社会功能的损害。4)伴有思维迟钝、注意力不集中、记忆力减退及日间困倦感。
1.2.2 中医诊断标准参照《中医病证诊断疗效标准》[9]和《中医内科学》[10]中不寐的诊断标准制定,中医辨证属于肝郁脾虚型:症见不寐多梦,睡而易醒,醒后不易入睡,可伴情绪抑郁或情绪低落,善太息,胸胁胀痛,神疲乏力,纳呆,腹痛肠鸣,便溏不爽,舌质淡胖或边有齿痕,苔薄白或薄腻,脉弦细弱。
1.3 纳入标准1)符合上述中西医诊断标准及中医证型为肝郁脾虚型。2)年龄18~65岁,男女不限。3)病程≥3个月。4)匹兹堡睡眠质量指数评定量表(PSQI)评分>7分且PSQI评分<16分。5)非过敏体质。6)自愿加入及签署知情同意书,且经河北中医药大学第一附属医院伦理委员会批准(批号:HBZY2021-KY-036-01)。
1.4 排除标准1)年龄<18岁或>65岁者。2)重度失眠者(PSQI评分≥16分)。3)发作性睡病、不宁腿综合征以及睡眠呼吸暂停综合征等其他睡眠障碍的患者。4)伴有重度抑郁[汉密尔顿抑郁量表(HAMD-17)评分>24分]、重度焦虑或有严重精神疾病者。5)伴有循环、呼吸、神经、消化、造血系统等严重原发性疾病或合并恶性肿瘤者。6)近1个月内使用过抗失眠、抗焦虑、抗抑郁等抗精神类药物者。7)妊娠期、哺乳期妇女或有怀孕意向者。8)拒绝签署知情同意书者。9)近1个月内参加其他临床试验者。
1.5 剔除与脱落标准1)治疗期间自行退出者。2)依从性差,未按照本试验要求进行治疗而影响疗效判定者。3)治疗过程中出现严重不良反应者。
1.6 治疗方法 1.6.1 观察组1)给予基于疏肝健脾法拟定的中药免煎颗粒(广州一方制药有限公司)。方药组成:茯苓15 g,白术9 g,陈皮9 g,柴胡6 g,香附12 g,枳壳9 g,郁金9 g,莲子15 g,合欢皮12 g,白芍15 g,玫瑰花6 g,薏苡仁12 g,生龙骨30 g,生牡蛎30 g,炒酸枣仁15 g,1剂/日,早晚饭后1 h热开水冲服;上述中药免煎颗粒均由河北中医药大学第一附属医院中药房提供。2)在中药基础上,同时予双歧杆菌乳杆菌三联活菌片(金双歧,内蒙古双奇药业股份有限公司,国药准字S19980004),每日2次,每次4片,饭后20~30 min服用。
1.6.2 对照组给予右佐匹克隆片(文飞,江苏天士力帝益药业有限公司,国药准字H20070069),每日1次,每次2 mg,睡前20~30 min服用。
1.6.3 疗程及注意事项两组疗程均为4周,疗程结束后评价疗效。治疗期间,两组患者均予常规睡眠卫生教育及心理辅导,建议适当活动、起居规律,并要求睡前忌饮酒、喝咖啡等。
1.7 观察指标 1.7.1 睡眠质量评估采用PSQI评估患者的睡眠改善情况,主要包括入睡时间、睡眠时间、睡眠效率、睡眠质量、睡眠障碍、日间功能障碍等6个因子评分及总分。观察两组患者治疗前1 d、治疗结束后1 d及停药2周后随访时患者的PSQI评分情况。
1.7.2 抑郁程度评估采用HAMD-17评估患者的抑郁程度及情绪改善情况。观察两组患者治疗前1 d、治疗结束后1 d及停药2周后随访时患者的HAMD-17评分情况。
1.7.3 胃肠道症状评估采用胃肠道症状量表(GSRS)评估患者的胃肠道症状改善情况,主要选取腹痛、腹胀、肠鸣、稀便、腹泻5个条目。观察两组患者治疗前1 d、治疗结束后1 d及停药2周后随访时患者的GSRS评分情况。
1.7.4 实验室指标水平检测在治疗前1 d、治疗结束后1 d,两组患者均采集空腹外周静脉血3~5 mL,经离心处理后,由实验室专业人员采用酶联免疫吸附法(ELISA)检测血清5-羟色胺(5-HT)、褪黑素(MT)、血管活性肠肽(VIP)水平。
1.7.5 多导睡眠图(PSG)监测在治疗前1 d、治疗结束后1 d,2组患者均进行连续7 h的PSG监测。主要选取总睡眠时间(TST)、睡眠潜伏期(SL)、觉醒时间(AWT)3项睡眠参数,并要求监测当天不午睡。
1.7.6 不良反应及安全性观察2组患者治疗过程中是否出现头晕头痛、恶心呕吐、口干口苦、乏力等常见不良反应。在治疗前1 d、治疗结束后1 d检查肝功能、肾功能、血常规等指标,并评价两组用药的安全性。
1.8 疗效评定标准参照《中药新药临床研究指导原则(试行)》[11]制定。痊愈:睡眠时间恢复正常或维持6 h以上,醒后精神较佳。显效:症状明显改善或时间延长3 h以上,睡眠相对深沉。有效:睡眠时间延长不足3 h,但症状较前稍改善。无效:无任何好转或者比以前更严重。愈显率=(痊愈+显效)/总例数×100%;总有效率=(痊愈+显效+有效)/总例数×100%。
1.9 统计学方法采用SPSS 26.0统计软件处理分析数据。计量资料用均数±标准差(x±s)表示,若符合正态分布及方差齐性,组间比较采用独立样本t检验,组内比较采用配对样本t检验,PSQI、HAMD-17、GSRS评分则采用重复测量方差分析;反之,则用秩和检验。计数资料用率或构成比表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
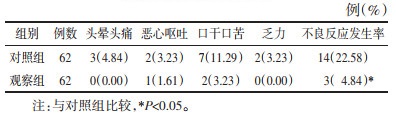
2 结果 2.1 两组患者治疗前后及随访时PSQI评分比较治疗前,两组患者PSQI各因子评分及总分比较,差异均无统计学意义(P>0.05)。治疗4周后及停药2周随访时,两组患者的PSQI各因子评分及总分均低于治疗前(P<0.05);观察组PSQI的睡眠时间、睡眠质量、睡眠障碍、日间功能障碍等各因子评分及总分的降低程度显著优于对照组(P<0.05)。而治疗4周后观察组的入睡时间评分和睡眠效率评分与对照组比较,差异均无统计学意义(P>0.05)。见表 1。
|
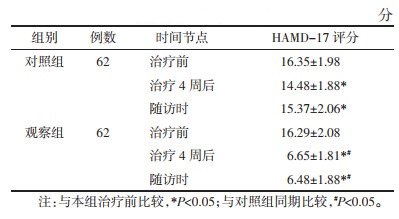
治疗前,两组患者的HAMD-17评分比较,差异无统计学意义(P>0.05)。治疗4周后及停药2周随访时,两组患者的HAMD-17评分均低于治疗前(P<0.05);观察组的HAMD-17评分降低程度显著优于对照组(P<0.05)。见表 2。
|
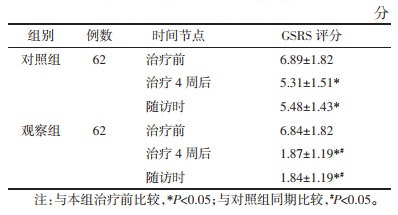
治疗前,两组患者的GSRS评分比较,差异无统计学意义(P>0.05)。治疗4周后及停药2周随访时,两组患者的GSRS评分均低于治疗前(P<0.05);观察组的GSRS评分降低程度显著优于对照组(P<0.05)。见表 3。
|
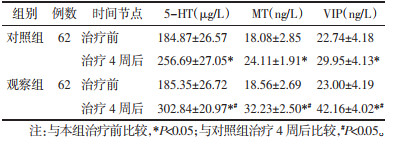
治疗前,两组患者血清5-HT、MT及VIP水平比较,差异无统计学意义(P>0.05)。治疗4周后,两组患者血清5-HT、MT及VIP水平均高于治疗前(P<0.05);观察组血清5-HT、MT及VIP水平均显著高于对照组(P<0.05)。见表 4。
|
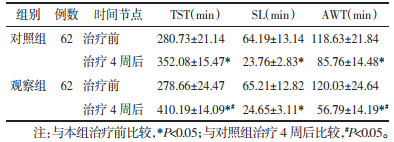
治疗前,两组患者PSG的TST、SL、AWT等3项参数值比较,差异无统计学意义(P>0.05)。治疗4周后,两组患者的3项参数值均优于治疗前(P<0.05);观察组的TST、AWT参数值的改善程度显著优于对照组(P<0.05),而SL参数值的改善程度与对照组比较,差异无统计学意义(P>0.05)。见表 5。
|
治疗4周后,观察组的愈显率为70.97%,高于对照组的45.16%(P<0.05)。而观察组总有效率为91.94%,对照组为80.65%,两组比较,差异无统计学意义(P>0.05)。见表 6。
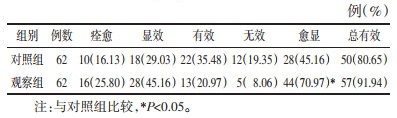
治疗期间,观察组不良反应发生率为4.84%,显著低于对照组的22.58%(P<0.05);且两组患者的肝功能、肾功能、血常规等指标均未见明显异常。见表 7。
失眠的发病机制较为复杂,目前尚不十分明确,西医学公认的病理机制观点是过度觉醒假说和3P假说,主要表现为中枢神经系统的兴奋和抑制功能失调。5-HT是一种联系脑-肠轴系统重要的单胺类神经递质,不仅可通过脑内5-HT1A受体、5-HT2受体增加深睡眠[12],也可作用于肠运动神经元上的受体,调节胃肠道蠕动及黏膜分泌[13]。MT是松果体分泌的吲哚类激素,通过激活MT1和MT2受体来抑制神经元活动和诱导相位转变,以达到镇静催眠和调节睡眠觉醒周期的作用[14-15]。VIP属于肽能神经递质之一,既能增加快动眼睡眠期(REM)和非快动眼睡眠期(NREM)睡眠时间而提高睡眠效率[16],又是松弛胃肠道、参与肠蠕动调节的重要成分[17]。肠道菌群是脑-肠轴系统的重要组成部分,可参与γ-氨基丁酸(GABA)能系统的调节过程,激活下丘脑-垂体-肾上腺轴(HPA),介导其他潜在的神经通路调节,以此来影响睡眠节律[18]。此外,有研究证实,肠道菌群可通过自身及其代谢产物,促进宿主肠嗜铬细胞合成释放5-HT,进而影响睡眠觉醒[19]。
目前失眠主要通过心理、药物、物理及中医等方法进行干预。其中,对于治疗失眠或失眠伴焦虑、抑郁等其他精神障碍疾病,国内失眠诊治专家共识首推认知行为疗法(CBT)[20]。但由于CBT治疗失眠主观性较大,且价格昂贵、疗程较长,单纯应用此方法又会面临患者的依从性问题,故在临床难以有效且完整实施[21]。药物疗法因具有携带方便、见效快等优势,在临床上是主流疗法,主要分为苯二氮类药物、非苯二氮类药物(non-BZDs)、褪黑素受体激动剂、食欲素受体拮抗剂和抗抑郁类药物。对于药物的选择性,中国成人失眠诊断与治疗指南(2017版)首推non-BZDs[1]。右佐匹克隆是一种短效non-BZDs,相较于传统的苯二氮类药物,其起效快,半衰期短,不易产生药物蓄积,但仍存在口苦、头晕、恶心等不良反应[22]。因此,寻找一种治疗失眠的新途径是非常必要的。
失眠,在中医上属“不寐”的范畴,《灵枢·大惑论》指出:“卫气不得入于阴,常留于阳……故目不瞑矣。”卫气不能入于阴分而与营气相交是失眠的重要机制。历代医家学者又指出脏腑功能失调以致心神被扰,神不守舍而不得安寐。病位在心,与肝、脾等脏腑关系密切。如《血证·卧寐》言:“肝病不寐者,肝藏魂,人寤则魂游于目,寐则魂返于肝,若阳浮于外,魂不入肝,则不寐。”肝藏血,血舍魂,肝血充足,魂有所舍,若肝气郁滞,郁久化火,伤及阴血,则魂不守舍,魂不藏肝而夜卧不宁。再者《类证治裁·不寐》云:“思虑伤脾,脾血亏损,经年不寐。”脾藏意,主思,思虑过多可致气结伤脾,脾虚则气血生化乏源,导致脏腑失养,功能失常而难以入眠。成立教授结合长期的临床经验,亦认为失眠与肝脾失调紧密相关,一方面,情志不畅伤肝,肝失疏泄、气机不畅、经脉滞涩,营卫之气运行受阻,阳不入阴而发为失眠,可伴有情绪低落、善太息、胸胁胀痛;另一方面,劳累、思虑过度伤脾,脾失健运,气血生化乏源,气血亏虚、神失所养而发为失眠,可伴有神疲乏力、纳呆、便溏,故失眠的主要病机为肝失疏泄,脾失健运,营卫运行不畅,神失所养。基于此,成立教授采用疏肝健脾中药联合益生菌治疗失眠。
方中柴胡、香附、郁金、合欢皮、玫瑰花疏肝解郁,透达肝经郁滞,使气机畅通,营卫正常运行,则夜卧得安。茯苓、莲子、白术、薏苡仁健脾助运,渗湿止泻,脾得健运,气血充足,心神得养,则夜寐自安。辅以生龙骨、生牡蛎重镇收涩之品,止烦除惊,安神定志;陈皮、枳壳理气健脾,调畅气机;白芍、炒酸枣仁养血补肝,宁心入寐。诸药配伍,肝郁得疏,脾虚得补,营卫运行畅通,心神得养,夜寐得安,诸证自除。据现代药理学研究,龙骨与牡蛎化学成分近似,均有镇静催眠、抗惊厥作用[23];茯苓主要成分茯苓酸可以提高GABA受体α和β亚基水平、降低γ亚基水平实现镇静催眠作用[24];柴胡主要成分柴胡皂苷使小鼠的催眠时间延长,自发性获得癫痫明显减少,表现良好的镇静催眠效果[25];酸枣仁主要成分黄酮类物质可通过调节5-HT1A受体,达到其抗焦虑、镇静催眠作用[26];白芍主要成分芍药苷可提高脑脊液中内源性物质5-HT的水平,发挥镇静催眠作用[27];白术主要成分白术内酯Ⅱ和白术内酯Ⅲ通过调节体内GABA水平而起到镇静催眠、抗焦虑效果[28],此外,白术还可通过降低缺氧神经细胞的凋亡基因及蛋白水平,增加抗凋亡基因及蛋白的产生,使神经细胞凋亡减少而改善神经系统功能[29];合欢皮通过抑制谷氨酸引起的氧化应激反应而改善睡眠障碍、焦虑状态,并且可降低脑组织的神经损伤[30]。香附通过降低皮质酮诱导的乳酸脱氢酶释放水平,减少细胞凋亡而发挥神经细胞保护作用[31]。
本研究结果显示,治疗4周后,在PSQI、HAMD-17、GSRS评分方面,观察组PSQI的睡眠时间、睡眠质量、睡眠障碍、日间功能障碍等各因子评分、PSQI总分、HAMD-17评分及GSRS评分的降低程度优于对照组(P<0.05)。这表明疏肝健脾中药联合益生菌能够提高患者的睡眠质量,改善抑郁情绪及胃肠道功能。在实验室指标方面,观察组的血清5-HT、MT、VIP水平均显著高于对照组(P<0.05),提示疏肝健脾中药联合益生菌可能通过调节相关神经递质及激素水平来治疗失眠。在PSG监测方面,观察组的TST、AWT参数值改善程度显著优于对照组(P<0.05),而SL的改善程度虽低于对照组,但差异无统计学意义(P>0.05)。这说明疏肝健脾中药联合益生菌较口服右佐匹克隆片治疗失眠疗效相当或更优。在不良反应方面,治疗期间,观察组不良反应发生率为4.84%,明显低于对照组的22.58%(P<0.05),表明疏肝健脾中药联合益生菌具有较高的安全性。停药2周后随访时,观察组PSQI的睡眠时间、睡眠质量、睡眠障碍、日间功能障碍等各因子评分、PSQI总分、HAMD-17评分及GSRS评分的降低程度仍优于对照组(P<0.05)。这表明疏肝健脾中药联合益生菌改善失眠具有较好的长期疗效。一方面,通过服用疏肝健脾中药,患者肝郁得疏,脾气健运,脏腑正常功能得以恢复,保持协调及稳定,营卫运行明显改善;另一方面,通过服用中药及益生菌,患者肠道菌群状况显著改善且保持稳态,进而更好地调节与睡眠相关的神经递质及激素水平,故能改善睡眠,且长期效应显著。
综上所述,疏肝健脾中药联合益生菌可有效提高患者的睡眠质量,改善抑郁情绪及胃肠道功能,提升相关神经递质和激素的水平,临床疗效确切,远期疗效显著,且不良反应较少,安全性较高。然而,该研究的病例数量、观察时间相对不足,故今后应进行大样本多中心研究。因此,疏肝健脾中药联合益生菌治疗失眠(肝郁脾虚型)的临床疗效有待深入观察研究。
| [1] |
中华医学会神经病学分会, 中华医学会神经病学分会睡眠障碍学组. 中国成人失眠诊断与治疗指南(2017版)[J]. 中华神经科杂志, 2018, 51(5): 324-335. DOI:10.3760/cma.j.issn.1006-7876.2018.05.002 |
| [2] |
GARLAND S N, JOHNSON J A, SAVARD J, et al. Sleeping well with cancer: a systematic review of cognitive behavioral therapy for insomnia in cancer patients[J]. Neuropsychiatric Disease and Treatment, 2014, 10: 1113-1124. |
| [3] |
中国中医科学院失眠症中医临床实践指南课题组. 失眠症中医临床实践指南(WHO/WPO)[J]. 世界睡眠医学杂志, 2016, 3(1): 8-25. |
| [4] |
LI Y Y, HAO Y L, FAN F, et al. The role of microbiome in insomnia, circadian disturbance and depression[J]. Frontiers in Psychiatry, 2018, 9: 669. DOI:10.3389/fpsyt.2018.00669 |
| [5] |
黄倩, 曾霖, 王高祥, 等. 基于微生物-肠-脑轴理论中医调节肠道菌群治疗失眠研究进展[J]. 天津中医药, 2022, 39(4): 538-544. DOI:10.11656/j.issn.1672-1519.2022.04.25 |
| [6] |
赵子婷, 牟方波. 柴胡加龙骨牡蛎汤联合耳穴压豆治疗肝郁化火型失眠的随机平行对照研究[J]. 中医药信息, 2022, 39(10): 52-56. |
| [7] |
刘俊贤, 许环宇, 刘卓晖, 等. 舒眠胶囊与右佐匹克隆治疗抑郁症轻中度失眠障碍的疗效对比[J]. 中国现代药物应用, 2021, 15(18): 156-158. |
| [8] |
SATEIA M J. International classification of sleep disorders-third edition: highlights and modifications[J]. Chest, 2014, 146(5): 1387-1394. DOI:10.1378/chest.14-0970 |
| [9] |
国家中医药管理局. 中医病证诊断疗效标准[S]. 北京: 中国医药科技出版社, 2012.
|
| [10] |
周仲瑛. 中医内科学[M]. 2版. 北京: 中国中医药出版社, 2007: 146-152.
|
| [11] |
国家中医药管理局. 中药新药临床研究指导原则: 试行[M]. 北京: 中国医药科技出版社, 2002.
|
| [12] |
MONTI J M. Serotonin control of sleep-wake behavior[J]. Sleep Medicine Reviews, 2011, 15(4): 269-281. DOI:10.1016/j.smrv.2010.11.003 |
| [13] |
LUO M, ZHUANG X J, TIAN Z Y, et al. Alterations in short-chain fatty acids and serotonin in irritable bowel syndrome: a systematic review and meta-analysis[J]. BMC Gastroenterology, 2021, 21(1): 14. DOI:10.1186/s12876-020-01577-5 |
| [14] |
DOGHRAMJI K. Melatonin and its receptors: a new class of sleep-promoting agents[J]. Journal of Clinical Sleep Medicine, 2007, 3: S17-S23. |
| [15] |
梁竹, 魏玮, 陶利. 褪黑素在治疗睡眠障碍中的研究进展[J]. 解放军药学学报, 2014, 30(1): 82-85. |
| [16] |
MURCK H, GULDNER J, COLLA-MÜLLER M, et al. VIP decelerates non-REM-REM cycles and modulates hormone secretion during sleep in men[J]. The American Journal of Physiology, 1996, 271(4 Pt 2): R905-R911. |
| [17] |
JAYAWARDENA D, GUZMAN G, GILL R K, et al. Expression and localization of VPAC1, the major receptor of vasoactive intestinal peptide along the length of the intestine[J]. American Journal of Physiology Gastrointestinal and Liver Physiology, 2017, 313(1): G16-G25. DOI:10.1152/ajpgi.00081.2017 |
| [18] |
范晓萱, 赵斌, 张青青, 等. 肠道菌群在失眠症发病机制中的研究进展[J]. 中国临床新医学, 2021, 14(12): 1246-1249. |
| [19] |
YANO J M, YU K, DONALDSON G P, et al. Indigenous bacteria from the gut microbiota regulate host serotonin biosynthesis[J]. Cell, 2015, 161(2): 264-276. DOI:10.1016/j.cell.2015.02.047 |
| [20] |
中华医学会神经病学分会, 中华医学会神经病学分会睡眠障碍学组, 中华医学会神经病学分会神经心理与行为神经病学学组. 中国成人失眠伴抑郁焦虑诊治专家共识[J]. 中华神经科杂志, 2020, 53(8): 564-574. |
| [21] |
蒋晓江, 郝凤仪, 陈南西, 等. 慢性失眠症的团体认知行为疗法[J]. 中国临床神经科学, 2017, 25(1): 112-118. |
| [22] |
柴健. 右佐匹克隆临床应用的研究进展[J]. 继续医学教育, 2020, 34(8): 140-142. |
| [23] |
张晗, 张磊, 刘洋. 龙骨、牡蛎化学成分、药理作用比较研究[J]. 中国中药杂志, 2011, 36(13): 1839-1840. |
| [24] |
陈庆. 茯苓质量控制及药理学研究进展[J]. 亚太传统医药, 2020, 16(8): 154-157. |
| [25] |
江楠, 于靖, 杨莉, 等. 中药柴胡皂苷药理作用的研究进展[J]. 环球中医药, 2018, 11(5): 796-800. |
| [26] |
LIU J, ZHAI W M, YANG Y X, et al. GABA and 5-HT systems are implicated in the anxiolytic-like effect of spinosin in mice[J]. Pharmacology Biochemistry and Behavior, 2015, 128: 41-49. DOI:10.1016/j.pbb.2014.11.003 |
| [27] |
李越峰, 徐富菊, 张泽国, 等. 芍药苷改善睡眠作用机制研究[J]. 中国临床药理学杂志, 2015, 31(1): 56-58. |
| [28] |
SINGHUBER J, BABURIN I, KAHLIG H, et al. GABA (A) receptor modulators from Chinese herbal medicines traditionally applied against insomnia and anxiety[J]. Phytomedicine, 2012, 19: 334-340. DOI:10.1016/j.phymed.2011.10.009 |
| [29] |
胡微煦, 向勤, 文珠, 等. 白术多糖抗神经细胞缺氧性凋亡的机制研究[J]. 中药药理与临床, 2013, 29(4): 84-88. |
| [30] |
艾敏, 李双双, 侯豹, 等. 合欢皮改善荷瘤小鼠异常行为及谷氨酸所诱导神经损伤的研究[J]. 华西药学杂志, 2022, 37(2): 163-168. |
| [31] |
JIA H M, LIU Y, YU M, et al. Neuroprotective effect of cyperi rhizome against corticosterone-induced PC12 cell injury via suppression of Ca2+ overloading[J]. Metabolites, 2019, 9(11): 244. DOI:10.3390/metabo9110244 |
2. Sleep Center, First Affiliated Hospital of Hebei University of Chinese Medicine, Shijiazhuang 050010, China
 2024, Vol. 41
2024, Vol. 41