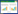文章信息
- 周峰, 薛淑祯, 赵国桢, 等.
- ZHOU Feng, XUE Shuzhen, ZHAO Guozhen, et al.
- 中医药治疗脓毒症临床试验结局指标分析
- Outcome indicators in clinical trials with traditional Chinese medicine treatment of sepsis
- 天津中医药, 2024, 41(3): 323-331
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(3): 323-331
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.03.11
-
文章历史
- 收稿日期: 2023-12-21
2. 北京中医药大学, 北京 100029;
3. 首都医科大学, 北京 100069;
4. 中国中医科学院中医临床基础医学研究所, 北京 100700
脓毒症是一种机体对感染反应失调而引起的生理、病理和生物学异常的危及生命的综合征[1]。最近一项关于全球脓毒症的研究[2]表明,2017年全球有4 890万例脓毒症病例和1 100万例的相关死亡病例。脓毒症高发病率、病死率以及所产生的巨大的经济负担,导致其已经成为一个全球性公共卫生问题[3]。然而,对脓毒症缺乏病理生理学方面的准确认识,导致目前的治疗方案仍以抗感染、液体复苏、脏器支持、机械通气、血管活性药物等对症治疗为主[4]。越来越多的证据表明,中医药以其多通路、多靶点、多效应作用治疗脓毒症的疗效确切[5],尤其是在抗炎、调节免疫、缓解临床症状、改善预后等方面[6]。
但是目前中医药临床研究方法学较为薄弱,特别是结局指标方面的问题尤为突出:规范性差、选择不合理、异质性大等[7],导致单项研究价值的下降以及中医药同类研究很难做到合并和比较分析,导致研究资源的严重浪费。核心结局指标集(COS)是同一医疗保健领域的所有临床试验都应测量和报告最小的指标集合,研制方法学完善、得到临床专家共识的COS是解决上述问题的关键[8]。本研究旨在提取、合并及分析近两年中医药干预脓毒症的随机对照试验(RCTs)中结局指标的使用情况,为相关COS的研究奠定基础。
1 资料与方法 1.1 文献来源计算机检索中国知网(CNKI)、万方数据库(Wanfang Data)、中文科技期刊数据库(VIP)、中国生物医学文献服务系统(SinoMed)、PubMed、Embase与Cochrane Library数据库。为了保证检索的全面性,还会对中国临床试验注册中心和ClinicalTrails.gov中的试验方案进行检索。
1.2 检索策略中文检索词包括“脓毒症”“血液中毒”“脓毒血症”“感染性休克”“脓毒性休克”“多器官功能障碍”以及与中医药相关的词汇,如“中医药”“中药”“针灸”“推拿”“艾灸”“气功”“穴位贴敷”等。英文检索词包括:Sepsis、Bloodstream Infection、Pyemia、Pyohemia、Blood Poisonings、Medicine、Chinese Traditional、Zhong Yi Xue、Traditional Tongue Diagnoses等。检索时间为2021年1月1日到2022年11月1日。
1.3 纳入标准明确诊断为脓毒症且年龄≥18岁的患者;干预措施包括所有与中医药相关或中医学理论指导下的治疗;文献类型设定为RCT。对于患者其他信息(性别、病程、种族),对照组干预措施以及纳入研究语言种类均不进行限定。
1.4 排除标准患者诊断为脓毒症合并并发症:胃肠功能障碍、凝血功能障碍、心肌损伤、肺功能损伤、肝功能损伤、肾损伤、脑损伤;非中文核心期刊的论文;无法获取全文的研究;单页纸的研究;会议论文;学位论文。
1.5 文献筛选将题录信息导入NoteExpress 3.7.0软件,软件去重后阅读题录信息完成初次筛选。然后对符合条件的文献全文阅读,以确定是否最终纳入。筛选工作由两名研究者独立完成并交叉核对。遇到分歧时,请教第3名研究者,如果认同前两名研究者中任何一方的观点,则以第3名研究者的判断为准。如果3名研究者意见均不一致,则讨论决定或咨询相关领域的专家。
1.6 资料提取预先设计资料提取表,条目包括作者人口学信息、样本量、年龄、诊断标准、干预措施、中医证型、疗程、结局指标。
1.7 质量评价采用Cochrane偏倚风险评估工具对研究的偏倚风险进行评估,对“随机序列生成,分配隐藏,受试者和研究人员盲法,结局评价者盲法,结局数据完整性,选择性报告,其他偏倚”7个方面作出低、高或未知风险的评估。
1.8 统计分析首先对筛选过的结局指标进行标准化:1)根据结局指标的相似性进行排序。2)将所有结果的原始定义和名称统一采用标准化术语。3)去除重复结果,对相同结果进行合并,合并结果将被拆分为两个单独的结果。在Excel中对结果进行描述性分析:纳入文献的基本特征、结局指标特征及分类、高频结局指标的使用、诊断标准的选择、指标组合使用情况。
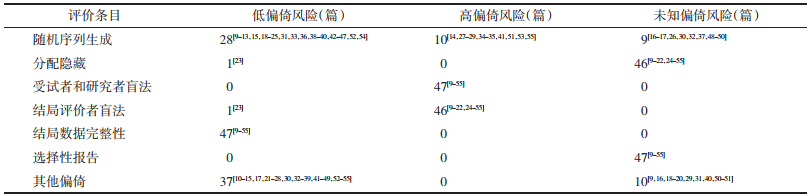
2 结果 2.1 文献检索计算机检索7个中英文数据库和两个临床试验注册库,共获得文献14 254篇,软件去重后剩余8 868篇文献,进一步通过题录信息筛选后剩余658篇文献,阅读全文后决定最终纳入47篇核心期刊文献[9-55]和6篇[56-61]临床试验注册方案。文献筛选流程图见图 1。
|
| 图 1 文献筛选流程图 Fig. 1 Literature screening process |
规范检索后共纳入53项研究6 320例患者,其中中文核心期刊47篇,试验方案6篇。样本量范围为40~1 520例。平均年龄范围为38.7~75.9岁。其中,共有27项研究报告了中医证型[9, 13, 16, 18-25, 28-31, 37-39, 42-45, 47, 50, 52, 54, 58],包括热毒炽盛证[9, 19, 21, 24-25, 37, 42-43, 47]、阳气暴脱证[13, 18, 22, 28-31, 45, 52, 54]、气营两燔证[16]、气阴两虚证[19, 50, 58]、热入营血证[20]、外感发热证[23]、阳虚水泛证[38]、大肠燥热证[39]、脾虚湿盛证[44]。中医干预措施包括中药汤剂[10-11, 20-22, 24-26, 37-39, 42-44, 47-48, 59-60]、颗粒剂[9, 55]、中药注射液[12-19, 24, 27, 29-35, 40, 46, 49-53, 56, 58, 61],五行音乐疗法[10]、刮痧[23]、中药灌胃[28]、中药灌肠[41]、艾灸[36]、电针[45, 52, 57]。纳入文献基本特征见表 1。
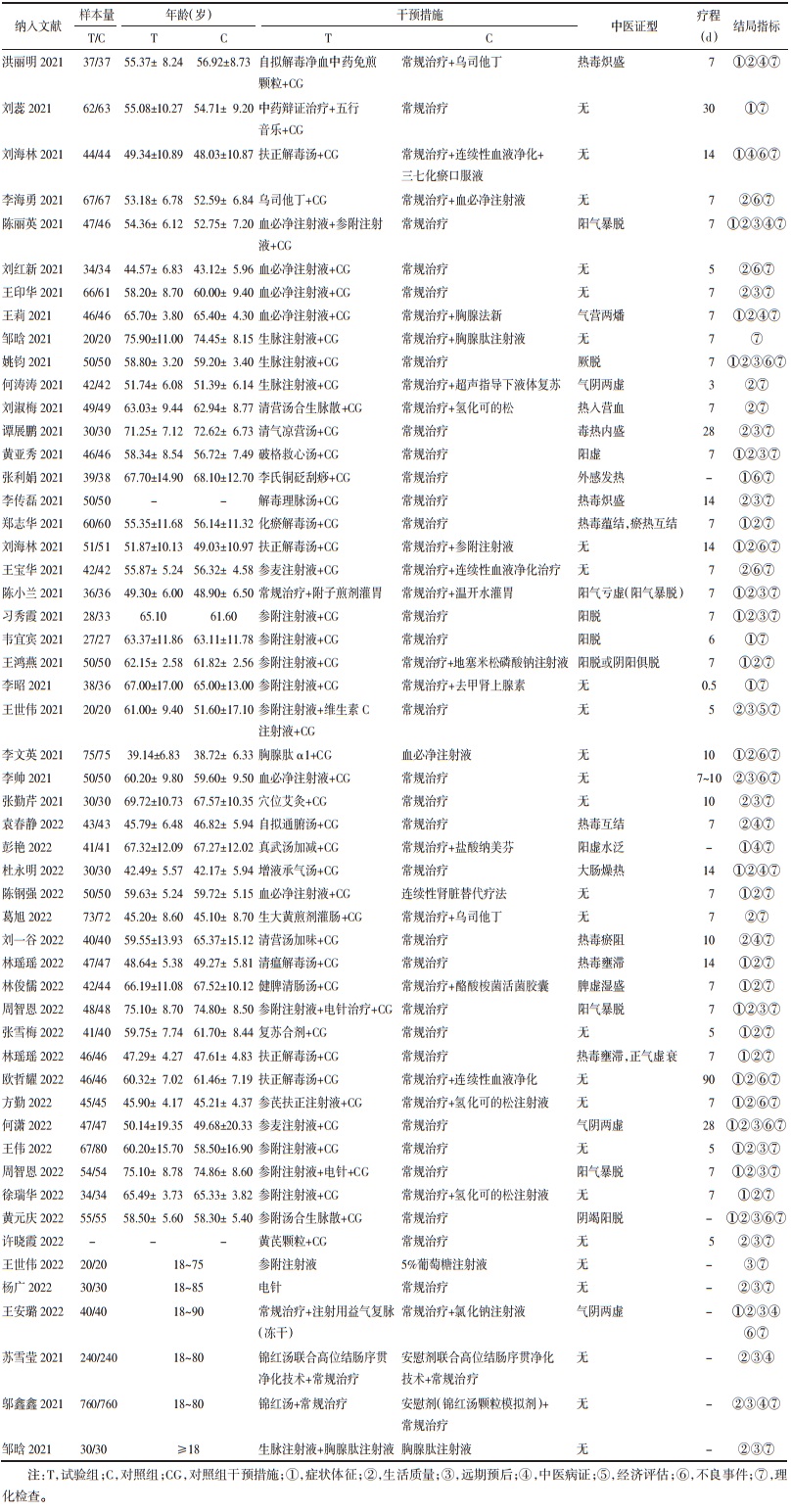
对47篇核心期刊文献[9-55]进行偏倚风险评估,见表 2。随机序列生成方面,24项研究[10, 13, 15, 19-25, 31, 33, 36, 38-40, 42-47, 52, 54]使用随机数字表分组被评为低风险,1项研究[11]使用信封法被评为低风险,1项研究[18]使用抛硬币的方法被评为低风险,1项研究[28]根据入院时间分组被评为高风险,9项研究[14, 27, 29, 34-35, 41, 51, 53, 55]根据治疗方法分组被评为高风险,9项研究[16-17, 26, 30, 32, 37, 48-50]被评为未知偏倚风险。分配隐藏方面,1项研究[23]使用不透光信封法被评为低风险,其余研究[9-22, 24-55]均未提及,被评为未知偏倚风险。所有研究[9-55]均未对受试者和研究人员设盲,均评为高风险。1项研究[23]对结局评价者设盲,被评为低风险,其余[9-22, 24-55]被评为高风险。所有研究[9-55]数据完整,数据完整性被评为低风险。选择性报告方面,所有研究[9-55]均被评为未知偏倚风险。37项研究[10-15, 17, 21-28, 30, 32-39, 41-49, 52-55]由政府资助,其他偏倚被评为低风险,其余[9, 16, 18-20, 29, 31, 40, 50-51]被评为未知偏倚风险。
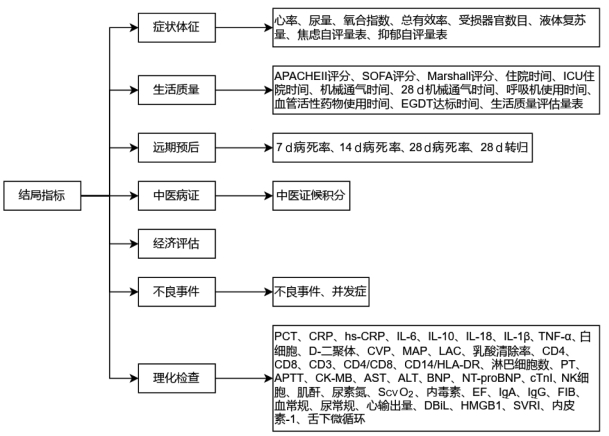
53项研究共报告了569个结局指标,161种结局指标,平均每项研究报告11个结局指标。对使用次数≥2次的结局指标进行分类分析,参考《中医药临床试验核心指标集研制技术规范》[62],依照指标的功能属性分为7个部分,见图 2。
|
| 注:PCT,降钙素原;IL-6,白介素-6;IL-10,白介素-10;IL-18,白介素-18;IL-1β,白介素-1β;CVP,中心静脉压;MAP,平均动脉压;LAC,乳酸;APTT,活化部分凝血酶时间;PT,凝血酶原时间;CK-MB,肌酸激酶同工酶;TNF-α,肿瘤坏死因子-α;AST,天门冬氨酸氨基转移酶;ALT,丙氨酸氨基转移酶;hs-CRP,超敏C反应蛋白;CRP,C反应蛋白;BNP,脑钠肽;NT-proBNP,氨基末端脑钠肽前体;cTnI,心肌肌钙蛋白Ⅰ;ScvO2,中心静脉血氧饱和度;EF,左室射血分数;IgA,免疫球蛋白A;IgG,免疫球蛋白G;FIB,纤维蛋白原;DBiL,直接胆红素;HMGB1,血清高迁移率族蛋白B1;SVRI,外周血管阻力指数。 图 2 结局指标分类图 |
使用频率最高的15个结局指标为:急性生理与慢性健康(APACHEⅡ)评分、降钙素原、序贯器官衰竭(SOFA)评分、C反应蛋白、总有效率、28 d病死率、白介素-6、平均动脉压、重症监护室(ICU)住院时间、乳酸、不良事件、肿瘤坏死因子-α、CD4、CD8和中医证候积分,见表 3。
53项研究采用的脓毒症诊断标准共计11种[1, 63-72],种类及频数见表 4。
纳入的53项研究中,有10项研究[12, 16, 20, 25, 27, 36, 39, 42, 47-48]同时使用APACHEⅡ评分和降钙素原;有5项研究[22, 29, 34, 53, 55]同时使用APACHEⅡ评分、降钙素原、SOFA评分;有5项研究[14, 24, 33, 35, 58]同时使用APACHEⅡ评分、降钙素原、SOFA评分、C反应蛋白;有2项研究[31, 40]同时使用APACHEⅡ评分、降钙素原、SOFA评分、C反应蛋白、总有效率。
3 讨论 3.1 纳入研究的合理性结局指标作为试验设计和分析的重要部分,纳入文献质量对结局指标质量有重要影响。本研究的文献筛选方法从两个方面提升结局指标质量。第一,考虑到只纳入高质量文献会导致结局指标具有局限性,纳入全部类型的文献又会导致工作量繁重,可行性较差。所以本研究仅纳入核心期刊发表的RCT,整体质量较高且指标选择较为全面。第二,本研究开始前初步检索相关文献数量较多,参考《中医药核心指标集研究中指标池构建相关影响因素分析》[7],本研究限制文献发表年份为近2年,基本可以包含新老指标,且可以保证结局指标的时效性和临床代表性。
3.2 纳入研究的局限性 3.2.1 偏倚风险较大对47项RCTs的偏倚风险评估结果显示,纳入研究方法学质量较差,偏倚风险较高。大多数研究都采用了主观性的结局指标,例如总有效率、APACHEⅡ评分、SOFA评分等,且所有研究均未对受试者和实验人员设盲,导致受试者和试验人员主观因素对结果的影响较大,增加了信息偏倚。所有研究均未提前注册,选择性报告偏倚和发表偏倚较高,可能导致结局指标选择更加偏向阳性结果,影响临床试验的真实性。
3.2.2 诊断标准差异较大纳入研究中,91%的研究报告了脓毒症的诊断标准,但诊断标准间差异较大。目前国内和国际上脓毒症诊断标准种类较多,尽管国内和国际学者们对脓毒症的定义和诊断标准不断探索和完善,但由于人群体质和地理因素等的差异存在,尚未形成公认的脓毒症诊断标准。未来可以通过建立中国脓毒症患者诊断标准的专家共识来实现诊断标准的标准化、一体化,避免同类研究难以合并导致研究资源的浪费。
3.3 结局指标选取的合理性应用频次最高的两项指标分别是APACHEⅡ评分、PCT。APACHEⅡ评分是重症监护中应用最多的评分系统[73],可准确评估患者的病情,指导进一步治疗以及预测脓毒症患者的病死率。PCT是一种广泛应用于脓毒症的诊断,治疗和预后评估炎症指标。大量研究表明[74-75],PCT相比于传统炎症指标具有明显的优势,例如持续时间长,特异性高,数值与疾病严重程度呈正相关等。脓毒症以其高发病率、高病死率、预后较差等已经成为ICU患者的主要死亡原因,APACHEⅡ评分和PCT均可以准确、快速评估患者病情,指导进一步治疗。
3.4 结局指标选取的局限性 3.4.1 结局指标选取异质性大单项研究中,结局指标选取数量最少为3个,最多为38个,结局指标选取异质性大,指标离散程度高,且纳入研究中指标组合使用随意性较大。上述问题会导致研究结果脱离临床需求,临床结果应用价值严重受损,同类研究难以进行合并分析结果。这可以通过建立中医药治疗脓毒症相关的COS来解决,规定临床研究中必须报告的最小指标集合,有助于减少临床研究中的偏倚,提升研究价值。
3.4.2 忽视中医特色指标、安全性指标和经济学指标纳入研究均采用了中医相关的治疗,但仅有11项研究选择了中医证候积分这项指标。指标选择过分关注理化检查,缺乏中医特色。且中医证候积分作为结局指标主观性较大,作为疗效评价的指标缺乏真实性和代表性,这恰恰是中医临床研究质量较低的原因之一。53项研究中仅有1项研究[33]选择了“人均费用”作为结局指标,其余均未报道经济学指标,中医相关的特色治疗如针灸、推拿等,治疗费用和西药相比普遍较低,所以经济学指标也应作为临床研究的结局指标之一。纳入本研究中的14项研究[11-12, 14, 18, 23, 26-27, 34-35, 48-50, 54, 58]报告了不良事件,2项研究[41, 43]报告了并发症。据2018年度统计中药不良反应占比14.6%[76],因此所有中医药临床研究均应详细报告不良反应发生情况,无不良反应也需在文中提及。
3.4.3 结局指标报告不规范第一,结局指标类型随意转换,例如对于连续性变量的临床疗效指标,多转化为等级资料显效、有效、无效,最终以“总有效率”指标进行统计学分析,且不同研究间疗效评价标准也不统一。上述问题导致研究原始数据缺失,严重影响数据的二次合并分析。第二,结局指标主次不分。主要结局指标是直接与试验目的有本质联系的观察指标,通常只预设1个;次要指标是指与试验目的相关的具有辅助性质的指标,通常可预设多个。指标主次不分、杂乱无序,会严重影响研究的质量和可信度。第三,结局指标存在相似交叉条目,例如生活质量评分以8个维度来进行评估,在中医证候积分以及其他多项评分量表中均有重复交叉的现象。
3.4.4 测量工具及时点不统一纳入研究在结局指标的测量工具的选择具有很大的异质性。例如,同一结局指标“总有效率”,测量工具的选择就包括了4种[67, 69, 77-79]。目前中国研究者已经逐步开展COS的研究工作,但对测量工具的选择却缺乏关注,所以COS的研究人员应在完成后,为每一个结局指标确定相应的测量工具并推广到临床应用当中。相同指标测量时点差异较大,如远期预后指标病死率的测量时点就包括7、14、28 d等。测量时点多且跨度较大,导致指标的差异性增加,严重影响指标的临床有效性和可信度。
3.5 结局指标应用的思考自古以来,中医药的发展源于临床观察和经验的总结,其发展路线遵循实践到理论到实践的原则,其中临床疗效是核心所在。临床试验证据等级最高的就是系统评价和Meta分析,但临床研究过程中发现,大量同类研究因为结局指标的选择、描述、测量等问题难以合并分析,导致研究资源的严重浪费。对此,建立中医药相关的COS是解决问题的关键。自从2012年中国研究者注册了第1项中医药领域的COS之后,陆续出现了一系列相关的技术规范和专家共识,但是COS的研制尚未有成熟和公认的方法和体系。中医药COS应该以中医临床为基点,借鉴西医研究方法,取其精华去其糟粕,构建具有中医药特色,适合中国临床研究的COS。
4 总结本研究通过分析近两年中医药治疗脓毒症RCTs中结局指标的选择现状,提出了目前结局指标应用的优势和局限性,为后续COS的研制提供参考。但本研究尚存在一些局限性:纳入研究数量较少;仅纳入中医药干预的研究,未与西医学干预研究中的结局指标进行对比分析等。未来仍需纳入新发表的高质量文献进行补充以及与脓毒症的西医结局指标域进行对比分析,规范指标选择和报告,推动中医特色临床评价体系的进步与发展。
| [1] |
SINGER M, DEUTSCHMAN C S, SEYMOUR C W, et al. The third international consensus definitions for sepsis and septic shock(sepsis-3)[J]. JAMA, 2016, 315(8): 801-810. DOI:10.1001/jama.2016.0287 |
| [2] |
RUDD K E, JOHNSON S C, AGESA K M, et al. Global, regional, and national sepsis incidence and mortality, 1990-2017:analysis for the global burden of disease study[J]. The Lancet, 2020, 395(10219): 200-211. DOI:10.1016/S0140-6736(19)32989-7 |
| [3] |
REINHART K, DANIELS R, KISSOON N, et al. Recognizing sepsis as a global health priority-a WHO resolution[J]. The New England Journal of Medicine, 2017, 377(5): 414-417. DOI:10.1056/NEJMp1707170 |
| [4] |
CECCONI M, EVANS L, LEVY M, et al. Sepsis and septic shock[J]. The Lancet, 2018, 392(10141): 75-87. DOI:10.1016/S0140-6736(18)30696-2 |
| [5] |
姜爽, 梁群. 中医药治疗脓毒症的进展研究[J]. 中国中医急症, 2022, 31(8): 1299-1302. DOI:10.3969/j.issn.1004-745X.2022.08.048 |
| [6] |
FAN T T, CHENG B L, FANG X M, et al. Application of Chinese medicine in the management of critical conditions: a review on sepsis[J]. The American Journal of Chinese Medicine, 2020, 48(6): 1315-1330. DOI:10.1142/S0192415X20500640 |
| [7] |
张明妍, 蔡慧姿, 牛柏寒, 等. 中医药核心指标集研究中指标池构建相关影响因素分析[J]. 中国循证医学杂志, 2021, 21(4): 464-468. |
| [8] |
张明妍, 李凯, 蔡慧姿, 等. 临床试验核心指标集研究发展概况及其在中医药领域的关键问题[J]. 中医杂志, 2021, 62(2): 108-113. DOI:10.3969/j.issn.0411-8421.2021.02.018 |
| [9] |
洪丽明, 李乐辉, 吴国平. 自拟解毒净血中药免煎颗粒剂联合乌司他丁治疗热毒炽盛型脓毒血症的疗效观察[J]. 中国中医急症, 2021, 30(7): 1275-1278. DOI:10.3969/j.issn.1004-745X.2021.07.040 |
| [10] |
刘蕊, 万思琪, 徐雅新. 中医辨证施护联合五行音乐对ICU脓毒症卧床患者负性情绪、睡眠质量和炎性因子的影响[J]. 长春中医药大学学报, 2021, 37(3): 619-622. |
| [11] |
刘海林, 霍娟勇, 燕垚旬. 中药扶正解毒汤联合三七化瘀口服液对脓毒血症患者中医证候积分的影响[J]. 中国药业, 2021, 30(15): 92-95. DOI:10.3969/j.issn.1006-4931.2021.15.026 |
| [12] |
李海勇, 王海燕, 刘丽静, 等. 血必净注射液联合乌司他丁治疗创伤性脓毒症临床效果及对炎性因子、肝功能影响[J]. 临床误诊误治, 2021, 34(7): 24-28. DOI:10.3969/j.issn.1002-3429.2021.07.006 |
| [13] |
陈丽英, 张彩虹, 卞阳阳, 等. 血必净注射液联合参附注射液治疗脓毒性休克阳气暴脱证疗效观察及对血清炎症指标和心肌损伤标志物的影响[J]. 河北中医, 2021, 43(5): 762-766. DOI:10.3969/j.issn.1002-2619.2021.05.012 |
| [14] |
刘红新, 孟舰, 武小娟, 等. 血必净注射液辅助治疗对脓毒症患者病情及微小高迁移率族蛋白B1、微小RNA-223表达的影响[J]. 解放军医药杂志, 2021, 33(2): 93-96. DOI:10.3969/j.issn.2095-140X.2021.02.021 |
| [15] |
王印华, 王宝华, 庞楠, 等. 血必净注射液对脓毒症患者的免疫调理作用[J]. 中国中西医结合急救杂志, 2021, 28(2): 132-135. DOI:10.3969/j.issn.1008-9691.2021.02.002 |
| [16] |
王莉, 朱瑞卿, 丛晓, 等. 血必净联合胸腺法新对革兰阴性菌血流感染所致脓毒症患者免疫功能、心肾靶器官损害的影响[J]. 现代中西医结合杂志, 2021, 30(16): 1755-1759. DOI:10.3969/j.issn.1008-8849.2021.16.010 |
| [17] |
邹晗, 钱何布, 赵宏胜. 胸腺肽联合生脉注射液对免疫功能低下脓毒症患者细胞免疫功能的影响[J]. 中国中西医结合急救杂志, 2021, 28(2): 136-140. DOI:10.3969/j.issn.1008-9691.2021.02.003 |
| [18] |
姚钧, 张茜利, 宣娟娟, 等. 生脉注射液治疗重症监护室脓毒症休克患者临床研究[J]. 新中医, 2021, 53(17): 94-97. |
| [19] |
何涛涛, 曹樟全, 张洪波. 生脉注射液联合超声指导下液体复苏治疗脓毒性休克临床研究[J]. 新中医, 2021, 53(20): 74-78. |
| [20] |
刘淑梅, 阳建军. 清营汤合生脉散加减治疗脓毒症(热入营血证)的临床研究[J]. 中国中医急症, 2021, 30(2): 309-311. DOI:10.3969/j.issn.1004-745X.2021.02.034 |
| [21] |
谭展鹏, 王媛媛, 郭世俊, 等. 清气凉营汤对脓毒症患者HMGB1、sRAGE及免疫功能的影响[J]. 中国中医急症, 2021, 30(1): 71-73, 80. |
| [22] |
黄亚秀, 李少萍, 黄永莲, 等. 破格救心汤治疗脓毒性休克的疗效观察[J]. 中国中医急症, 2021, 30(3): 488-491. DOI:10.3969/j.issn.1004-745X.2021.03.030 |
| [23] |
张利娟, 郑静霞, 徐艳, 等. 李氏铜砭刮痧对脓毒症外感发热患者即时退热效果的影响[J]. 现代中西医结合杂志, 2021, 30(34): 3845-3849. DOI:10.3969/j.issn.1008-8849.2021.34.019 |
| [24] |
李传磊, 谢云, 郑志煌, 等. 解毒理脉汤治疗热毒炽盛型脓毒症的临床研究[J]. 中华危重病急救医学, 2021, 33(7): 815-820. DOI:10.3760/cma.j.cn121430-20201228-00776 |
| [25] |
郑志华, 周广军. 化瘀解毒汤对脓毒症患者血清炎症因子水平和APACHEⅡ评分的影响[J]. 中国中医急症, 2021, 30(11): 1984-1986. DOI:10.3969/j.issn.1004-745X.2021.11.026 |
| [26] |
刘海林, 霍娟勇, 燕垚旬. 扶正解毒汤联合参麦注射液对脓毒血症患者体液免疫功能的影响[J]. 中国药业, 2021, 30(9): 74-76. DOI:10.3969/j.issn.1006-4931.2021.09.022 |
| [27] |
王宝华, 张宗芳, 王飞飞, 等. 参麦注射液联合早期连续性血液净化治疗对脓毒症患者血清CRP、PCT、凝血功能指标的影响及预后分析[J]. 解放军医药杂志, 2021, 33(12): 101-104, 108. DOI:10.3969/j.issn.2095-140X.2021.12.024 |
| [28] |
陈小兰, 陶福正, 郑道国, 等. 参麦注射液联合附子灌胃改善脓毒症休克患者心功能临床研究[J]. 新中医, 2021, 53(7): 77-80. |
| [29] |
习秀霞, 李景荣. 参附注射液治疗脓毒性休克患者的疗效观察[J]. 中国中医急症, 2021, 30(8): 1453-1455. DOI:10.3969/j.issn.1004-745X.2021.08.036 |
| [30] |
韦宜宾, 吴瑕, 蒙竹韵, 等. 参附注射液用于脓毒症休克早期复苏的疗效分析及对呼气末二氧化碳的影响[J]. 中医药学报, 2021, 49(10): 67-71. |
| [31] |
王鸿燕, 赵月娥, 林泽辉, 等. 参附注射液联合糖皮质激素治疗脓毒症的疗效观察[J]. 中国中医急症, 2021, 30(3): 518-520. DOI:10.3969/j.issn.1004-745X.2021.03.040 |
| [32] |
李昭, 吴彩军, 刘力, 等. 参附注射液联合去甲肾上腺素在脓毒症休克治疗中的应用[J]. 中国急救复苏与灾害医学杂志, 2021, 16(5): 519-521. DOI:10.3969/j.issn.1673-6966.2021.05.014 |
| [33] |
王世伟, 吕丹, 龚好, 等. 参附联合维生素C对脓毒性休克患者血管内皮损伤的保护作用研究[J]. 临床急诊杂志, 2021, 22(10): 641-646. |
| [34] |
李文英, 张锐, 汪得喜, 等. 血必净注射液联合胸腺肽α1对重症肺炎合并脓毒症患者血气指标、炎症因子及免疫功能的影响[J]. 现代生物医学进展, 2021, 21(8): 1502-1506. |
| [35] |
李帅, 鹿兴, 徐磊. 血必净注射液治疗ICU脓毒症患者的临床观察[J]. 中草药, 2021, 52(12): 3656-3660. DOI:10.7501/j.issn.0253-2670.2021.12.023 |
| [36] |
张勤芹, 张浩, 周菲儿, 等. 艾灸对脓毒症患者免疫功能影响的临床研究[J]. 中国中医急症, 2021, 30(1): 74-76, 108. |
| [37] |
袁春静, 焦浩, 贾月霞. 自拟通腑汤治疗脓毒症患者临床观察[J]. 中国中医急症, 2022, 31(5): 827-830. DOI:10.3969/j.issn.1004-745X.2022.05.019 |
| [38] |
彭艳, 肖飞. 真武汤加减联合盐酸纳美芬对老年脓毒性休克患者血流动力学及免疫功能的影响[J]. 陕西中医, 2022, 43(7): 897-901. DOI:10.3969/j.issn.1000-7369.2022.07.020 |
| [39] |
杜永明, 张汉洪, 王森. 增液承气汤联合常规治疗对大肠燥热型脓毒血症患者的临床疗效[J]. 中成药, 2022, 44(4): 1126-1130. DOI:10.3969/j.issn.1001-1528.2022.04.015 |
| [40] |
陈钢强, 王剑荣. 血必净注射液联合CRRT治疗脓毒症合并多器官功能障碍临床研究[J]. 新中医, 2022, 54(4): 98-101. |
| [41] |
葛旭, 王国兴. 生大黄保留灌肠联合乌司他丁对脓毒症合并MODS患者免疫内稳态及炎症水平的影响[J]. 医学综述, 2022, 28(9): 1795-1800. DOI:10.3969/j.issn.1006-2084.2022.09.023 |
| [42] |
刘一谷, 郭应军. 清营汤联合西医治疗对脓毒症患者炎症反应及凝血功能的影响[J]. 广州中医药大学学报, 2022, 39(2): 265-270. |
| [43] |
林瑶瑶, 林先萍, 霍娟勇. 清瘟解毒汤联合常规治疗对热毒壅滞型细菌性脓毒血症患者的临床疗效[J]. 中成药, 2022, 44(1): 87-91. |
| [44] |
林俊儒, 华云玮, 李放. 健脾清肠汤治疗脓毒症腹泻的临床疗效及对患者肠道功能和炎症指标的影响[J]. 河北中医, 2022, 44(3): 378-382. DOI:10.3969/j.issn.1002-2619.2022.03.007 |
| [45] |
周智恩, 卢萍, 姚娟, 等. 回阳救逆综合疗法对脓毒症休克患者液体复苏及预后的影响研究[J]. 现代中西医结合杂志, 2022, 31(11): 1461-1465. DOI:10.3969/j.issn.1008-8849.2022.11.001 |
| [46] |
张雪梅, 郭文辉, 于秋香, 等. 复苏合剂对感染性休克患者舌下微循环及相关因素的影响[J]. 中国中西医结合杂志, 2022, 42(8): 968-972. |
| [47] |
林瑶瑶, 霍娟勇, 刘海林. 扶正解毒汤联合常规治疗对热毒壅滞、正气虚衰型脓毒血症患者的临床疗效[J]. 中成药, 2022, 44(6): 1825-1828. DOI:10.3969/j.issn.1001-1528.2022.06.018 |
| [48] |
欧哲耀, 林文燕, 邓小彦. 扶正解毒汤对脓毒血症患者临床疗效的影响[J]. 实用临床医药杂志, 2022, 26(7): 22-25. |
| [49] |
方勤, 柳彦涛, 王建辉. 参芪扶正注射液联合氢化可的松治疗脓毒症的临床研究[J]. 现代药物与临床, 2022, 37(3): 552-556. |
| [50] |
何潇. 参麦注射液对脓毒性休克患者炎症因子及预后的影响[J]. 新中医, 2022, 54(7): 107-110. |
| [51] |
王伟, 秦超, 卜克, 等. 参附注射液治疗脓毒症休克67例疗效观察[J]. 安徽医药, 2022, 26(7): 1458-1462. DOI:10.3969/j.issn.1009-6469.2022.07.043 |
| [52] |
周智恩, 卢萍, 姚娟, 等. 参附注射液联合电针治疗脓毒症休克临床研究[J]. 新中医, 2022, 54(19): 116-120. |
| [53] |
徐瑞华, 张会珍, 张娆娆. 参附注射液辅助治疗脓毒症的效果及对患者血清PCT、hs-CRP及免疫指标的影响[J]. 海南医学, 2022, 33(1): 10-13. |
| [54] |
黄元庆, 周明亮, 周皓岚. 参附汤合生脉散治疗脓毒症休克阴竭阳脱证[J]. 长春中医药大学学报, 2022, 38(10): 1117-1121. |
| [55] |
许晓霞, 陈坚波, 钟旭军, 等. 不同剂量黄芪对脓毒症患者外周血T淋巴细胞亚群、NK细胞、血清PAF水平及短期预后的影响[J]. 中华医院感染学杂志, 2022, 32(4): 481-485. |
| [56] |
王世伟. 参附注射液在脓毒症治疗中的作用和意义研究[EB/OL]. (2022-05-24)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=166792.
|
| [57] |
杨广. 电针足三里、气海、关元治疗通过PD-1等通路治疗脓毒症患者免疫功能的临床研究[EB/OL]. (2022-05-08)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=168069.
|
| [58] |
王安璐. 注射用益气复脉(冻干)治疗脓毒症气阴两虚证的随机、单盲、安慰剂对照试验[EB/OL]. (2022-10-21)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=135462.
|
| [59] |
苏雪莹. 基于"截断扭转"策略的中医药防治脓毒症循证评价及效应机制研究—锦红汤联合高位结肠序贯净化技术治疗脓毒症临床研究[EB/OL]. (2021-08-02)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=129810.
|
| [60] |
邬鑫鑫. 基于"截断扭转"策略的中医药防治脓毒症循证评价及效应机制研究锦红汤内服治疗脓毒症的临床研究[EB/OL]. (2021-11-23)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=120730.
|
| [61] |
邹晗. 生脉注射液联合胸腺肽对免疫功能低下脓毒症患者细胞免疫功能的影响: 一项前瞻、随机、对照临床研究[EB/OL]. (2021-07-06)[2022-11-05]. http://www.chictr.org.cn/showproj.aspx?proj=122302.
|
| [62] |
张明妍, 张俊华, 张伯礼, 等. 中医药临床试验核心指标集研制技术规范[J]. 中华中医药杂志, 2021, 36(2): 924-928. |
| [63] |
曹钰, 柴艳芬, 邓颖, 等. 中国脓毒症/脓毒性休克急诊治疗指南(2018)[J]. 感染、炎症、修复, 2019, 20(1): 3-22. |
| [64] |
RHODES A, EVANS L E, ALHAZZANI W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock: 2016[J]. Intensive Care Medicine, 2017, 43(3): 304-377. |
| [65] |
中华医学会重症医学分会, 严静. 中国严重脓毒症/脓毒性休克治疗指南(2014)[J]. 中华内科杂志, 2015, 54(6): 557-581. |
| [66] |
DELLINGER R P, LEVY M M, RHODES A, et al. Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock, 2012[J]. Intensive Care Medicine, 2013, 39(2): 165-228. |
| [67] |
BONKAT G, PICKARD R, BARTOLETTI R, et al. EAU guidelines on urological infections(2017). [EB/OL]. (2017-04-03)[2022-11-05]. http://uroweb.org/guideline/urological-infections/.
|
| [68] |
ZHANG Z, SMISCHNEY J N, ZHANG H, et al. AME证据系列001:转化医学协会: 脓毒症诊断和早期识别的临床实践指南[J]. 临床与病理杂志, 2016, 36(10): 1467-1476. |
| [69] |
中国中西医结合学会急救医学专业委员会, 《中国中西医结合急救杂志》编辑委员会. 脓毒症中西医结合诊治专家共识[J]. 中华危重病急救医学, 2013, 25(4): 194-197. |
| [70] |
LEVY M M, FINK M P, MARSHALL J C, et al. 2001 SCCM/ESICM/ACCP/ATS/SIS international sepsis definitions conference[J]. Intensive Care Medicine, 2003, 29(4): 530-538. |
| [71] |
高戈, 冯喆, 常志刚, 等. 2012国际严重脓毒症及脓毒性休克诊疗指南[J]. 中华危重病急救医学, 2013, 25(8): 501-505. |
| [72] |
王仲, 魏捷, 朱华栋, 等. 中国脓毒症早期预防与阻断急诊专家共识[J]. 实用休克杂志(中英文), 2020, 4(3): 168-177, 185. |
| [73] |
周利平, 邓跃林, 唐朝喜. APACHEⅡ评分引入MODS评分系统对急诊内科危重患者预后的预测价值[J]. 中国现代医学杂志, 2004, 14(9): 116-118. |
| [74] |
ASSICOT M, BOHUON C, GENDREL D, et al. High serum procalcitonin concentrations in patients with sepsis and infection[J]. The Lancet, 1993, 341(8844): 515-518. |
| [75] |
杜斌, 陈德昌, 潘家绮, 等. 降钙素原与白介素-6的相关性优于传统的炎症指标[J]. 中国危重病急救医学, 2002, 14(8): 474-477. |
| [76] |
国家药品不良反应监测年度报告(2018年)[J]. 中华药物评价, 2019, 36(6): 476-480.
|
| [77] |
中华人民共和国卫生部. 中药新药临床研究指导原则: 第1辑[M]. 北京, 1993: 37-39.
|
| [78] |
国家中医药管理局. 中药新药临床研究指导原则[S]. 北京: 中国医药科技出版社, 2002.
|
| [79] |
王蔚文. 临床疾病诊断与疗效判断标准[M]. 北京: 科学技术文献出版社, 2010: 478-480.
|
2. Beijing University of Chinese Medicine, Beijing 100029, China;
3. Capital Medical University, Beijing 100069, China;
4. Institute of Basic Research in Chinese Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China
 2024, Vol. 41
2024, Vol. 41