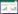文章信息
- 李静, 王小英, 武苗, 等.
- LI Jing, WANG Xiaoying, WU Miao, et al.
- 参莲胶囊联合奥希替尼对EGFR突变的晚期非小细胞肺癌(气阴两虚证)的疗效分析
- Effect analysis of Shenlian Capsule combined with osimertinib on advanced EGFR mutated non-small cell lung cancer (qi and yin deficiency syndrome)
- 天津中医药, 2024, 41(4): 432-435
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(4): 432-435
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.04.06
-
文章历史
- 收稿日期: 2023-10-10
2. 涉县中医院肿瘤科, 邯郸 056400
肺癌是全球发病率和病死率最高的恶性肿瘤之一,不仅严重影响人类健康,还给患者和社会带来了巨大的经济负担[1]。肺癌中最常见的组织学类型是非小细胞肺癌,占比约为80%~85%[2]。参莲胶囊的功效是活血化瘀、清热解毒、利湿行气、解郁,常用于由热毒内阻、气血瘀滞而导致的中晚期肺癌患者。奥希替尼靶向表皮生长因子受体,选择性及不可逆性较高,对表皮生长因子受体(EGFR)突变的非小细胞肺癌患者的生存期有一定的延长作用[3-4]。奥希替尼治疗突变的EGFR非小细胞肺癌患者有较高的安全性[5]。本研究通过探讨参莲胶囊联合奥希替尼对EGFR突变的晚期非小细胞肺癌(气阴两虚证)的疗效、肿瘤标志物、不良反应和生活质量的影响,旨在为临床应用提供一定的参考价值。
1 资料与方法 1.1 一般资料选取2021年4月—2022年4月本院收治的EGFR突变的晚期非小细胞肺癌患者110例,按照随机数表法分2组,对照组(55例)与研究组(55例)的性别,年龄,身体质量指数和病程,TMN分期,病理类型,EGFR基因类型无统计学意义(P>0.05),并且有可比性。见表 1。
纳入标准:1)经病理组织以及基因检测确诊为EGFR突变的非小细胞肺癌;2)年龄20~80岁,男女不限;3)预计生存期3个月以上;4)符合中医辨证气阴两虚证;5)患者、家属知情同意。排除标准:1)精神病患者;2)对治疗药物过敏者;3)孕期或哺乳期妇女;4)合并其他恶性肿瘤者;5)有传染病者;6)合并心、肝、肾等脏器严重功能或器质性病变者;7)合并免疫疾病、严重感染及其他代谢性疾病者;8)入组前接受化疗、放疗。本研究经医院伦理委员会批准(20210308)。
1.2 诊断标准 1.2.1 西医诊断标准符合《非小细胞肺癌血液EGFR基因突变检测中国专家共识》[6]规范中国EGFR血液检测,推动肺癌精准治疗中判定标准。
1.2.2 中医诊断标准参照《中医内科学》[7]辨证为气阴两虚证:胸痛,咳嗽痰少,咳声低弱,神疲乏力,自汗或盗汗,气短喘促,口干舌燥,苔白,舌质红或淡,面色晄白,身体瘦弱,脉细弱。
1.3 治疗方法 1.3.1 对照组采用奥希替尼(生产厂家:泰瑞沙,Astra Zeneca AB生产,国药准字:2101144,规格:80 mg×30片)每日1次,每次1片,连续服用60 d。
1.3.2 研究组在上述治疗基础上再口服参莲胶囊(生产厂家:山西澳迩药业有限公司,国药准字Z10940039)口服,每次6粒,每日3次,连续用药60 d。
1.4 观察指标 1.4.1 疗效评价治疗后参照实体瘤疗效评价标准(RECIST1.1)[8-9]进行疗效评价。1)完全缓解(CR):所有靶病灶消失,无新病灶出现,且肿瘤标志物正常,至少维持4周。2)部分缓解(PR):靶病灶最大径之和减少≥30%,至少维持4周。3)疾病稳定(SD):靶病灶最大径之和缩小未达PR,或增大未达PD。4)疾病进展(PD):靶病灶最大径之和至少增加≥20%,及其绝对值增加至少5 mm,出现新病变也视为PD。
1.4.2 酶联免疫吸附试验检测癌胚抗原(CEA),细胞角蛋白19片段(CYFRA21-1),糖类抗原125(CA125)水平抽取所有患者空腹肘静脉血5mL,静置后离心(3000 r/min,10 min,离心半径15 cm),然后取上清液,储存到-80 ℃冰箱,采用酶联免疫吸附试验测定(从江苏三联生物工程有限公司购买试剂盒)血清CEA、CYFRA21-1、CA125水平。于治疗前、治疗3个月后分别进行一次测定。
1.4.3 用药安全性观察并记录患者用药期间出现的包括间歇性肺炎、皮疹、恶心、呕吐、贫血、腹泻等在内的不良反应。
1.4.4 两组患者生活质量评分采用欧洲癌症研究和治疗组织肿瘤患者生存质量量表(EORTCQLQ-LC43)[10]评定患者生活质量,各个项目得分范围:0~100分,得分越高表明生活质量越好。主要评定角色功能、生理功能、认知功能、社会功能、情感功能、总健康状况,包括相关症状困扰、整体的生活质量及身体活动状态的评估。
1.5 统计学方法以SPSS25.0分析数据。计数资料以例(%)表示,行χ2检验;符合正态分布的计量资料以均数±标准差(x±s)表示,组间比较采用独立样本t检验,同组内治疗前后比较采用配对t检验,P < 0.05为差异有统计学意义。
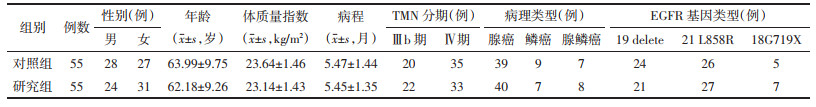
2 结果 2.1 两组疗效比较研究组总有效率高于对照组,差异有统计学意义(P < 0.01)。见表 2。
治疗后,两组患者血清CEA,CA125和CYFRA21-1水平低于治疗前,研究组血清CEA,CA125和CYFRA21-1水平低于对照组,差异均有统计学意义(P < 0.05或P < 0.01)。见表 3。

|
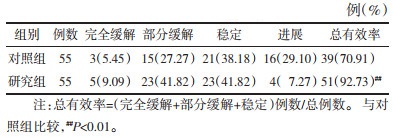
研究组不良反应发生率(9.09%,5/55)低于对照组(25.45%,14/55),差异有统计学意义(P < 0.05)。见表 4。
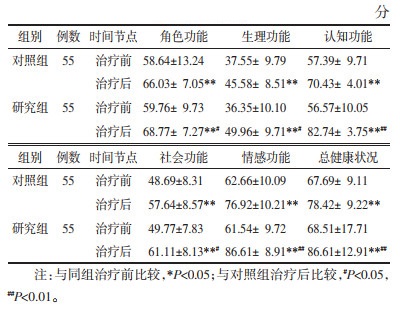
治疗前,研究组和对照组患者角色功能、生理功能、认知功能、社会功能、情感功能、总健康状况评分差异无统计学意义(P>0.05)。治疗后研究组和对照组患者角色功能、生理功能、认知功能、社会功能、情感功能、总健康状况评分均较治疗前增加,治疗后研究组角色功能、生理功能、认知功能、社会功能、情感功能、总健康状况评分高于对照组,差异均有统计学意义(P < 0.05)。见表 5。
|
非小细胞肺癌是发生于肺泡上皮的恶性肿瘤,但近年来发病趋势倾向年轻化[11],并且该病在早期没有出现任何症状,容易出现扩散和转移,不易诊断,治疗难度较大,预后或治疗效果较差[12]。参莲胶囊药物成分主要由山豆根,三棱,防己,补骨脂,半枝莲,苦参,苦杏仁,丹参,莪术,白扁豆,乌梅组成。参莲胶囊可减轻放化疗同步中的不良反应,缓解中晚期肺癌患者临床症状,恢复血液系统功能,改善患者生存质量[13]。奥希替尼在抑制人类表皮生长因子受体(EGFR)酪氨酸激酶活性的基础上可以阻断下游信号传导,抑制肿瘤细胞增殖,可作为辅助治疗优选药物。
CEA是临床判断多种肿瘤存在的常用指标,是一种酸性糖蛋白,属于非器官特异性肿瘤相关抗原,对腺癌敏感度较高[14];CYFRA21-1是特异性及灵敏性较高的肿瘤标志物,在肿瘤上皮细胞内广泛存在,在细胞癌变凋亡时大量释放进入血液,对非小细胞肺癌的诊断有较大的应用价值[15]。CA125来源于体腔上皮细胞,是一种大分子糖蛋白,发生病变时在血清中会呈现升高趋势[16]。本研究结果提示,参莲胶囊联合奥希替尼能明显降低非小细胞肺癌患者的肿瘤标志物水平。与朱朝勇等[17]研究中奥希替尼联合厄洛替尼治疗EGFR-T790M突变的非小细胞肺癌的肿瘤治疗效果较好结果类似。
据报道,奥希替尼联合贝伐单抗一线治疗EGFR敏感突变阳性晚期非小细胞肺癌时,联合组的有效率较高,是一种安全可行的治疗方式[18]。本研究结果也提示,参莲胶囊联合奥希替尼能降低非小细胞肺癌患者不良反应,提高非小细胞肺癌患者治疗效果,改善生活质量。
综上所述,参莲胶囊联合奥希替尼对晚期EGFR突变的非小细胞肺癌(气阴两虚证)的治疗效果较好,并具有安全性,还可以有效降低血清CEA,CA125和CYFRA21-1水平,提高生活质量的作用,在临床上有着广阔应用前景。但本研究中样本量较小且未进行多中心研究,使结果具有局限性,后期将使用大样本量进行多中心研究,对其进行验证。
| [1] |
BRAY F, FERLAY J, SOERJOMATARAM I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA: a Cancer Journal for Clinicians, 2018, 68(6): 394-424. DOI:10.3322/caac.21492 |
| [2] |
LIN J, CARTER C A, MCGLYNN K A, et al. A prognostic model to predict mortality among non-small-cell lung cancer patients in the U.S. military health system[J]. Journal of Thoracic Oncology, 2015, 10(12): 1694-1702. DOI:10.1097/JTO.0000000000000691 |
| [3] |
CHO J H, LIM S H, AN H J, et al. Osimertinib for patients with non-small-cell lung cancer harboring uncommon EGFR mutations: a multicenter, open-label, phase Ⅱ trial(KCSG-LU15-09)[J]. Journal of Clinical Oncology, 2020, 38(5): 488-495. DOI:10.1200/JCO.19.00931 |
| [4] |
LEONETTI A, SHARMA S, MINARI R, et al. Resistance mechanisms to osimertinib in EGFR-mutated non-small cell lung cancer[J]. British Journal of Cancer, 2019, 121(9): 725-737. DOI:10.1038/s41416-019-0573-8 |
| [5] |
邵岚, 张沂平. 奥希替尼治疗晚期非小细胞肺癌的疗效及影响因素[J]. 中国新药与临床杂志, 2020, 39(3): 155-161. |
| [6] |
吴一龙. 《非小细胞肺癌血液EGFR基因突变检测中国专家共识》规范中国EGFR血液检测, 推动肺癌精准治疗[J]. 浙江医学, 2015, 37(24): 1959-1960. |
| [7] |
周仲瑛. 中医内科学[M]. 2版. 北京: 中国中医药出版社, 2007.
|
| [8] |
杨学宁, 吴一龙. 实体瘤治疗疗效评价标准: RECIST[J]. 循证医学, 2004, 4(2): 85-90, 111. |
| [9] |
邢影, 董量, 付浩宇, 等. 晚期非小细胞肺癌患者营养状况及其影响因素调查[J]. 临床肺科杂志, 2020, 25(7): 1013-1016. |
| [10] |
ZHANG L, SU Y J, HUA Y N, et al. Validation of EORTC QLQ-LC43 for Chinese patients with lung cancer[J]. Lung Cancer, 2014, 85(1): 94-98. DOI:10.1016/j.lungcan.2014.04.006 |
| [11] |
尤静, 杨丹, 李东明, 等. 同步推量调强放疗在局部晚期非小细胞肺癌中的应用[J]. 中国肺癌杂志, 2019, 22(11): 696-701. |
| [12] |
史玉卿. 非小细胞肺癌组织中VEGF和Endostatin的表达意义[J]. 实用癌症杂志, 2019, 34(1): 30-33. |
| [13] |
齐创, 王文萍, 幸茂晖. 参莲胶囊联合同步放化疗治疗中晚期非小细胞肺癌临床观察[J]. 辽宁中医药大学学报, 2012, 14(4): 185-186. |
| [14] |
李岚. 非小细胞肺癌患者化疗前后血清多种指标水平的变化及临床意义[J]. 临床肺科杂志, 2018, 23(1): 178-181. |
| [15] |
ZHANG D G, WANG L S, YANG Z J. Recurrent Syncope associated with lung cancer[J]. Case Reports in Medicine, 2015, 2015: 309784. |
| [16] |
杨扬, 樊美荣, 王鲁, 等. 血清VEGF对非小细胞肺癌患者治疗疗效评估的指导意义[J]. 标记免疫分析与临床, 2018, 25(8): 1085-1090. |
| [17] |
朱朝勇, 曹淑琴. 奥希替尼联合厄洛替尼治疗EGFR-T790M突变的非小细胞肺癌的疗效[J]. 实用癌症杂志, 2019, 34(8): 1328-1330, 1361. |
| [18] |
冯霞, 肖建, 敬梅, 等. 奥希替尼联合贝伐珠单抗一线治疗EGFR敏感突变阳性晚期非小细胞肺癌的临床疗效观察[J]. 临床和实验医学杂志, 2022, 21(16): 1697-1700. |
2. Department of Oncology, Shexian Traditional Chinese Medicine Hospital, Handan 056400, China
 2024, Vol. 41
2024, Vol. 41