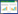文章信息
- 王沫初, 付娜静, 石艳丽, 等.
- WANG Mochu, FU Najing, SHI Yanli, et al.
- UPLC-MS/MS方法测定醒脑静注射液中5种成分的含量与方法研究
- Contents of 5 components in Xingnaojing Injection were determined by UPLC-MS/MS method
- 天津中医药, 2024, 41(9): 1187-1191
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(9): 1187-1191
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.09.19
-
文章历史
- 收稿日期: 2024-04-23
2. 华北理工大学冀唐学院, 唐山 063000
醒脑静注射液是由清代著名医学家吴鞠通所著的《温病条辨》中的经典方剂“安宫牛黄丸”拆方而来[1],该方剂中包含了麝香、冰片、郁金、栀子等中药材[2],后经现代制药技术提取制成静脉注射液。醒脑静注射液中含有莪术二酮、吉马酮、左旋樟脑、姜黄素和麝香酮等化学成分[3],具有醒脑开窍、清热解毒等功效[4]。醒脑静注射液最先收载于地方标准,1998年收载于《卫生部药品标准》第17册,2003年再次提高标准为国家药品监督管理局国家药品标准WS3-B-3353-98-2003[5]。现行质量标准仍然是2003年的国家药品标准,标准中仅采用气相色谱法以醒脑静中冰片的含量(不低于0.7 g/L)为指标进行质量控制,亟待完善。同时,近年来因其成分复杂,质量控制不够规范,在国际发展中受到一定的限制。因此,准确、快速地测定醒脑静注射液中的主要药效成分,对加强该药的质量控制具有重要意义。
当前,醒脑静注射液的检测方法主要包括紫外光谱法(UV)[2]、气相色谱法(GC)[6-7]、高效液相色谱法(HPLC)、高效液相紫外检测法(HPLC-UV)、气相色谱质谱联用(CG-MS)[8-10]等。当选用GC或CG-MS方法进行研究醒脑静中关键有效成分时,可能会导致麝香酮和吉马酮的色谱峰过高,使分析结果失真。同时,紫外吸收较弱,不易检测到这些微量成分的色谱峰,降低实验结果的准确性。而超高效液相色谱-质谱联用(UPLC-MS)技术是基于液相色谱仪对检测物先进行初步分离,然后再经由质谱的质量分析器按质荷比大小进行分离,最终通过检测器得到质谱图[11],从而实现定性与定量分析。由于具有定性准确、分析时间短、灵敏度高、专属性强等优势,UPLC-MS已经被广泛应用于中药化学成分分析和质量控制领域。
目前为止,研究者多聚焦于对醒脑静注射液中麝香酮、冰片以及龙脑等成分的含量测定[12-15],而现代药理学研究显示,郁金挥发油具有抗炎、抗病毒等作用,这说明醒脑静注射液的清热解毒功能可能与来自郁金的活性成分有关[8, 16]。基于此,本研究拟选择郁金挥发油的活性成分莪术二酮、吉马酮和姜黄素,以及醒脑静注射液的另外两种活性成分左旋樟脑和麝香酮这5种成分为检测指标,建立醒脑静注射液中上述5种成分的含量测定方法,从而为有效控制醒脑静注射液质量提供依据。
1 材料 1.1 仪器Waters Acquity UPLC-TQD型液质联用仪(Waters公司,美国);-80 ℃超低温冰箱(安徽中科都菱商用电器股份有限公司);SCILOGEX D2012高速台式离心机(济南鑫驰医疗科技有限公司);Vortex genie2振荡器(山东欧莱博仪器有限公司);KQ3200超声波清洗器[迈福(山东)科学仪器股份有限公司];万分之一天平(天津市德安特传感技术有限公司)。
1.2 试药对照品:莪术二酮(批号:111800,纯度≥99.8%)、吉马酮(批号:111665,纯度≥99.8%)、左旋樟脑(批号:111749,纯度≥99.9%)、姜黄素(批号:110823,纯度≥98.1%)和麝香酮(批号:110719,纯度≥99.2%)均购自中国食品药品检定研究院。样品醒脑静注射液的6个批号分别为220518、220612、220815、220912、221005、221101,规格10 mL,生产企业为无锡济煜山禾药业股份有限公司。试剂甲醇、乙酸铵、甲酸和超纯水均为色谱纯。
2 方法与结果 2.1 色谱条件色谱柱为ACQUITY HSS® T3 C18柱(2.1 mm×100 mm,1.8 μm),流动相A为0.1%甲酸水+2 mmol乙酸铵,流动相B为甲醇+0.1%甲酸。梯度洗脱程序为:0~0.5 min,95% A;0.5~1.0 min,95%→5% A;1.0~2.7 min,5% A;2.7~3.4 min,5%→95% A;3.4~4.0 min,95% A。流速:0.4 mL/min;柱温:40 ℃;进样量:5 μL。每次进行前预平衡5 min。
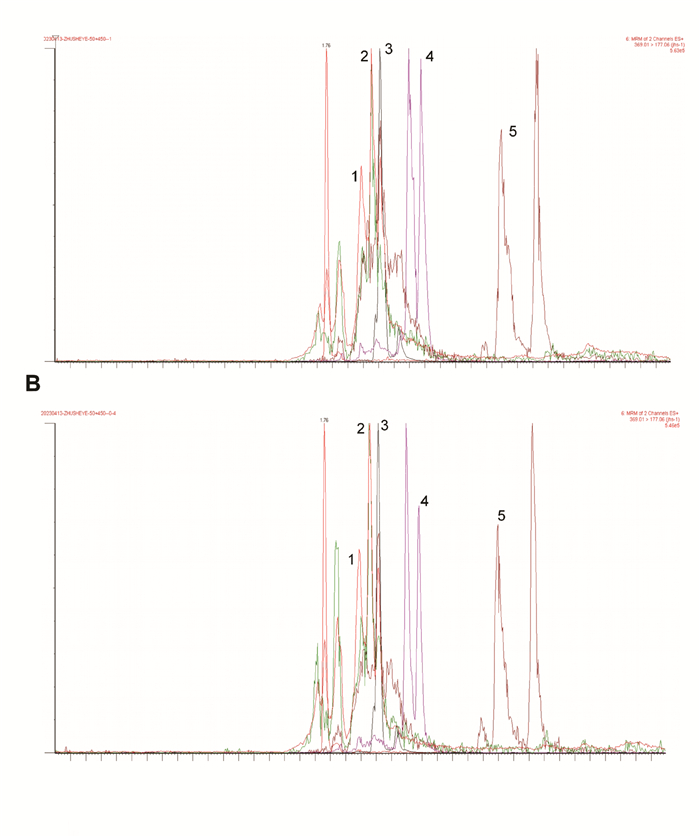
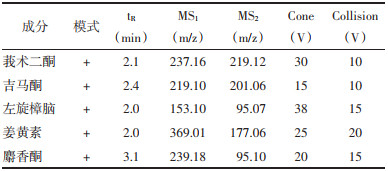
2.2 质谱条件三重四级杆质谱仪配置ESI电离源,采用动态多反应监测(dMRM)模式进行正离子扫描,优化后的质谱参数如下:离子源温度600 ℃;毛细管电压:2.50 kV;脱溶剂气温度:600 ℃;脱溶剂气流速:1 000 L/h;锥孔反吹气:20 L/h。莪术二酮、吉马酮、左旋樟脑、姜黄素和麝香酮的色谱图见图 1,其相应的质谱参数见表 1。
|
| 注:A,对照品色谱图;B,醒脑静注射液样品色谱图。1,姜黄素;2,左旋樟脑;3,莪术二酮;4,吉马酮;5,麝香酮。 图 1 醒脑静注射液中5种成分的色谱图 Fig. 1 Representative MRM chromatograms of 5 components of Xingnaojing Injection |
|
精密称取莪术二酮、吉马酮、左旋樟脑、姜黄素和麝香酮对照品适量,置于1.5 mL的离心管中,加入1∶1的甲醇-水溶液,使之溶解(不能迅速溶解的对照品可用超声波清洗机助溶),制备浓度为1 mg/mL的对照品储备液。量取上述浓度为1 mg/mL对照品储备液适量,加甲醇-水稀释并摇匀,分别配成100、10和1 μg/mL的溶液备用。
2.4 供试品溶液的制备精密量取不同批次醒脑静注射液50 μL,置1.5 mL离心管中,加甲醇-水稀释至500 μL作为供试品溶液备用。
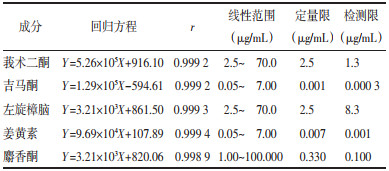
2.5 线性关系考察取10 μg/mL的对照品储备液(除麝香酮对照品),用甲醇-水作稀释溶剂,分别制成10、4、2、1、0.25、0.05和0.025 μg/mL浓度梯度的系列标准溶液;取100 μg/mL的麝香酮对照品溶液,用甲醇-水分别稀释至50、20、10、5、2.5和1 μg/mL。按照“2.1”和“2.2”项下的条件进行实验,记录各待测品的峰面积。以浓度X为横轴,峰面积Y为纵轴,作出标准曲线。分析相关数据,记录各检测成分的回归方程、相关系数和线性范围,并计算其定量限和检测限。结果见表 2。
|
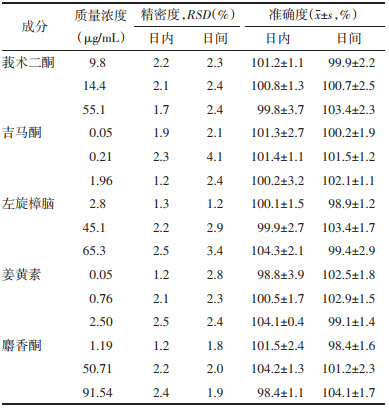
取本品(批号:221101)按“2.4”项下方法制备供试品溶液,连续进样6次,记录各成分峰面积的RSD均小于6%,结果见表 3。表明该方法具有良好的精密度。
|
将样品按“2.4”项下方法制备得到供试品溶液,选取每一浓度6份样本分析,5种成分注射液样品经3次冻融循环和进样器12 h均比较稳定,结果见表 4,表明其在上述条件下稳定。
取样品按“2.4”项下方法制备供试品溶液6份,按“2.1”和“2.2”项下检测条件测定,记录其峰面积,将峰面积代入线性方程计算各成分含量。测得各成分含量RSD分别为莪术二酮1.73%、吉马酮2.35%、左旋樟脑2.94%、姜黄素2.08%和麝香酮2.84%,证明该方法的重复性较好。
2.9 加样回收率实验精密量取6份已知含量的醒脑静注射液样品100 μL,分别加入等体积的莪术二酮(浓度为20.0 μg/mL)、吉马酮(浓度为1.70 μg/mL)、左旋樟脑(浓度为30.0 μg/mL)、姜黄素(浓度为1.40 μg/mL)和麝香酮(浓度为12.0 μg/mL)对照品溶液混合,计算加样回收率,其平均加样回收率在98.2%~104.2%,结果见表 5。样品的加样回收率实验结果符合含量测定方法学的要求。
|
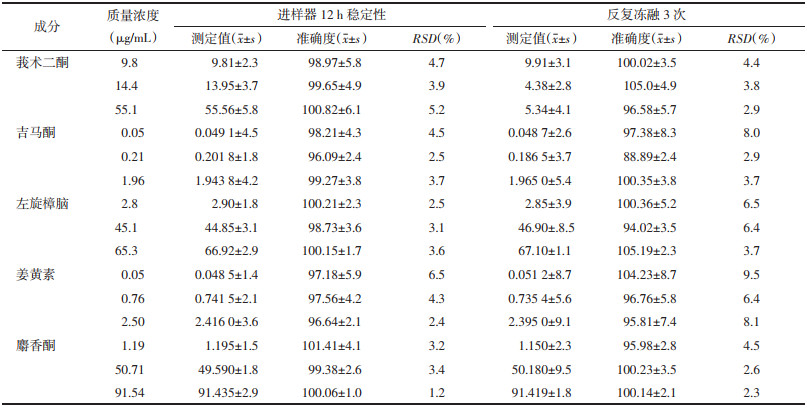
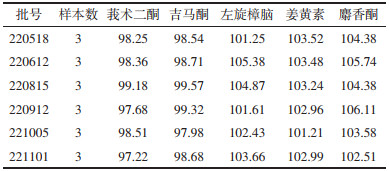
精密量取6个批号的醒脑静注射液样品50 μL,每个批号选取3个样本,加甲醇-水稀释至500 μL,按“2.1”和“2.2”项下的方法进样测定,并计算待测成分的含量。6批样品中莪术二酮、吉马酮、左旋樟脑、姜黄素和麝香酮含量测定结果分别为19.4~20.4、1.6~1.8、29.0~31.0、1.3~1.4和11.6~12.4 μg/mL。见表 6。
该方剂中麝香为君药,麝香酮是其主要有效成分,具有开窍醒脑功能[17]。栀子为臣药,清热利尿[18]。莪术二酮和吉马酮是郁金挥发油中的主要成分,现代药理实验研究结果表明,莪术二酮对血小板聚集也有明显的抑制作用,吉马酮具有较强的抗肿瘤活性,调节糖脂代谢作用[19];左旋樟脑来源于冰片中,具有兴奋、强心、消炎等药理作用,还具有通窍醒神,辟秽利气,消肿止痛,杀虫止痒的功效[20];姜黄素具有抗氧化、预防老年痴呆、抗炎等作用[21]。本研究选用这5种指标性成分作为醒脑静注射液的标志物,采用UPLC-MS/MS方法对其进行了含量测定,一次性针对其中的目标成分进行检测,进而能够保证对其进行更为全面的质量控制。
3.2 色谱条件优化本实验对甲醇与乙腈、甲醇+0.1%甲酸作为流动相进行考察,结果发现甲醇+0.1%甲酸作为流动相时,麝香酮、姜黄素、吉马酮、莪术二酮和左旋樟脑的色谱峰形较尖锐,无拖尾现象,且各成分的响应值较高,因此选择甲醇溶液+0.1%甲酸作为流动相进行梯度洗脱。然后对不同的色谱柱温(20、30、40 ℃)进行考察,结果发现柱温越高,色谱出峰越快,峰形较窄,但柱温对各成分的测定影响不大,综合考虑选择40 ℃。最后对不同进样量(2、5、10 μL)进行评价,结果显示3者峰形差异不大,而当进样体积为10 μL时,色谱峰形稍微拖尾,且峰不对称。因此,综合考虑后选择5 μL作为该实验的进样体积。
3.3 质谱条件的优化5种成分多为碱性,碱性化合物宜采用正离子模式进行扫描,响应值会更高,信号更稳定。向流动相中加酸可以改善拖尾峰形,利于准确定量,因此本实验中质谱条件是在正离子模式下进行优化,采用液相结合质谱的方法,首先对上述5种成分进行母离子扫描,同时优化锥孔电压,保证离子的响应值最高,然后分别对每个化合物逐个优化其离子,通过调整不同的碰撞电压来选取响应值最高的离子作为定量离子,另一个响应强度次之的作为定性离子,从而确定每个化合物测定的质谱参数。然后通过编辑dMRM模式,采用上述的色谱条件作为分离条件,对每个化合物进行定量分析。
4 结论因醒脑静注射液不良反应发生较为常见,醒脑静注射液被列入江西、山西等各地方医院的药品监控目录。最新《中华人民共和国卫生部药品标准》中对其进行质量控制的方法为薄层色谱法,该方法定性方便,但定性没有液相色谱准确,且定量分析误差较大。2020版《中华人民共和国药典》暂时没有记载醒脑静注射液的质量控制要求。本实验建立了可同时测定莪术二酮、吉马酮、左旋樟脑、姜黄素和麝香酮5种指标性成分的UPLC-MS/MS方法。与其他方法相比,该方法样品前处理简便,结果准确稳定、重现性好,分析时间短,对醒脑静注射液的质量控制研究具有重要意义,为醒脑静注射液的进一步开发奠定了基础。
| [1] |
岳茂兴, 李奇林, 吕传柱, 等. 急危重病(症)救治中醒脑静注射液临床应用专家共识[J]. 中华卫生应急电子杂志, 2019, 5(2): 65-70. |
| [2] |
黄凯毅, 魏丹妮, 方金阳, 等. 紫外光谱法快速测定醒脑静注射液一次提取过程中9种成分[J]. 中国中药杂志, 2017, 42(19): 3755-3760. |
| [3] |
张莉, 陈飞, 红玉, 等. 固相萃取-手性气相色谱法测定醒脑静注射液中右旋龙脑和麝香酮的含量[J]. 海峡药学, 2017, 29(4): 68-70. |
| [4] |
李敏雅. 醒脑静注射液治疗急性缺血性脑卒中临床疗效观察[J]. 海峡药学, 2011, 23(7): 153-155. |
| [5] |
国家食品药品监督管理局. 国家药品标准WS3-B-3353-98-2003[S]. 2003.
|
| [6] |
高文分, 袁文娟, 王梅. 气相色谱法拆分醒脑静注射液中龙脑对映体及含量测定[J]. 药物分析杂志, 2012, 32(5): 873-876. |
| [7] |
方颖, 赵希贤, 赵鸣舒, 等. 气相色谱法同时测定醒脑静注射液中麝香酮、龙脑、樟脑、异龙脑的含量[J]. 中国实验方剂学杂志, 2012, 18(8): 96-99. |
| [8] |
杨立新, 刘薇薇, 甘国锋, 等. HPLC测定醒脑静注射液中莪术二酮及吉马酮的含量[J]. 中国实验方剂学杂志, 2013, 19(17): 136-139. |
| [9] |
YANG L X, FENG W H, XIA B H, et al. HPLC specific chromatograms of Xingnaojing Injection[J]. China Journal of Chinese Materia Medica, 2016, 41(9): 1640-1645. |
| [10] |
PAN W D, YANG L X, FENG W H, et al. Determination of five sesquiterpenoids in Xingnaojing Injection by quantitative analysis of multiple components with a single marker[J]. Journal of Separation Science, 2015, 38(19): 3313-3323. DOI:10.1002/jssc.201500494 |
| [11] |
熊晓莉, 万书源, 龚来觐, 等. 现代化中药质量控制中液质联用技术的应用与展望[J]. 现代盐化工, 2022, 49(3): 73-75. |
| [12] |
陈琴华, 李鹏, 张卓. GC-MS-SIM法测定醒脑静注射液中麝香酮的含量[J]. 中国医院药学杂志, 2009, 29(5): 422-423. |
| [13] |
汪秀月. 气相色谱法测定醒脑静注射液中麝香酮含量[J]. 海峡药学, 2011, 23(11): 66-67. |
| [14] |
吴小英. 毛细管气相色谱法测定醒脑静葡萄糖注射液中冰片和麝香酮含量[J]. 安徽医药, 2008, 12(2): 129-130. |
| [15] |
冯明霞, 王桂兰, 闻京伟. 气相色谱法同时测定醒脑静氯化钠注射液中冰片及麝香酮的含量[J]. 中国药事, 2006, 20(9): 549-551. |
| [16] |
傅品悦, 钟静, 梁明坤, 等. 桂郁金的活性成分姜黄素对抑郁症作用机制研究进展[J]. 中华中医药学刊, 2020, 38(3): 160-163. |
| [17] |
周文杰, 李宁, 谢兴文, 等. 天然麝香的化学成分及药理研究进展[J]. 时珍国医国药, 2022, 33(1): 185-188. |
| [18] |
陈冠宁. 栀子的药物成分及药理作用研究进展[J]. 特种经济动植物, 2022, 25(11): 20-22, 32. |
| [19] |
袁晓旭, 杨明明, 赵桂琴. 郁金化学成分及药理作用研究进展[J]. 承德医学院学报, 2016, 33(6): 487-489. |
| [20] |
司文文. 左旋樟脑通过表观调控应激颗粒生成抗中风损伤研究[D]. 广州: 广州中医药大学, 2019.
|
| [21] |
陈乔, 陈光辉, 陈强. 姜黄素对阿尔茨海默病及帕金森病的相同作用机制研究进展[J]. 亚太传统医药, 2023, 19(5): 234-239. |
2. Jitang College of North China University of Science and Technology Tangshan 063000, China
 2024, Vol. 41
2024, Vol. 41