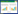文章信息
- 张峰楠, 杨昕彤, Opoku Bonsu Francisa, 等.
- ZHANG Fengnan, YANG Xintong, Opoku Bonsu Francisa, et al.
- 糖尿病视网膜病变炎症相关生物标志物及中药治疗研究进展
- Research progress on inflammation related biomarkers and traditional Chinese medicine treatment of diabetic retinopathy
- 天津中医药, 2025, 42(1): 118-124
- Tianjin Journal of Traditional Chinese Medicine, 2025, 42(1): 118-124
- http://dx.doi.org/10.11656/j.issn.1672-1519.2025.01.20
-
文章历史
- 收稿日期: 2024-09-20
2. 组分中药国家重点实验室, 天津 301617
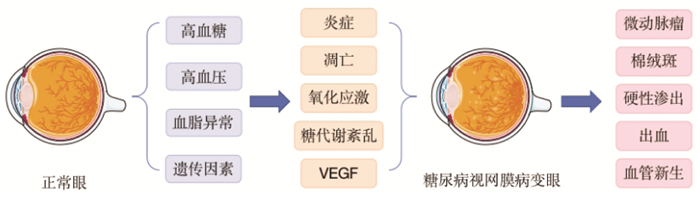
糖尿病是一种慢性代谢性疾病,其特征是胰岛素绝对或相对缺乏,以及高血糖、血脂异常和神经血管损伤。这种损害不仅会影响患者身体健康,降低他们的生活质量,也给社会带来巨大的经济负担。DR是糖尿病的常见并发症,是工作年龄成人失明最常见的原因[1]。根据视网膜出现的病理表现不同,可分为非增殖性DR和增殖性DR。非增殖性DR主要表现为如微动脉瘤、出血、软硬渗出物和视网膜水肿等,随着严重程度增加,发展成为以新生血管形成、视网膜脱离为特征的增殖性DR[2]。DR的发生发展是多种危险因素的共同作用,如炎症、氧化应激、细胞凋亡、血管内皮生长因子(VEGF)增加以及糖代谢紊乱等(见图 1)。视网膜作为耗氧量最高的组织之一,极易受到氧化应激的影响,进而导致炎症发生、神经退行性变和血管病变,抑制氧化应激可以延缓DR的进展[3-4]。糖尿病视网膜周细胞的丢失或凋亡是血管完整性丧失的核心,也是DR的标志事件之一,周细胞凋亡会造成视网膜微动脉瘤形成、血管异常渗漏、视网膜水肿以及缺血,进而引起增殖性DR的发展[5]。随着血-视网膜屏障(BRB)的损伤,越来越多的葡萄糖被泄漏到视网膜实质中,使细胞对葡萄糖的摄取和代谢增加,激活多种生化过程,其中包括炎症反应[6]。炎症在DR的发病机制中起着至关重要的作用,慢性高血糖诱导的炎症存在于DR的不同阶段,释放的炎性细胞因子可导致BRB破坏和血管生成,这是DR视力损害的罪魁祸首,反之,炎症介质的上调会加剧BRB损害,增加血管内皮细胞的通透性和功能障碍[7]。炎症发病机制得到越来越多的关注与认同,更多的炎症通路以及DR的抗炎治疗被报道。因此,了解传统和新型炎症生物标志物可能在DR早期诊断和后期治疗中发挥重要作用,甚至可以找到治疗DR更有效的方法。
|
| 图 1 糖尿病视网膜病变发病机制 Fig. 1 Pathogenesis of diabetic retinopathy |
目前,DR的治疗方法除了对血糖、血压和血清胆固醇的控制之外,还有激光和抗VEGF治疗,如玻璃体内注射法瑞西单抗、雷珠单抗、贝伐单抗和阿柏西普等[8-11]。但这些疗法通常成本较高、副作用明显和治疗时间较长,导致患者依从性差。中医药作为中国传统医学瑰宝普遍应用于DR治疗中,使得治疗方式并不局限于西医疗法。且中药具有多成分多靶点的作用特点,决定了其可通过多种途径中缓解DR症状,包括改善炎症反应、缓解氧化应激、抑制细胞凋亡和血管新生等,在延缓DR进程上发挥着积极的作用,具有疗效好、价格低、副作用少、易得等优点。慢性炎症贯穿于DR整个病程,故中药的抗炎作用显得尤为关键。文章简要讨论了糖尿病视网膜病变有关炎症的生物标志物,并探讨了部分中药单体和传统中药复方在糖尿病视网膜病变中抗炎作用机制。
1 炎症相关生物标志物长期慢性高血糖诱发的炎症反应存在于DR的不同发展阶段,在DR的发病机制中起着重要作用。视网膜中氧化应激和血管生成的激活都可以作为启动炎症反应的开关,如血管紧张素Ⅱ(Ang-Ⅱ)诱导核因子-κB(NF-κB)的下游信号通路促进肿瘤坏死因子-α(TNF-α)和白细胞介素(IL)的上调,NF-κB还可通过环氧化酶2(COX2)上调类花生酸介导的促炎反应[12-13]。VEGF除了参与血管生成外,还通过诱导几种促炎介质(如细胞黏附分子和COX2)来产生某些炎症反应[13]。此外,由氧化应激诱导的小胶质细胞的活化也是炎症因子产生的主要来源[14]。晚期糖基化终末产物诱导组织因子(TF)通过上调IL-1β介导的反应和血管功能障碍来介导炎症;通过MAPK通路与RAGE相互作用以及高血压诱导的VEGF和细胞间黏附分子(ICAM-1)表达增加,加剧DR相关的炎症反应[15]。炎性因子的释放导致视网膜微血管的反应性增生,新生血管渗漏,BRB损伤从而加剧视网膜中炎症因子的积累,造成不可逆的视力损害,见表 1。因此,发现并干预与DR有关炎症生物标志物是对治疗DR至关重要。
ICAM-1是黏附分子免疫球蛋白超基因家族的成员,介导循环白细胞(包括单核细胞、淋巴细胞和多形核细胞)的附着和跨内皮迁移,参与炎症。糖尿病对不同组织中ICAM-1的诱导作用不同,其中对视网膜的影响最大,是其他组织的3倍多,表明ICAM-1在DR中发挥重要作用[16]。Yao等[17]通过分析ICAM-1和DR之间关系,发现在DR患者中通常存在着ICAM-1水平升高,并与DR严重程度正相关。Zhou等[18]通过构建糖尿病大鼠,与对照组相比,模型组大鼠出现视网膜水肿,视网膜通透性增加,视网膜屏障破坏等病理表现,ICAM-1、VCAM-1和VEGF表达升高,使用血管内皮抑制素后,抑制ICAM-1和VCAM-1的表达,降低血管内皮细胞中炎性因子的释放,发挥预防糖尿病视网膜病变的作用。
1.2 TNF-αTNF-α是由T淋巴细胞、单核细胞和巨噬细胞合成的细胞因子,在炎症、血管新生和细胞凋亡中发挥作用,相较于健康人,DR患者中TNF-α水平显著升高[19]。Liu等[20]发现,在高糖环境中,米勒细胞释放的TNF-α激活了表皮生长因子受体(EGFR)/NF-κB通路,增加线粒体自噬,促进细胞凋亡,动物实验证明,阻断TNF-α/EGFR通路可以减轻糖尿病小鼠的BRB破坏,所以抑制TNF-α可能是治疗DR的有效途径之一。
1.3 VEGFVEGF是一种有效的促血管生长因子,刺激血管内皮细胞的生长和增殖,在健康眼睛中表达较低,在DR患者的视网膜中水平显著升高,是PDR主要的血管生成因子[21]。Zhang等[22]使用大鼠模型研究VEGF/蛋白激酶C(PKC)/内皮素(ET)/NF-κB/ICAM-1信号通路在DR中作用,结果表明在诱导糖尿病后,大鼠体质量降低,血糖升高,ICAM-1表达增加,PKC/ET/NF-κB/通路被激活,使用PKCβ2抑制剂抑制VEGF后,PKC/ET/NF-κB/ICAM-1通路也被抑制。所以VEGF是DR治疗中的重要靶点,抑制VEGF的表达可以有效减少视网膜血管渗漏,降低视网膜炎症,保护视网膜[23]。
1.4 Toll样受体4(TLR4)TLR4是一种模式识别受体,负责识别内源性和外源性配体,启动炎症和免疫反应,参与体内各种生理和病理活动[24]。Bayan等[25]研究证明,在糖尿病视网膜中,TLR4表达增加,从而导致各种病理途径的激活,造成视网膜损伤,抑制TLR4后可有效缓解DR。Wang等[26]则证明了,骨髓来源的TLR4在DR期间对维持炎症反应起到关键作用,TLR4缺失后可以缓解糖尿病炎症状态。这些发现证明了TLR4是DR抗炎治疗中的关键靶点,抑制TLR4可能是DR治疗的有效途径。
1.5 信号传导及转录激活蛋白3(STAT3)STAT3是能与DNA结合的蛋白质独特家族STAT的一种亚型,广泛存在于各类组织和细胞中,参与细胞外细胞因子和生长因子的应答,正常生理情况下,STAT3的活化迅速而短暂,但在肿瘤细胞中激活并呈高水平表达[27]。Yun等[28]研究表明,视网膜小胶质细胞中STAT3激活使TNF-α表达增加,进而下调AKT/p70S6激酶信号传导,导致视网膜内炎症增加和周细胞凋亡;使用特异性敲除STAT3小鼠发现,TNF-α表达增加和周细胞凋亡情况都被抑制。综上可知,STAT3激活与炎症有关,而慢性持续性炎症与视网膜病变密切相关。
1.6 基质金属蛋白酶-9(MMP-9)MMP是一个由超过25种锌依赖性蛋白酶组成的家族,可降解细胞外基质,并在器官发育、炎症和损伤中发挥核心作用,MMP-9激活后可作用于多种炎症底物和线粒体[29]。最近的研究表明[29-30],糖尿病视网膜病变患者和动物的视网膜中MMP-9和基质金属蛋白酶-2(MMP-2)显著增加,小胶质细胞中的MMP-9和TLR4信号通路被激活,有助于糖尿病诱导的炎症反应。因此,视网膜中MMP-9的激活可能在糖尿病视网膜病变的发病机制中起关键作用。
1.7 对氧磷酶-1(PON1)PON1是一种与高密度脂蛋白(HDL)相关的脂质催乳糖酶,能够防止低密度脂蛋白(LDL)和细胞膜氧化,同时有助于HDL的抗氧化功能,HDL-PON1复合体活性的降低在各种具有炎症反应的疾病中普遍存在,从而促进炎症和动脉粥样硬化[31]。通过分析1型糖尿病患者血清PON1浓度及其活性发现,血糖值较高患者的PON1浓度以及活性均显著低于血糖较低的患者;相较于无视网膜病变糖尿病患者,伴有视网膜病变患者的PON1活性更高,这可能与PON1基因第54位的L/L多态性有关[32]。在2型糖尿病中,与视网膜病变患者相比,无视网膜病变者PON1活性表现出升高,但血清PON浓度没有差异[33]。综上所述,PON1参与到DR发展过程中,这可能与高密度脂蛋白的功能有关,包括逆胆固醇转运、抗炎抗氧化作用等,但具体发病机制仍需进一步实验研究。
2 中医药对糖尿病视网膜病变的防治作用糖尿病视网膜病变在中医学中被称为消渴目病,消渴日久而肝肾亏损,双目失于濡养;阴虚后期虚火上炎,灼伤目络;疾病后期气阴两虚,痰瘀互结,甚而阴阳两亏,损伤目络[34]。中药在调节免疫失衡和免疫炎症方面有独特的作用和优势,以其多成分多靶点的特点作用于机体,在慢性病防治中发挥越来越多的作用,尤其是在高血糖持续作用下慢性炎症的发生。视网膜作为全身组织耗氧量最多组织之一,中药抗炎作用更加明显。
2.1 中药提取物 2.1.1 三七皂苷三七皂苷(PNS)是三七主根的主要活性成分,具有抗炎、抗氧化、神经保护和免疫调节等多种生物活性,在心血管疾病中发挥着重要作用。Wang等[35]研究表明,与对照组相比,链脲佐菌素(STZ)诱导的糖尿病大鼠给予PNS后,血清中TNF-α、IL-6和IL-1β水平降低,NF-κB信号通路被抑制,同时,PNS抑制了视网膜内核层厚度的减少,无细胞毛细血管的增加,并上调(紧密连接蛋白-1)Claudin-1和闭合蛋白(Occludin)蛋白表达减轻了BRB破坏,下调ICAM-1和VACM-1的蛋白表达增加,显著消除了小胶质细胞的活化,逆转了白细胞黏附的增加,同时细胞实验结果显示,PNS及其主要成分抑制NF-κB信号通路的激活来抑制细胞炎症反应的发展,减轻视网膜损伤。
2.1.2 桔梗皂苷D桔梗皂苷D(PLD)是从中药桔梗中分离提取的一种三萜类生物活性皂苷,具有抗炎、抗氧化和抗糖尿病等活性。Song等[36]研究结果表明,PLD减轻高糖诱导的炎症,如TNF-α、IL-1β、IL-6的产生减少,并阻止氧化应激,降低ROS的产生和丙二醛(MDA)水平,增加超氧化物歧化酶和谷胱甘肽(GSH)的活性,此外,PLD抑制HG诱导的人视网膜上皮细胞(ARPE细胞)中TLR4/髓分化因子88(MyD88)/NF-κB通路的激活,增强核转录因子红系2相关因子2(Nrf2)/血红素氧合酶1(HO-1)的活化,减轻DR大鼠的视网膜损伤。综上所述,这些发现表明PLD在体内和体外均可抑制DR的进展,体现了PLD对DR的保护作用。
2.1.3 白芦藜醇白藜芦醇是一种非黄酮类多酚化合物,是植物受到刺激时产生的一种抗毒素,主要来源于虎杖和葡萄,有抗氧化、抗炎、抗癌及心血管保护等作用。Chen等[37]研究表明,白藜芦醇显著恢复了STZ诱导的糖尿病大鼠中胰岛素水平,并明显降低了视网膜血管通透性、视网膜损伤和IL-1β、IL-6、TNF-α、VEGF、IFN-γ等炎症因子的表达,并通过激活对氧磷酶1(PON1)减轻视网膜炎症和DR损伤。综上所述,白藜芦醇在治疗DR中具有一定的潜力。
2.1.4 黄芪甲苷黄芪多年来一直用于抗肿瘤、免疫调节、抗氧化、抗炎、抗糖尿病,黄芪甲苷作为黄芪中主要活性物质,在糖尿病视网膜病变动物模型中表现出多重保护作用。Ding等[38]研究表明,黄芪甲苷可减少神经节细胞在视网膜中的凋亡,抑制视网膜醛糖还原酶(AR)的激活以及NF-κB和细胞外信号调节激酶1/2(ERK1/2)磷酸化的过表达,降低IL-1β、IL-6、VEGF、VCAM-1等炎症因子的表达,降低视网膜炎症,改善DR进展。
2.1.5 芍药苷芍药苷是一种单萜糖苷,主要从毛茛科植物中提取,是中药白芍和赤芍的主要成分,对小胶质细胞具有强大的免疫调节作用,广泛应用于自身免疫性疾病,如肝炎、系统性红斑狼疮、风湿性关节炎等[39]。Zhu等[40]研究发现,高糖诱导小胶质细胞(BV2细胞)后,通过p38/NF-κB信号通路、HMGB1/TLR4信号通路诱导激活MMP-9,芍药苷通过细胞因子信号转导3(SOCS3)抑制BV2细胞中MMP-9激活,使用TLR4抑制剂后,这种抑制作用消失,说明芍药苷诱导的SOCS3释放依赖于TLR4受体;同时体内实验证明,芍药苷可以降低STZ诱导糖尿病小鼠血糖,抑制炎症表达,增加视网膜各细胞层厚度,结构恢复清晰。综上所述,在糖尿病视网膜病变中,芍药苷通过上调SOCS3抑制TLR4/NF-κB通路,抑制高葡萄糖诱导的视网膜小胶质细胞MMP-9表达和炎症反应。
2.1.6 毛兰素据中国古代医学书籍记载,石斛在临床上具有改善视力的功能,毛兰素是从石斛茎中提取出来的一种天然联苄类化合物,具有多种药理活性,如抗肿瘤、抗炎、抗糖尿病视网膜病变等作用。Zhang等[41]证明毛兰素可以降低STZ诱导的糖尿病小鼠视网膜中Claudin1和Occludin表达的降低,保护BRB;同时毛兰素在体内和体外均可以降低小胶质细胞活化、ERK1/2磷酸化、NF-κB转录活化和TNF-α表达升高,使用ERK1/2抑制剂可以抑制NF-κB的激活;通过分子对接结果显示,毛兰素和葡萄糖转运蛋白1(GLUT1)存在相互作用,GLUT1抑制剂可以抑制ERK1/2/NF-κB信号通路的激活,上述结果说明毛兰素通过减少细胞内葡萄糖摄取和消除下游ERK1/2/NF-κB信号通路的激活来抑制小胶质细胞细胞引发的视网膜炎症,从而减轻DR发展过程中BRB的分解。
2.1.7 姜黄素姜黄素是从姜黄中提取出来的一种亲脂性多酚,具有强大的抗氧化以及抗炎作用,在传统中医上有数千年的应用历史,它在糖尿病、癌症、哮喘以及其他许多疾病中都有防治作用,最近研究发现,姜黄素在眼科疾病的治疗中具有极大潜力[42]。Yao等[43]研究结果表明,姜黄素可以降低自发性糖尿病大鼠视网膜中促炎因子(TNF-α、IFN-γ、IL-1)、氧化应激标志物(SOD、MDA、GPX、CAT)以及VEGF的表达,且降低效果称剂量依赖性。细胞实验证明[44],姜黄素通过干扰ROS/PI3K/AKT/mTOR信号通路抑制高糖诱导视网膜色素上皮细胞(RPEC)的炎症损伤。
2.1.8 隐丹参酮隐丹参酮,也称隐丹参或丹参酮C,是一种来源于丹参具有生物活性的化合物,在抗癌、抗氧化、抗炎以及对组织器官保护上都发挥着重要作用[45]。Yu等[46]研究中证明,通过构建OIR小鼠模型模拟增殖性DR中血管新生,发现隐丹参酮可以抑制模型组中病理性视网膜血管新生和管腔闭塞情况,改善小鼠视觉功能并减少细胞凋亡;与模型组相比,隐丹参酮处理后,小鼠视网膜中p-STAT3、TNF-α、IL-6、VCAM-1和ICAM-1蛋白水平显著降低。提示隐丹参酮可以抑制血管生成条件下内皮细胞中STAT3磷酸化,降低炎症反应。
2.2 中药复方 2.2.1 复方血栓通复方血栓通由三七、丹参、黄芪组成,可以有效治疗视网膜中央静脉,视网膜中央动脉和分支动脉闭塞等眼底血管疾病。有研究发现[47],复方血栓通作用于PPAR信号通路,延缓视网膜厚度变薄,视网膜神经节细胞丢失减少,减轻视网膜结构紊乱和水肿,降低了视网膜细胞的凋亡。Jian等[48]研究发现,尽管复方血栓通对糖尿病大鼠的体质量和血糖没有影响,依旧可以降低血浆黏度,抑制无细胞毛细血管的生成和周细胞的丢失,以及降低高血糖环境下VEGF、ICAM-1和ET-1的过度表达来发挥抗DR作用。这表明复方血栓通对抑制炎症反应,减少细胞凋亡对DR起保护作用,可能在未来针对DR的治疗策略中发挥作用。
2.2.2 复方丹参滴丸复方丹参滴丸由丹参、三七和冰片组成,具有活血化瘀、理气止痛的功效,是治疗气滞血瘀的常见中成药。临床试验证明复方丹参滴丸对DR患者在毛细血管瘤、渗出物以及出血有明显改善作用[49]。Xu等[50]研究,使用db/db小鼠建立DR模型,模型组出现视网膜水肿、细胞排列紊乱、血管通透性增加和毛细血管闭塞等典型DR症状,使用复方丹参滴丸治疗后,这些DR症状有不同程度的缓解,糖尿病导致视网膜内炎症和凋亡情况也被抑制,IL-1β、IL-6和TNF-α的水平下降,B淋巴细胞瘤-2(Bcl-2)的表达增加,Bax表达降低。这些研究表明,复方丹参滴丸对高糖引起的视网膜炎症反应具有抑制作用,提示复方丹参滴丸可能是一种有效的DR治疗药物。
2.2.3 生蒲黄汤生蒲黄汤由生蒲黄、旱莲草、藕节、丹参等11味中药组成,已经应用于前房出血、年龄相关性黄斑变性和早期眼内出血的治疗。Li等[51]发现,生蒲黄汤可以有效降低STZ诱导的糖尿病大鼠视网膜炎症,降低糖尿病大鼠眼内TNF-α、ICAM-1的表达水平,抑制磷酸化κB抑制因子激酶β(p-IKKβ)、p-NF-κB和NF-κB抑制蛋白α(IκBα)的表达。同时抑制NF-κB向核内转移。这些结果表明,生蒲黄汤可能通过抑制NF-κB信号通路来减少视网膜炎症,从而在改善DR方面发挥作用。
3 总结与展望糖尿病是一种全身性慢性的代谢性疾病,DR作为糖尿病最常见的微血管并发症之一,约有1/3的糖尿病患者都表现出不同程度的视网膜病变。大量研究表明在DR的发生发展过程中有多种发病机制的参与,如氧化应激、炎症反应、晚期糖基化终末产物异常堆积、血管新生等,因此,文章着重讨论了参与DR的炎症生物标志物,发现激动或抑制这些蛋白表达对DR的防治疗效确切,可以更有针对性地开发抗DR药物。
现在DR的治疗多停留在西药和玻璃体内注射抗VEGF药物等有创治疗,治疗效果单一,正常眼组织被破坏,副作用及眼内感染风险增加。多活性化合物和多靶点的特点决定了中医药在治疗DR方面具有很大的优势。研究表明,中药提取物及其复方制剂对DR具有治疗作用,其中在DR引起的炎症方面具有显著疗效,可以从多方面降低眼内炎症环境,保护视网膜病变,中药在DR中的抗炎机制总结表见开放科学标识码(OSID)。然而更多的中药单体或复方制剂仅停留在细胞水平或者是动物水平上,不能完全模拟药物在人体中的代谢过程以及作用机制。目前中药对糖尿病并发症的研究还不够深入,临床试验较少。由于研究方法的局限性以及病情发展的复杂性,发病机制的不明确性,中药抗DR作用机制还需进一步探索。
综上所述,炎症反应在DR的发展过程中扮演着重要角色,中药在DR治疗中具有独特优势,探讨中药对DR引起的炎症反应的作用机制可以为进一步DR治疗方式的开发提供参考。中医药是中国传统医学瑰宝,应继续加大研究力度,助力发挥中医治疗糖尿病并发症的优势,从而更好地服务DR患者,促进中医药事业的发展。
| [1] |
ZHENG Y F, HE M G, CONGDON N. The worldwide epidemic of diabetic retinopathy[J]. Indian Journal of Ophthalmology, 2012, 60(5): 428-431. DOI:10.4103/0301-4738.100542 |
| [2] |
YANG Z W, TAN T E, SHAO Y, et al. Classification of diabetic retinopathy: Past, present and future[J]. Frontiers in Endocrinology, 2022, 13: 1079217. DOI:10.3389/fendo.2022.1079217 |
| [3] |
WILLIAMS M, HOGG R E, CHAKRAVARTHY U. Antioxidants and diabetic retinopathy[J]. Current Diabetes Reports, 2013, 13(4): 481-487. DOI:10.1007/s11892-013-0384-x |
| [4] |
ALFONSO-MUÑOZ E A, BURGGRAAF-SÁNCHEZ DE LAS MATAS R, MATAIX BORONAT J, et al. Role of oral antioxidant supplementation in the current management of diabetic retinopathy[J]. International Journal of Molecular Sciences, 2021, 22(8): 4020. DOI:10.3390/ijms22084020 |
| [5] |
SUN W J, AN X D, ZHANG Y H, et al. The ideal treatment timing for diabetic retinopathy: The molecular pathological mechanisms underlying early-stage diabetic retinopathy are a matter of concern[J]. Frontiers in Endocrinology, 2023, 14: 1270145. DOI:10.3389/fendo.2023.1270145 |
| [6] |
ZHANG C Y, GU L M, XIE H, et al. Glucose transport, transporters and metabolism in diabetic retinopathy[J]. Biochimica et Biophysica Acta Molecular Basis of Disease, 2024, 1870(3): 166995. DOI:10.1016/j.bbadis.2023.166995 |
| [7] |
LIU Y, YANG Z Q, LAI P L, et al. Bcl-6-directed follicular helper T cells promote vascular inflammatory injury in diabetic retinopathy[J]. Theranostics, 2020, 10(9): 4250-4264. DOI:10.7150/thno.43731 |
| [8] |
NETWORK D R C R, WELLS J A, GLASSMAN A R, et al. Aflibercept, bevacizumab, or ranibizumab for diabetic macular edema[J]. New England Journal of Medicine, 2015, 372(13): 1193-1203. DOI:10.1056/NEJMoa1414264 |
| [9] |
WANG D X, WANG H, WU S, et al. Intravitreal ranibizumab alone or in combination with calcium dobesilate for the treatment of diabetic macular edema in nonproliferative diabetic retinopathy patients: 12-month outcomes of a retrospective study[J]. International Journal of Clinical Practice, 2022, 2022: 6725225. |
| [10] |
BROWN D M, BOYER D S, CSAKY K, et al. Intravitreal nesvacumab(antiangiopoietin 2) plus aflibercept in diabetic macular edema: Phase 2 ruby randomized trial[J]. Retina, 2022, 42(6): 1111-1120. DOI:10.1097/IAE.0000000000003441 |
| [11] |
TAKAMURA Y, YAMADA Y, MORIOKA M, et al. Turnover of microaneurysms after intravitreal injections of faricimab for diabetic macular edema[J]. Investigative Ophthalmology & Visual Science, 2023, 64(13): 31. |
| [12] |
EL-ASRAR A M. Role of inflammation in the pathogenesis of diabetic retinopathy[J]. Middle East African Journal of Ophthalmology, 2012, 19(1): 70-74. DOI:10.4103/0974-9233.92118 |
| [13] |
BEHL T, KOTWANI A. Exploring the various aspects of the pathological role of vascular endothelial growth factor(VEGF) in diabetic retinopathy[J]. Pharmacological Research, 2015, 99: 137-148. DOI:10.1016/j.phrs.2015.05.013 |
| [14] |
GRIGSBY J G, CARDONA S M, POUW C E, et al. The role of microglia in diabetic retinopathy[J]. Journal of Ophthalmology, 2014, 2014: 705783. |
| [15] |
SEMERARO F, CANCARINI A, DELL'OMO R, et al. Diabetic retinopathy: Vascular and inflammatory disease[J]. Journal of Diabetes Research, 2015, 2015: 582060. |
| [16] |
SIDDIQUI K, GEORGE T P, MUJAMMAMI M, et al. The association of cell adhesion molecules and selectins(VCAM-1, ICAM-1, E-selectin, L-selectin, and P-selectin) with microvascular complications in patients with type 2 diabetes: A follow-up study[J]. Frontiers in Endocrinology, 2023, 14: 1072288. DOI:10.3389/fendo.2023.1072288 |
| [17] |
YAO Y, DU J H, LI R, et al. Association between ICAM-1 level and diabetic retinopathy: A review and meta-analysis[J]. Postgraduate Medical Journal, 2019, 95(1121): 162-168. DOI:10.1136/postgradmedj-2018-136102 |
| [18] |
ZHOU J H, XIE Z G. Endostatin inhibits blood-retinal barrier breakdown in diabetic rats by increasing the expression of ICAM-1 and VCAM-1 and decreasing the expression of VEGF[J]. Computational and Mathematical Methods in Medicine, 2022, 2022: 5105866. |
| [19] |
YAO Y, LI R, DU J H, et al. Tumor necrosis factor-α and diabetic retinopathy: Review and meta-analysis[J]. Clinica Chimica Acta, 2018, 485: 210-217. DOI:10.1016/j.cca.2018.06.028 |
| [20] |
LIU Y, LI L L, PAN N X, et al. TNF-α released from retinal Müller cells aggravates retinal pigment epithelium cell apoptosis by upregulating mitophagy during diabetic retinopathy[J]. Biochemical and Biophysical Research Communications, 2021, 561: 143-150. DOI:10.1016/j.bbrc.2021.05.027 |
| [21] |
EL-SEHRAWY A A, ELKHAMISY E M, BADAWI A E, et al. Subclinical hypothyroidism in patients with diabetic retinopathy: Role of vascular endothelial growth factor[J]. Endocrine, Metabolic & Immune Disorders Drug Targets, 2022, 22(5): 502-509. |
| [22] |
ZHANG M Y, ZHOU M, CAI X, et al. VEGF promotes diabetic retinopathy by upregulating the PKC/ET/NF-κB/ICAM-1 signaling pathway[J]. European Journal of Histochemistry, 2022, 66(4): 3522. |
| [23] |
WANG J J, XU X L, ELLIOTT M H, et al. Müller cell-derived VEGF is essential for diabetes-induced retinal inflammation and vascular leakage[J]. Diabetes, 2010, 59(9): 2297-2305. DOI:10.2337/db09-1420 |
| [24] |
KIM H J, KIM H, LEE J H, et al. Toll-like receptor 4(TLR4): New insight immune and aging[J]. Immunity & Ageing, 2023, 20(1): 67. |
| [25] |
BAYAN N, YAZDANPANAH N, REZAEI N. Role of toll-like receptor 4 in diabetic retinopathy[J]. Pharmacological Research, 2022, 175: 105960. |
| [26] |
WANG H, SHI H J, ZHANG J, et al. Toll-like receptor 4 in bone marrow-derived cells contributes to the progression of diabetic retinopathy[J]. Mediators of Inflammation, 2014, 2014: 858763. |
| [27] |
GUANIZO A C, FERNANDO C D, GARAMA D J, et al. STAT3:A multifaceted oncoprotein[J]. Growth Factors, 2018, 36(1/2): 1-14. |
| [28] |
YUN J H, LEE D H, JEONG H S, et al. STAT3 activation in microglia increases pericyte apoptosis in diabetic retinas through TNF-α/AKT/p70S6 kinase signaling[J]. Biochemical and Biophysical Research Communications, 2022, 613: 133-139. |
| [29] |
KOWLURU R A, ZHONG Q, SANTOS J M. Matrix metalloproteinases in diabetic retinopathy: Potential role of MMP-9[J]. Expert Opinion on Investigational Drugs, 2012, 21(6): 797-805. |
| [30] |
RODRIGUES M, XIN X B, JEE K, et al. VEGF secreted by hypoxic Müller cells induces MMP-2 expression and activity in endothelial cells to promote retinal neovascularization in proliferative diabetic retinopathy[J]. Diabetes, 2013, 62(11): 3863-3873. |
| [31] |
MACKNESS M, MACKNESS B. Human paraoxonase-1(PON1): Gene structure and expression, promiscuous activities and multiple physiological roles[J]. Gene, 2015, 567(1): 12-21. |
| [32] |
KORDONOURI O, JAMES R W, BENNETTS B, et al. Modulation by blood glucose levels of activity and concentration of paraoxonase in young patients with type 1 diabetes mellitus[J]. Metabolism, 2001, 50(6): 657-660. |
| [33] |
MACKNESS B, DURRINGTON P N, ABUASHIA B, et al. Low paraoxonase activity in type Ⅱ diabetes mellitus complicated by retinopathy[J]. Clinical Science, 2000, 98(3): 355-363. |
| [34] |
田久卓, 李长辉. 中药干预糖尿病视网膜病变氧化应激机制的研究进展[J]. 中医临床研究, 2024, 16(11): 47-53. |
| [35] |
WANG Y R, SUN X, XIE Y M, et al. Panax notoginseng saponins alleviate diabetic retinopathy by inhibiting retinal inflammation: Association with the NF-κB signaling pathway[J]. Journal of Ethno- pharmacology, 2024, 319(Pt 1): 117135. |
| [36] |
SONG Y M, LV P L, YU J N. Platycodin D inhibits diabetic retinopathy via suppressing TLR4/MyD88/NF-κB signaling pathway and activating Nrf2/HO-1 signaling pathway[J]. Chemical Biology & Drug Design, 2024, 103(1): e14419. |
| [37] |
CHEN Y H, MENG J, LI H, et al. Resveratrol exhibits an effect on attenuating retina inflammatory condition and damage of diabetic retinopathy via PON1[J]. Experimental Eye Research, 2019, 181: 356-366. |
| [38] |
DING Y Z, YUAN S T, LIU X Y, et al. Protective effects of astragaloside Ⅳ on db/db mice with diabetic retinopathy[J]. PLoS One, 2014, 9(11): e112207. |
| [39] |
JIANG F J, ZHAO Y L, WANG J B, et al. Comparative pharmacokinetic study of paeoniflorin and albiflorin after oral administration of Radix Paeoniae Rubra in normal rats and the acute cholestasis hepatitis rats[J]. Fitoterapia, 2012, 83(2): 415-421. |
| [40] |
ZHU S H, LIU B Q, HAO M J, et al. Paeoniflorin suppressed high glucose-induced retinal microglia MMP-9 expression and inflammatory response via inhibition of TLR4/NF-κB pathway through upregulation of SOCS3 in diabetic retinopathy[J]. Inflammation, 2017, 40(5): 1475-1486. |
| [41] |
ZHANG T Y, OUYANG H, MEI X Y, et al. Erianin alleviates diabetic retinopathy by reducing retinal inflammation initiated by microglial cells via inhibiting hyperglycemia-mediated ERK1/2-NF-κB signaling pathway[J]. FASEB Journal, 2019, 33(11): 11776-11790. |
| [42] |
WANG L Y, XU J Y, YU T Y, et al. Efficacy and safety of curcumin in diabetic retinopathy: A protocol for systematic review and meta-analysis[J]. PLoS One, 2023, 18(4): e0282866. |
| [43] |
YAO B, XIN Z K, WANG D. The effect of curcumin on on intravitreal proinflammatory cytokines, oxidative stress markers, and vascular endothelial growth factor in an experimental model of diabetic retinopathy[J]. Journal of Physiology and Pharmacology, 2023, 74(6): 667-676. |
| [44] |
RAN Z L, ZHANG Y L, WEN X Y, et al. Curcumin inhibits high glucose-induced inflammatory injury in human retinal pigment epithelial cells through the ROS-PI3K/AKT/mTOR signaling pathway[J]. Molecular Medicine Reports, 2019, 19(2): 1024-1031. |
| [45] |
WU Y H, WU Y R, LI B, et al. Cryptotanshinone: A review of its pharmacology activities and molecular mechanisms[J]. Fitoterapia, 2020, 145: 104633. |
| [46] |
YU Y, QIN X, CHEN X, et al. Suppression of retinal neovascularization by intravitreal injection of cryptotanshinone[J]. Biochemical and Biophysical Research Communications, 2024, 720: 150065. |
| [47] |
SUN H H, CHAI X L, LI H L, et al. Fufang Xueshuantong alleviates diabetic retinopathy by activating the PPAR signalling pathway and complement and coagulation cascades[J]. Journal of Ethnopharmacology, 2021, 265: 113324. |
| [48] |
JIAN W J, YU S Y, TANG M K, et al. A combination of the main constituents of Fufang Xueshuantong Capsules shows protective effects against streptozotocin-induced retinal lesions in rats[J]. Journal of Ethnopharmacology, 2016, 182: 50-56. |
| [49] |
LIAN F M, WU L, TIAN J X, et al. The effectiveness and safety of a Danshen-containing Chinese herbal medicine for diabetic retinopathy: A randomized, double-blind, placebo-controlled multicenter clinical trial[J]. Journal of Ethnopharmacology, 2015, 164: 71-77. |
| [50] |
XU X Y, WANG M C, ZHANG S X, et al. Compound Danshen dripping pills prevent early diabetic retinopathy: Roles of vascular protection and neuroprotection[J]. Frontiers in Pharmacology, 2024, 15: 1294620. |
| [51] |
LI W C, SHEN X H, WANG Y P, et al. The effect of Shengpuhuang-Tang on retinal inflammation in streptozotocin-induced diabetic rats by NF-κB pathway[J]. Journal of Ethnopharmacology, 2020, 247: 112275. |
2. State Key Laboratory of Component-Based Chinese Medicine, Tianjin 301617, China
 2025, Vol. 42
2025, Vol. 42