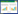文章信息
- 王睿, 赵雪梅, 李达, 等.
- WANG Rui, ZHAO Xuemei, LI Da, et al.
- 花青素通过上调IGFBP-4抑制滑膜Wnt/β-catenin信号通路缓解小鼠膝骨关节炎疼痛研究
- Research of anthocyanins relieve osteoarthritis pain in mice by up-regulating IGFBP-4 which inhibits synovial Wnt/β-catenin signaling pathway
- 天津中医药, 2025, 42(3): 343-352
- Tianjin Journal of Traditional Chinese Medicine, 2025, 42(3): 343-352
- http://dx.doi.org/10.11656/j.issn.1672-1519.2025.03.13
-
文章历史
- 收稿日期: 2024-10-29
2. 河北省慢性疾病基础医学重点实验室, 唐山 063210
骨关节炎(OA)是以软骨侵蚀、滑膜炎症、软骨下骨骨赘形成为特征的致残性疾病[1]。膝骨关节炎(KOA)是OA最高发的形式, 其引发的关节疼痛和功能障碍严重影响患者生活质量。KOA疼痛机制复杂, 关节炎症、外周敏化和中枢敏化均参与其中[2]。KOA释放的组胺、P物质、肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)等能通过伤害感受器的轴浆运输影响关节、脊髓背根神经节(DRG)和脊髓背角, 诱发外周敏化[3-4]。Wnt信号通路参与啮齿类动物神经病理性疼痛发病机制和OA形成的关键环节, Wnt3a、Wnt5a在多种疼痛模型中表达上调, 施加Wnt信号通路拮抗剂可减轻疼痛[5-6]。胰岛素生长因子结合蛋白4(IGFBP-4)已被证实是Wnt/β-catenin信号通路抑制剂, 目前在OA中的研究集中于骨和软骨保护[7-8]。课题前期研究发现IGFBP-4转基因小鼠能缓解KOA诱发的机械痛敏和热痛敏, 提示IGFBP-4对KOA疼痛有一定的保护作用。花青素是一类常见于植物和中草药的黄酮类化合物, 因强大的抗炎抗氧化能力被熟知, 已被用于治疗神经退行性疾病和预防骨质流失[9]。花青素通过抑制炎症因子产生及细胞外基质降解保护关节软骨, 同时对多种疼痛模型表现出镇痛作用[10-11]。且有研究提示花青素上调空腹高血糖患者IGFBP-4表达, 抑制OA中Wnt/β-catenin通路级联反应[11-12], 花青素缓解KOA疼痛的内在机制是否与Wnt/β-catenin通路和IGFBP-4相关尚不明确。故本研究用花青素和IGFBP-4过表达及敲减腺病毒处理OA模型, 探讨花青素是否通过调控IGFBP-4表达影响Wnt/β-catenin通路而达到镇痛效果。
1 材料 1.1 主要材料与仪器IGFBP-4腺病毒(上海吉凯基因, 220705);花青素(西安杨凌萃健, 230203);鼠抗IGFBP-4抗体(美国ABclonal, A2008);兔抗Wnt-3a、β-catenin抗体(杭州华安生物, HA500193 ET1601);兔抗TRPV1抗体(美国Abcom, AB305299);Von Frey纤维丝(美国DanMic Global); 智能热板仪(安徽正华生物); 免疫印记电泳槽、电泳仪、凝胶成像系统(美国Bio-Rad)。
1.2 动物分组与模型构建SPF级3月龄C57/BL6雄性小鼠80只, 购自北京华阜康生物科技有限公司, 许可证号: 111251231100099075。本研究中涉及操作均符合国家和华北理工大学动物实验伦理委员会要求和批准(伦理编号: 2023-SY-022)。
小鼠随机分为8组, 每组10只: 正常组(NC)、对照组(Sham)、OA组、花青素治疗组(AC), IGFBP-4过表达组(BP4+OA)、IGFBP-4过表达对照组(CON267+OA)、IGFBP-4敲减组(BP4-OA)、IGFBP-4敲减对照组(CON098+OA)。去除小鼠膝关节处毛发, 乙醇消毒, 除NC组和Sham组外, 其余6组小鼠每膝关节腔内注射4 μL 5 mg/mL碘乙酸(MIA)建立OA模型; Sham组注射等量1×磷酸盐缓冲液(PBS); AC组在MIA造模后1 d开始腹腔注射花青素200 mg/(kg·d), 至28 d。MIA造模后3 d注射腺病毒: BP4+OA组、BP4-OA组每膝关节腔注射5 μL腺病毒(携带AD-lgfbp4、AD-lgfbp4-RNAi标记绿色荧光蛋白), 滴度为1×108 PFU/mL; CON267+OA组、CON098+OA组每膝关节注射5 μL 1×108 PFU/mL相应的空载腺病毒, 每7 d注射1次, 共注射4次。各组行为学实验结束后眼球取血, 脱臼处死小鼠, 血液静置离心吸取血清, 滑膜和DRG放入无酶冻存管中, -80℃冰箱保存; 膝关节、DRG放入多聚甲醛中固定行形态学检测。
2 方法 2.1 疼痛行为学检测 2.1.1 Von Frey法检测缩足机械阈值(PWMT)于注射花青素和腺病毒后1、3、7、14、21、28 d进行测试, 用0.008~4.0 g纤维丝垂直于小鼠后爪跖面, 施加压力至纤维丝轻微弯曲, 持续2~3 s。出现抬爪、缩足或跳跃记为"X"; 小鼠没有反应记为"O", 间隔10 s施加更高力度纤维丝, 以4 g为临界值, 每个力度纤维丝重复测3次, 计算小鼠产生疼痛所需的力, 以g表示, 通过测量PWMT衡量小鼠机械痛阈变化。
2.1.2 热板法检测缩足热潜伏期(PWTL)于注射花青素和腺病毒后1、3、7、14、21、28 d进行测试, 热板仪温度设为(55±1)℃, 记录小鼠为逃避热刺激出现抬爪、舔爪或跳跃反应的时间, 随即将小鼠取出。以60 s为临界值, 每只小鼠测试3次间隔15 min, 3次平均值为测试数据, 通过测量PWTL衡量小鼠热痛阈变化。
2.2 小动物活体成像注射腺病毒后1 d用活体成像技术监测膝关节内IGFBP-4腺病毒自带的增强型绿色荧光蛋白(EGFP)信号。脱颈处死小鼠, 从股骨中部剪断股骨, 保留膝、踝关节置于拍摄柜中拍摄(EGFP: 激发波长484 nm, 发射波长507 nm), Living Image 4.4软件分析数据。
2.3 酶联免疫吸附实验(ELISA)按照P物质小鼠ELISA检测试剂盒说明书操作, 于450 nm波长检测各组P物质的OD值, 绘制标准曲线并计算相应浓度。
2.4 形态学检测 2.4.1 苏木精-伊红(HE)染色、尼氏染色HE染色: 关节置于脱钙液中37℃ 7 d, 脱水后石蜡包埋, 8 μm切片脱蜡水化、行HE染色、乙醇脱水、中性树胶封片、光学显微镜观察。尼氏染色: DRG脱水后石蜡包埋, 5 μm切片脱蜡水化、行尼氏染色、乙醇脱水、中性树胶封片、光学显微镜观察。
2.4.2 免疫组织化学染色根据说明书将石蜡切片进行以下操作: 抗原修复、阻断过氧化物酶、血清封闭、一抗孵育、辣根酶标记链霉卵白素孵育、DAB显色、苏木素复染、流水反蓝、乙醇脱水、树脂胶封片。免疫反应阳性细胞在镜下呈棕黄色, Image J软件测定阳性细胞平均光密度值(AOD)。
2.5 蛋白免疫印迹(Western blot)实验研磨组织加入等比例RIPA和PMSF, 冰上裂解提取总蛋白, 测蛋白浓度, 加入相应体积蛋白上样缓冲液, 煮沸制备蛋白样品。聚丙烯酰胺凝胶电泳分离蛋白, 转膜, 封闭, 加入抗体4℃孵育过夜。次日加入二抗室温孵育, TBST漂洗10 min×3次, 加入化学发光液显影, Image J分析数据, 以目的蛋白/β-actin代表蛋白相对表达量。
2.6 统计学分析Graphpad Prism 8.0进行统计学分析。计量资料满足正态分布和方差齐, 以均数±标准差(x±s)表示。多组间比较用One-way ANOVA或Two-way ANOVA方差分析, P < 0.05为差异有统计学意义。
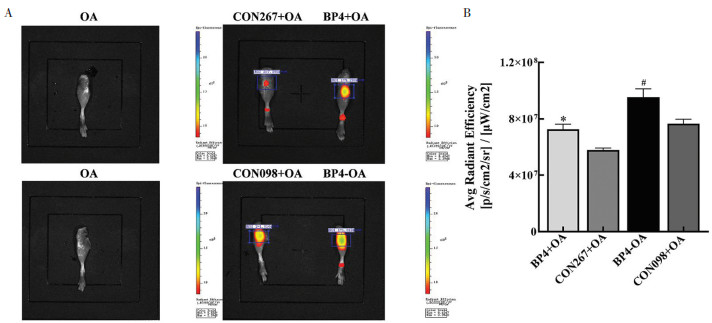
3 结果 3.1 小动物活体成像检测IGFBP-4腺病毒自带的EGFP荧光信号和荧光辐射效率验证腺病毒膝关节腔注射是否成功。OA组未捕捉到荧光信号, BP4+OA组、CON267+OA组、BP4-OA组、CON098+OA组观察到明显荧光信号, 见图 1A。与CON267+OA组比较, BP4+OA组荧光辐射率升高(P < 0.05);与CON098+OA组比较, BP4-OA组荧光辐射率升高(P < 0.05), 见图 1B。
|
| 注:图A,小动物活体成像;图B,辐射效率。与CON267+OA组比较,*P < 0.05;与CON098+OA组比较,#P < 0.05。 图 1 IGFBP-4腺病毒关节腔注射结果 Fig. 1 Results of IGFBP-4 adenovirus injection into articular cavity |
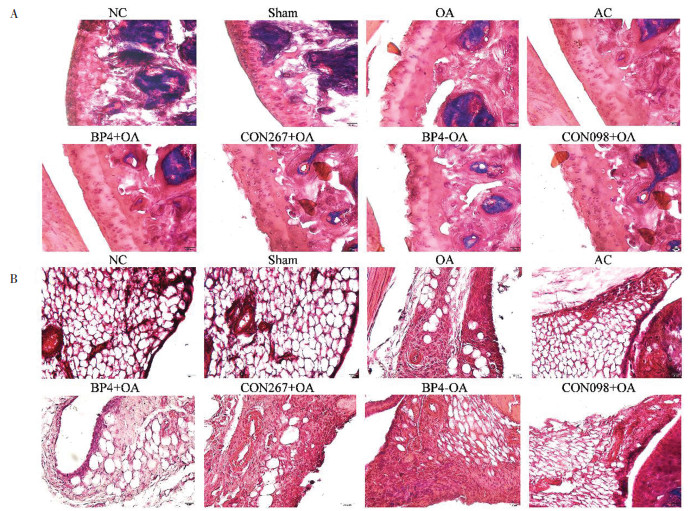
对造模28 d小鼠膝关节进行观察, 并进行OARSI评分和滑膜炎症评分比较, HE染色: NC组和Sham组关节表面无缺损, 软骨细胞排列整齐, 滑膜无增生无炎细胞浸润; OA组、CON267+OA组、CON098+OA组软骨局部凹陷缺损、软骨层次混乱、滑膜层增生明显、炎症细胞浸润; 与OA组和CON267+OA组比, AC组和BP4+OA组软骨表面较平整凹陷缺损减少, 滑膜层增生减轻, 炎症细胞浸润减少; 与CON098+OA组比较, BP4-OA组关节表面缺损增加, 滑膜层增生明显伴大量炎症细胞浸润, 并可见滑膜血管增生, 见图 2。
|
| 注:图A,关节软骨HE染色;图B,滑膜HE染色。 图 2 各组关节软骨、滑膜HE染色(×40) Fig. 2 HE staining of articular cartilage and synovial in each group(×40) |
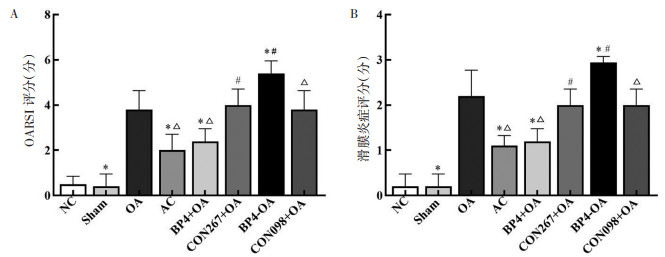
OARSI评分和滑膜炎症评分: NC组和Sham组OARSI评分和滑膜炎症评分差异无统计学意义(P > 0.05);与Sham组比较, OA组OARSI评分和滑膜炎症评分升高(P < 0.05);与OA组比较, AC组OARSI和滑膜炎症评分降低(P < 0.05)。BP4+OA组OARSI评分和滑膜炎症评分较CON267+OA组及OA组下降(P < 0.05);BP4+OA组与AC组两评分差异无统计学意义(P > 0.05)。BP4-OA组OARSI评分和滑膜炎症评分较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC组(P < 0.05), 见图 3。
|
| 注:图A,OARSI评分;图B,滑膜炎症评分。与OA组比较,*P < 0.05;与BP4+OA组比较,#P < 0.05;与BP4-OA组比较,△P < 0.05。 图 3 各组OARSI评分、滑膜炎症评分比较 Fig. 3 Comparison of OARSI score and synovial inflammation score in each group |
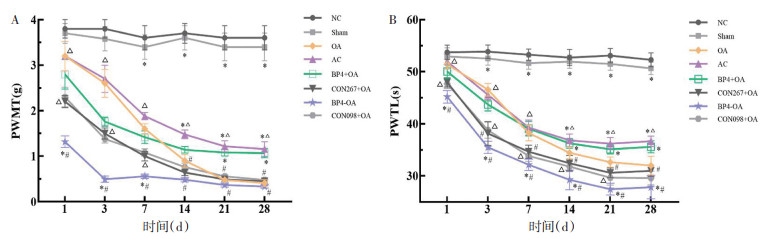
各组小鼠纤维丝实验测得的PWMT比较。NC组和Sham组PWMT处于基础水平, 差异无统计学意义(P > 0.05);与Sham组比较, OA组PWMT在第7~28天持续下降(P < 0.05);与OA组比较, AC组PWMT在第7~28天下降趋势变缓(P < 0.05)。CON267+OA组与CON098+OA组PWMT变化与OA组趋势相似, 差异无统计学意义(P > 0.05)。BP4+OA组PWMT较CON267+OA组在第14~28天升高(P < 0.05);BP4-OA组PWMT较CON098+OA组在第1~3天下降, 7 d略有回升, 但仍低于CON098+OA组(P < 0.05), 且BP4-OA组第1~28天的PWMT低于BP4+OA组及OA组(P < 0.05), 见图 4A。
|
| 注:图A,PWMT结果;图B,PWTL结果。与OA组比较,*P<0.05;与BP4+OA组比较,#P<0.05;与BP4-OA组比较,△P<0.05。 图 4 各组PWMT、PWTL结果 Fig. 4 PWMT and PWTL results in each group |
各组小鼠热板实验测得的PWTL比较。NC组和Sham组PWTL处于基础水平, 差异无统计学意义(P > 0.05);与Sham组比较, OA组PWTL在第3~28天降低(P < 0.05);与OA组比较, AC组PWTL在第14~28天逐渐升高(P < 0.05)。CON267+OA组与CON098+OA组PWTL变化与OA组趋势相似, 差异无统计学意义(P > 0.05)。BP4+OA组PWTL相较CON267+OA组在第3~28天升高(P < 0.05);BP4-OA组PWTL相较CON098+OA组在第1~21天持续下降(P < 0.05), 且BP4-OA组第1~28天的PWTL低于BP4+OA组及OA组(P < 0.05), 见图 4B。
3.4 血清P物质含量检测比较造模28 d各组小鼠血清中P物质含量。NC组和Sham组血清P物质含量差异无统计学意义(P > 0.05);与Sham组比较, OA组P物质含量升高(P < 0.05);与OA组比较, AC组P物质含量降低(P < 0.05)。BP4+OA组P物质含量较CON267+OA组及OA组降低(P < 0.05);BP4+OA组与AC组P物质含量差异无统计学意义(P > 0.05)。BP4-OA组P物质含量较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC(P < 0.05), 见表 1。
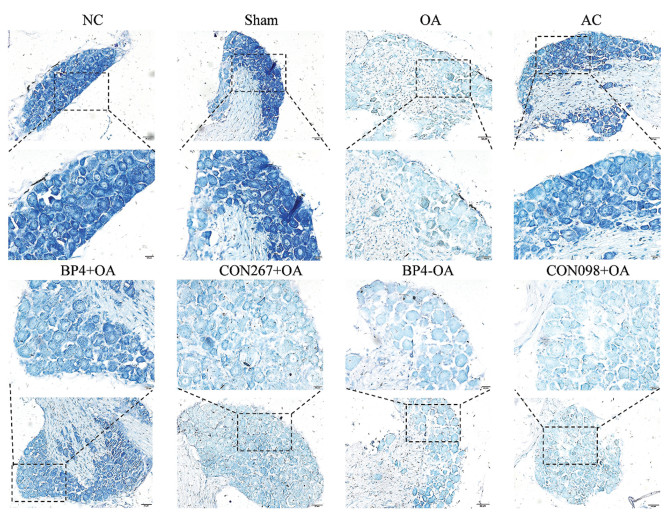
NC组与Sham组神经元胞体饱满, 细胞核清晰可见, 可见中央型尼氏小体; OA组、CON267+OA、CON098+OA组神经元细胞核偏移甚至消失, 胞浆呈空泡状改变, 部分尼氏体溶解, 尼氏染色明显变浅。与OA组和CON267+OA组比较, AC组和BP4+OA组部分神经元细胞核可见, 胞浆空泡状改变减轻, 尼氏染色有所恢复。与CON098+OA组比较, BP4-OA组绝大多数神经元细胞核消失, 胞浆空泡状加剧, 尼氏体溶解, 见图 5。
|
| 图 5 各组DRG尼氏染色结果(×20,×40) Fig. 5 Results of DRG's staining in each group(×20, ×40) |
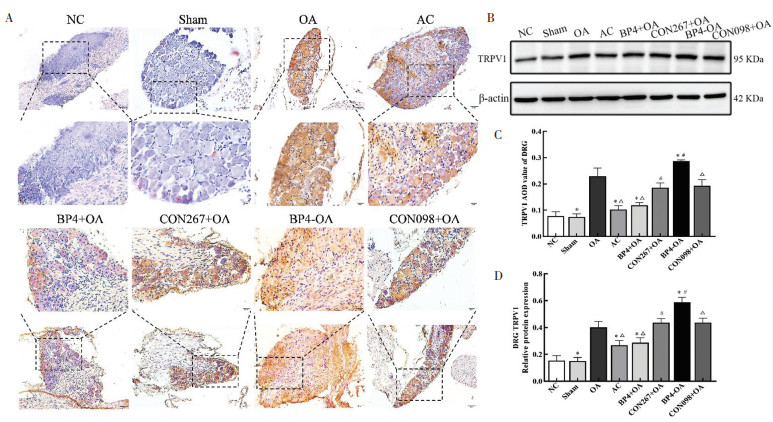
比较造模28 d各组小鼠DRG中TRPV1蛋白阳性表达(定位于细胞质和细胞膜), 见图 6A。NC组和Sham组TRPV1阳性表达差异无统计学意义(P > 0.05);与Sham组比较, OA组TRPV1阳性表达升高(P < 0.05);与OA组比较, AC组TRPV1阳性表达降低(P < 0.05)。BP4+OA组TRPV1阳性表达较CON267+OA组及OA组下降(P < 0.05);BP4+OA组与AC组阳性表达差异无统计学意义(P > 0.05)。BP4-OA组TRPV1阳性表达较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC组(P < 0.05), 见图 6C。
|
| 注:图A,TRPV1 IHC染色;图B,Western blot条带;图C,TRPV1 IHC染色AOD值;图D,TRPV1蛋白表达量。与OA组比较,*P<0.05;与BP4+ OA组比较,#P<0.05;与BP4-OA组比较,△P<0.05。 图 6 各组DRG中TRPV1蛋白表达量比较(×20,×40) Fig. 6 Comparison of TRPV1 protein expression levels of DRG in each group(×20, ×40) |
比较造模28 d各组小鼠DRG中TRPV1蛋白表达水平, 目标蛋白条带见图 6B。NC组和Sham组TRPV1表达水平差异无统计学意义(P > 0.05);与Sham组比较, OA组TRPV1表达水平升高(P < 0.05);与OA组比较, AC组TRPV1蛋白表达水平降低(P < 0.05)。BP4+OA组TRPV1蛋白表达水平较CON267+OA组及OA组下降(P < 0.05);BP4+OA组与AC组TRPV1表达水平差异无统计学意义(P > 0.05)。BP4-OA组TRPV1蛋白表达水平较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC组(P < 0.05), 见图 6D。
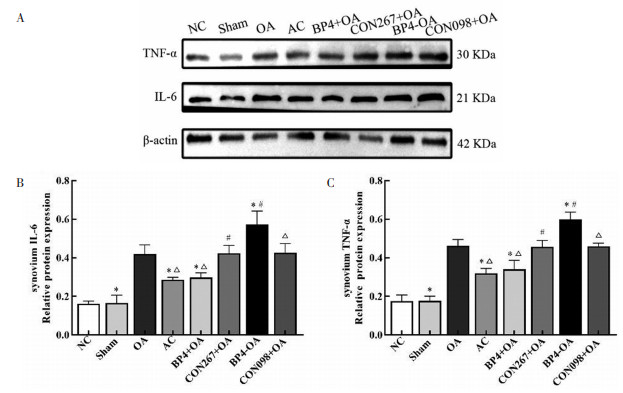
3.7 滑膜炎症因子TNF-α、IL-6蛋白相对表达量检测比较造模28 d各组小鼠滑膜中TNF-α、IL-6蛋白表达水平, NC组和Sham组TNF-α、IL-6蛋白表达水平差异无统计学意义(P > 0.05);与Sham组比较, OA组TNF-α、IL-6蛋白表达水平升高(P < 0.05);与OA组比较, AC组TNF-α、IL-6蛋白表达水平降低(P < 0.05)。BP4+OA组TNF-α、IL-6蛋白表达水平较CON267+OA组及OA组下降(P < 0.05);BP4+OA组与AC组两蛋白表达水平差异无统计学意义(P > 0.05)。BP4-OA组TNF-α、IL-6蛋白表达水平较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC组(P < 0.05), 见图 7。
|
| 注:图A,Western blot条带;图B,IL-6蛋白表达量;图C,TNF-α蛋白表达量。与OA组比较,*P<0.05;与BP4+OA组比较,#P<0.05;与BP4-OA组比较,△P<0.05。 图 7 各组滑膜TNF-α、IL-6蛋白表达量比较 Fig. 7 Comparison of TNF-α and IL-6 protein expression levels of synovium in each group |
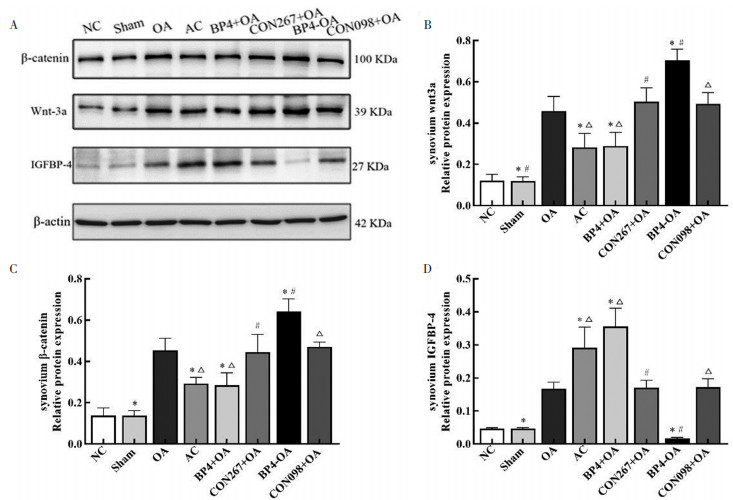
比较造模28 d各组小鼠滑膜中Wnt-3a、β-catenin蛋白表达水平, 目标蛋白条带见图 8A。NC组和Sham组Wnt-3a、β-catenin蛋白表达水平差异无统计学意义(P > 0.05);与Sham组比较, OA组Wnt-3a、β-catenin蛋白表达水平升高(P < 0.05);与OA组比较, AC组Wnt-3a、β-catenin蛋白水平表达降低(P < 0.05)。BP4+OA组Wnt-3a、β-catenin蛋白表达水平较CON267+OA组及OA组下降(P < 0.05);BP4+OA组与AC组两蛋白表达水平差异无统计学意义(P > 0.05)。BP4-OA组Wnt-3a、β-catenin蛋白水平表达较CON098+OA组及OA组升高(P < 0.05), 且明显高于BP4+OA组及AC组(P < 0.05), 见图 8B、图 8C。
|
| 注:图A,Western blot条带;图B,Wnt3a蛋白表达量;图C,β-catenin蛋白表达量;图D,IGFBP-4蛋白表达量。与OA组比较,*P<0.05;与BP4+OA组比较,#P<0.05;与BP4-OA组比较,△P<0.05。 图 8 各组滑膜Wnt3a、β-catenin、IGFBP-4蛋白表达量比较 Fig. 8 Comparison of Wnt3a, β-catenin and IGFBP-4 protein expression levels of synovium in each group |
比较造模28 d各组小鼠滑膜中IGFBP-4蛋白表达水平, 目标蛋白条带见图 8A。NC组和Sham组滑膜IGFBP-4差异无统计学意义(P > 0.05);OA组IGFBP-4表达水平高于NC组和Sham组(P < 0.05);与OA组比较, AC组滑膜IGFBP-4表达水平升高(P < 0.05)。CON267+OA组、CON098+OA组IGFBP-4蛋白表达水平与OA组相近, 差异无统计学意义(P > 0.05)。BP4+OA组滑膜IGFBP-4表达水平较CON267+OA组及OA组升高(P < 0.05);与BP4+OA组比较, AC组IGFBP-4表达水平降低, 但差异无统计学意义(P > 0.05)。BP4-OA组滑膜IGFBP-4表达水平较CON098+OA组及OA组降低(P < 0.05), 且明显低于BP4+OA组及AC组(P < 0.05), 见图 8D。
4 讨论疼痛是KOA病程中持续存在且最难解决的问题, 长期服用镇痛药引发的诸多不良反应使能安全有效治疗疼痛的新疗法需求巨大。因此无毒副作用的黄酮类化合物引起广泛关注, 其中, 花青素能通过减轻关节软骨损伤和炎症缓解OA疼痛, 但关于花青素其他的镇痛机制研究未见报道。
活体成像结果提示腺病毒关节腔注射成功; 滑膜IGFBP-4蛋白Western Blot结果说明腺病毒成功转导模型小鼠的滑膜细胞。MIA诱导的OA模型常被用于研究OA疼痛相关的神经生物学。HE染色发现: OA组软骨表面缺损不连续, 滑膜层增厚纤维化可见炎细胞浸润, 与OA病理变化一致, 提示模型构建成功。AC组软骨缺损程度、滑膜增生和炎细胞浸润减轻, 说明花青素对软骨和滑膜损伤有缓解作用。KOA疼痛与外周敏化和中枢敏化密切相关, 疼痛相关行为学是确定动物模型致敏的常用方法, 结果显示: OA组机械痛阈和热痛阈持续降低至28 d; AC组机械痛阈下降趋势变缓, 热痛阈下降变缓且略有回升, 或许与黄酮类化合物能减少对热感觉敏感的TRPV1有关[13], 行为学结果支持花青素缓解KOA诱发的机械和热痛觉过敏。
P物质是一种传递疼痛信号的神经肽, 血清中P物质含量可量化疼痛水平, 报道发现OA大鼠血清中P物质含量异常升高[14]。结果显示: OA组血清P物质含量升高, AC组含量下降, 提示花青素能减少P物质释放缓解小鼠疼痛。DRG是伤害性感受器胞体聚集地也是最先感知KOA疼痛的区域, 故选择DRG为检测外周敏化的首发站。P物质到达DRG后可能通过影响神经元核仁和尼氏体的功能, 使DRG对感知疼痛变得敏感。尼氏染色显示: OA组DRG神经元核仁偏移, 尼氏体消失; AC组DRG核仁、尼氏体数量和尼氏染色有所恢复, 说明花青素能减轻DRG形态损伤。P物质使小直径DRG中TRPV1通道对低阈值刺激变得敏感, 诱发通道敏化[15], TRPV1是广泛研究的疼痛门户与DRG敏化密切相关[16-17]。结果说明: OA组DRG的TRPV1表达升高, AC组TRPV1表达被抑制, TRPV1的IHC染色得到一致结果。提示花青素通过抑制P物质释放和TRPV1通道激活, 缓解DRG的损伤及敏化, 减轻脊髓部位的敏化状态。
异常放电使DRG增加其游离于滑膜的神经末梢对炎症因子敏感性[18], 同时滑膜炎症与患者疼痛呈正相关, 因此在滑膜进一步探究花青素缓解外周敏化的机制。TNF-α、IL-6参与滑膜炎症使滑膜致敏, 同时通过轴浆运输使伤害性感受器致敏[5], 可见伤害性神经元和神经末梢致敏是双向性的。结果发现: OA组TNF-α、IL-6表达升高, AC组逆转了此结果, 提示花青素减轻外周滑膜炎症和敏化。阻断Wnt通路可抑制神经性疼痛的产生及病理损伤[6, 19], 花青素降低了Wnt通路下游基因TNF-α、IL-6表达, 或许其通过抑制Wnt信号通路发挥镇痛作用。结果发现OA组滑膜Wnt3a、β-catenin表达升高, AC组Wnt3a、β-catenin表达降低, 提示花青素通过抑制Wnt/β-catenin信号通路减轻滑膜炎症和敏化, 但花青素通过何种机制与Wnt/β-catenin通路产生联系尚不明确。IGFBP-4能竞争性与细胞膜上Wnt受体结合, 阻断Wnt/β-catenin信号通路转导, 保护缺血的心脏[7-8], 加之花青素上调高血糖患者血清中IGFBP-4表达[12], 推测花青素通过IGFBP-4影响Wnt/β-catenin信号通路。结果发现OA组滑膜IGFBP-4表达较Sham组升高, AC组滑膜IGFBP-4表达较OA组升高, 且显著高于Sham组, 提示花青素可能通过上调滑膜IGFBP-4表达抑制Wnt/β-catenin通路, 减少滑膜炎症因子和DRG中致敏因子释放, 缓解KOA小鼠疼痛。
为了进一步验证花青素和IGFBP-4之间的靶向联系, 用IGFBP-4过表达和敲减腺病毒处理OA模型。BP4+OA组滑膜Wnt/β-catenin通路蛋白Wnt3a、β-catenin、TNF-α、IL-6表达降低, BP4-OA组Wnt/β-catenin信号通路蛋白表达较CON098+OA组和OA组升高, 明显高于AC组和BP4+OA组, 提示IGFBP-4在滑膜也发挥Wnt信号通路抑制剂作用, 并通过抑制Wnt/β-catenin信号通路来缓解滑膜炎症。滑膜炎症产生的TNF-α、IL-6等能诱发DRG炎症和敏化, 结果发现: BP4+OA组DRG尼氏体数量和尼氏染色有所恢复、P物质含量及TRPV1表达降低; BP4-OA组DRG损伤进一步加重, P物质含量和TRPV1表达高于CON098+OA组和OA组, 明显高于AC组和BP4+OA组, 说明IGFBP-4抑制TRPV1通道激活, 缓解DRG形态损伤和敏化状态。行为学结果提示: BP4+OA组机械痛阈值、热痛阈值逐渐回升; BP4-OA组比较CON098+OA组和OA组机械和热疼痛阈值进一步降低, 说明IGFBP-4发挥与花青素相似的抵抗痛觉过敏作用。以上结果提示: IGFBP-4通过抑制滑Wnt/β-catenin信号通路和滑膜炎症, 降低P物质释放和TRPV1激活, 减轻DRG损伤及敏化, 缓解模型小鼠疼痛。
综合研究结果提示花青素可能通过上调滑膜IGFBP-4表达、抑制Wnt/β-catenin通路和滑膜炎症, 使滑膜和DRG敏感性降低, 抑制痛敏因子P物质和TRPV1激活, 减轻KOA小鼠的外周敏化和疼痛。
| [1] |
YUNUS M H M, NORDIN A, KAMAL H. Pathophysiological perspective of osteoarthritis[J]. Medicina, 2020, 56(11): 614. DOI:10.3390/medicina56110614 |
| [2] |
林璐璐, 石广霞, 屠建锋, 等. 膝骨关节炎疼痛机制研究进展[J]. 中国疼痛医学杂志, 2022, 28(6): 454-459. |
| [3] |
DUAN Y W, CHEN S X, LI Q Y, et al. Neuroimmune mechanisms underlying neuropathic pain: The potential role of TNF-α-necroptosis pathway[J]. International Journal of Molecular Sciences, 2022, 23(13): 7191. DOI:10.3390/ijms23137191 |
| [4] |
CHANG C T, JIANG B Y, CHEN C C. Ion channels involved in substance P-mediated nociception and antinociception[J]. International Journal of Molecular Sciences, 2019, 20(7): 1596. DOI:10.3390/ijms20071596 |
| [5] |
BOAKYE P A, TANG S J, SMITH P A. Mediators of neuropathic pain; focus on spinal microglia, CSF-1, BDNF, CCL21, TNF-α, Wnt ligands, and interleukin 1β[J]. Frontiers in Pain Research, 2021, 2: 698157. DOI:10.3389/fpain.2021.698157 |
| [6] |
GAO Y, ZHOU S Y, PAN Y Z, et al. Wnt3a inhibitor attenuates remifentanil-induced hyperalgesia via downregulating spinal NMDA receptor in rats[J]. Journal of Pain Research, 2020, 13: 1049-1058. DOI:10.2147/JPR.S250663 |
| [7] |
ZHU W D, SHIOJIMA I, ITO Y, et al. IGFBP-4 is an inhibitor of canonical Wnt signalling required for cardiogenesis[J]. Nature, 2008, 454(7202): 345-349. DOI:10.1038/nature07027 |
| [8] |
BACH L A. Insulin-like growth factor binding proteins 4-6[J]. Best Practice & Research Clinical Endocrinology & Metabolism, 2015, 29(5): 713-722. |
| [9] |
LIU J Q, ZHOU H B, SONG L, et al. Anthocyanins: Promising natural products with diverse pharmacological activities[J]. Molecules, 2021, 26(13): 3807. DOI:10.3390/molecules26133807 |
| [10] |
王静, 陈泽峰, 和春霞, 等. 花青素对完全弗氏佐剂诱导慢性炎性痛的镇痛作用及其机制[J]. 中国应用生理学杂志, 2018, 34(5): 476-480. |
| [11] |
XU Y, HE J, HE J. Cyanidin attenuates the high hydrostatic pressure-induced degradation of cellular matrix of nucleus pulposus cell via blocking the Wnt/β-catenin signaling[J]. Tissue & Cell, 2022, 76: 101798. |
| [12] |
YANG L P, LIU Z M, LING W H, et al. Effect of anthocyanins supplementation on serum IGFBP-4 fragments and glycemic control in patients with fasting hyperglycemia: A randomized controlled trial[J]. Diabetes, Metabolic Syndrome and Obesity, 2020, 13: 3395-3404. DOI:10.2147/DMSO.S266751 |
| [13] |
WANG Z Y, LING D Y, WU C X, et al. Baicalin prevents the up-regulation of TRPV1 in dorsal root ganglion and attenuates chronic neuropathic pain[J]. Veterinary Medicine and Science, 2020, 6(4): 1034-1040. DOI:10.1002/vms3.318 |
| [14] |
HUANG Y F, LIN Q, TAN X, et al. Rehmannia alcohol extract inhibits neuropeptide secretion and alleviates osteoarthritis pain through cartilage protection[J]. Heliyon, 2023, 9(9): e1932. |
| [15] |
SCULPTOREANU A, AURA KULLMANN F, DE GROAT W C. Neurokinin 2 receptor-mediated activation of protein kinase C modulates capsaicin responses in DRG neurons from adult rats[J]. The European Journal of Neuroscience, 2008, 27(12): 3171-3181. |
| [16] |
SHUBA Y M. Beyond neuronal heat sensing: Diversity of TRPV1 heat-capsaicin receptor-channel functions[J]. Frontiers in Cellular Neuroscience, 2021, 14: 612480. |
| [17] |
LAPOINTE T K, BASSO L, IFTINCA M C, et al. TRPV1 sensitization mediates postinflammatory visceral pain following acute colitis[J]. American Journal of Physiology Gastrointestinal and Liver Physiology, 2015, 309(2): G87-G99. |
| [18] |
ZHANG R X, REN K, DUBNER R. Osteoarthritis pain mechanisms: Basic studies in animal models[J]. Osteoarthritis and Cartilage, 2013, 21(9): 1308-1315. |
| [19] |
DESHMUKH V, O'GREEN A L, BOSSARD C, et al. Modulation of the Wnt pathway through inhibition of CLK2 and DYRK1A by lorecivivint as a novel, potentially disease-modifying approach for knee osteoarthritis treatment[J]. Osteoarthritis and Cartilage, 2019, 27(9): 1347-1360. |
2. Hebei Key Laboratory for Chronic Diseases, Tangshan 063210, China
 2025, Vol. 42
2025, Vol. 42