文章信息
- 康维娜, 李学永, 路新卿.
- KANG Weina, LI Xueyong, LU Xinqing.
- 马齿苋多糖调节TLR4/NF-κB信号通路对大鼠溃疡性结肠炎的影响
- Effect of portulaca oleracea polysaccharide on ulcerative colitis in rats by regulating TLR4/NF-κB signaling pathway
- 天津中医药, 2025, 42(3): 353-361
- Tianjin Journal of Traditional Chinese Medicine, 2025, 42(3): 353-361
- http://dx.doi.org/10.11656/j.issn.1672-1519.2025.03.14
-
文章历史
- 收稿日期: 2024-09-24
溃疡性结肠炎(UC)是一种病变部位在结直肠的炎性肠病, 以腹泻、腹痛、便脓血等为主要临床特征, 表现出反复发作、迁延难愈的特点, 影响患者生活质量, 且具有一定的癌变风险[1]。目前研究认为炎症、氧化应激及肠上皮细胞过度凋亡是UC的重要推动因素[2-3], 而Toll样受体4(TLR4)/核转录因子-κB(NF-κB)信号通路在炎症、氧化应激和细胞凋亡的病理机制中发挥作用[4-5]。近年来病理学研究证实, TLR4/NF-κB信号通路在肠道损伤过程中处于异常高度活化状态, 与UC疾病进展关系密切[6]。马齿苋多糖(POP)为中药马齿苋的主要活性成分之一, 研究证实, POP对UC动物模型炎症具有一定的抑制作用[7], 但其作用机制尚未阐明。本研究旨在探讨POP调节TLR4/NF-κB信号通路对UC大鼠结肠组织损伤的影响, 以期为POP治疗UC提供参考。
1 材料与方法 1.1 动物通过河北省实验动物中心[SCXK(冀)2021-002]购买40只7周龄雄性SD大鼠, 200~240 g, 在通风良好、恒温恒湿、模拟自然光照周期的清洁级动物房饲养, 进食饮水不限。本研究经邯郸市第一医院伦理委员会审批通过[审批号: HDYYLL(K)2022-019]。
1.2 药物与试剂POP(货号WKQ-0029205, 纯度≥ 90%)、TLR4抑制剂瑞沙托维(TAK-242, 货号WKQ-0020021)、TLR4激动剂脂多糖(LPS, 货号WKQ-0003274)购自四川维克奇公司; 葡聚糖硫酸钠(货号MB5535-1)、放射免疫沉淀法(RIPA)裂解液(货号MA0152)、增强化学发光试剂(ECL, 货号MA0186)和苏木精-伊红(HE)染色(货号MB9898-2)、原位末端标记法(TUNEL)染色(货号MA0223-1)试剂盒购自大连美仑生物技术公司; 干扰素(IFN)-γ(货号JM-01605R2)、白细胞介素(IL)-1β(货号JM-01454R1)、IL-10(货号JM-01602R1)、丙二醛(MDA, 货号JM-10323R1)、超氧化物歧化酶(SOD, 货号JM-01793R2)、过氧化氢酶(CAT, 货号JM-10334R2)试剂盒购自江苏晶美生物科技公司; 活性氧(ROS, 批号20220413)试剂盒购自上海恒斐生物公司; 肿瘤坏死因子(TNF)-α(货号SEKR-0009)、髓过氧化物酶(MPO, 货号SEKR-0073)购自北京索莱宝公司; 二奎磷甲酸(BCA)法蛋白定量试剂盒、RNA提取液(货号G3013)、一步法实时聚合酶链式反应(RT-PCR)试剂盒(货号G3335)购自武汉赛维尔生物科技公司; TLR4(货号bs-1021R)、NF-κB p65(货号bs-23216R)、B淋巴细胞瘤-2(Bcl-2)相关X蛋白(Bax, 货号bs-28034R)、β-肌动蛋白(β-actin, bs-0061R)抗体和免疫球蛋白(Ig)G二抗购自北京博奥森生物技术公司; Bcl-2(货号ab194583)抗体购自英国Abcam公司; 剪切型半胱氨酸蛋白酶-3(Cleaved Caspase-3)抗体(货号AF7022)购自美国Affinity公司。
1.3 仪器KD型石蜡包埋机(浙江金华科迪仪器公司); HM325型石蜡组织切片机、MFC型酶标仪(美国Thermo Fisher公司); YD-AB型摊烤片机(浙江益迪设备公司); DS-Qi2型荧光显微镜(日本尼康公司); S1010E型高速低温离心机(美国Scilogex公司); Mini型电泳仪和转印槽(美国Bio-Rad公司); AlphaEaseFC型蛋白条带灰度分析系统(美国Alphalnnotech公司); RS232C型核酸测定仪、Realplex2型RT-PCR仪(德国Eppendorf公司)。
1.4 分组与造模按随机数字表法, 将饲养7 d后的大鼠随机分为正常(Normal)组、模型(Model)组、POP组、POP+TAK-242组和POP+LPS组, 每组8只。除Normal组外, 其他4组参照文献[8]报道的方法连续7 d自由饮用5%葡聚糖硫酸钠溶液以制备UC动物模型。
1.5 给药治疗POP组灌胃10 mg/kg POP[7]和腹腔注射生理盐水, POP+TAK-242组灌胃10 mg/kg POP和腹腔注射3 mg/kg TAK-242[9], POP+LPS组灌注10 mg/kg POP和腹腔注射0.4 mg/kg LPS[10], Normal组和Model组灌胃生理盐水和腹腔注射生理盐水, 灌胃和腹腔注射体积均为5 mL/kg, 1次/d给药连续治疗2周。
1.6 大鼠一般状态观察及疾病活动指数(DAI)评分治疗完成后, 观察大鼠毛发、精神状态、饮食、大便状况、便血情况、体质量变化等一般状态。从体质量、大便状况、便血情况3个方面进行DAI评分[11]: 1)体质量持续升高或无下降, 记0分; 体质量下降率≤ 5%、5%~10%、10%~15%、≥ 15%, 分别记1、2、3、4分。2)大便形态正常, 记0分; 大便松散, 记1分; 大便呈糊状, 记2分; 稀便, 记3分; 水样便, 记4分。3)大便潜血阴性, 记0分; 大便潜血阳性, 记2分; 便血, 记4分。DAI评分=(体质量评分+大便状况评分+便血情况评分)/3。
1.7 结肠长度测量及结肠黏膜损伤指数(CMDI)评分腹腔注射45 mg/kg戊巴比妥钠麻醉后颈椎脱臼处死大鼠, 开腹取结肠、测量其长度。纵向剖开肠管, 清除结肠内容物, 用生理盐水冲洗干净。CMDI评分标准[11]: 未见损伤, 记0分; 结肠黏膜水肿, 肠壁未见溃疡, 记1分; 结肠肠壁变厚, 肠壁未见溃疡, 记2分; 结肠肠壁出现直径≤ 1 cm, 记3分; 结肠肠壁出现直径1~2 cm溃疡灶, 结肠与周边无粘连时记4分、有粘连时记5分。
1.8 HE、TUNEL染色观察结肠组织病理变化和细胞凋亡将部分结肠组织置于福尔马林溶液固定72 h, 经脱水、石蜡包埋、切片、展片、烤片等步骤处理后, 分别按试剂盒说明行HE染色和TUNEL染色并观察肠组织病理变化。计数TUNEL染色切片中细胞总数和凋亡细胞数, 凋亡指数=凋亡细胞数/细胞总数×100%。
1.9 酶联免疫吸附法(ELISA)检测结肠组织中炎症因子水平和氧化应激指标取部分结肠组织按1:9(质量体积比)加入4℃生理盐水, 研磨匀浆, 离心半径10 cm, 3 500 r/min离心10 min, 取上清液, 通过酶标仪检测结肠组织炎症因子IFN-γ、TNF-α、IL-1β、IL-10、MPO水平和氧化应激指标(ROS、MDA水平和SOD、CAT活性)。
1.10 蛋白免疫印迹(Western blot)法检测结肠组织中TLR4、NF-κB p65、Bcl-2、Bax、Cleaved Caspase-3蛋白表达取100 mg结肠组织, 加RIPA裂解液提取总蛋白、BCA法测定浓度、95℃水浴10 min变性, 依次通过电泳分离、湿法转至PVDF膜、蛋白封闭液室温封闭60 min处理后, 加TLR4(1:1 000)、NF-κB p65(1:1 000)、Bcl-2(1:1 000)、Bax(1:1 000)、Cleaved Caspase-3(1:800)、β-actin(1:2 000)抗体稀释液4℃孵育过夜, 加IgG二抗(1:4 000)稀释液室温孵育90 min, ECL显色后分析蛋白条带灰度值, 以β-actin为内参对目标蛋白进行半定量分析。
1.11 RT-PCR法检测结肠组织中TLR4、NF-κB p65、Bcl-2、Bax、Cleaved Caspase-3 mRNA表达取50 mg结肠组织, 加RNA提取液提取总RNA, 通过核酸测定仪检测总RNA纯度后, 通过一步法RT-PCR试剂盒逆转录为cDNA, RT-PCR扩增反应: 95℃预变性2 min一次; 95℃变性10 s、60℃退火30 s、72℃延伸30 s, 循环40次。然后以β-actin为内参, 运用2-ΔΔCt公式计算目标基因表达量。引物序列见表 1。
运用SPSS 20.0进行数据统计学分析, 计量资料符合正态分布以均数±标准差(x±s)表示, 多组间比较采用one-way ANOVA, 组间多重比较采用LSD-t检验, P < 0.05表示差异有统计学意义。
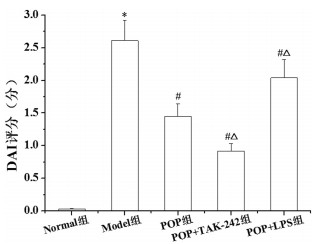
2 结果 2.1 POP对UC大鼠状态和DAI评分的影响Normal组大鼠毛发滑顺、有光泽, 反应灵敏, 摄食量正常, 大便形态正常, 潜血阴性, 体质量持续升高。Model组大鼠毛发粗糙、污浊、无光泽, 反应迟钝, 摄食量明显减少, 大便稀溏、不同程度便血, 肛周有稀便黏连, 体质量降低。与Model组比较, POP组、POP+TAK-242组和POP+LPS组大鼠一般状态呈不同程度改善, 改善效果POP+TAK-242组 > POP组 > POP+LPS组。与Normal组比较, Model组DAI评分明显升高(P < 0.05);与Model组比较, POP组、POP+TAK-242组和POP+LPS组DAI评分明显降低(P < 0.05);与POP组比较, POP+TAK-242组DAI评分明显降低, POP+LPS组DAI评分明显升高(P < 0.05)。见图 1。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 1 各组大鼠DAI评分比较 Fig. 1 Comparison of DAI scores of rats in each group |
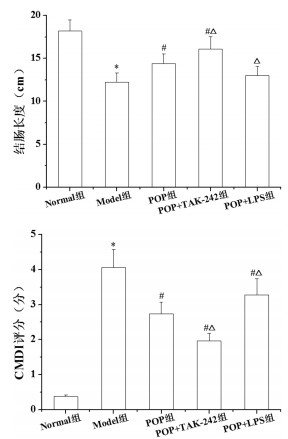
与Normal组比较, Model组结肠长度明显降低, CMDI评分明显升高(P < 0.05)。与Model组比较, POP组和POP+TAK-242组结肠长度明显升高(P <0.05), POP组、POP+TAK-242组和POP+LPS组CMDI评分明显降低(P < 0.05)。与POP组比较, POP+TAK-242组结肠长度明显升高, CMDI评分明显降低(P < 0.05);POP+LPS组结肠长度明显降低, CMDI评分明显升高(P < 0.05)。见图 2。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 2 各组大鼠结肠组织长度、CMDI评分比较 Fig. 2 Comparison of colon tissue length, CMDI scores of rats in each group |
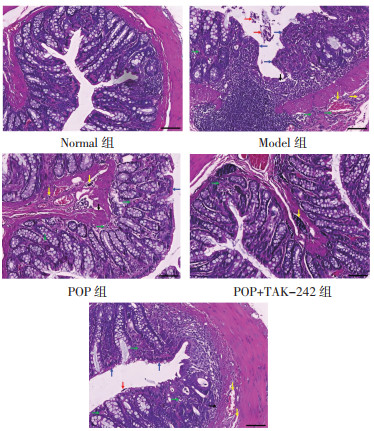
Normal组大鼠结肠组织层次清晰, 结构完整, 腺体丰富, 肠黏膜绒毛排列整齐。Model组结肠组织层次不清, 肠黏膜水肿, 上皮成块状脱落, 绒毛变短或消失, 腺体数量减少, 大量炎性细胞浸润, 黏膜层可见溃疡面, 损及肌层。与Model组比较, POP组、POP+TAK-242组和POP+LPS组结肠组织上述病理变化不同程度改善, 改善效果POP+TAK-242组 > POP组 > POP+LPS组。见图 3。
|
| 注:黑色箭头表示肠黏膜水肿,红色箭头表示上皮块状脱落,蓝色箭头表示绒毛变短或消失,绿色箭头表示炎性细胞浸润,黄色箭头表示溃疡面。刻度尺:50 μm。 图 3 各组大鼠结肠组织病理变化比较(HE染色,×200) Fig. 3 Comparison of pathological changes in colon tissues of rats in each group(HE staining, ×200) |
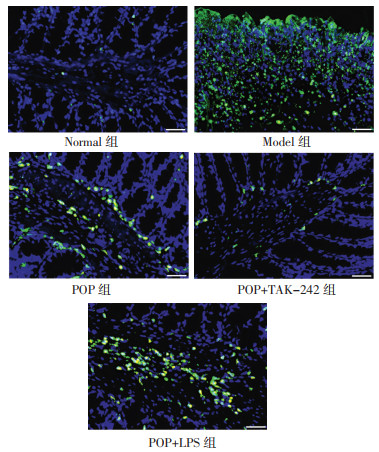
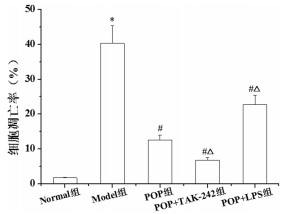
与Normal组比较, Model组结肠细胞凋亡数量明显增多, 凋亡指数明显升高(P < 0.05)。与Model组比较, POP组、POP+TAK-242组和POP+LPS组结肠细胞凋亡数量不同程度减少, 凋亡指数均明显降低(P < 0.05)。与POP组比较, POP+TAK-242组凋亡指数明显降低, POP+LPS组凋亡指数明显升高(P < 0.05)。见图 4、图 5。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。刻度尺:50 μm。 图 4 各组大鼠结肠细胞凋亡状况比较(TUNEL染色,×200) Fig. 4 Comparison of apoptosis status of colon cells of rats in each group(TUNEL staining, ×200) |
|
| 图 5 各组大鼠结肠组织细胞凋亡率比较 Fig. 5 Comparison of apoptosis rate of colon cells of rats in each group |
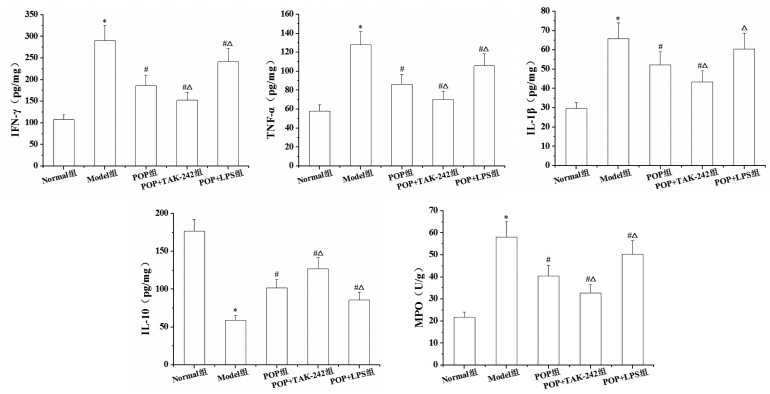
与Normal组比较, Model组结肠组织中炎症因子IFN-γ、TNF-α、IL-1β、MPO水平明显升高, IL-10水平明显降低(P < 0.05)。与Model组比较, POP组、POP+TAK-242组和POP+LPS组结肠组织中IFN-γ、TNF-α、IL-1β(POP+LPS组除外)、MPO水平明显降低, IL-10水平明显升高(P < 0.05)。与POP组比较, POP+TAK-242组结肠组织中IFN-γ、TNF-α、IL-1β、MPO水平明显降低, IL-10水平明显升高(P < 0.05);POP+LPS组结肠组织中IFN-γ、TNF-α、IL-1β、MPO水平明显升高, IL-10水平明显降低(P < 0.05)。见图 6。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 6 各组大鼠结肠组织中炎症因子水平比较 Fig. 6 Comparison of inflammatory factors level in colon tissues of rats in each group |
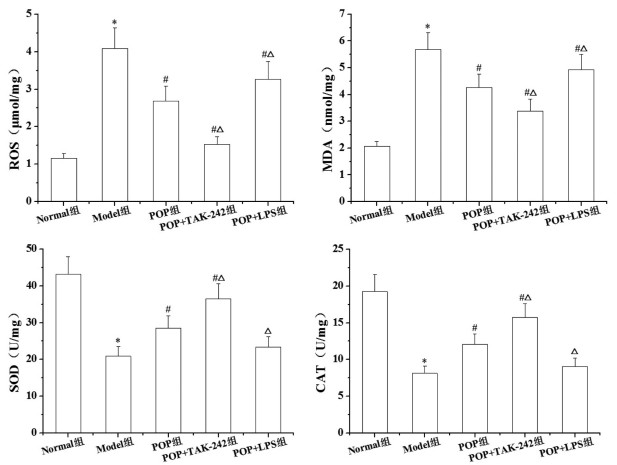
与Normal组比较, Model组结肠组织ROS、MDA水平明显升高, SOD、CAT活性明显降低(P < 0.05)。与Model组比较, POP组、POP+TAK-242组和POP+LPS组结肠组织中ROS、MDA水平明显降低, SOD(POP+LPS组除外)、CAT(POP+LPS组除外)活性明显升高(P < 0.05)。与POP组比较, POP+TAK-242组结肠组织中ROS、MDA水平明显降低, SOD、CAT活性明显升高(P < 0.05);POP+LPS组结肠组织中ROS、MDA水平明显升高, SOD、CAT活性明显降低(P < 0.05)。见图 7。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 7 各组大鼠结肠组织中氧化应激指标比较 Fig. 7 Comparison of inflammatory factors level in colon tissues of rats in each group |
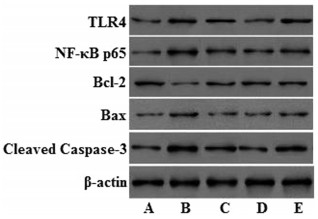
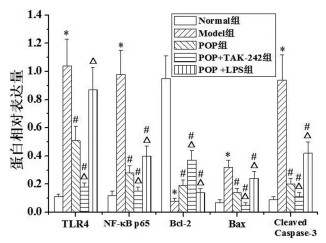
与Normal组比较, Model组TLR4、NF-κB p65、Bax、Cleaved Caspase-3蛋白表达水平明显升高, Bcl-2表达水平明显降低(P < 0.05)。与Model组比较, POP组、POP+TAK-242组和POP+LPS组TLR4(POP+LPS组除外)、NF-κB p65、Bax、Cleaved Caspase-3表达水平明显降低, Bcl-2表达水平明显升高(P < 0.05)。与POP组比较, POP+TAK-242组TLR4、NF-κB p65、Bax、Cleaved Caspase-3表达水平明显降低, Bcl-2表达水平明显升高(P < 0.05);POP+LPS组TLR4、NF-κB p65、Bax、Cleaved Caspase-3表达水平明显升高, Bcl-2表达水平明显降低(P < 0.05)。见图 8、图 9。
|
| 注:A,Normal组;B,Model组;C,POP组;D,POP+TAK-242组;E,POP +LPS组。 图 8 各组大鼠结肠组织TLR4、NF-κB p65、Bcl-2、Bax、Cleaved Caspase-3蛋白表达状况 Fig. 8 Expression of TLR4, NF-κB p65, Bcl-2, Bax, Cleaved Caspase-3 protein in colon tissues of rats in each group |
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 9 各组大鼠结肠组织TLR4、NF-κB p65、Bcl-2、Bax、Cleaved Caspase-3蛋白表达水平比较 Fig. 9 Comparison of protein expression level of TLR4, NF-κB p65, Bcl-2, Bax, Cleaved Caspase-3 mRNA in colon tissues of rats in each group |
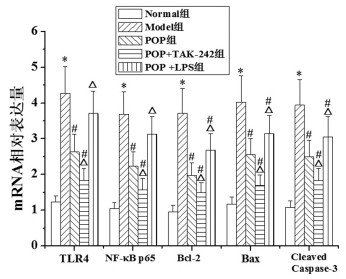
与Normal组比较, Model组结肠组织TLR4、NF-κB p65、Bax、Cleaved Caspase-3 mRNA表达水平明显升高, Bcl-2 mRNA表达水平明显降低(P < 0.05)。与Model组比较, POP组、POP+TAK-242组和POP+LPS组结肠组织TLR4(POP+LPS组除外)、NF-κB p65(POP+LPS组除外)、Bax、Cleaved Caspase-3 mRNA表达水平明显降低, Bcl-2 mRNA表达水平明显升高(P < 0.05)。与POP组比较, POP+TAK-242组TLR4、NF-κB p65、Bax、Cleaved Caspase-3 mRNA表达水平明显降低, Bcl-2 mRNA表达水平明显升高(P < 0.05);POP+LPS组TLR4、NF-κB p65、Bax、Cleaved Caspase-3 mRNA表达水平明显升高, Bcl-2 mRNA表达水平明显降低(P < 0.05)。见图 10。
|
| 注:与Normal组比较,*P<0.05;与Model组比较,#P<0.05;与POP组比较,△P<0.05。 图 10 各组大鼠结肠组织TLR4、NF-κB p65、Bcl-2、Bax、Cleaved Caspase-3 mRNA表达水平比较 Fig. 10 Comparison of expression level of TLR4, NF-κB p65, Bcl-2, Bax, Cleaved Caspase-3 mRNA in colon tissues of rats in each group |
UC是一种较常见的慢性、弥漫性炎性肠病, 在中国发病率超过2/10万, 且呈现逐年上升趋势, 发病机制复杂、治疗周期漫长, 多发于20~30岁和50~70岁两个年龄段, 不但影响患者生活质量, 更为严重的是UC将显著增加患癌风险, 是医药工作者关注的热点之一[12]。目前, 临床上主要采取氨基水杨酸类药物、免疫抑制剂、抗菌药物、糖皮质激素等一种或多种药物联合治疗, 但免疫抑制剂、糖皮质激素等药物长期应用往往引发广泛的毒副作用, 且长期疗效并不理想。因此, 寻找疗效确切且毒副作用小的UC新型治疗药物具有重要的临床意义。
中医将UC归属于"泄泻""痢疾""肠癖""久痢"等范畴, 其病位在肠腑, 脾胃虚弱、气机壅滞、湿热浊毒内蕴为其主要病机, 可分为大肠湿热型、脾虚湿蕴型、热毒炽盛型、寒热错杂型、肝郁脾虚型、脾肾阳虚型等, 其中大肠湿热型较为多见[13-14]。马齿苋取自马齿苋科植物马齿苋的干燥地上部分入药, 首载于《本草经集注》, 现为《中国药典(一部)》收录中药品种, 味酸性寒, 归脾经、大肠经, 具有清热利湿、解毒消肿、凉血止血、止痢等功效。良好的动物模型是病理生理学、药理学等研究的基础, UC动物模型制备方法主要有诱导法(化学试剂诱导、微生物诱导、食物诱导等)、基因敲除法(屏障蛋白基因敲除、抗炎因子基因敲除等)、联合法等, 其中化学试剂诱导法是最经典、最常用的UC动物模型制备方法, 该方法具有操作简便、复制性强、与人类病理特点近似等优势, 其中葡聚糖硫酸钠是最常用的化学诱导试剂, 葡聚糖硫酸钠诱导法也是中医学大肠湿热型UC动物模型制备的常用方法[14-15]。本实验采用连续7 d自由饮用5%葡聚糖硫酸钠溶液的方法制备UC大鼠模型, 结果显示, UC模型大鼠表现出毛发无光泽、反应迟钝、摄食量减少、大便稀溏、便血、体质量降低等状态, 结肠长度明显降低, DAI评分和CMDI评分明显升高; 结肠组织呈现组织层次不清, 肠黏膜水肿, 上皮成块状脱落, 绒毛变短或消失, 腺体数量减少, 大量炎性细胞浸润, 黏膜层可见溃疡面等病理变化, 这与王小天等[16]报道相似。经POP治疗可明显改善UC大鼠一般状态, 提高结肠长度, 降低DAI评分和CMDI评分, 减轻结肠组织病变, 提示POP具有减轻UC大鼠结肠组织损伤的作用。
POP能够减轻UC大鼠结肠组织损伤可能与下列因素有关, 1)UC疾病使肠黏膜免疫系统受损失衡导致促炎因子IFN-γ、TNF-α、IL-1β分泌并抑制抑炎因子IL-10分泌, 并且TNF-α和IL-1β具有炎性趋化属性, 促进中性粒细胞等白细胞向受损部位聚集并进一步释放促炎因子, 从而加重炎症反应并促进炎性浸润[17-18]。MPO为中性粒细胞分泌的一种过氧化物酶, 其水平能够反映炎性浸润程度, 研究发现UC患者病情程度与MPO水平呈正相关。Wu等[19]报道通过药物抑制炎症反应可有效减轻UC大鼠结肠组织损伤。本研究发现, UC模型大鼠结肠组织中IFN-γ、TNF-α、IL-1β水平和MPO活性明显升高, IL-10水平明显降低, 说明UC大鼠出现较强的炎症反应。POP抗炎作用良好, 可明显降低UC大鼠结肠组织中IFN-γ、TNF-α、IL-1β水平和MPO活性并明显提高IL-10水平, 提示POP可能通过抑制炎症反应减轻UC大鼠结肠组织损伤。2)UC发生发展过程中, 持续的炎性环境导致结肠组织血管异常收缩, 致使肠黏膜缺氧缺血而过度生成ROS, 超过SOD(将ROS转化为H2O2和O2)、CAT(将转化H2O2为H2O)等内源性抗氧化酶还原清除ROS能力, 过剩的ROS将损伤生物分子膜、蛋白质、核酸等(氧化应激损伤), 并且其终产物之一的MDA具有生物毒性[20]。本研究发现, UC模型大鼠结肠组织中ROS、MDA水平明显升高, SOD、CAT活性明显降低, 说明UC大鼠出现氧化应激损伤。POP具有抗氧化作用, 可明显降低UC大鼠结肠组织ROS、MDA水平, 明显提高SOD和CAT活性, 提示POP可能通过抑制氧化应激损伤减轻UC大鼠结肠组织损伤。3)肠上皮细胞过度凋亡是UC进展的重要原因, Cleaved Caspase-3可诱导细胞结构蛋白、功能蛋白、核酸等生物大分子降解而促使细胞凋亡, 被认为是细胞凋亡的关键启动因子[21]。本研究发现, UC模型大鼠结肠细胞凋亡指数和结肠组织中Cleaved Caspase-3蛋白、mRNA表达水平明显升高。POP有抑制细胞凋亡作用, 可明显降低UC大鼠结肠细胞凋亡指数和结肠组织中Cleaved Caspase-3蛋白、mRNA表达水平, 提示POP可能通过抑制结肠细胞凋亡减轻UC大鼠结肠组织损伤。与潘中武等[22]报道相似。
TLR4是Toll样受体(TLRs)家族蛋白中研究最为广泛的亚型之一, 在先天免疫系统中作用明显, 能够被多种病原分子模式识别并直接或间接诱导促炎因子表达, 进而促进炎症反应[23]。体外细胞实验、动物体内实验和临床研究结果均表明UC疾病过程大量病原体入侵刺激TLR4高表达并高度活化, 并诱导下游靶蛋白NF-κB表达上调与活化[24-26]。NF-κB以p65亚基和p50亚基二聚体形式存在, 活化NF-κB入核后p65亚基与DNA顺式反应元件κB序列结合而诱导促炎因子IFN-γ、TNF-α、IL-1β等表达, 从而加重炎症损伤[27]。Bax和Bcl-2通过影响线粒体膜孔道通透性而参与细胞线粒体凋亡途径的调节, 病理状态下二者由细胞质移位至线粒体膜, Bax能够形成同源二聚体"Bax-Bax"或与Bcl-2形成异源二聚体"Bax-Bcl-2", "Bax-Bax"可在线粒体膜形成高通透性孔道, 导致线粒体内容物细胞色素C等由线粒体进入细胞质, 细胞色素C诱导Caspase-3活化进而启动细胞凋亡程序; 而"Bax-Bcl-2"则不具备上述活性, 所以Bcl-2具有抑制细胞凋亡的生物学作用[28]。本研究发现, UC模型大鼠结肠组织TLR4、NF-κB p65、Bax、Cleaved Caspase-3蛋白和mRNA表达水平明显升高, Bcl-2蛋白和mRNA表达水平明显降低; 经POP治疗可明显降低UC大鼠结肠组织TLR4、NF-κB p65、Bax、Cleaved Caspase-3蛋白和mRNA表达水平, 明显升高Bcl-2蛋白和mRNA表达水平, 说明下调TLR4/NF-κB信号通路可能是POP减轻UC大鼠结肠组织损伤的重要分子机制。本研究还发现, POP+TAK-242组对UC大鼠一般状态、DAI评分、结肠长度、CMDI评分、炎症因子水平、氧化应激指标、结肠组织病理变化、细胞凋亡、TLR4/NF-κB信号通路相关蛋白和mRNA表达的作用明显强于POP组, POP+LPS组对各项指标的作用则明显弱于POP组, 从而进一步证实了POP减轻UC大鼠结肠组织损伤的作用机制与下调TLR4/NF-κB信号通路有关。
综上所述, POP具有减轻UC大鼠结肠组织损伤的作用, 可能与下调TLR4/NF-κB信号通路通路, 进而抑制炎症、氧化应激和细胞凋亡有关。本研究结果为UC(尤其是中医学大肠湿热型UC)的临床治疗及新药研发提供了新的思路。但本研究尚存在一些局限性, 首先未设置阳性药物组和POP药物梯度, 未能阐明POP最佳药物剂量; 其次未能阐明POP是否适合中医学所有类型的UC。课题组下一步将针对上述不足之处开展后续研究。
| [1] |
关清, 崔妙玲, 莫焱, 等. 溃疡性结肠炎症状群的研究进展[J]. 广西医学, 2023, 45(6): 713-717. |
| [2] |
DONG X F, LU K, LIN P C, et al. Saccharina japonica ethanol extract ameliorates depression/anxiety-like behavior by inhibiting inflammation, oxidative stress, and apoptosis in dextran sodium sulfate induced ulcerative colitis mice[J]. Frontiers in Nutrition, 2021, 8: 784532. DOI:10.3389/fnut.2021.784532 |
| [3] |
SHAHID M, RAISH M, AHMAD A, et al. Sinapic acid ameliorates acetic acid-induced ulcerative colitis in rats by suppressing inflammation, oxidative stress, and apoptosis[J]. Molecules, 2022, 27(13): 4139. DOI:10.3390/molecules27134139 |
| [4] |
SARAWI W S, ALHUSAINI A M, FADDA L M, et al. Nano-curcumin prevents cardiac injury, oxidative stress and inflammation, and modulates TLR4/NF-κB and MAPK signaling in copper sulfate-intoxicated rats[J]. Antioxidants, 2021, 10(9): 1414. DOI:10.3390/antiox10091414 |
| [5] |
WU H, WU R, LIU T X, et al. Peroxiredoxin 6 alleviates high glucose-induced inflammation and apoptosis in HK-2 cells by inhibiting TLR4/NF-κB signaling[J]. Annals of Translational Medicine, 2023, 11(2): 41. DOI:10.21037/atm-22-6063 |
| [6] |
黄星星, 任晓芳, 张聪伟, 等. 中药复方干预TLR4/NF-κB相关通路治疗溃疡性结肠炎的研究进展[J]. 现代中西医结合杂志, 2022, 31(21): 3031-3035. |
| [7] |
范文涛, 王攀红, 王倩. 马齿苋多糖对溃疡性结肠炎大鼠肠组织IL-6/STAT3及NF-κB的影响[J]. 中国应用生理学杂志, 2018, 34(3): 263-267. |
| [8] |
蔺晓源, 宁杭, 李开楊, 等. 健脾益肠散对溃疡性结肠炎大鼠NLRP3/ASC/Caspase-1信号通路的影响[J]. 中国实验方剂学杂志, 2023, 29(16): 154-161. |
| [9] |
张杰, 李红, 王进海, 等. 肠道微生态对腹泻型肠易激综合征的影响及其作用机制探讨[J]. 世界临床药物, 2019, 40(5): 340-346. |
| [10] |
黄文炼, 刘鸿雁, 任丽蓉, 等. 栀子苷抑制TLR4/RIP3/NF-κB信号通路对急性胰腺炎大鼠肠损伤的影响[J]. 四川医学, 2022, 43(12): 1178-1184. |
| [11] |
许话, 严红梅, 陈斓. 仙茅苷对溃疡性结肠炎大鼠JAK/STAT/NF-κB信号通路的影响[J]. 中国药师, 2022, 25(3): 406-413. |
| [12] |
史瑞, 李军祥, 沈洪, 等. 溃疡性结肠炎中医诊疗专家共识(2023)[J]. 中华中医药杂志, 2024, 39(1): 288-296. |
| [13] |
刘嫣然, 王惠娟. 从内痈分期论治溃疡性结肠炎[J]. 中医学报, 2021, 36(9): 1881-1884. |
| [14] |
尹园缘, 宾东华, 刘颖, 等. 溃疡性结肠炎病证结合动物模型的制备与评价[J]. 中国实验方剂学杂志, 2022, 28(15): 207-215. |
| [15] |
田家华, 索小涛, 马晨曦, 等. 溃疡性结肠炎动物模型构建方法的研究进展[J]. 山东医药, 2024, 64(13): 111-114. |
| [16] |
王小天, 王月, 彪雅宁, 等. 燮理汤对溃疡性结肠炎小鼠TLR4/NF-κB/HIF-1α通路的影响[J]. 中国实验方剂学杂志, 2023, 29(8): 142-149. |
| [17] |
文雨薇, 李科, 吕弯弯, 等. 黄芪多糖APS-Ⅰ、APS-Ⅱ制备及其对溃疡性结肠炎小鼠抗炎活性[J]. 中草药, 2024, 55(14): 4759-4770. |
| [18] |
冯云, 朱军, 潘蓓, 等. 溃疡性结肠炎患者肠道双歧杆菌、肠球菌及真杆菌失调及血清TLR4、MPO表达与疾病活动度的关系[J]. 临床医学, 2023, 43(11): 9-12. |
| [19] |
WU D S, ZHANG Y, ZOU B, et al. Shaoyao decoction alleviates TNBS-induced ulcerative colitis by decreasing inflammation and balancing the homeostasis of Th17/Treg cells[J]. BMC Complementary Medicine and Therapies, 2023, 23(1): 424. |
| [20] |
LIN C, ZHOU Z H, ZHANG L J, et al. Gegen Qinlian Decoction relieves ulcerative colitis via adjusting dysregulated Nrf2/ARE signaling[J]. Evidence-Based Complementary and Alternative Medicine, 2022, 2022: 2934552. |
| [21] |
MICHAELY L M, RISSMANN M, ARMANDO F, et al. Rift valley fever virus non-structural protein S is associated with nuclear translocation of active Caspase-3 and inclusion body formation[J]. Viruses, 2022, 14(11): 2487. |
| [22] |
潘中武, 李泽朋, 陈晓, 等. 基于线粒体氧化应激损伤探讨白杨素对溃疡性结肠炎大鼠的保护作用及机制[J]. 中药材, 2023, 46(12): 3081-3090. |
| [23] |
CHOUDHARY V, GRIFFITH S, CHEN X S, et al. Pathogen-associated molecular pattern-induced TLR2 and TLR4 activation increases keratinocyte production of inflammatory mediators and is inhibited by phosphatidylglycerol[J]. Molecular Pharmacology, 2020, 97(5): 324-335. |
| [24] |
钱珂文, 王楚棋, 张淑怡, 等. 基于TLR4-Ig融合蛋白探究TLR4信号在溃疡性结肠炎中的关键作用[J]. 海军军医大学学报, 2024, 45(5): 535-543. |
| [25] |
李娜, 王磊, 柳越冬, 等. 优化溃结方对溃疡性结肠炎大鼠结肠Toll样受体/髓样分化因子88/核转录因子κB信号通路的影响[J]. 河北中医, 2024, 46(6): 953-958. |
| [26] |
蔡楚泉, 李忆岚, 陈卓, 等. 溃结汤灌肠治疗对湿热夹瘀型溃疡性结肠炎患者肠黏膜屏障功能和外周血单核细胞TLR4/NF-κB信号通路的影响[J]. 现代生物医学进展, 2024, 24(3): 596-600. |
| [27] |
LIU W X, LI Y, WU Z Z, et al. Heparin alleviates LPS-induced endothelial injury by regulating the TLR4/MyD88 signaling pathway[J]. Experimental and Therapeutic Medicine, 2021, 22(6): 1397. |
| [28] |
MOHANY M, AHMED M M, AL-REJAIE S S. The role of NF-κB and bax/bcl-2/caspase-3 signaling pathways in the protective effects of sacubitril/valsartan(entresto) against HFD/STZ-induced diabetic kidney disease[J]. Biomedicines, 2022, 10(11): 2863. |
 2025, Vol. 42
2025, Vol. 42