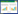文章信息
- 范立荣, 李松林, 李函舟, 等.
- FAN Lirong, LI Songlin, LI Hanzhou, et al.
- 基于Nrf2/HO-1信号通路探讨三黄益肾胶囊对糖尿病肾病大鼠氧化应激的影响
- Effect of Sanhuang Yishen Capsule on oxidative stress in rats with diabetic nephropathy based on Nrf2/HO-1 signaling pathway
- 天津中医药, 2025, 42(3): 381-386
- Tianjin Journal of Traditional Chinese Medicine, 2025, 42(3): 381-386
- http://dx.doi.org/10.11656/j.issn.1672-1519.2025.03.17
-
文章历史
- 收稿日期: 2024-10-07
2. 河北省沧州中西医结合医院, 沧州 061000;
3. 天津中医药大学中西医结合学院, 天津 301617
糖尿病肾病(DKD)是糖尿病最常见的微血管并发症之一, 其发病率逐年上升, 在全球范围内, DKD的病死率高于其他类型的慢性肾脏病, 同时DKD是终末期肾衰竭(ESRD)的主要诱因, 严重危害患者的生命健康[1]。目前, 中国针对DKD的治疗主要从控制血糖、血压以及调节血脂等几个方面着手[2]。美国糖尿病协会强调了营养、降糖药物的选择以及对心血管疾病和血压的管理的重要性, 但相关药物的应用存在一定的不良反应, 如胰高糖素样肽-1受体激动剂的应用可能会导致胃肠道不良事件、低血糖、注射部位反应、胰腺炎、肿瘤及胆囊疾病的发生[3], 恩格列净、卡格列净能够促进尿糖的排出, 但会增加尿路感染、急性肾损伤, 甚至骨折及坏疽等不良事件的风险[4]。因此, 寻找新的治疗药物并探索相关机制研究刻不容缓。
DKD作为一种由长期高血糖引起的慢性肾脏疾病, 氧化应激和慢性炎症反应是推动DKD进展的关键环节[5]。核因子红系2相关因子2(Nrf2)是内源性抗氧化系统中最重要的信号传导分子, 在机体维持氧化还原稳态中发挥重要作用, 可激活多种抗氧化酶基因的表达[6]。Nrf2的下游蛋白血红素氧合酶1(HO-1)能催化血红素降解, 降解产物胆绿素是重要的抗氧化酶, 因而Nrf2/HO-1信号通路表现出抗氧化能力。研究发现, 通过调控Nrf2及其下游HO-1基因及蛋白表达, 能够显著改善DKD氧化应激水平和相关炎症反应, 从而减轻DKD肾损伤[7-8]。三黄益肾胶囊(SHYS)是本院应用多年的院内制剂, 具有益气养阴、健脾补肾、活血化瘀的功效, 对糖尿病及其并发症DKD的临床疗效显著, 但作用机制尚不明确。本研究通过高脂饲料联合STZ注射建立DKD大鼠, 观察SHYS对DKD大鼠的氧化应激水平及Nrf2/HO-1信号通路的影响。
1 材料与方法 1.1 材料 1.1.1 动物40只8周龄, 体质量为(200±20)g的SPF级雄性SD大鼠, 购自北京华阜康生物科技股份有限公司(货号: SCXK(京)2021-0031)。饲养环境保持在25℃, 相对湿度为50%~70%, 正常昼夜。河北省沧州中西医结合医院伦理委员会批准(CZX2022-KY-023)。
1.1.2 药物SHYS购自河北省沧州中西医结合医院(批号Z20050795)。厄贝沙坦购自浙江华海药业股份有限公司, 国药准字H20030016。
1.1.3 试剂高脂饮食(HFD)购于北京斯贝福生物技术有限公司。链脲佐菌素(STZ)(批号: S8050), BCA蛋白检测试剂盒(批号: PC0020), 购于Solarbio生物技术有限公司, 肌酐(Cr)、尿素氮(BUN)、尿蛋白、超氧化物歧化酶(SOD)、丙二醛(MDA)、谷胱甘肽过氧化物酶(GSH-PX)检测试剂盒(批号: C011-2-1, C013-2-1, C035-2-1, A001-3-2, A003-1-2, A005-1-2)购于南京建成生物工程研究所; 大鼠白细胞介素(IL)-6酶联免疫吸附实验测定(ELISA)试剂盒(联科生物技术股份有限公司, 批号: EK306), IL-1βELISA试剂盒(联科生物技术股份有限公司, 批号: EK301B)及肿瘤坏死因子-α(TNF-α)ELISA试剂盒(联科生物技术股份有限公司, 批号: EK382), RNA提取、cDKDA反转录、扩增试剂盒(批号分别为: DP419、KR106-02、FP205-02), 购于天根生物科技有限公司。
1.2 方法 1.2.1 分组与模型制备喂养1周后, 大鼠随机分为正常组(8只)进行常规饲养, 造模组(32只)予高糖高脂饲料。造模组于第7周末进行腹腔注射STZ 30 mg/kg, 注射前12 h禁食不禁水。以3 d后尾静脉采血为检测指标, 随机血糖≥ 16.7 mmol/L, 视为糖尿病大鼠模型成功。继续喂养7 d, 当24 h UTP> 30 mg/24 h, 证明DKD模型成功。
1.2.2 给药方法造模的大鼠随机分为4组, 分别是模型组、厄贝沙坦组、SHYS低、高剂量组, 各8只。按照人-大鼠体表面积进行换算(1:6.25)后, SHYS低(0.81 g/kg)、高(1.62 g/kg)剂量组, 阳性药组给予厄贝沙坦(30 mg/kg)进行灌胃, 正常组、模型组予等体积蒸馏水, 连续4周, 标准饮食。
1.2.3 检测指标与方法 1.2.3.1 生化指标检测在造模成功后的第1、2、4、6、8周, 每周称量大鼠体质量, 并于固定时间测量大鼠尾静脉血糖, 记录空腹血糖(FBG)值。第8周收集24 h尿液检测尿蛋白含量。最后对大鼠麻醉处死, 腹主动脉取血, 检测Cr、BUN水平。
1.2.3.2 肾组织病理学染色肾脏摘取后, 使用10%的福尔马林溶液对肾脏组织进行固定处理, 随后进行石蜡包埋并切片。切片分别进行苏木精-伊红(HE)染色、Masson染色以及天狼星红染色, 最后在光学显微镜下观察大鼠肾组织的病理改变情况。
1.2.3.3 氧化应激及炎症反应相关指标检测应用试剂盒检测造模给药后各组大鼠肾组织中SOD、MDA、GSH-PX水平。
1.2.3.4 Nrf2/HO-1信号通路关键因子检测采用定量聚合酶链反应(qPCR)法对肾组织中Nrf2、HO-1 mRNA表达水平进行检测。分别在大鼠肾组织中取100 mg, 提取总RNA, 逆转录合成cDKDA; 以β-actin为内参, 进行qPCR分析。反应扩增条件为95℃ 30 s, 95℃ 15 s, 60℃ 60 s, 循环40次。引物序列见表 1。
采用蛋白免疫印迹(Western blot)法, 对肾组织中Nrf2/HO-1信号通路关键因子Nrf2、HO-1蛋白水平进行检测。将大鼠肾脏组织中加入RIPA裂解液, 进行匀浆后离心处理, 以提取总蛋白并测定其浓度。随后, 将蛋白进行分离, 并转印至PVDF膜上。使用5%脱脂奶粉在4℃条件下封闭过夜, 次日取出膜后, 加入一抗(稀释比为1:1 000), 在室温下孵育2 h。洗膜后, 再加入二抗(稀释比为1:5 000), 同样在室温下孵育2 h。之后, 用TTBS洗膜, 并采用ECL化学发光法进行显影检测。扫描电泳条带图像, 选取β-actin作为内参来检测蛋白表达情况。最后, 应用Image J软件计算各条带的平均光密度值。
1.3 统计学方法使用统计学软件SPSS 29.0分析实验数据。对于符合正态分布的计量资料, 采用t检验进行分析, 结果以均数±标准差(x±s)的形式表示; 两组之间的比较也采用t检验, P < 0.05为差异具有统计学意义。
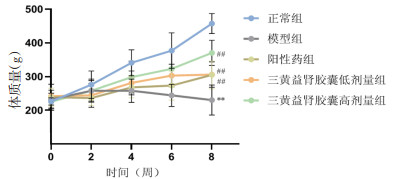
2 结果 2.1 SHYS对DKD大鼠体质量、FBG的影响给药结束后, 随着时间推移模型组体质量下降, 各干预组大鼠体质量增加。结果见图 1。
|
| 注:与正常组比较,**P<0.01;与模型组比较,##P<0.01。 图 1 SHYS对DKD大鼠体质量的影响 Fig. 1 Effect of Sanhuang Yishen Capsules on body weight of DKD rats |
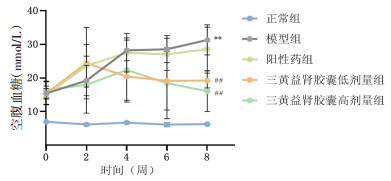
SHYS干预4周后, SHYS低、高剂量组大鼠FBG显著降低。结果见图 2。
|
| 注:与正常组比较,**P<0.01;与模型组比较,##P<0.01。 图 2 SHYS对DKD大鼠FBG的影响 Fig. 2 The effect of Sanhuang Yishen Capsules on FBG in DKD rats |
结果显示, 模型组大鼠血清中Cr、BUN水平以及24 h UTP水平升高, 厄贝沙坦及高剂量SHYS可降低DKD大鼠血清Cr、BUN水平以及24 h UTP水平。结果见表 2。
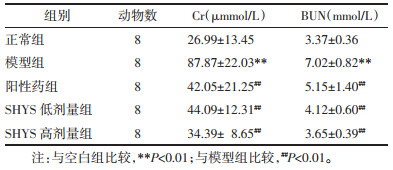
|
HE染色结果显示, 正常组肾小球内皮细胞扁平且紧密排列; 肾小管结构正常, 基底膜细线均匀。模型组中, 肾小球与肾小管均现脂肪变性, 肾小管局灶性变性萎缩, 肾小球基底膜稍增厚且系膜增生。各给药组缓解程度不一, 厄贝沙坦组与SHYS高剂量组效果更显。Masson染色见, 正常组大鼠肾小球、肾小管结构无异常; 模型组大鼠肾小管扩张, 肾小球系膜区及基底膜胶原增生明显。SHYS干预后, DKD大鼠肾小球及小管间质胶原沉积显著减少。天狼星红染色表明, 模型组肾脏间质、血管壁胶原沉积, 肾小球细动脉管壁变厚, SHYS组病变较轻。结果见图 3。
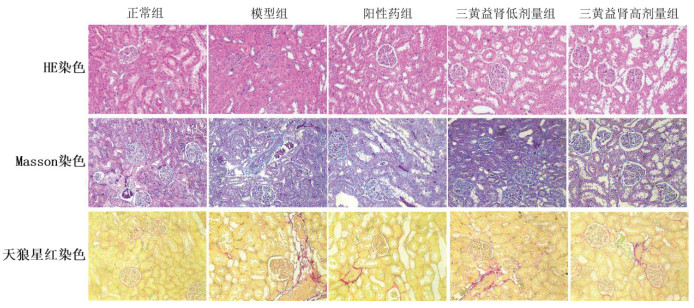
|
| 图 3 SHYS对DKD大鼠肾组织病理表现的影响(×100) Fig. 3 The effect of Sanhuang Yishen Capsules on the pathological manifestations of kidney tissue in DKD rats(×100) |
通过检测各组大鼠肾组织匀浆中SOD、MDA及GSH-PX水平, 进行评估。模型组大鼠肾组织匀浆中SOD及GSH-PX活性显著降低, MDA水平显著增高; 各干预组均可显著提高DKD大鼠肾组织匀浆中SOD及GSH-PX活性, 降低MDA水平。结果见表 3。
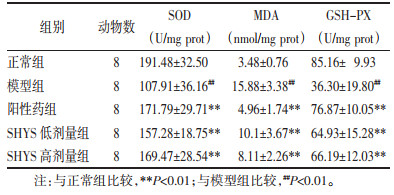
|
ELISA结果显示, 模型组大鼠血清中促炎因子IL-6、IL-1β及TNF-α水平升高; 厄贝沙坦及SHYS干预可降低DKD大鼠血清中IL-6、IL-1β及TNF-α水平。结果见图 4。
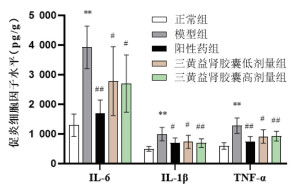
|
| 注:与正常组比较,**P<0.01;与模型组比较,#P<0.05,##P<0.01。 图 4 SHYS对DKD大鼠IL-6、IL-1β及TNF-α水平的影响 Fig. 4 The effect of Sanhuang Yishen Capsules on IL-6, IL-1 β, and TNF - α levels in DKD rats |
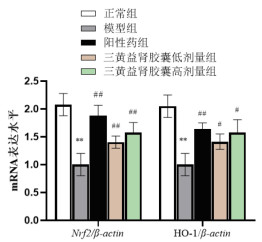
qPCR结果表明, 模型组肾组织中Nrf2与HO-1mRNA表达均显著上调; 阳性药组、SHYS低、高剂量组肾组织中Nrf2与HO-1 mRNA表达水平均显著上调(P < 0.01或P < .05)。结果见图 5。
|
| 注:与正常组比较,**P<0.01;与模型组比较,#P<0.05,##P<0.01。 图 5 SHYS对DKD大鼠mRNA表达水平的影响 Fig. 5 The effect of Sanhuang Yishen Capsules on mRNA expression levels in DKD rats |
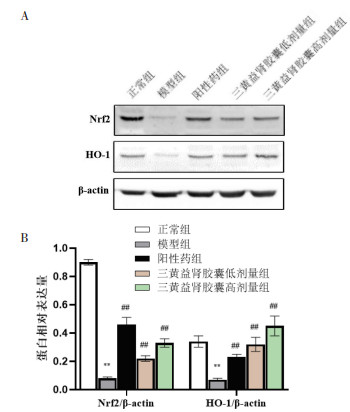
Western blot检测显示, 相较于正常组, 模型组肾脏中的Nrf2和HO-1蛋白表达量均明显降低(P < 0.01);而阳性药组、SHYS的低剂量及高剂量组, 其肾脏中Nrf2和HO-1蛋白的表达量则显著提升(P < 0.01), 其中以高剂量组更为明显。结果见图 6。
|
| 注:图A,Nrf2、HO-1Westernblot结果图片;图B,Nrf2、HO-1Westernblot灰度值量化分析结果。与正常组比较,**P<0.01;与模型组比较,##P<0.01。 图 6 Nrf2与HO-1蛋白相对表达量 Fig. 6 Relative expression levels of Nrf2 and HO-1 proteins |
DKD属于西医学病名, 中医古籍中无确切的记载, 根据临床表现可将其归属为"水肿""尿浊"范畴, 病位在肾, 与脾相关, 病机为消渴日久伤及脾肾所致, 脾的运化失常, 肾的气化失司, 水液代谢失常、精微渗漏于下则为尿浊, 病久发为消渴肾病。脾运化水液, 以肾气蒸化及肾阳温煦为依托; 肾主水液输布代谢的同时, 又依赖于脾气和脾阳的协助, 因此, 脾肾亏虚为DKD发病的核心病机。SHYS在DKD的临床治疗中取得了良好的疗效, 但其机制不明。本研究使用高脂饲料联合STZ注射建立DKD模型大鼠, 模型组出现血糖水平≥ 16.7mmol/L, 24 h UTP>30 mg/24 h, 肾小管呈现局部变性及萎缩现象, 肾小球基底膜有轻微增厚, 同时系膜细胞出现增生, 即视为造模成功。经SHYS治疗后, DKD模型大鼠的血清Cr、BUN浓度及24 h尿总蛋白含量均有所下降, 肾脏病理改变明显好转。
有研究表明, 在DKD的发生发展过程中, 炎症反应是一个关键环节[9-10]。长期高血糖状态能够诱发机体出现慢性炎症[11], 促使免疫细胞, 如巨噬细胞、T淋巴细胞在肾组织中浸润, 生成大量促炎因子, 如IL-1β, IL-6和TNF-α等[12], 进一步加剧DKD的发生发展[13]。分泌的促炎因子会进一步损害肾小球系膜细胞以及肾间质加重蛋白尿产生, 甚至促成肾纤维化[14]。在本研究中, SHYS干预后降低DKD大鼠血清中炎症因子IL-1β、TNF-α以IL-6及水平, 证实其具有减轻炎症反应的作用。此外, 持续性高血糖状态会诱发活性氧(ROS)的过度产生, 导致氧化应激反应, 进而引起一系列代谢紊乱, 如脂质过氧化等[15]。MDA作为脂质过氧化的最终产物, 与生物体的氧化应激反应呈现出正相关性, 细胞的损伤程度可由其表达水平反映[16]。SOD和GSH-PX是抗氧化系统的关键酶, 在氧化应激反应中发挥重要作用, 具有减轻DKD肾脏氧化应激损伤的作用[17-18]。在本研究中, SHYS干预后, DKD大鼠肾组织SOD和GSH-PX活性升高、MDA水平降低, 表明其能够减轻肾脏氧化应激水平。
Nrf2/HO-1信号通路是抗氧化应激反应的重要信号通路[19]。Nrf2是一种在生理状态下处于低转录水平的转录因子, 其活性依赖于keap1的调节。在氧化应激条件下, Nrf2从细胞质转移至细胞核中, 通过调节抗氧化反应元件(ARE)介导的抗氧化蛋白和Ⅱ相解毒酶的表达, 从而上调血红素降解过程中HO-1等内源性抗氧化剂的表达[20]。HO-1是一种重要的抗氧化酶, 能够通过催化血红素降解生成一氧化碳、胆绿素、亚铁离子, 发挥抗氧化作用。在本研究中, 实施SHYS干预措施后, 提升了DKD大鼠肾脏内Nrf2和HO-1基因及其蛋白质的表达量, 证实SHYS能够激活Nrf2/HO-1信号通路, 增加肾组织中SOD和GSH-PX水平, 同时降低MDA水平, 抑制肾脏中氧化应激, 减轻促炎因子(IL-6、IL-1β以及TNF-α)的释放从而缓解DKD大鼠肾损伤。
综上所述, SHYS能够有效改善DKD大鼠体质量下降、FBG升高、肾功能损伤及肾组织的病理变化, 尤以SHYS高剂量组最为明显, 其机制可能与激活Nrf2/HO-1信号通路改善肾脏氧化应激损伤和降低促炎因子释放有关。
| [1] |
LI X J, SUO P, WANG Y N, et al. Arachidonic acid metabolism as a therapeutic target in AKI-to-CKD transition[J]. Frontiers in Pharmacology, 2024, 15: 1365802. DOI:10.3389/fphar.2024.1365802 |
| [2] |
中华中医药学会, 北京中医药大学东直门医院, 北京中医药大学. 糖尿病肾脏疾病中西医结合诊疗指南[J]. 北京中医药大学学报, 2024, 47(4): 580-592. |
| [3] |
SODHI M, REZAEIANZADEH R, KEZOUH A, et al. Risk of gastrointestinal adverse events associated with glucagon-like peptide-1 receptor agonists for weight loss[J]. JAMA, 2023, 330(18): 1795-1797. DOI:10.1001/jama.2023.19574 |
| [4] |
SABANCI R, SAAED M, BANDI A, et al. Beyond the benefits: A case study on the complications of sodium-glucose co-transporter-2(SGLT2) inhibitors(euglycemic diabetic ketoacidosis(DKA) and takotsubo cardiomyopathy)[J]. Cureus, 2024, 16(2): e55068. |
| [5] |
LI J L, LI L X, ZHANG Z, et al. Ferroptosis: An important player in the inflammatory response in diabetic nephropathy[J]. Frontiers in Immunology, 2023, 14: 1294317. DOI:10.3389/fimmu.2023.1294317 |
| [6] |
MTHEMBU S X H, MAZIBUKO-MBEJE S E, MOETLEDIWA M T, et al. Sulforaphane: A nutraceutical against diabetes-related complications[J]. Pharmacological Research, 2023, 196: 106918. DOI:10.1016/j.phrs.2023.106918 |
| [7] |
ALA M. Sestrin2 signaling pathway regulates podocyte biology and protects against diabetic nephropathy[J]. Journal of Diabetes Research, 2023, 2023: 8776878. |
| [8] |
JIN T, CHEN C. Umbelliferone delays the progression of diabetic nephropathy by inhibiting ferroptosis through activation of the Nrf-2/HO-1 pathway[J]. Food and Chemical Toxicology, 2022, 163: 112892. DOI:10.1016/j.fct.2022.112892 |
| [9] |
YANG M, ZHANG C. The role of innate immunity in diabetic nephropathy and their therapeutic consequences[J]. Journal of Phar- maceutical Analysis, 2024, 14(1): 39-51. DOI:10.1016/j.jpha.2023.09.003 |
| [10] |
CHEN J H, LIU Q H, HE J H, et al. Immune responses in diabetic nephropathy: Pathogenic mechanisms and therapeutic target[J]. Frontiers in Immunology, 2022, 13: 958790. DOI:10.3389/fimmu.2022.958790 |
| [11] |
YANG J, LIU Z S. Mechanistic pathogenesis of endothelial dysfunction in diabetic nephropathy and retinopathy[J]. Frontiers in Endocrinology, 2022, 13: 816400. DOI:10.3389/fendo.2022.816400 |
| [12] |
WANG Y H, LIU J X, WANG H G, et al. Mesenchymal stem cell-derived exosomes ameliorate diabetic kidney disease through the NLRP3 signaling pathway[J]. Stem Cells, 2023, 41(4): 368-383. DOI:10.1093/stmcls/sxad010 |
| [13] |
BAI Y, LI H, DONG J. Up-regulation of miR-20a weakens inflammation and apoptosis in high-glucose-induced renal tubular cell mediating diabetic kidney disease by repressing CXCL8 expression[J]. Archives of Physiology and Biochemistry, 2022, 128(6): 1603-1610. DOI:10.1080/13813455.2020.1785506 |
| [14] |
ZHANG Q L, LIU X C, SULLIVAN M A, et al. Protective effect of yi Shen Pai du formula against diabetic kidney injury via inhibition of oxidative stress, inflammation, and epithelial-to-mesenchymal transition in db/db mice[J]. Oxidative Medicine and Cellular Longevity, 2021, 2021: 7958021. DOI:10.1155/2021/7958021 |
| [15] |
MASENGA S K, KABWE L S, CHAKULYA M, et al. Mechanisms of oxidative stress in metabolic syndrome[J]. International Journal of Molecular Sciences, 2023, 24(9): 7898. DOI:10.3390/ijms24097898 |
| [16] |
HUANG Q, OUYANG D S, LIU Q. Isoeucommin A attenuates kidney injury in diabetic nephropathy through the Nrf2/HO-1 pathway[J]. FEBS Open Bio, 2021, 11(8): 2350-2363. DOI:10.1002/2211-5463.13251 |
| [17] |
LI Y C, GUO S, YANG F, et al. Huayu Tongluo Recipe attenuates renal oxidative stress and inflammation through the activation of AMPK/Nrf2 signaling pathway in streptozotocin-(STZ-) induced diabetic rats[J]. Evidence-Based Complementary and Alternative Medicine, 2021, 2021: 5873007. |
| [18] |
FENG X M, WANG S, SUN Z C, et al. Ferroptosis enhanced diabetic renal tubular injury via HIF-1α/HO-1 pathway in db/db mice[J]. Frontiers in Endocrinology, 2021, 12: 626390. DOI:10.3389/fendo.2021.626390 |
| [19] |
DANG R Z, WANG M Y, LI X H, et al. Edaravone ameliorates depressive and anxiety-like behaviors via Sirt1/Nrf2/HO-1/Gpx4 pathway[J]. Journal of Neuroinflammation, 2022, 19(1): 41. DOI:10.1186/s12974-022-02400-6 |
| [20] |
RADWAN S M, ALQULALY M, ELSAEED M Y, et al. L-carnitine reverses methotrexate-induced nephrotoxicity in experimental rat model: Insight on SIRT1/PGC-1α/Nrf2/HO-1 axis[J]. Journal of Applied Toxicology, 2023, 43(11): 1667-1675. DOI:10.1002/jat.4503 |
2. Cangzhou Hospital of Combined Traditional Chinese and Western Medicine, Cangzhou 061000, China;
3. College of Integrative Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
 2025, Vol. 42
2025, Vol. 42