文章信息
- 陈世川, 贾福运, 徐强.
- CHEN Shichuan, JIA Fuyun, XU Qiang.
- 中医药通过增加GPX4的表达抑制铁死亡防治慢性心力衰竭研究进展
- Research progress on preventing and treating chronic heart failure by increasing the expression of GPX4 and inhibiting ferroptosis by traditional Chinese medicine
- 天津中医药, 2025, 42(3): 397-403
- Tianjin Journal of Traditional Chinese Medicine, 2025, 42(3): 397-403
- http://dx.doi.org/10.11656/j.issn.1672-1519.2025.03.19
-
文章历史
- 收稿日期: 2024-06-12
慢性心力衰竭(CHF)是由多种原因导致心脏结构和功能异常改变,使心室收缩和(或)舒张功能发生障碍引起的一组复杂临床综合征,是各类心脏疾病发生发展的终末期阶段,全球有超过6 400万人受到心力衰竭影响,其发病机制极为复杂,包括心肌结构和功能异常、炎症反应的激活等多种因素[1]。随着人口老龄化问题的不断加剧,CHF的患病率、病死率和住院率居高不下,且呈现上升趋势,逐渐成为一个重要的临床和公共卫生问题,为全球医疗保健系统带来巨大负担[2-3]。
铁死亡的概念最早于2012年由Dixon等[4]首先提出,与细胞凋亡、坏死、自噬和其他类型的细胞死亡不同,其特征是脂质过氧化物的积累和氧化还原失衡,最终导致细胞膜破裂而死亡[5-6]。而且经历铁死亡的细胞会出现线粒体萎缩、外膜破裂、线粒体嵴的减少或消失,而细胞核大小无明显变化等形态学特征[7-8]。种种迹象表明,铁死亡是一种铁依赖性调节细胞死亡新形式[9-10]。目前,已知参与铁死亡的调控途径包括铁代谢、线粒体活性以及氨基酸、脂质和糖代谢等[5]。谷胱甘肽过氧化物酶4(GPX4)是一种重要的细胞内调节因子,在维持体内氧化还原稳态方面发挥重要作用[11]。研究表明,GPX4与铁死亡密切相关,是该过程的关键拮抗剂,通过上调GPX4的表达可以有效抑制细胞铁死亡进程[12]。诸多研究及临床实践表明,中医药治疗CHF确有疗效,本研究旨在探究GPX4、铁死亡与CHF之间的关系,并对中医药通过增加GPX4的表达抑制铁死亡防治CHF进行综述,以期为中医药治疗CHF提供新思路。
1 GPX4、铁死亡和CHF的相关性分析 1.1 GPX4是铁死亡的关键拮抗剂铁死亡是由细胞内氧化还原失衡引起、由多种氧化还原酶的异常表达驱动的,能够使细胞抗氧化系统失活,该过程会使细胞内脂质过氧化物积累,与细胞内游离的铁离子发生芬顿反应,产生大量活性氧(ROS),细胞内过量的ROS会增强细胞氧化应激,导致蛋白质、DNA和脂质等细胞成分的损伤,最终导致细胞死亡[13]。谷胱甘肽(GSH)是一种存在于哺乳动物组织中的三肽,是人体含量最丰富的抗氧化剂,大部分分布在细胞质中,小部分分布在线粒体和内质网中,GSH是GPX4的关键底物,GPX4主要是利用GSH作为辅助因子来抵抗脂质过氧化[13-14]。GPX4是一种单体谷胱甘肽过氧化物酶,具有催化脂质过氧化物的还原作用,GPX4在铁死亡进程中扮演重要角色,其介导的GSH代谢途径是对抗铁死亡的重要防御机制,其可以将细胞内的脂质过氧化物通过还原反应转换成无毒的脂质醇,从而抑制脂质过氧化,保护细胞和组织免受自由基的损伤,而铁死亡的特征正是脂质氢过氧化物的增加,所以GPX4是细胞避免发生铁死亡进程的重要保护剂[12]。相反,GPX4的缺失或功能障碍可以导致细胞内过氧化物的积累,诱导细胞铁死亡发生,引起细胞死亡[15-16],早在2014年,Friedmann等[17]的研究中发现,通过破坏小鼠体内的GPX4,直接诱导了细胞铁死亡,引发小鼠急性肾功能衰竭而死亡,GPX4对铁死亡的影响就已经得到初步印证。
随着研究的不断深入,已经证实作为抗氧化系统关键成分的GSH/GPX4轴在防止脂质过氧化介导的铁死亡中可能起着关键作用,而GPX4正是铁死亡进程的关键拮抗剂[18]。
1.2 铁死亡是CHF发生发展的关键环节目前的研究表明,CHF的病理生理学涉及到炎症、细胞死亡、活性氧产生增加、能量代谢受损、线粒体功能障碍、自噬障碍等过程[19],铁死亡正是CHF的病理生理机制中不可缺少的关键环节[20-21]。早在2018年,Liu等[22]在实验中得出结论,以细胞铁含量增加和相关脂质过氧化物积累为特征的铁死亡,能够催化心肌细胞氧化应激,可能是心功能不全期间细胞死亡的潜在机制,提示铁死亡和CHF有密切关系。为进一步探究其机制,Fang等[23]实验证明,在铁蛋白H缺乏型心肌细胞中过表达溶质载体家族7成员11(SLC7A11)可以恢复GSH水平,从而抑制铁死亡,减轻心肌纤维化和心脏肥大,并显著降低CHF相关基因的表达。随着研究的不断深入,Li等[24]从实验中发现,心力衰竭小鼠心肌细胞的PGAM5 mRNA表达水平受到抑制,且进一步证实PGAM5抑制了心力衰竭中Keap1/Nrf2信号通路对ROS诱导的心肌细胞氧化应激和铁死亡,揭示了铁死亡的相关机制。同时Chen等[25]实验也可证明,心肌细胞氧化应激及铁死亡与心力衰竭密切相关。随后,Xiong等[26]通过生物信息学和实验证明,通过抑制射血分数保留型心力衰竭(HFpEF)小鼠心肌组织的铁死亡,能够显著改善HFpEF小鼠心脏舒张功能障碍和肺充血等HFpEF相关表型,进一步证实了铁死亡对小鼠心肌组织的影响。由此可见,铁死亡可以直接或间接影响CHF的发生发展,故探求两者之间的关系和机制研究具有重要临床意义。
1.3 GPX4是防治CHF的新方向心肌细胞铁死亡会加快CHF进展,GPX4是铁死亡进程中的一个重要调节因子,通过影响GPX4的表达,可以有效抑制心肌细胞铁死亡,进而达到防治慢性心力衰竭的目的。Zhuang等[27]发现,miR-375-3p拮抗剂促进了心脏成纤维细胞的抗氧化能力,增加了GPX4的表达,减少了GPX4介导的铁死亡过程,防止心肌纤维化,延缓了心力衰竭进程。Yang等[16]发现血管紧张素Ⅳ可以增加心肌细胞内GPX4的表达进而抑制心肌细胞铁死亡,改善阿霉素诱导的心脏毒性,减少了心肌损伤,延缓心力衰竭进展。由此可见,GPX4作为铁死亡的重要调节因子,可能是治疗CHF的新方向。
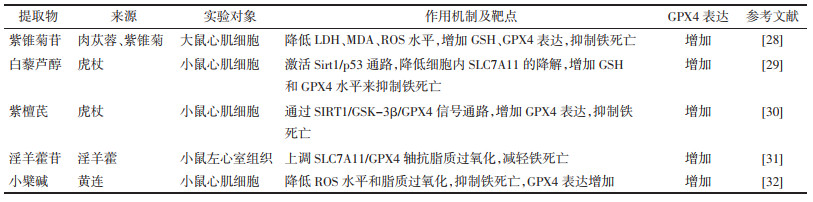
2 中医药通过增加GPX4表达抑制铁死亡防治心力衰竭 2.1 中药提取物紫锥菊苷(ECH)是一种源自天然草本肉苁蓉和紫锥菊的化合物,对防治心力衰竭具有重要作用。Ma等[28]从体内、体外实验观察到,ECH显著降低了阿霉素诱导的CHF模型大鼠血清内乳酸脱氢酶(LDH)、丙二醛(MDA)以及B型钠脑肽(BNP)水平,降低了脂质活性氧(ROS)水平,增加了GSH、GPX4的表达,且增加CHF大鼠的左心室射血分数。这些发现表明,ECH可以通过影响GPX4表达抑制铁死亡来减少阿霉素诱导的心脏损伤,显示了其治疗CHF的潜在价值。
白藜芦醇是一种非黄酮类多酚有机化合物,是中药虎杖的有效成分之一,具有抗氧化、抗炎、心血管保护等作用。Zhang等[29]将白藜芦醇作用于心力衰竭模型小鼠,发现其可以通过激活心力衰竭中Sirt1/p53通路,降低心肌细胞内SLC7A11的降解以及增加GSH和GPX4水平来抑制心肌细胞铁死亡,降低了心力衰竭小鼠血清内BNP水平并增加其左心室射血分数,改善了心力衰竭小鼠的心肌肥大及纤维化,改善心脏功能。
紫檀芪(PTS)是白藜芦醇的去甲基化衍生物,具有很强的抗炎和抗氧化活性。为进一步深入研究,Zhang等[30]通过实验证明,PTS通过SIRT1/GSK-3β/GPX4通路发挥其心脏保护作用,经PTS处理的血管紧张素Ⅱ诱导的心力衰竭模型小鼠心肌细胞能显著增加GPX4表达,降低ROS和脂质过氧化物水平。在体外实验中发现,经PTS处理的小鼠左心室射血分数、左心室缩短分数、心脏指数均显著增加,缓解心脏重塑。证明PTS可以通过抑制心肌细胞铁死亡,改善CHF小鼠心脏功能。
淫羊藿苷(ICA)是传统中药淫羊藿的主要成分之一,对治疗心肌缺血、心律失常等循环系统疾病具有潜在作用。唐文静等[31]最新研究表明,ICA可以通过上调SLC7A11/ GPX4轴抗脂质过氧化,提升GPX4表达,抑制铁死亡的发生,改善异丙肾上腺素(ISO)引起的小鼠左心室射血分数降低,减轻ISO所致的左心室组织病理损伤以及铁离子过度积累,延缓心力衰竭进程。
小檗碱(BBR)是中药黄连中分离出的一种生物碱,是黄连抗菌的有效成分。Yang等[32]通过实验证实了BBR可以通过减少心肌细胞中的脂质过氧化物来抑制心肌细胞铁死亡,从而保护心肌细胞免受损伤,预防心力衰竭的发生,其机制可能与减少细胞内ROS积累和增加GPX4表达有关。
综上,中药提取物通过增加GPX4表达抑制铁死亡防治心力衰竭列举见表 1。
|
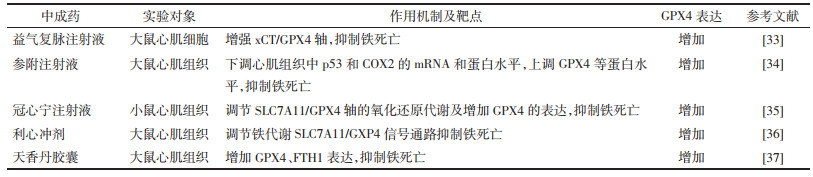
Guo等[33]通过实验发现,益气复脉注射液能够显著降低脓毒症诱发心肌损伤模型大鼠体内铁含量,降低脂质过氧化相关因子(ROS、MDA和4-HNE)水平,增强胱氨酸谷氨酸反向转运蛋白(xCT)/GPX4轴使GPX4的表达增加,进一步抑制心肌细胞铁死亡来减轻大鼠心肌损伤,同时能够显著降低大鼠血清内心肌损伤标志物(包括cTnI、CK-MB和LDH)水平,改善心功能,预防心力衰竭的发生。
王梓仪等[34]的研究结果表明,参附注射液可以下调ISO诱导的CHF模型大鼠心肌细胞中抑癌基因p53和环氧合酶2(COX2)的mRNA和蛋白水平,上调GPX4等蛋白水平,减少ROS的蓄积,参附注射液的干预显著提升了CHF大鼠左心室射血分数、左心室短轴缩短率,显著降低血清N端脑钠肽前体蛋白(NT-proBNP)水平,心功能明显好转,证明参附注射液可以通过抑制铁死亡改善CHF大鼠的氧化应激损伤,减缓CHF的发生发展。
冠心宁注射液的主要成分有丹参和川芎,具有活血化瘀、通脉养心的功效。Wang等[35]实验结果显示,冠心宁注射液能显著提升心力衰竭模型小鼠的心脏射血分数、心输出量、左心室容积,改善心功能,并降低血清NT-proBNP水平,减缓CHF进程,其作用机制与调节SLC7A11/GPX4轴的氧化还原代谢及增加GPX4的表达有关。
同样,於悦等[36]最新研究发现,经利心冲剂(黄芪30 g,黄精15 g,补骨脂12 g,葶苈子12 g,益母草30 g)处理的心力衰竭模型大鼠的心肌组织中GPX4表达明显升高,利心冲剂可通过调节铁代谢和SLC7A11/GXP4信号通路抑制心肌细胞铁死亡,减轻心肌氧化应激,且能减少肥大的心肌细胞数量,缓解心力衰竭大鼠心肌损伤。
天香丹胶囊在治疗冠心病、心绞痛、心肌损伤方面效果显著。岳远佳等[37]通过动物实验探讨其作用机制,观察到天香丹胶囊能够显著升高心肌缺血模型大鼠心肌细胞内GPX4的表达,降低心肌组织铁含量及氧化应激水平,减少心肌细胞铁死亡的发生,显著降低血清心肌损伤标志物CTnI水平,预防因心肌缺血损伤而导致的心力衰竭发生。
综上,中成药通过增加GPX4表达抑制铁死亡防治心力衰竭列举见表 2。
|
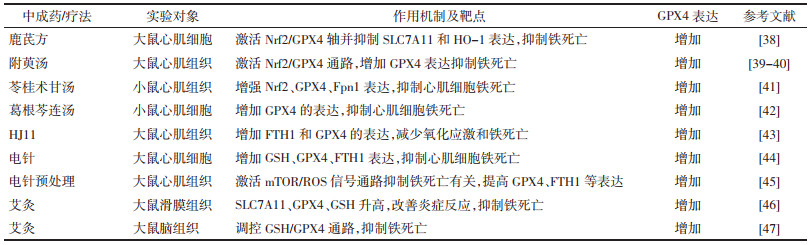
鹿芪方由著名中医专家周华教授创制,已投入临床使用数年,用于治疗心血管疾病。该方剂由鹿茸、黄芪、红花等成分组成,具有温补心气心阳、活血利水的功效。Cheng等[38]研究表明,鹿芪方能够激活心力衰竭模型小鼠心肌细胞Nrf2/GPX4信号转导轴,增加了GPX4的表达,通过抑制心肌细胞铁死亡减缓心力衰竭进展,同时还能减轻心肌肥厚和纤维化,改善心力衰竭症状。
附萸汤(山萸肉30 g,制附子9 g,炙甘草10 g)具有益气温阳、祛瘀通络的功效。之前研究发现附萸汤能够通过调控心肌细胞自噬、改善心肌梗死后心力衰竭大鼠心室重构[39]。王青青等[40]通过实验证实,附萸汤能够通过激活Nrf2/GPX4通路,使心力衰竭模型大鼠心肌组织Nrf2、SLC7A11和GPX4蛋白表达均显著升高,进而抑制心肌细胞铁死亡,同时能显著提高其左心室射血分数、左室舒末期内径等心功能指标,改善心力衰竭大鼠心肌纤维化。
苓桂术甘汤出自《金匮要略》,具有温阳化饮,健脾利湿之功效。Yang等[41]发现,苓桂术甘汤能够显著降低阿霉素诱导的心肌损伤模型小鼠体内MDA、LDH和CK水平,增强Nrf2、GPX4和铁转运蛋白(Fpn1)的蛋白表达,抑制心肌细胞铁死亡,改善心脏收缩功能,减缓心力衰竭发展进程。
葛根芩连汤是中医传统方剂,出自《伤寒论》,有解表清里之功效。余洁英等[42]发现,暴露于湿热环境后出现湿热综合征的小鼠会出现心肌肥厚和纤维化、心脏舒张功能减低等现象,湿热综合征可能会加重心肌细胞铁死亡,而葛根芩连汤可以增加GPX4的表达,减弱心肌细胞氧化应激,抑制心肌细胞铁死亡,有效改善小鼠心室重构和心脏舒张功能,延缓心力衰竭发展。
HJ11方是一种新型中药方剂,由清热剂四妙勇安汤加减而来,其成分尚处于保密阶段。Zhang等[43]在实验中发现,HJ11促进了心肌缺血再灌注损伤模型大鼠心肌组织中FTH1和GPX4的表达,减弱了心肌组织氧化应激和铁死亡,同时通过超声心动图监测HJ11可以显著改善其心室壁运动功能,且能够保护心肌细胞结构、避免炎症细胞浸润,避免了由心肌缺血再灌注损伤导致的心力衰竭。
2.4 中医特色疗法蒋志明等[44]将电针应用于心肌缺血损伤模型大鼠双侧“神门”“通里”穴,观察到电针治疗后的大鼠心肌组织中GSH、GPX4、FTH1的表达上升,心肌细胞排列、心肌纤维断裂情况有所改善,证明电针可以抑制心肌细胞铁死亡,改善心肌缺血损伤,有效防治CHF的发生发展。
Xiao等[45]同样通过实验证明,电针预处理对大鼠心肌缺血再灌注损伤具有保护作用,其机制可能涉及通过电针参与mTOR/ROS信号通路抑制铁死亡有关,该过程显著提高了GPX4、FTH1等物质的表达,抑制了心肌细胞铁死亡,减少了心肌损伤,同时显著提升大鼠左心室射血分数、左心室短轴缩短率,改善心功能,预防了CHF的发生。
彭传玉等[46]对类风湿性关节炎模型大鼠的“肾俞”“足三里”穴实施交替悬浮艾灸治疗,观察到艾灸组大鼠体内SLC7A11、GSH含量和GPX4表达均显著提高,认为艾灸可以改善炎症反应、调节铁死亡相关因子。Zhang等[47]的实验证明,艾灸可以通过减少脂质过氧化物的产生,促进GSH和GPX4的表达,减少活性氧的积累,抑制铁死亡,改善大鼠脑缺血再灌注损伤。虽然艾灸通过影响铁死亡进程防治CHF的研究尚有不足,但上述实验也可为今后的研究提供参考。
综上,中药复方及中医特色疗法通过增加GPX4表达抑制铁死亡防治心力衰竭列举见表 3。
|
中医学往往将心力衰竭归于“心痹”“喘证”“水肿”等相关范畴,其病位在心,与肝脾肺肾等脏腑密切相关,其病机归属本虚标实之证,本虚在于患者先天不足或患病日久,可见气血阴阳亏虚,脏腑功能失调、心失所养;标实在于饮瘀痰毒等实邪的积累,以瘀血阻滞、水饮内停最为多见[48]。其中医治法在于通过温补心阳、益气养阴、活血化瘀、利水消肿等,来改善心力衰竭症状。
铁死亡是一种新型铁依赖性细胞死亡形式,在心血管疾病的发生发展过程中扮演重要角色,其过程中涉及到的游离铁过量和有毒的脂质过氧化物沉积,与中医学中饮瘀痰毒等病理产物的积累有异曲同工之处,这种病理产物长期附着于心之血脉中,瘀滞在心,血脉不通,则出现胸闷、胸痛等症状;瘀血阻滞,水运受阻,则气喘、水肿、喘息不得卧。传统中医理论与心肌细胞铁死亡机制相结合的研究尚有不足,因此基于心力衰竭的病因病机分析,中医药通过抑制铁死亡来防治慢性心力衰竭,可能为临床提供新思路。
中医药防治CHF确有疗效,具有广阔研究和应用前景,较常规西医治疗有多成分、多靶点、多通路的优势,但也因其成分复杂,很多机制尚不明确,还需进一步研究和讨论。就目前的研究来看,对于中医药通过增加GPX4的表达抑制铁死亡防治CHF的研究尚处于初步阶段,还需要开展大量的基础研究及临床试验提供更多、更充分的理论依据。
| [1] |
DICK S A, EPELMAN S. Chronic heart failure and inflammation[J]. Circulation Research, 2016, 119(1): 159-176. DOI:10.1161/CIRCRESAHA.116.308030 |
| [2] |
ROGER V L. Epidemiology of heart failure: A contemporary perspective[J]. Circulation Research, 2021, 128(10): 1421-1434. DOI:10.1161/CIRCRESAHA.121.318172 |
| [3] |
SAVARESE G, BECHER P M, LUND L H, et al. Global burden of heart failure: A comprehensive and updated review of epidemiology[J]. Cardiovascular Research, 2022, 118(17): 3272-3287. |
| [4] |
DIXON S J, LEMBERG K M, LAMPRECHT M R, et al. Ferroptosis: An iron-dependent form of nonapoptotic cell death[J]. Cell, 2012, 149(5): 1060-1072. DOI:10.1016/j.cell.2012.03.042 |
| [5] |
JIANG X J, Brent R STOCKWELLB E, CONRAD M. Ferroptosis: Mechanisms, biology and role in disease[J]. Nature Reviews Molecular Cell Biology, 2021, 22(4): 266-282. DOI:10.1038/s41580-020-00324-8 |
| [6] |
XU X, XU X D, MA M Q, et al. The mechanisms of ferroptosis and its role in atherosclerosis[J]. Biomedicine & Pharmacotherapy, 2024, 171: 116112. |
| [7] |
ZHANG X, SUN J, WANG J, et al. The role of ferroptosis in diabetic cardiovascular diseases and the intervention of active ingredients of traditional Chinese medicine[J]. Frontiers in Pharmacology, 2023, 14: 1286718. DOI:10.3389/fphar.2023.1286718 |
| [8] |
CHEN X, COMISH P B, Tang D, et al. Characteristics and biomarkers of ferroptosis[J]. Frontiers in Cell and Developmental Biology, 2021, 9: 637162. DOI:10.3389/fcell.2021.637162 |
| [9] |
LIU J, KANG R, TANG D. Signaling pathways and defense mechanisms of ferroptosis[J]. The FEBS Journal, 2022, 289(22): 7038-7050. DOI:10.1111/febs.16059 |
| [10] |
KERKHOVE L, GEIRNAERT F, DUFAIT I, et al. Ferroptosis: Frenemy of radiotherapy[J]. International Journal of Molecular Sciences, 2024, 25(7): 3641. DOI:10.3390/ijms25073641 |
| [11] |
FORCINA G C, DIXON S J. GPX4 at the crossroads of lipid homeostasis and ferroptosis[J]. Proteomics, 2019, 19(18): e1800311. DOI:10.1002/pmic.201800311 |
| [12] |
ZHANG W, LIU Y, LIAO Y, et al. GPX4, ferroptosis, and diseases[J]. Biomedicine & Pharmacotherapy, 2024, 174: 116512. |
| [13] |
ZHANG X D, LIU Z Y, WANG M S, et al. Mechanisms and regulations of ferroptosis[J]. Frontiers in Immunology, 2023, 14: 1269451. DOI:10.3389/fimmu.2023.1269451 |
| [14] |
BERTERO E, MAACK C. Ins and outs of glutathione in cardiac ischemia/reperfusion injury[J]. Circulation Research, 2023, 133(10): 877-879. DOI:10.1161/CIRCRESAHA.123.323715 |
| [15] |
XIE Y, KANG R, KLIONSKY D J, et al. GPX4 in cell death, autophagy, and disease[J]. Autophagy, Taylor & Francis, 2023, 19(10): 2621. |
| [16] |
YANG L, GUAN J, LUO S, et al. Angiotensin Ⅳ ameliorates doxorubicin-induced cardiotoxicity by increasing glutathione peroxidase 4 and alleviating ferroptosis[J]. Toxicology and Applied Pharmacology, 2023, 479: 116713. DOI:10.1016/j.taap.2023.116713 |
| [17] |
FRIEDMANN A J P, SCHNEIDER M, PRONETH B, et al. Inactivation of the ferroptosis regulator Gpx4 triggers acute renal failure in mice[J]. Nature Cell Biology, 2014, 16(12): 1180-1191. DOI:10.1038/ncb3064 |
| [18] |
LI F J, LONG H Z, ZHOU Z W, et al. System Xc-/GSH/GPX4 axis: An important antioxidant system for the ferroptosis in drug-resistant solid tumor therapy[J]. Frontiers in Pharmacology, 2022, 13: 910292. DOI:10.3389/fphar.2022.910292 |
| [19] |
FANG W, XIE S, DENG W. Ferroptosis mechanisms and regulations in cardiovascular diseases in the past, present, and future[J]. Cell Biology and Toxicology, 2024, 40(1): 17. DOI:10.1007/s10565-024-09853-w |
| [20] |
YANG L, CAI X, LI R. Ferroptosis induced by pollutants: an emerging mechanism in environmental toxicology[J]. Environmental Science & Technology, 2024, 58(5): 2166-2184. |
| [21] |
LV C, ZHOU L, MENG Y, et al. PKD knockdown mitigates Ang Ⅱ-induced cardiac hypertrophy and ferroptosis via the JNK/P53 signaling pathway[J]. Cellular Signalling, 2024, 113: 110974. DOI:10.1016/j.cellsig.2023.110974 |
| [22] |
LIU B, ZHAO C, LI H, et al. Puerarin protects against heart failure induced by pressure overload through mitigation of ferroptosis[J]. Biochemical and Biophysical Research Communications, 2018, 497(1): 233-240. DOI:10.1016/j.bbrc.2018.02.061 |
| [23] |
FANG X, CAI Z, WANG H, et al. Loss of cardiac ferritin H facilitates cardiomyopathy via Slc7a11-mediated ferroptosis[J]. Circulation Research, 2020, 127(4): 486-501. DOI:10.1161/CIRCRESAHA.120.316509 |
| [24] |
LI S, WEN P, ZHANG D, et al. PGAM5 expression levels in heart failure and protection ROS-induced oxidative stress and ferroptosis by Keap1/Nrf2[J]. Clinical and Experimental Hypertension, 2023, 45(1): 2162537. DOI:10.1080/10641963.2022.2162537 |
| [25] |
CHEN Y, GUO X, ZENG Y, et al. Oxidative stress induces mitochondrial iron overload and ferroptotic cell death[J]. Scientific Reports, 2023, 13(1): 15515. DOI:10.1038/s41598-023-42760-4 |
| [26] |
XIONG Y, LIU X, JIANG L, et al. Inhibition of ferroptosis reverses heart failure with preserved ejection fraction in mice[J]. Journal of Translational Medicine, 2024, 22(1): 199. DOI:10.1186/s12967-023-04734-y |
| [27] |
ZHUANG Y, YANG D, SHI S, et al. MiR-375-3p promotes cardiac fibrosis by regulating the ferroptosis mediated by GPX4[J]. Computational Intelligence and Neuroscience, 2022, 2022: 9629158. |
| [28] |
MA Y, YANG X, JIANG N, et al. Echinacoside ameliorates doxorubicin-induced cardiac injury by regulating GPX4 inhibition-induced ferroptosis[J]. Experimental and Therapeutic Medicine, 2023, 27(1): 29. DOI:10.3892/etm.2023.12317 |
| [29] |
ZHANG W, QIAN S, TANG B, et al. Resveratrol inhibits ferroptosis and decelerates heart failure progression via Sirt1/p53 pathway activation[J]. Journal of Cellular and Molecular Medicine, 2023, 27(20): 3075-3089. DOI:10.1111/jcmm.17874 |
| [30] |
ZHANG F, ZENG Z, ZHANG J, et al. Pterostilbene attenuates heart failure by inhibiting myocardial ferroptosis through SIRT1/GSK-3β/GPX4 signaling pathway[J]. Heliyon, Elsevier, 2024, 10(3): e24562. |
| [31] |
唐文静, 罗亚丹, 朱尽染, 等. 淫羊藿苷通过上调SLC7A11/GPX4轴减轻铁死亡改善心力衰竭[J]. 遵义医科大学学报, 2024, 47(3): 211-217. |
| [32] |
YANG K T, CHAO T H, WANG I C, et al. Berberine protects cardiac cells against ferroptosis[J]. Tzu-Chi Medical Journal, 2022, 34(3): 310-317. |
| [33] |
GUO L, LI P, WANG Y, et al. Yiqi Fumai Injection ameliorated sepsis-induced cardiomyopathy by inhibition of ferroptosis via xCT/GPX4 Axis[J]. Shock, 2024, 61(4): 638-645. |
| [34] |
王梓仪, 张倩, 郭瑾, 等. 基于铁死亡介导的氧化应激探讨慢性心力衰竭大鼠的发病机制及参附注射液的干预作用[J]. 中国中药杂志, 2023, 48(19): 5285-5293. |
| [35] |
WANG C, ZHOU J, WANG S, et al. Guanxining Injection alleviates fibrosis in heart failure mice and regulates SLC7A11/GPX4 axis[J]. Journal of Ethnopharmacology, 2023, 310: 116367. DOI:10.1016/j.jep.2023.116367 |
| [36] |
於悦, 高想, 张锋莉, 等. 利心冲剂对心力衰竭大鼠铁代谢SLC7A11/GXP4信号通路的调控作用[J]. 现代中西医结合杂志, 2023, 32(23): 3230-3235. |
| [37] |
岳远佳, 姜林, 吉钊, 等. 天香丹减轻心肌缺血损伤的作用机制研究[J]. 中国循证心血管医学杂志, 2024, 16(1): 35-38. |
| [38] |
CHENG P, WANG X, LIU Q, et al. Luqi formula attenuates cardiomyocyte ferroptosis via activating Nrf2/GPX4 signaling axis in heart failure[J]. Phytomedicine, 2024, 125: 155357. DOI:10.1016/j.phymed.2024.155357 |
| [39] |
马金苗, 顼志兵, 朱杰, 等. 附萸汤改善心力衰竭大鼠的心室重构: 基于抑制AMPK/mTOR通路介导的细胞自噬[J]. 南方医科大学学报, 2023, 43(3): 466-473. |
| [40] |
王青青, 张莉芬, 马金苗, 等. 附萸汤通过调控Nrf2/GPX4介导的铁死亡对心力衰竭大鼠心肌纤维化的影响[J]. 中国中药杂志, 2024, 49(3): 789-797. |
| [41] |
YANG Y, ZHAO C, ZHAO C, et al. Linggui Zhugan Decoction protects against doxorubicin-induced myocardial injury by downregulating ferroptosis[J]. Journal of Pharmacy and Pharmacology, 2024, 76(4): 405-415. |
| [42] |
余洁英, 林育浩, 周凤华, 等. 葛根芩连汤对糖尿病湿热型小鼠心脏舒张功能的影响[J]. 中国中药杂志, 2022, 47(10): 2705-2711. |
| [43] |
ZHANG F, LI Z, GAO P, et al. HJ11 Decoction restrains development of myocardial ischemia-reperfusion injury in rats by suppressing ACSL4-mediated ferroptosis[J]. Frontiers in Pharmacology, 2022, 13: 1024292. |
| [44] |
蒋志明, 张辽, 刘磊, 等. 电针心经激活核因子E2相关因子2/血红素氧合酶信号通路抑制铁死亡改善急性心肌缺血[J]. 针刺研究, 2023, 48(5): 461-468. |
| [45] |
XIAO Y, DING L. Mechanistic study of electroacupuncture preconditioning in alleviating myocardial ischemia-reperfusion injury in rats: Involvement of mTOR/ROS signaling pathway to inhibit ferroptosis[J]. The International Journal of Neuroscience, 2024, 10: 1-9. |
| [46] |
彭传玉, 胡玲, 吴子建, 等. 艾灸对佐剂性关节炎大鼠膝关节滑膜组织中调控铁死亡相关因子的影响[J]. 针刺研究, 2022, 47(1): 21-26. |
| [47] |
ZHANG J, CAI W, WEI X, et al. Moxibustion ameliorates cerebral ischemia-reperfusion injury by regulating ferroptosis in rats[J]. Clinical and Experimental Pharmacology and Physiology, 2023, 50(10): 779-788. |
| [48] |
邰晚秋, 刘国鑫, 姜德友. 中医药内治法治疗心衰病研究进展[J]. 中国中医急症, 2023, 32(10): 1877-1880. |
 2025, Vol. 42
2025, Vol. 42