文章信息
- 张祎, 晁利平, 陈秋, 董勇喆, 李晓霞, 王涛
- ZHANG Yi, CHAO Li-ping, CHEN Qiu, DONG Yong-zhe, LI Xiao-xia, WANG Tao
- 维药蜀葵花黄酮类成分的分离与结构鉴定
- Isolation and structural identification of the Flavonoids from the flowers of Althaea rosea
- 天津中医药大学学报, 2016, 35(1): 36-39
- Journal of Tianjin University of Traditional Chinese Medicine, 2016, 35(1): 36-39
- http://dx.doi.org/10.11656/j.issn.1673-9043.2016.01.10
-
文章历史
- 收稿日期: 2015-10-20
蜀葵花为锦葵科蜀葵属蜀葵[Althaea rosea (Linn.) Cavan.]的干燥花,别名为淑气花、一丈红、麻杆花、棋盘花等[1],是维吾尔、蒙古等少数民族常用中草药,在维吾尔族民间自古就有用蜀葵花外敷消肿的习惯。其可全草入药,味甘甜,性凉,有清热解毒,止血消肿,排脓,利尿通淋的功效,用于治疗痈肿疮疡,烧烫伤,吐血、血崩,肠炎,痢疾,梅核气等症,并能解河豚毒[2]。笔者在应用多种色谱法对其95%乙醇(EtOH)提取物的化学成分进行研究的过程中,共分离鉴定了9个黄酮类单体化合物,并利用与文献类似的方法对它们进行了结构鉴定[3, 4, 5, 6, 7]。其中,6、7为首次从蜀葵属中分离得到,9为首次从该植物中分离得到的化合物。见图 1。
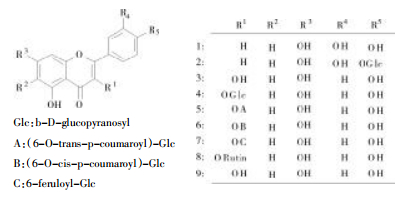
|
| 图 1 蜀葵花中分离到的黄酮类化合物(1~9) |
旋转蒸发仪(德国IKA公司,IKA RV 10、上海亚荣生化仪器厂,RE52CS),薄层色谱硅胶预板、高效硅胶GF254(天津思利达科技有限公司),正相柱色谱用硅胶(48~75 μm),薄层色谱用硅胶H(10~40 μm,青岛海洋化工厂),Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司),D101大孔吸附树脂(净品级,天津海光化工有限公司),ODS(Chromatorex ODS MB,40~75 μm,日本Fuji Silisia Chemical公司),高效液相色谱(HPLC)用分析柱以及制备柱型号分别为Cosmosil 5C18-MS-II(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm,日本 Nacalai Tesque公司),Bruker 500 MHz NMR超导核磁共振波谱仪(瑞士Bruker公司,Avance Ⅲ 500MR)。
氯仿、甲醇、乙腈、丙酮、冰醋酸等色谱纯或分析纯试剂购自天津康科德科技有限公司。蜀葵花采自新疆吉木萨尔(人工种植),由天津中医药大学中药标本馆李天祥副教授鉴定为蜀葵的干燥花(A. rosea L.),植物标本存放于天津中医药大学中医药研究院。
2 提取与分离取干燥蜀葵花(5.0 kg),粉碎,经95% EtOH加热回流提取,减压回收溶剂,真空干燥,得浸膏。上述浸膏(380 g)经D101大孔吸附树脂处理(H2O→ 70% EtOH→95% EtOH),得到H2O、70% EtOH、95% EtOH洗脱物分别为171 g、169 g及12 g。其中70% EtOH洗脱物(120 g),经硅胶柱色谱层析[CHCl3-MeOH(100∶0 →100∶5,v/v)→CHCl3-MeOH-H2O(10∶3∶1→6∶4∶1,v/v/v,下层)],得到12个组分(Fr.1~12)。
Fr.2(8.6 g)经硅胶柱色谱层析[石油醚-乙酸乙酯(100∶0→2∶1,v/v)]及Sephadex LH-20柱层析[CHCl3-MeOH(1∶1,v/v)],得到山柰酚(3,70.3 mg)。Fr.3(9.0 g)经ODS柱色谱层析[MeOH-H2O(30∶70 →100∶0,v/v)和制备型高效液相色谱法(PHPLC)分离制备[MeOH-H2O(55∶45,v/v)+ 1% HAc],得到木犀草素(1,77.0 mg)。
Fr.4(10.0 g)经PHPLC分离制备[MeOH-H2O(40∶60→45∶55→55∶45,v/v)+1% HAc],得到13 个组分(Fr.4-1~4-13)。Fr.4-4 经PHPLC分离制备[MeOH-H2O(40∶60,v/v)+ 1% HAc],得到山奈酚-3-O-β-D-葡萄糖苷(4,208.4 mg)。Fr.4-7 经PHPLC分离制备[MeOH-H2O(50∶50,v/v)+ 1% HAc],得到了山柰酚-3-O-(6″-O-反式对香豆酰基)-β-D-吡喃葡萄糖苷(5,8.0 mg)。Fr.4-8 经PHPLC 分离制备[MeOH-H2O(50∶50,v/v)+ 1% HAc],得山柰酚-3-O-(6″-O-顺式对香豆酰基)-β-D-吡喃葡萄糖苷(6,29.1 mg)及山柰酚-3-O-(6″-O-阿魏酰基)-β-D-吡喃葡萄糖苷(7,21.3 mg)。
Fr.7(11.9 g)经甲醇溶解后离心,将上清液(4.9 g)经ODS柱层析[MeOH-H2O(20%→30%→40%→60%→100%)],得到5个组分(Fr.7-1~7-5)。Fr.7-3经PHPLC分离制备[MeOH-H2O(35∶65,v/v)+ 1% HAc],得到了木犀草素-4′-O-β-D-吡喃葡萄糖苷(2,14.1 mg)、山奈酚-3-O-芸香糖苷(8,40.5 mg)及山奈酚-4′-O-β-D-吡喃葡萄糖苷(9,6.4 mg)。
3 结构鉴定化合物1:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 287.0553 [M+H]+,确定其分子式为C15H10O6(Calcd for C15H11O6,287.055 0)。1H-NMR(500 MHz,DMSO-d6):δ 6.24(1H,br. s,H-6),6.49(1H,br. s,H-8),6.68(1H,s,H-3),6.95(1H,d,J=8.5 Hz,H-5′),7.45(2H,m,H-2′ and 6′)、13.01(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[8]相对照,鉴定该化合物为木犀草素(luteolin)。
| 位置 | 1a | 2a | 3a | 4a | 5a | 6a | 7a | 7b | 8a | 9a |
| 注:a:氘代试剂为DMSO-d6; b:氘代试剂为CD3OD。 | ||||||||||
| 2 | 163.9 | 163.0 | 147.2 | 156.1 | l56.5 | 156.2 | 156.1 | 158.3 | 156.4 | 156.2 |
| 3 | 102.9 | 103.8 | 136.1 | 133.1 | 132.9 | 132.9 | 133.3 | 135.2 | 133.1 | 136.2 |
| 4 | 181.6 | 181.5 | 176.3 | 177.4 | 176.8 | 177.0 | 177.3 | 179.2 | 177.3 | 176.0 |
| 5 | 161.5 | 161.3 | 161.2 | 161.1 | 160.9 | 161.1 | 161.5 | 162.9 | 161.1 | 160.6 |
| 6 | 98.9 | 99.0 | 98.7 | 98.6 | 99.4 | 99.1 | 100.0 | 104.1 | 98.7 | 98.2 |
| 7 | 164.2 | 165.0 | 164.5 | 164.1 | 164.3 | 165.3 | 164.9 | 166.5 | 164.3 | 164.2 |
| 8 | 93.9 | 94.0 | 94.0 | 93.6 | 94.0 | 93.8 | 94.7 | 95.1 | 93.7 | 93.5 |
| 9 | 157.3 | 157.3 | 156.7 | 156.3 | 155.8 | 156.5 | 157.0 | 158.7 | 156.8 | 158.4 |
| 10 | 103.7 | 103.4 | 103.5 | 103.9 | 101.2 | 103.2 | 103.4 | 105.5 | 103.8 | 103.0 |
| 1' | 121.6 | 124.7 | 122.2 | 120.8 | 120.7 | 120.7 | 121.3 | 122.9 | 120.8 | 124.3 |
| 2' | 113.4 | 113.5 | 130.0 | 130.8 | 130.6 | 130.6 | 130.6 | 131.2 | 130.8 | 129.0 |
| 3' | 145.8 | 146.9 | 115.9 | 115.0 | 115.7 | 115.0 | 116.3 | 116.8 | 115.0 | 116.0 |
| 4' | 149.7 | 148.5 | 159.7 | 159.8 | 159.9 | 159.9 | 160.5 | 161.2 | 159.8 | 160.6 |
| 5' | 116.0 | 115.9 | 115.9 | 115.0 | 115.7 | 115.0 | 116.3 | 116.8 | 115.0 | 116.0 |
| 6' | 119.0 | 118.3 | 130.0 | 130.8 | 130.6 | 130.6 | 130.6 | 131.2 | 130.8 | 129.0 |
| 1'' | 101.2 | 100.8 | 101.2 | 101.7 | 105.5 | 101.3 | 99.9 | |||
| 2'' | 73.1 | 74.1 | 74.1 | 74.7 | 75.9 | 74.1 | 73.1 | |||
| 3'' | 75.8 | 76.3 | 76.2 | 76.7 | 78.1 | 76.3 | 76.5 | |||
| 4'' | 69.7 | 69.8 | 69.8 | 70.5 | 71.9 | 69.8 | 69.6 | |||
| 5'' | 77.2 | 77.4 | 74.0 | 74.6 | 75.9 | 75.6 | 77.0 | |||
| 6'' | 60.6 | 60.7 | 62.9 | 63.4 | 64.4 | 66.8 | 60.5 | |||
| 1''' | 124.7 | 125.2 | 127.1 | 100.7 | ||||||
| 2''' | 130.1 | 113.7 | 114.3 | 70.3 | ||||||
| 3''' | 115.0 | 147.3 | 148.3 | 70.5 | ||||||
| 4''' | 159.8 | 150.1 | 150.9 | 71.8 | ||||||
| 5''' | 115.0 | 115.7 | 116.0 | 68.2 | ||||||
| 6''' | 130.1 | 122.6 | 124.0 | 17.6 | ||||||
| 7''' | 144.6 | 145.2 | 146.6 | |||||||
| 8''' | 113.5 | 113.9 | 114.7 | |||||||
| 9''' | 166.1 | 166.7 | 168.8 | |||||||
| -OCH3 | 56.1 | 56.7 | ||||||||
化合物2:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 449.108 7 [M+H]+,确定其分子式为C21H20O11(Calcd for C21H21O11,449.107 8)。1H-NMR(500 MHz,DMSO-d6):δ 4.87(1H,d,J=7.5 Hz,H-1")、6.19(1H,d,J=1.5 Hz,H-6)、6.48(1H,J=1.5 Hz,H-8)、6.80(1H,s,H-3)、7.25(1H,J = 8.5 Hz,H-5′),7.50(1H,br. s,H-2′)、7.53(1H,m,br. d,ca. J=9 Hz,H-6′)、12.90(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[9]相对照,鉴定该化合物为木犀草素-4′-O-β-D-吡喃葡萄糖苷(luteolin-4′-O-β-D-glucopyranoside)。
化合物3:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 287.056 3 [M+H]+,确定其分子式为C15H10O6(Calcd for C15H11O6,287.055 0)。1H-NMR(500 MHz,DMSO-d6):δ 6.25(1H,br. s,H-6)、6.49(1H,br. s,H-8)、6.98(2H,d,J=8.5 Hz,H-3′,5′)、8.10(2H,d,J=8.5 Hz,H-2′,6′)、12.52(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[10]相对照,鉴定该化合物为山奈酚(kaempferol)。
化合物4:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 449.109 1 [M+H]+,确定其分子式为C21H20O11(Calcd for C21H21O11,449.107 8)。1H-NMR(500 MHz,DMSO-d6):δ 5.47 (1H,d,J=7.5 Hz,H-1″),6.21(1H,d,J=2.0 Hz,H-6),6.44(1H,d,J=2.0 Hz,H-8),6.89(2H,d,J=8.5,H-3′,5′),8.05(2H,d,J=8.5 Hz,H-2′,6′),12.62(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[11]相对照,鉴定该化合物为山柰酚-3-O-β-D-吡喃葡萄糖苷(kaempferol-3-O-β-D-glucopyranoside)。
化合物5:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 595.144 1 [M+H]+,确定其分子式为C30H26O13(Calcd for C30H27O13,595.144 6)。1H-NMR(500 MHz,DMSO-d6):δ [4.04(1H,dd,J=6.5、12.0 Hz),4.28(1H,br. d,ca. J=12 Hz),H2-6],5.42(1H,d,J=7.5 Hz,H-1″),6.13(1H,d,J=16.0 Hz,H-8”’),6.28(1H,br. s,H-6),6.39(1H,br. s,H-8),6.79(2H,d,J=8.5 Hz,H-3”’,5”’),6.84(2H,d,J=8.5 Hz,H-3′,5′),7.35(1H,d,J=16.0 Hz,H-7”’),7.38(2H,d,J=8.5 Hz,H-2”’,6”’),7.98(2H,d,J=8.5 Hz,H-2′,6′),12.51(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[12]相对照,鉴定该化合物为山柰酚-3-O-(6″-O-反式对香豆酰基)-β-D-吡喃葡萄糖苷(kaempferol-3-O-(6″-O-trans-p-coumaroyl)-β-D-glucopyranoside)。
化合物6:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 595.144 9 [M+H]+,确定其分子式为C30H26O13(Calcd for C30H27O13,595.144 6)。1H-NMR(500 MHz,DMSO-d6):δ [4.10(1H,dd,J=6.0、12.0 Hz)、4.18(1H,br. d,ca. J=12 Hz),H2-6″],5.40(1H,d,J=7.5 Hz,H-1″),5.49(1H,d,J=13.0 Hz,H-8”’),6.16(1H,br. s,H-6),6.31(1H,br. s,H-8),6.68(1H,d,J=13.0 Hz,H-7”’),6.72(2H,d,J=8.5 Hz,H-3”’,5”’),6.85(2H,d,J=9.0 Hz,H-3′,5′),7.56(2H,d,J=8.5 Hz,H-2”’,6”’),7.95(2H,d,J=9.0 Hz,H-2′,6′),12.53(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[13]相对照,鉴定该化合物为山柰酚-3-O-(6″-O-顺式对香豆酰基)-β-D-吡喃葡萄糖苷(Kaempferol-3-O-(6″-O-cis-p-coumaroyl)-β-D-glucopyranoside)。
化合物7:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 625.155 0 [M+H]+,确定其分子式为C31H28O14(calcd for C31H29O14,625.155 2)。1H-NMR(500 MHz,CD3OD):δ 3.88(3H,s,3”’-OCH3),5.31(1H,d,J=7.5 Hz,H-1″),6.05(1H,d,J=16.0 Hz,H-8”’),6.13(1H,br. s,H-6),6.26(1H,br. s,H-8),6.80(1H,d,J=8.0 Hz,H-5”’),6.80(2H,d,J=8.5 Hz,H-3′,5′),7.26(2H,d,J=8.5 Hz,H-2′,6′),7.36(1H,d,J=16.0 Hz,H-7”’),7.53(1H,br. d,ca. J=8 Hz,H-6”’),7.83(1H,br. s,H-2”’)。其1H-NMR谱、13C-NMR(125 MHz,CD3OD,表 1)谱数据与文献[14]相对照,鉴定该化合物为山柰酚-3-O-(6″-O-阿魏酰基)-β-D-吡喃葡萄糖苷(kaempferol 3-O-β-D-(6″-feruloylglucoside))。
化合物8:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 595.166 2 [M+H]+,确定其分子式为C27H30O15(Calcd for C27H31O15,595.165 7)。1H-NMR(500 MHz,DMSO-d6):δ 1.01(3H,d,J=6.5 Hz,6″′-CH3),4.41(1H,br. s,H-1″′),5.33(1H,d,J=7.5 Hz,H-1″),6.23(1H,d,J=2.0 Hz,H-6),6.43(1H,d,J=2.0 Hz,H-8),6.91(2H,d,J=8.5 Hz,H-3′,5′),8.01(2H,d,J=8.5 Hz,H-2′,6′),12.57(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[15]相对照,鉴定该化合物为山奈酚-3-O-芸香糖苷(Kaempferol 3-O-rutinoside)。
化合物9:黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 449.107 8 [M+H]+,确定其分子式为C21H20O11(Calcd for C21H21O11,449.107 8)。1H-NMR(500 MHz,DMSO-d6):δ 4.99(1H,d,J=7.0 Hz,H-1″),6.20(1H,br. s,H-6),6.47(1H,br. s,H-8),7.19(2H,d,J=8.5 Hz,H-3′,5′),8.14(2H,d,J=8.5 Hz,H-2′,6′),12.42(1H,s,5-OH)。其1H-NMR谱、13C-NMR(125 MHz,DMSO-d6,表 1)谱数据与文献[16]作对照,鉴定该化合物为山奈酚-4′-O-β-D-吡喃葡萄糖苷(kaempferol 4′-O-β-D-glucopyranoside)。
化合物1~9中13C-NMR数据见表 1。
4 结论本课题运用色谱和波谱学方法对蜀葵花的化学成分进行研究,从中分离鉴定了9 个黄酮类单体成分,分别为木犀草素(1)、木犀草素-4′-O-β-D-吡喃葡萄糖苷(2)、山奈酚(3)、山柰酚-3-O-β-D-吡喃葡萄糖苷(4)、山柰酚-3-O-(6″-O-反式对香豆酰基)-β-D-吡喃葡萄糖苷(5)、山柰酚-3-O-(6″-O-顺式对香豆酰基)-β-D-吡喃葡萄糖苷(6)、山柰酚-3-O-(6″-O-阿魏酰基)-β-D-吡喃葡萄糖苷(7)、山奈酚-3-O-芸香糖苷(8)、山奈酚-4′-O-β-D-吡喃葡萄糖苷(9)。其中化合物6、7为首次从蜀葵属中分离得到,9为首次从该植物中分离得到。
5 讨论蜀葵花是维吾尔族常用药材,在新疆广泛种植、资源丰富。临床上蜀葵花用途广泛,已用于眼皮炎肿、耳底炎、乳腺炎等各种炎症[17]。但蜀葵花药理作用的物质基础和作用机制尚未明确,没有建立起质量标准,未能充分挖掘和研究蜀葵独特的药用功效,尚未开发出中药产品,不能满足国内外市场的需求。本课题对蜀葵花的化学成分进行研究,为蜀葵花进一步开发和利用提供了坚实的物质基础。
| [1] | 张 祎, 陈 秋, 刘丽丽, 等. 维药蜀葵花化学成分的分离与鉴定(I)[J]. 沈阳药科大学学报, 2013, 30(5): 335-341. |
| [2] | 王晓丽, 张红秋, 崔红梅. 蜀葵辅助治疗河豚鱼中毒的疗效观察[J]. 中华全科医学, 2010, 8(4): 525-526. |
| [3] | 吴 帅, 刘二伟, 张 祎, 等. 川续断中化学成分的研究[J]. 天津中医药大学学报, 2010, 29(3): 147-150. |
| [4] | 吴克磊, 康利平, 熊呈琦, 等. 蒺藜全草中甾体皂苷类化学成分研究[J]. 天津中医药大学学报, 2012, 31(4): 225-228. |
| [5] | 刘丽丽,李晓霞,陈 玥, 等, 槐米化学成分研究I[J]. 天津中医药大学学报. 2014, 33(4): 230-233. |
| [6] | 邓 屾, 刘丽丽, 陈 玥, 等. 益母草化学成分研究Ⅲ[J]. 2014, 33(6): 362-365. |
| [7] | 刘丽丽,李晓霞,陈 玥, 等, 槐米中酚酸类化学成分研究I[J]. 天津中医药大学学报. 2014, 33(1): 39-41. |
| [8] | 陈晓珍, 李国友, 吴晓青, 等. 血满草的化学成分[J]. 应用与环境生物学报, 2010, 16 (2): 197-201. |
| [9] | 景永帅, 杨 娟, 汪 冶, 等. 光枝勾儿茶中蒽醌-苯并异色满苯醌二聚体成分[J]. 中国药学杂志, 2011, 46 (9): 661-664. |
| [10] | 解红霞, 张金花, 张宏桂, 等. 蒙药玉簪花的化学成分研究[J]. 中国药学杂志, 2009, 44 (10): 733-735. |
| [11] | 常仁龙, 孙佳明, 张 博, 等. 核桃楸叶化学成分研究[J]. 中成药, 2009, 31 (7): 1082-1085. |
| [12] | 肖 皖, 李 宁, 倪 慧, 等. 小秋葵化学成分的分离与鉴定[J]. 沈阳药科大学学报, 2009, 26 (10): 782-784. |
| [13] | Jaromir B, Lutoslawa S. Phenylpropanoid esters from Lamium album flowers[J]. Phytochemistry, 1994, 38 (4): 997-1001. |
| [14] | Catalono S, Bilia AR, Martinozzi M, et al. Kaempferol 3-O-β-D-(6″-feruloylglucoside) from Polylepis incana[J]. Phytochemistry, 1994, 37 (6): 1777-1778. |
| [15] | 何枢衡, 张 祎, 葛丹丹, 等. 中药半枝莲黄酮类成分的分离与结构鉴定[J]. 沈阳药科大学学报, 2011, 28 (3): 182-185. |
| [16] | Ishikura N, Hayashida S. Kaempferol glycosides in the seed-coat of Ophiopogon jaburan (Kunth) Lodd[J]. Agricultural and Biological Chemistry, 1979, 43 (9): 1923-1926. |
| [17] | 盛 萍, 堵年生, 杨学斌, 等. 维吾尔药材蜀葵子的鉴别研究[J]. 新疆中医药, 2003, 21 (4): 38-40. |
 2016, Vol. 35
2016, Vol. 35




