文章信息
- 晁利平, 阮静雅, 刘艳霞, 韩立峰, 王涛, 张祎
- CHAO Li-ping, RUAN Jing-ya, LIU Yan-xia, HAN Li-feng, WANG Tao, ZHANG Yi
- 绵萆薢化学成分的分离与结构鉴定
- Isolation and structural identification of constituents from Dioscoreae spongiosae Rhizoma
- 天津中医药大学学报, 2016, 35(5): 336-339
- Journal of Tianjin University of Traditional Chinese Medidine, 2016, 35(5): 336-339
- http://dx.doi.org/10.11656/j.issn.1673-9043.2016.05.13
-
文章历史
收稿日期: 2016-05-04
作为传统中药,绵萆薢(Dioscoreae spongiosae Rhizoma)以其干燥根茎入药,具有利湿去浊,祛风除痹之功效,用于治疗膏淋、白浊、白带过多、风湿痹痛、关节不利、腰膝疼痛等症[1],主产于湖南、湖北、浙江、江西、福建、广东及广西等地[2]。绵萆薢中含有的化学成分主要为甾体、二芳基庚烷、木脂素、有机酸及酯等[3]。药理活性研究表明,绵萆薢及其有效成分具有抗骨质疏松[4]、抗心肌缺血、抗肿瘤[5]、抗真菌、调血脂、降尿酸[6]、预防动脉粥样硬化等作用。临床上用于治疗乳糜尿、慢性前列腺炎、骨质疏松、风湿及类风湿性关节炎及骨关节炎等症状。
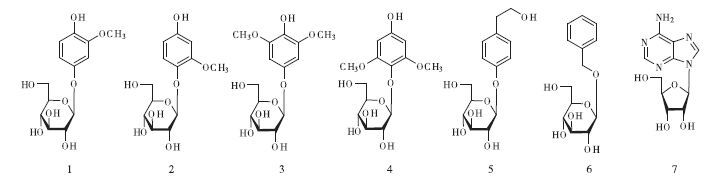
笔者在对绵萆薢化学成分研究的过程中,利用与文献[7-13]类似的方法,分离鉴定出7 个单体化合物。其中,1~3 为首次从薯蓣属中分离得到,4~7 为首次从该植物中分离得到,结构见图 1。
|
| 图 1 绵萆薢中分离得到的化合物1~7 |
Bruker 500MR 超导核磁共振波谱仪(瑞士Bruker公司,Avance Ⅲ 500MR),大孔吸附树脂(天津海光化工有限公司),ODS(Chromatorex ODS MB,40~75 μm,日本YMC 有限公司);Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司),Cosmosil 5C18-MS-Ⅱ制备柱和分析柱(250 mm×4.6 mm和250 mm×20 mm,均为5 μm,Japan,Nacalai Tesque 公司),TLC Silica gel 60 F254(Aluminium sheets 20 cm × 20 cm,德国Merck 公司)。
色谱/分析纯氯仿、甲醇、乙腈、丙酮、冰醋酸等试剂购自天津康科德科技有限公司。
绵萆薢购自河北安国,由天津中医药大学李天祥副教授鉴定为薯蓣科植物绵萆薢(Dioscorea spongiosa J. Q. Xi, M. Mizuno et W. L. Zhao)。
2 提取与分离取绵萆薢干燥根(7.8 kg)经18、16 倍量70% EtOH 加热回流2 次(3、2 h),合并滤液,减压回收溶剂,得浸膏1 150.0 g。上述浸膏(1 000.0 g)经D101 大孔吸附树脂处理(H2O → 95% EtOH → Acetone),得到H2O、95% EtOH 和Acetone 洗脱物分别为725.0、245.0 及1.9 g。
95% EtOH 洗脱物(150.0 g)经硅胶柱层析[CHCl3-MeOH(100:1 → 100:3 → 100:7,V/V)→ CHCl3-MeOH-H2O(10:3:1 →7:3:1 → 6:4:1,V/V/V,下层)],共得12 个组分(Fr.1~12)。
Fr. 6(14.0 g)经ODS 柱层析[MeOH-H2O(20:80 → 30:70 → 40:60 → 50:50 → 60:40 → 70:30 → 80:20 → 100:0,V/V)],得到17 个组分(Fr. 6-1~6-17)。Fr. 6-1(1 170.0 mg)经制备型高效液相色谱法(PHPLC)分离制备[H3CN-H2O(3:97,V/V)],得到17 个组分(Fr.6-1-1~6-1-17)。Fr. 6-1-6(26.9 mg)、6-1-9(13.8 mg)、6-1-11(29.0 mg)、Fr. 6-1-14(90.9 mg)分别经Sephadex LH-20 凝胶柱层析(MeOH),得到Tachioside(1,20.0 mg)、Isotachioside(2,7.9 mg)、3,5-二甲氧基熊果苷(3,25.6 mg)和2,6-二甲氧基-4-羟基-苯酚-1-O-β-D-吡喃葡萄糖苷(4,36.3 mg)。Fr. 6-1-15(119.4 mg)经PHPLC 分离制备[MeOH-H2O(8:92,V/V)+1% HAc],得到腺苷(7,50.0 mg)和淫羊藿次苷D2(5,36.0 mg)。Fr. 6-3(241.0 mg)经PHPLC 分离制备[H3CN-H2O(10:90,V/V)+1% HAc],得到苯甲醇-O-β-D-吡喃葡萄糖苷(6,9.8 mg)。
3 结构鉴定化合物1:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 301.093 2 [M-H]-,确定其分子式为C13H18O8(Calcd for C13H17O8,301.092 9)。1H-NMR(500 MHz,C5D5N): δ 7.14(1H,br. s,H-3),7.04(1H,br. d,ca. J=9 Hz,H-5),7.13(1H,d,J=8.5 Hz,H-6),5.54(1H,d,J = 7.0 Hz,H-1′),4.36(2H,m,overlapped,H-2′ and H-3′),4.32(1H,dd,J = 7.5、8.0 Hz,H-4′),4.10(1H,m,H-5′),[4.38(1H,dd,J = 4.5、11.5 Hz)、4.57(1H,br. d,ca. J = 12 Hz),H2-6'],3.70(3H,s,2-OCH3)。其1H-、13C-NMR(125 MHz,C5D5N,见表 1)谱数据与文献[14]相对照,鉴定该化合物为Tachioside。
| 位置 | 1a | 2b | 3c | 4a | 5b | 6b | 7c |
| 1 | 143.3 | 141.1 | 150.2 | 129.5 | 134.2 | 139.1 | |
| 2 | 149.0 | 152.5 | 94.9 | 154.5 | 130.8 | 129.3 | 152.3 |
| 3 | 103.5 | 101.8 | 148.0 | 95.2 | 117.8 | 129.2 | |
| 4 | 152.1 | 154.9 | 130.2 | 155.9 | 157.6 | 128.7 | 149.0 |
| 5 | 109.5 | 107.6 | 148.0 | 095.2 | 117.8 | 129.2 | 119.3 |
| 6 | 116.4 | 120.5 | 094.9 | 154.5 | 130.8 | 129.3 | 156.1 |
| 7 | 039.4 | 071.8 | |||||
| 8 | 064.3 | 139.9 | |||||
| 2-OCH3 | 55.8 | 056.6 | 056.5 | ||||
| 3-OCH3 | 055.7 | ||||||
| 5-OCH3 | 055.7 | ||||||
| 6-OCH3 | 056.5 | ||||||
| 1' | 103.7 | 104.3 | 101.5 | 105.9 | 102.5 | 103.4 | 087.9 |
| 2' | 075.1 | 075.1 | 073.2 | 076.0 | 074.9 | 075.2 | 073.4 |
| 3' | 078.6 | 078.1 | 076.7 | 078.3 | 078.0 | 078.2 | 70.6 |
| 4' | 071.6 | 071.4 | 70.7 | 071.7 | 071.3 | 071.8 | 085.8 |
| 5' | 078.9 | 077.8 | 77.1 | 078.5 | 077.9 | 078.1 | 61.6 |
| 6' | 062.6 | 062.6 | 60.8 | 062.7 | 062.5 | 062.9 | |
| 注:a:氘代试剂为吡啶;b:氘代试剂为甲醇;c:氘代试剂为二甲基亚砜。 | |||||||
化合物2:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 301.092 8 [M-H]-,确定其分子式为C13H18O13(Calcd for C13H17O13,301.092 9)。1H-NMR(500 MHz,CD3OD):δ 6.46(1H,d,J = 2.0 Hz,H-3),6.30(1H,dd,J = 2.0、8.5 Hz,H-5),7.02(1H,d,J = 8.5 Hz,H-6),4.70(1H,d,J = 7.0 Hz,H-1'),3.44(2H,m,overlapped,H-2′and H-5′),3.33(1H,dd,J = 7.5、8.0 Hz,H-3′),3.38(1H,dd,J = 8.0、9.5 Hz,H-4′),[3.69(1H,dd,J = 5.5、12.0 Hz)、3.86(1H,br. d,ca. J = 12 Hz),H2-6′,3.81(3H,s,2-OH3)。其1H-、13C-NMR(125 MHz,CD3OD,见表 1)谱数据与文献[15]相对照,鉴定该化合物为Isotachioside。
化合物3:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 331.103 9 [M-H]-,确定其分子式为C14H20O9(Calcd for C14H19O9,331.103 5)。1H-NMR(500 MHz,DMSO-d6):δ 6.38(2H,s,H-2, 6),4.69(1H,d,J = 7.5 Hz,H-1′),3.20(1H,dd,J = 7.5、9.0 Hz,H-2′),3.26(1H,dd,J = 9.0、9.0 Hz,H-3′),3.11(1H,dd,J = 9.0、9.0 Hz,H-4′),3.30(1H,m,H-5′),[3.40(1H,dd,J = 5.0、12.0 Hz)、3.72(1H,m,overlapped),H2-6′],3.72(6H,s,3,5-OH3)。其1H-、13C-NMR(125 MHz,DMSO-d6,见表 1)谱数据与文献[16]相对照,鉴定该化合物为3, 5-二甲氧基熊果苷(koaburaside)。
化合物4:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 331.104 2 [M-H]-,确定其分子式为C14H20O9(Calcd for C14H19O9,331.103 5)。1H-NMR(500 MHz,C5D5N):δ 6.55(2H,s,H-3, 5),5.53(1H,d,J = 7.0 Hz,H-1′),4.28(3H,m,overlapped,H-2′-4′),3.88(1H,m,H-5′),[4.30(1H,dd,J = 5.5、12.0 Hz)、4.38(1H,dd,J = 2.0、11.5 Hz),H2-6′],3.70(6H,s,2, 6-OH3)。其1H-、13C-NMR(125 MHz,C5D5N,见表 1)谱数据结合1H-1H COSY、HSQC、HMBC等2D-NMR 谱的解析,鉴定该化合物为文献[17]所报道的2, 6-二甲氧基-4-羟基-苯酚-1-O-β-D-吡喃葡萄糖苷(2, 6-dimethoxy-4-hydroxyphenol-1-O-β-D-glucopyranoside)。
化合物5:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 345.120 2 [M+COOH]-,确定其分子式为C14H20O7(Calcd for C15H21O9,345.119 1)。1H-NMR(500 MHz,CD3OD):δ 7.14(2H,d,J = 8.5 Hz,H-2, 6),7.02(2H,d,J=8.5 Hz,H-3, 5),2.76(2H,t,J = 7.0 Hz,H2-7),3.69(2H,t,J =7.0 Hz,H2-8),4.86(1H,d,J=7.0 Hz,H-1′),3.45(2H,m,overlapped,H-2′ and 3′),3.40(2H,overlapped,H-4′ and 5′),[3.69(1H,m,overlapped)、3.88(1H,dd,J=1.5、13.0 Hz),H2-6′]。其1H-、13C-NMR(125 MHz,CD3OD,见表 1)谱数据与文献[18]相对照,鉴定该化合物为淫羊藿次苷D2(Icariside D2)。
化合物6:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 315.110 0[M+COOH]-,确定其分子式为C13H18O6(Calcd for C14H19O8,315.108 5)。1H-NMR(500 MHz,CD3OD):δ 7.42(2H,br. d,ca. J= 7 Hz,H-2, 6),7.33(2H,t,J=7.0 Hz,H-3,5),7.27(1H,br. d,ca. J=7 Hz,H-4),4.67、4.93(1H each,both d,J=11.5 Hz,H2-7),4.35(1H,d,J = 7.0 Hz,H-1′),3.25(2H,m,H-2′ and 5′),3.35(1H,dd,J=7.5、8.0 Hz,H-3′),3.30(1H,dd,J = 8.0、8.0 Hz,H-4'),[3.69(1H,dd,J = 5.0、12.0 Hz)、3.90(1H,br. d,ca. J =12 Hz),H2-6′]。其1H-、13C-NMR(125 MHz,CD3OD,见表 1)谱数据与文献[19]相对照,鉴定该化合物为苯甲醇-O-β-D-吡喃葡萄糖苷(benzyl alcohol O-β-D-glucopyranoside)。
化合物7:白色粉末。高分辨Q-TOF-ESI-MS 给出其准分子离子峰m/z 266.090 2 [M-H]-,确定其分子式为C10H13N5O4(Calcd for C10H12N5O4,266.089 5)。1H-NMR(500 MHz,DMSO-d6):δ 8.17(1H,s,H-2),8.38(1H,s,H-8),7.38(2H,s,6-NH2),5.91(1H,d,J=5.5 Hz,H-1′),4.64(1H,dd,J=3.0、5.5 Hz,H-2′),4.18(1H,t,J=3.0 Hz,H-3′),4.00(1H,m,H-4′),[3.59(1H,dd,J=4.0、12.0 Hz)、3.71(1H,dd,J=3.0、12.0 Hz),H2-5′]。其1H-、13C-NMR(125 MHz,DMSO-d6,见表 1)谱数据与文献[20]相对照,鉴定该化合物为腺苷(Adenosine)。
4 结果为了进一步扩大对绵萆薢的开发与利用,笔者运用色谱和波谱学方法,对绵萆薢的化学成分进行了研究,分离并鉴定了以下7 个单体成分,分别是Tachioside(1)、Isotachioside(2)、3,5-二甲氧基熊果苷(3)、2,6-二甲氧基-4-羟基-苯酚-1-O-β-D-吡喃葡萄糖苷(4)、淫羊藿次苷D2(5)、苯甲醇-O-β-D-吡喃葡萄糖苷(6)、腺苷(7)。其中,化合物1~3 为首次从薯蓣属中分离得到,4~7 为首次从该植物中分离得到。
5 讨论绵萆薢最早记录于《神农本草经》,历史久远且疗效显著。但国内外对绵萆薢化学成分的研究报道尚少,据文献报道, 其化学成分主要是甾体皂苷、二芳基庚烷、木脂素类等;具有抗骨质疏松、抗心肌缺血、抗肿瘤、抗真菌、调血脂、降尿酸、预防动脉粥样硬化等药理作用。因此,进一步开发与利用该植物,加强其化学成分与药理活性的筛选,可对其临床治疗与应用有指导性意义。
| [1] | 中国药典委员会. 中国药典(一部)[S]. 北京:中国医药科技出版社, 2010. |
| [2] | 赵维良, 何君亚, 奚镜清. 再论绵萆薢的新种地位[J]. 中国中药杂志, 1994, 19 (4) : 199–200. |
| [3] | 晁利平, 刘艳霞, 瞿璐, 等. 绵萆薢的化学成分及药理作用研究进展[J]. 药物评价研究, 2015, 38 (3) : 325–330. |
| [4] | Yin J, Tezuka Y, Kouda K, et al. Antiosteoporotic Activity of the Water Extract of Dioscorea spongiosa[J]. Biol Pharm Bull, 2004, 27 (4) : 583–586. DOI:10.1248/bpb.27.583 |
| [5] | 李雪征. 绵萆薢抗肿瘤活性成分的研究[D]. 延吉:延边大学, 2002. http://cdmd.cnki.com.cn/article/cdmd-10184-2002101123.htm |
| [6] | 苏筠霞.李建华. 刘天喜, 等. 萆薢水提取物对尿酸性肾病大鼠TNF-α、MCP-1和ICAM-1表达的影响[J]. 中成药, 2013, 35 (5) : 1088–1092. |
| [7] | 王强, 张祎, 韩立峰, 等. 中药川续断化学成分的研究Ⅲ[J]. 天津中医药大学学报, 2014, 33 (2) : 108–111. |
| [8] | 刘丽丽, 李晓霞, 陈玥, 等. 槐米中酚酸类化学成分的研究[J]. 天津中医药大学学报, 2014, 33 (1) : 39–41. |
| [9] | 刘丽丽, 李晓霞, 陈玥, 等. 槐米化学成分研究Ⅰ[J]. 天津中医药大学学报, 2014, 33 (4) : 230–233. |
| [10] | 吴帅, 刘二伟, 张祎, 等. 川续断中化学成分的研究[J]. 天津中医药大学学报, 2010, 29 (3) : 147–150. |
| [11] | 邓屾, 刘丽丽, 陈玥, 等. 益母草化学成分研究Ⅲ[J]. 天津中医药大学学报, 2014, 33 (6) : 362–365. |
| [12] | 吴克磊, 康利平, 熊呈琦, 等. 蒺藜全草中甾体皂苷类化学成分研究[J]. 天津中医药大学学报, 2012, 31 (4) : 225–228. |
| [13] | 晁利平, 陈秋, 石萍萍, 等. 蜀葵花中二氢黄酮类成分的分离与结构鉴定[J]. 天津中医药大学学报, 2015, 34 (4) : 233–236. |
| [14] | 来国防, 王先友, 曹建新, 等. 水青树茎干中化学成分的提取与分离[J]. 河南大学学报:自然科学版, 2010, 40 (2) : 141–146. |
| [15] | 杨大松, 杨永平, 杨永红, 等. 秋枫化学成分的研究[J]. 天然产物研究与开发, 2013, 25 (8) : 1056–1059. |
| [16] | 贾凌云, 徐昙烨, 王晶, 等. 费菜茎叶化学成分的分离与鉴定(Ⅱ)[J]. 沈阳药科大学学报, 2014, 31 (9) : 673–676. |
| [17] | 李倩, 王学贵, 莫廷星, 等. 光叶铁仔根和茎化学成分研究[J]. 中草药, 2014, 45 (20) : 2904–2907. |
| [18] | 刘树民, 王宇, 张洪财, 等. 诺丽果的化学成分研究[J]. 中草药, 2012, 43 (11) : 2150–2153. |
| [19] | 夏芳, 孙建, 姜勇, 等. 白木香叶的化学成分研究(二)[J]. 中国中药杂志, 2013, 38 (19) : 3299–3303. |
| [20] | 赖先根, 赵玉英, 梁鸿. 黄蜀葵花化学成分的研究[J]. 中国中药杂志, 2006, 31 (19) : 1597–1600. |
 2016, Vol. 35
2016, Vol. 35




