文章信息
- 瞿璐, 刘艳霞, 李建良, 布淑阳, 王涛, 张祎
- QU Lu, LIU Yan-xia, LI Jian-liang, BU Shu-yang, WANG Tao, ZHANG Yi
- 祁菊叶化学成分的分离与结构鉴定
- Study on the constituents of Chrysanthemum morifolium Ramat. Qiju leaves
- 天津中医药大学学报, 2017, 36(1): 57-60
- Journal of Tianjin University of Traditional Chinese Medicine, 2017, 36(1): 57-60
- http://dx.doi.org/10.11656/j.issn.1673-9043.2017.01.14
-
文章历史
收稿日期: 2016-11-03
在中国,菊花(Chrysanthemum morifolium Ramat.)为常用大宗中药材,具有散风,平肝明目,清热解毒的功效,临床上主要用于治疗风热感冒,头痛眩晕,目赤肿痛,眼耳昏花等症[1-2]。现代药理作用表明菊花具有治疗冠心病、降低血压、预防高血脂、抗菌、抗病毒、抗炎及预防衰老等多种生理活性[3]。菊花产地广,用量大,但采摘菊花的同时,大量的叶被丢弃。菊的叶能否代替花入药,进而提高现有药用植物资源的再生能力和内在质量,是值得深入研究的一个课题。因此,本课题对河北安国产祁菊叶的化学成分进行了初步研究,为该植物的进一步研究与开发利用提供物质基础。
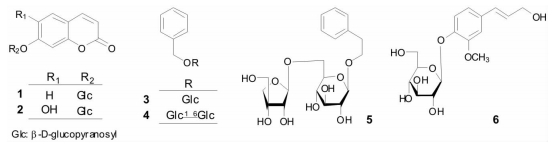
笔者采用多种色谱法相结合,对祁菊叶70%乙醇提取物的化学成分进行分离纯化,并通过理化性质及波谱分析鉴定了6个单体化合物的结构[4-7],分别为茵芋苷(1),菊苣苷(2),苯甲基-6-O-β-D-吡喃葡萄糖苷(3),苄醇-O-[β-D-吡喃葡萄糖(1→6)]-β-D-吡喃葡萄糖苷(4),icariside D1(5),松柏苷(6)。其中,化合物4、5为首次从菊属植物中分离得到。
1 实验材料与仪器正相柱色谱用硅胶(48~75 μm),ODS(Chromatorex ODS MB,40~75 μm,日本Fuji Silisia Chemical公司),Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司),D101大孔吸附树脂(净品级,天津海光化工有限公司),高效液相色谱法(HPLC)用分析柱以及制备柱型号分别为Cosmosil 5C18-MS-Ⅱ(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm,日本Nacalai Tesque公司),氘代试剂(北京崇熙科技孵化器公司)。
实验所用试剂(色谱纯或分析纯)均为天津康科德科技有限公司。
祁菊叶采集于河北安国,由天津中医药大学中药标本馆李天祥教授鉴定为(Chrysanthemum morifolium Ramat. Qiju)的干燥叶,标本保存于天津中医药大学中医药研究中心。
2 提取与分离取干燥祁菊叶3.0 kg,用10、8、8倍量70%乙醇(EtOH)溶液依次加热回流提取3次,减压回收溶剂,得浸膏260.1 g。取浸膏255 g溶于水,用CHCl3 -H2O萃取,得到CHCl3和H2O层萃取物分别为20.5 g和234.5 g。H2O层萃取物(225.0 g)经D101大孔吸附树脂柱分离(H2O→95% EtOH),得到H2O、95% EtOH洗脱物各155.1 g、55.1 g。取上述95% EtOH洗脱物(40.0 g)经硅胶柱层析[CHCl3 →CHCl3 -MeOH(100:5,V/V)→ CHCl3 -MeOH-H2O(20:3:1→10:3:1→7:3:1→6:4:1,V/V/V,下层)→ MeOH],得到15个组分(Fr. 1~Fr. 15)。Fraction 8-(3+4+5)(175.6 mg)经制备型高效液相色谱法(PHPLC)分离制备[CH3CN-H2O(13:87,V/V)+ 1% HAc],得到茵芋苷(1,5.6 mg)和松柏苷(6,5.6 mg)。Fraction 8-(7+8)(426.0 mg)经PHPLC分离制备[MeOH-H2O(20:80,V/V)+1% HAc],得到苯甲基-6-O-β-D-吡喃葡萄糖苷(3,44.7 mg)。Fraction 9(3.8 g)经PHPLC制备[MeOH-H2O(25:75→35:65→45:55→65:35→100:0,V/V)],得到26个组分[Fr. 9-1~Fr. 9-26]。Fraction 9-(4+5)(71.7 mg)经PHPLC分离制备[CH3CN-H2O(13:87,V/V)+ 1% HAc],得到菊苣苷(2,10.8 mg)。Fraction 9-14(177.9 mg)经PHPLC分离制备[CH3CN-H2O(18:82,V/V)+ 1% HAc],得到icariside D1(5,15.0 mg)。Fraction 10(4.6 g)经PHPLC制备[MeOH-H2O(25:75→35:65→45:55→65:35→100:0,V/V)],得到18个组分[Fr. 10-1~Fr. 10-18]。Fraction 10-3(168.4 mg)经PHPLC分离制备[CH3CN-H2O(8:92,V/V)+ 1% HAc],得到苄醇-O-[β-D-吡喃葡萄糖-(1→6)]-β-D-吡喃葡萄糖苷(4,7.9 mg)。化合物结构式,见图 1。
|
| 图 1 化合物1~6的结构 |
化合物1:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 359.053 5 [M+Cl]-,确定其分子式为C15H16O8(C15H16O8Cl,359.053 9)。1H NMR(CD3OD,400 MHz)谱数据:δ 6.28(1H,d,J=9.6 Hz,H-3),7.89(1H,d,J=9.6 Hz,H-4),7.56(1H,d,J=8.8 Hz,H-5),7.08(2H,m,H-6, 8),5.03(1H,d,J=7.2 Hz,H-1′),3.31~3.93(4H,H-2′~5′),[3.70(1H,dd,J=5.6、12.0 Hz),3.91(1H,br. d,ca. J=12 Hz),H2-6′]。13C NMR(CD3OD,100 MHz)谱数据:δ 163.1(C-2),115.2(C-3),145.5(C-4),130.4(C-5),115.2(C-6),162.2(C-7),105.0(C-8),114.3(C-9),156.7(C-10),101.9(C-1′),74.7(C-2′),77.9(C-3′),71.2(C-4′),78.3(C-5′),62.4(C-6′)。其1H、13C NMR谱数据与文献[8]相对照,并结合2D NMR谱的解析,鉴定该化合物为茵芋苷。
化合物2:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 339.072 0 [M-H]-,确定其分子式为C15H16O9(calcd for C15H15O9,339.072 2)。1H NMR(CD3OD,400 MHz)谱数据:δ 6.28(1H,d,J=9.6 Hz,H-3),7.82(1H,d,J=9.6 Hz,H-4),7.20(1H,s,H-5),7.04(1H,s,H-8),4.97(1H,d,J=6.8 Hz,H-1′),3.42~3.95(6H,H-2′~6′)。13C NMR(CD3OD,100 MHz)谱数据:δ 162.3(C-2),113.9(C-3),145.6(C-4),115.3(C-5),145.5(C-6),149.6(C-7),105.4(C-8),114.8(C-9),150.5(C-10),103.1(C-1′),74.7(C-2′),77.5(C-3′),71.3(C-4′),78.5(C-5′),62.3(C-6′)。其1H、13C NMR谱数据与文献[9]相对照,并结合2D NMR谱的解析,鉴定该化合物为菊苣苷。
化合物3:白色油状物。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 305.078 2 [M+Cl]-,确定其分子式为C13H18O6(calcd for C13H18O6Cl,305.079 7)。1H NMR(CD3OD,400 MHz)谱数据:δ 7.41(2H,d,J=7.6 Hz,H-2, 6),7.31(2H,d,J=7.6 Hz,H-3, 5),7.26(1H,t,J=7.6 Hz,H-4),[4.66(1H,d,J=11.6 Hz),4.92(1H,d,J=11.6 Hz)H2-7],4.35(1H,d,J=7.6 Hz,H-1′),3.29(1H,dd,J=7.6、8.0 Hz,H-2′),3.35(1H,dd,J=8.0、8.0 Hz,H-3′),3.32(1H,dd,J=8.0、8.0 Hz,H-4′),3.30(1H,m,H-5′),[3.44(1H,dd,J=5.2、12.0 Hz),3.90(1H,br. d,ca. J=12 Hz),H2-6′]。13C NMR(CD3OD,100 MHz)谱数据:δ 139.1(C-1),129.2(C-2, 6),129.3(C-3,5),128.7(C-4),71.8(C-7),103.3(C-1′),75.1(C-2′),78.1(C-3′),71.7(C-4′),78.0(C-5'),62.8(C-6′)。其1H、13C NMR谱数据与文献[10]相对照,并结合2D NMR谱的解析,鉴定该化合物为苯甲基-6-O-β-D-吡喃葡萄糖苷。
化合物4:白色固体。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 467.132 2 [M+Cl]-,确定其分子式为C19H28O11(calcd for C19H28O11Cl,467.132 6)。1H NMR(C5D5N,400 MHz)谱数据:δ 7.56(2H,d like,ca. J=8 Hz,H-2, 6),7.54(2H,t,J=8.4 Hz,H-3,5),7.25(1H,m,H-4),[4.82(1H,d,J=12.0 Hz),5.22(1H,d,J=12.0 Hz),H2-7],4.33(1H,d,J=7.2 Hz,H-1′),4.36(1H,d,J=7.2 Hz,H-1″),3.91~4.54(10H,m,H-2′~6′ and H-2″~6″)。13C NMR(C5D5N,100 MHz)谱数据:δ 138.9(C-1),128.5(C-2,6),128.6(C-3,5),127.7(C-4),71.6(C-7),103.9(C-1′),75.1(C-2′),77.4(C-3′),70.9(C-4′),78.5(C-5′),70.1(C-6′),105.6(C-1″),75.3(C-2″),78.5(C-3″),71.6(C-4″),78.5(C-5″),62.7(C-6″)。其1H、13C NMR谱数据与文献[11]相对照,并结合2D NMR谱的解析,鉴定该化合物为苄醇-O-[β-D-吡喃葡萄糖-(1→6)]-β-D-吡喃葡萄糖苷。
化合物5:白色油状物。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 451.135 8[M+Cl]-,确定其分子式为C19H28O10(calcd for C19H28O10Cl,451.137 6)。1H NMR(C5D5N,400 MHz)谱数据:δ 7.28(2H,d like,ca. J=8 Hz,H-2, 6),7.26(1H,t,J=7.2、8.0 Hz,H-3,5),7.18(1H,m,H-4),2.99(2H,dd,J=7.2、8.0 Hz,H2-7),[3.88(1H,dt,J=7.2、9.6 Hz),4.33(1H,dt,J=8.0、9.2 Hz)H2-8],4.82(1H,d,J=7.6 Hz,H-1′),4.00(1H,dd,J=7.6、8.0 Hz,H-2′),4.07(1H,dd,J=8.0、8.0 Hz,H-3'),4.04(1H,dd,J=8.0、8.0 Hz,H-4′),4.07(1H,m,H-5′),[4.21(1H,m),4.72(1H,br. d,ca. J=10 Hz),H2-6′],5.84(1H,d,J=2.8 Hz,H-1″),4.78(1H,d,J=2.4 Hz,H-2″),[4.53(1H,d,J=9.6 Hz),4.34(1H,d,J=9.6 Hz),H-5″],4.14(2H,s,H2-6″)。13C NMR(C5D5N,100 MHz)谱数据:δ 139.4(C-1),128.7(C-2,6),129.4(C-3,5),126.4(C-4),36.6(C-7),70.6(C-8),104.7(C-1′),75.0(C-2′),78.5(C-3′),71.6(C-4′),77.2(C-5′),68.8(C-6′),111.1(C-1″),77.9(C-2″),80.7(C-3″),74.9(C-4″),65.5(C-5″)。其1H、13C NMR谱数据与文献[12]相对照,并结合2D-NMR谱的解析,鉴定该化合物为icariside D1。
化合物6:白色无定形粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 377.101 0 [M+Cl]-,确定其分子式为C16H22O8(calcd for C16H22O8Cl,377.100 9)。1H NMR(CD3OD,400 MHz)谱数据:δ 7.07(1H,br. s,H-2),6.94(1H,br. d,ca. J=8 Hz,H-5),7.10(1H,d,J=7.6 Hz,H-6),6.54(1H,d,J=16.0 Hz,H-7),6.27(1H,dt,J=6.0、15.6 Hz,H2-8),4.20(2H,d,J=6.0 Hz,H2-9),4.89(1H,d,J=7.5 Hz,H-1′),3.31~3.86(6H,H-2′~6′),3.87(3H,s,2-OCH3)。13C NMR(CD3OD,100 MHz)谱数据:δ 147.6(C-1),150.9(C-2),111.4(C-3),133.7(C-4),117.9(C-5),120.8(C-6),128.9(C-7),131.3(C-8),63.7(C-9),102.8(C-1′),74.9(C-2′),77.8(C-3′),71.3(C-4′),78.2(C-5′),62.5(C-6′),56.7(2-OCH3)。其1H、13C NMR谱数据与文献[13]相对照,并结合2D NMR谱的解析,鉴定该化合物为松柏苷。
4 结果与讨论查阅相关文献时发现,多种药用植物的非药用部位均具有开发利用价值,如以三七茎叶为原料开发的新药七叶神安片,具有抗炎镇痛治疗偏头痛的效果[14]。还有以黄芪茎叶总黄酮为原料开发制得的新药黄芪茎叶解毒胶囊,具有治疗急性咽炎的作用[15]。这些研究即利用了药用植物的非药用部位减少了资源的浪费,且又产生了经济效益。祁菊叶产量很大,若能加以利用,既可保护生态,又可推动经济的发展。但是,需要有相应的科学研究加以佐证。笔者首先对其叶的化学成分进行研究,为祁菊植株不同部位的综合开发利用提供实验依据。在此过程中,从其70%乙醇提取物中鉴定了6个单体成分。其中,4、5为首次从菊属植物中分离得到。
| [1] | 国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社, 2015. |
| [2] | 瞿璐, 王涛, 董勇喆, 等. 菊花化学成分与药理作用的研究进展[J]. 药物评价研究, 2015, 38(1): 98–104. |
| [3] | 李英霞, 彭广芳, 王小梅, 等. 菊花的药理研究进展[J]. 时珍国医国药, 1998, 9(6): 580. |
| [4] | 吴帅, 刘二伟, 张祎, 等. 川续断中化学成分的研究[J]. 天津中医药大学学报, 2010, 29(3): 147–150. |
| [5] | 邓屾, 刘丽丽, 陈玥, 等. 益母草化学成分研究Ⅲ[J]. 天津中医药大学学报, 2014, 33(6): 362–365. |
| [6] | 刘丽丽, 李晓霞, 陈玥, 等. 槐米化学成分研究Ⅰ[J]. 天津中医药大学学报, 2014, 33(4): 230–233. |
| [7] | 刘丽丽, 李晓霞, 陈玥, 等. 槐米中酚酸类化学成分研究Ⅰ[J]. 天津中医药大学学报, 2014, 33(1): 39–41. |
| [8] | 汪豪, 杜慧斌, 朱峰妍, 等. 新疆一枝蒿化学成分的研究[J]. 中国药科大学学报, 2011, 42(4): 310–313. |
| [9] | Gawronska-Grzywacz M, Krzaczek T. Flavonoids and coumarins from Hieracium pilosella L.(Asteraceae)[J]. Acta Societatis Botanicorum Poloniae, 2009, 78(3): 189–195. |
| [10] | 羡冀, 罗显峰, 于韬, 等. 猴耳环叶化学成分的分离与鉴定[J]. 沈阳药科大学学报, 2014, 31(4): 262–265. |
| [11] | 戴好富, 谭宁华, 周俊. 北五味子中的配糖体成分[J]. 中国天然药物, 2006, 4(1): 49–51. |
| [12] | Miyase T, Ueno A, Takizawa N, et al. Studies on the glycosides of Epimedium grandiflorum MORR. var. thunbergianum (MIQ.) NAKAI. Ⅱ[J]. Chem Pharm Bull, 1987, 35(9): 371–3719. |
| [13] | Huang P, Gloria K, Pepter GW. Phenylpropanoid glycosides from Typhonium flagelliforme (Araceace)[J]. Natural Product Research and Development, 2004, 16(5): 403–405. |
| [14] | 黄跃进. 三七传统非药用部位的开发利用探讨[J]. 中医药信息, 1999, 16(6): 19–20. |
| [15] | 刘秋凤, 孙海波, 权文杰, 等. 黄芩叶解毒胶囊治疗急性咽炎的临床观察[J]. 内蒙古中医药, 2013, 32(20): 13–14. |
 2017, Vol. 36
2017, Vol. 36