文章信息
- 张娜张娜, 栾晓莹栾晓莹, 谢燕谢燕, 柏自松柏自松, 白洋白洋, 胡利民胡利民, 常艳旭常艳旭, 王萌王萌, 张鹏张鹏
- ZHANG Na, LUAN Xiao-ying, XIE Yan, BAI Zi-song, BAI Yang, HU Li-min, CHANG Yan-xu, WANG Meng, ZHANG Peng
- HPLC-ELSD测定心脑舒通胶囊中Terrestrinin A的含量
- Determination of Terrestrinin A from Xinnao Shutong capsules by HPLC-ELSD method
- 天津中医药大学学报, 2017, 36(2): 132-135
- Journal of Tianjin University of Traditional Chinese Medicine, 2017, 36(2): 132-135
- http://dx.doi.org/10.11656/j.issn.1673-9043.2017.02.14
-
文章历史
收稿日期: 2017-01-20
2. 天津国际生物医药联合研究院, 中药新药研发中心, 天津 300457
2. Tianjin International Joint Academy of Biomedicine, Research and Development Center of Traditional Chinese Drug, Tianjin 300457, China
心脑舒通胶囊由蒺藜科植物蒺藜(Tribulus terrestris L.)的干燥具果地上部分制备而来,具有活血化瘀、舒利血脉之功效。用于治疗原发性高血压、高脂血症、冠心病心绞痛、脑梗死后遗症,在防治心血管疾病等方面有显著疗效[1-3]。现代药理研究表明甾体皂苷类及黄酮类成分是蒺藜中的活性成分,主要具有抗心肌缺血和抗动脉粥样硬化的作用[4-7]。目前报道的对心脑舒通胶囊的质量控制研究,大多采用氯化钴法或者分光光度法测量总皂苷或总黄酮的含量,而缺乏对单一有效成分的含量控制。在制备心脑舒通胶囊的过程中,主要保留了甾体皂苷类成分,而黄酮类成分保留较少,因而采用黄酮类成分作为心脑舒通有效成分的控制指标是不适当的。由于大部分甾体皂苷分子内缺少发色团和助色基[8-10],无紫外吸收,使用紫外检测器(UV)时响应较差,检测灵敏度较低,故采用对无紫外吸收的甾体皂苷元的测定具有良好的稳定性,较高的灵敏度和重现性的蒸发光散射检测器(ELSD)来进行检测较为合适[11-13]。为了提高心脑舒通胶囊的质量控制方法,从心脑舒通胶囊中分离提纯化合物Terrestrinin A作为对照品[14],建立了高效液相色谱-蒸发光散射检测器(HPLC-ELSD)法对其在心脑舒通胶囊及总皂苷中的含量进行准确测定,从而可以有效控制药品质量,保证临床用药安全有效。
1 仪器与试药 1.1 仪器及试剂美国Waters公司的e2695高效液相色谱仪(在线脱气系统、四元泵、自动进样器、柱温箱、Empower数据处理系统、2424 ELS蒸发光散射检测器);SCIENTZ SB 25-12DTN超声波清洗机(宁波新芝生物科技股份有限公司);Millipore纯净水发生器(美国Millipore公司);XS205DU型十万分之一微量电子天平(Mettler Toledo公司)。乙腈(色谱纯,天津市康科德科技有限公司);超纯水。
1.2 试药供试对照品:Terrestrinin A由本实验室自制(经UV、NMR、MS等波谱鉴定,采用HPLC-ELSD面积归一化法测定纯度,检验纯度大于99.0%)。
供试样品:心脑舒通胶囊和心脑舒通总皂苷(特指未添加辅料、用于制备心脑舒通胶囊的蒺藜总皂苷),由吉林敖东药业股份有限公司提供,批号分别为:20100903064、20110107036、20110201100、20110701。
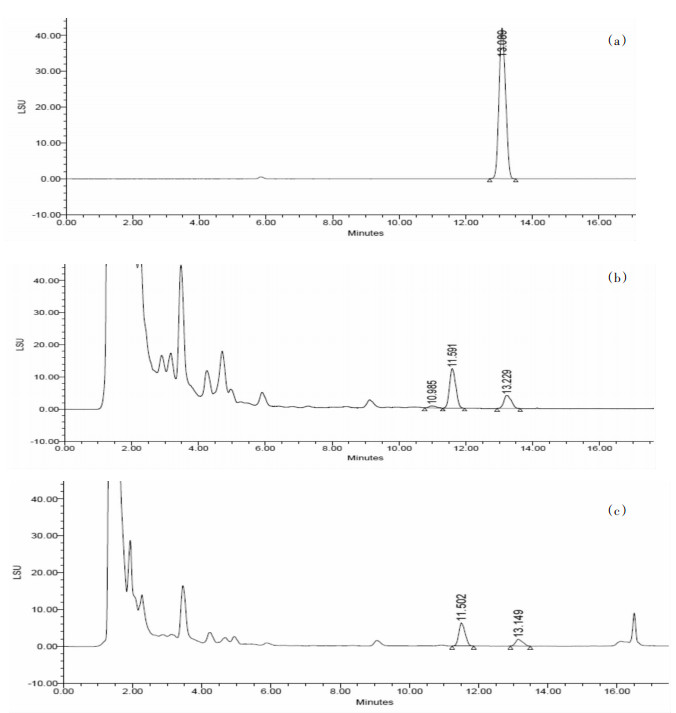
2 方法与结果 2.1 色谱条件系统适用性色谱柱:Hedra-C18柱(4.6 mm×150 mm,5 μm);流动相:乙腈(A)-水(B),梯度洗脱(0~13.5 min,30% A线性变为39% A,13.5~15 min,39% A线性变为95% A,15~23 min,95% A线性不变);流速:1.0 mL/min;柱温:40 ℃;漂移管温度:60 ℃;气体(N2)压力:30 psi;增益值:100;进样体积:20 μL。理论塔板数按Terrestrinin A计算大于15 000,Terrestrinin A与相邻色谱峰的分离度不低于4,拖尾因子不大于1.3,色谱图见图 1。
|
| 图 1 对照品(a)、样品(b)、总皂苷(c)的色谱图 |
取Terrestrinin A约25 mg,精密称定,置于25 mL容量瓶中,加40%的乙腈水溶液溶解并稀释至刻度,摇匀。
2.2.2 样品供试品溶液制备取样品约250 mg,精密称定,置于5 mL容量瓶中,加40%的乙腈水溶液3 mL溶解,超声萃取30 min,静置至室温,再加40%的乙腈水溶液至刻度,摇匀。14 000 r/min离心10 min后取上清溶液待测。
2.2.3 原料药供试品溶液配制取总皂苷约75 mg,精密称定,置于5 mL容量瓶中,加40%的乙腈水溶液3 mL溶解,超声萃取30 min,静置至室温,加40%的乙腈水溶液至刻度,摇匀。14 000 r/min离心10 min后取上清溶液待测。
2.3 标准曲线的绘制分别精密量取“2.2.1”项下的对照品储备液0.5、1、2、3、4、5 mL置于10 mL容量瓶中,加40%的乙腈水溶液至刻度,摇匀,得一系列不同浓度的对照品溶液;按“ 2.1”所述的色谱条件进样分析,记录色谱峰面积;以对照品溶液浓度的对数(lgC)为横坐标X,峰面积的对数(lgA)为纵坐标Y作图,得Terrestrinin A的线性回归方程: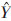
取“ 2.2.1”项下的对照品储备液逐级稀释,按上述色谱条件进行检测,在信噪比是10:1时测得Terrestrinin A的定量限是29.1 mg/L,在信噪比是3:1时测得的Terrestrinin A的检测限是16.2 mg/L。
2.5 精密度实验取线性实验中0.3 g/L浓度水平的对照品溶液,按上述色谱条件连续6次进样分析,记录色谱峰面积,计算Terrestrinin A的峰面积RSD为1.21%。
2.6 重复性实验取批号为20100903064的样品约250 mg,精密称定,按照“ 2.2.2”所述方法,平行配制6份样品溶液,按上述色谱条件进样分析,记录色谱峰面积并计算,含量RSD为1.62%。
2.7 稳定性实验取样品供试品溶液,室温保存,于0、2、4、6、12 h进样分析,记录Terrestrinin A的峰面积,计算含量RSD为1.90% 2.8加样回收率实验取已知Terrestrinin A含量的样品9份,每份约250 mg,精密称定,分成3组,按低(50%)、中(100%)、高(150%)浓度分别加入一定量的Terrestrinin A对照品,按照“ 2.2.2”项下样品供试品溶液,按上述色谱条件进行测定,结果表明本法具有良好的回收率。见表 1。
| 加入浓度 (mg/L) |
称样量 (mg) |
测得浓度 (mg/L) |
回收率 (%) |
平均回收率 (%) |
RSD值 (%) |
| 099.2 | 255.74 | 099.4 | 100.3 | ||
| 253.36 | 100.1 | 101.0 | |||
| 258.68 | 102.3 | 103.2 | |||
| 198.4 | 256.49 | 197.2 | 099.4 | ||
| 248.53 | 198.2 | 100.0 | 99.4 | 2.40 | |
| 253.65 | 200.0 | 100.9 | |||
| 297.6 | 246.27 | 285.7 | 096.0 | ||
| 244.62 | 286.3 | 096.2 | |||
| 250.83 | 290.7 | 097.7 |
分别取心脑舒通胶囊及总皂苷,按“ 2.2.2”所述方法,制备供试品溶液,按上述色谱条件进样分析,记录色谱图,以峰面积对数按外标法求得供试品溶液的浓度对数,并进一步计算出浓度及含量。含量测定结果见表 2。
心脑舒通胶囊中的活性成分是甾体皂苷类和黄酮类,其中甾体皂苷的含量远远大于黄酮类(总每粒黄酮醇苷的含量小于1 mg)[15-17]。甾体皂苷按结构可分为呋甾皂苷和螺甾皂苷两类[18],其中呋甾皂苷在心脑舒通胶囊中的含量约为每粒15 mg。甾体皂苷具有广泛的药理作用和重要的生物活性,如防治心血管疾病、降血糖、抗肿瘤、抗真菌、免疫调节等[19]。而据文献报道呋甾皂苷在抗血小板聚集、抗心率失常和增加心肌细胞营养性血流量等心脑血管系统方面的活性强于相应的螺甾皂苷[20],说明呋甾皂苷是心脑舒通胶囊的主要药效物质基础。目前研究报道蒺藜中含有的呋甾型皂苷超过20个,其结构差别很小[21],Terrestrinin A是呋甾皂苷的一种,在心脑舒通胶囊的药效物质中具有代表性,适合作为含量测定的指标成分。
本研究采用HPLC-ELSD的方法,首次对Terrestrinin A的色谱分离条件进行了优化并对其含量进行测定。本分析方法的精密度,稳定性,重复性的RSD值都小于2%,表明采用本法对样品中Terrestrinin A的含量测定,重复性良好,结果准确,灵敏度高,且专属性强,适用于心脑舒通胶囊的质量控制。
| [1] | 陶冶, 张允岭, 刘超, 等. 心脑舒通胶囊对急性脑缺血再灌注大鼠皮质单胺类神经递质的影响[J]. 天津中医药, 2008, 25(6): 503–505. |
| [2] | 李明娟, 瞿伟菁, 王熠非, 等. 蒺藜皂苷的降糖作用[J]. 中药材, 2002, 25(6): 420–422. |
| [3] | 曲晶. 心脑舒通胶囊的临床应用综述[J]. 中国卫生产业, 2011, 8(7): 60. |
| [4] | 李君玲, 杨松松. 蒺藜皂苷化学及药理研究概述[J]. 中医药学刊, 2006, 24(8): 1509–1511. |
| [5] | 吴克磊, 康利平, 熊呈琦, 等. 蒺藜全草中甾体皂苷类化学成分研究[J]. 天津中医药大学学报, 2012, 31(4): 225–228. DOI:10.11656/j.issn.1673-9043.2012.04.11 |
| [6] | 候爽, 陈长军, 杨博, 等. 蒺藜成分及主要药理作用研究进展[J]. 中国医药导报, 2014, 11(35): 156–158. |
| [7] | 曹惠玲, 陈浩宏, 许士凯. 蒺藜及其有效成分的药理与临床研究进展[J]. 中成药, 2001, 23(8): 602–604. |
| [8] | 祁海宏, 王春, 严伟民. 高效液相色谱法-蒸发光散射检测测定蒺藜皂苷1的含量[J]. 中国药事, 2006, 20(3): 158–159. |
| [9] | 孙耀军, 邹建. 皂苷不同测定方法的比较[J]. 江西食品工业, 2009, 2(2): 30–33. |
| [10] | 陈方, 宋海峰. 皂苷分析方法研究进展[J]. 天津中医药, 2005, 22(3): 257–259. |
| [11] | 宣伟东, 陈海生, 谭兴起, 等. HPLC-ELSD法测定刺蒺藜中甾体皂苷TTS-12含量[J]. 第二军医大学学报, 2005, 26(2): 222–223. |
| [12] | 郭尊武, 张利, 李炜. 高效液相色谱法-蒸发光散射检测法测定蒺藜中蒺藜新苷的含量[J]. 药物分析杂志, 2004, 24(3): 284–286. |
| [13] | 王桂玲, 解生旭, 赵宏峰, 等. HPLC-蒸发光散射检测法测定蒺藜中蒺藜皂苷A[J]. 中草药, 2005, 36(9): 1406–1407. |
| [14] | Huang JW, Tan CH, Jiang SH, et al. Terrestrinins A and B, two new steroid saponins from Tribulus Terrestris[J]. Journal of Asian Natural Products Research, 2003, 5(4): 285–290. DOI:10.1080/1028602031000111996 |
| [15] | 齐建红. 蒺藜皂苷的药理作用研究新进展[J]. 西安文理学院学报, 2013, 16(3): 26–29. |
| [16] | 占颖, 李朋收, 张舒媛, 等. 蒺藜皂苷在心血管疾病中的应用[J]. 河南中医, 2014, 34(8): 1504–1507. |
| [17] | 李炜, 杨飞快, 朱清风, 等. 心脑舒通胶囊中总黄酮醇苷的含量测定[J]. 西北药学杂志, 2009, 24(1): 10–11. |
| [18] | 李君玲, 杨松松. 蒺藜皂苷化学及药理研究概述[J]. 中医药学刊, 2006, 24(8): 1509–1510. |
| [19] | 张存莉, 吴战库, 马惠玲, 等. 甾体皂苷的生物活性研究进展[J]. 西北林学院学报, 2003, 18(2): 95–100. |
| [20] | 田全. 呋喃皂苷衍生物的合成及其抗癌活性研究[D]. 沈阳: 沈阳药科大学, 2003: 8-9. |
| [21] | 孙国珍, 张洁, 马百平. 蒺藜中甾体皂苷类化学成分及其药理活性研究进展[J]. 中草药, 2007, 38(7): 1111–1115. |
 2017, Vol. 36
2017, Vol. 36