文章信息
- 屠亚茹屠亚茹, 欧阳慧子欧阳慧子, 孙梦杰孙梦杰, 常艳旭常艳旭, 何俊何俊
- TU Ya-ru, OUYANG Hui-zi, SUN Meng-jie, CHANG Yan-xu, HE Jun
- UPLC-Q-TOF-MS/MS方法鉴定血必净注射液中20种化学成分
- Simultaneous identification of 20 components in Xuebijing injection by UPLC—Q—TOF-MS/MS
- 天津中医药大学学报, 2017, 36(3): 209-213
- Journal of Tianjin University of Traditional Chinese Medicine, 2017, 36(3): 209-213
- http://dx.doi.org/10.11656/j.issn.1673-9043.2017.03.13
-
文章历史
收稿日期: 2017-01-03
2. 天津中医药大学第一附属医院, 天津 300193
2. The First Affiliated Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
血必净注射液是由王今达教授以血府逐瘀汤组方为基础研制的复方中药制剂[1],由红花、赤芍、川芎、丹参、当归5味中药组成,其有效成分包括红花色素、黄酮苷、酚酸和苯乙基苷等[2]。研究表明,血必净注射液具有降低内毒素水平、调节免疫及炎性介质的作用[3-4],临床上主要用来治疗脓毒症和多器官功能障碍综合症[5-10],并可与抗生素联合用药用于治疗肺部感染[11]。
在以往的研究当中,对于血必净注射液的研究多集中于药理、药效方面,而有关药效成分的研究则相对较少。虽然已有相关文献对血必净注射液的化学成分进行了定量分析[2],但所采用的方法不够简单、灵敏,且所分析的化学成分相对较少。目前,对化学成分的分析方法主要有高效液相色谱法(HPLC)、超高夜相色谱法(UPLC)、气相色谱-质谱联用法(GC/MS)、高效液相色谱-质谱联用法(HPLC/MS)、超高液相色谱-质谱联用法(UPLC/MS),通过液质联用技术可以得到化合物的分子量、元素组成以及离子碎片等信息,对确定化合物的结构有重大意义。本实验建立了简便、灵敏的超高效液相色谱串联四级杆飞行时间质谱技术(UPLC-Q-TOF-MS/MS)定性分析方法,最终确定了血必净注射液中的20种化学成分,对丰富血必净注射液化学成分的研究以及确定其药效成分提供了参考。
1 仪器与试药 1.1 仪器Agilent 1290超高效液相色谱仪;Agilent Q-TOF 6520质谱仪(美国Agilent公司);Agilent MassHunter分析软件(美国Agilent公司);AX205型十万分之一天平(瑞士Mettler Toledo公司);Milli-Q超纯水制备仪(Millipore公司);3K15型高速离心机(美国Sigma公司);XW-80A型涡旋混合器(上海沪西分析仪器厂)。
1.2 试药对照品羟基红花黄色素A(批号MUST-12081605),芍药苷(批号MUST-16041901),芍药内酯苷(批号MUST-15091008),氧化芍药苷(批号MUST-15033010),苯甲酰芍药苷(批号MUST-15091010),阿魏酸(批号MUST-15091605),没食子酸(批号MUST-15042910),丹参素(批号MUST-15082714),绿原酸(批号MUST-15041814),丹酚酸A(批号MUST-15072110),丹酚酸C(批号MUST-15011305),金丝桃苷(批号MUST-16032113),迷迭香酸(批号MUST-16040512),购自成都曼斯特生物科技有限公司。咖啡酸(批号110885-200102),原儿茶酸(批号110809-200604),原儿茶醛(批号110810-201007),购自中国食品药品检定研究院。鸟苷(批号XMM0662),尿苷(批号XMM0664),洋川芎内酯I(批号2015039),购自天津士兰科技有限公司。血必净注射液购自天津红日药业股份有限公司,乙腈(美国Merck公司)、甲酸(美国ROE公司)为色谱纯。
2 方法 2.1 色谱条件色谱柱:ACQUITY UPLC® BEH C18柱(2.1 mm×100 mm,1.7 μm);流动相:A相0.1%甲酸水,B相乙腈,梯度洗脱,洗脱程序为:0~2 min,5%~15% B;2~4 min,15%~15% B;4~5 min,15%~18% B;5~12 min,18%~18% B;12~13 min,18%~20% B;13~15 min,20%~20% B;15~16 min,20%~21% B;16~18 min,21%~21% B;18~19 min,21%~22% B;19~24 min,22%~25% B;24~28 min,25%~50% B;28~34 min,50%~70% B;34~39 min,70%~85% B;39~43 min,85%~100% B;43~45 min,100%~100% B;流速:0.3 mL/min;柱温:30 ℃;进样量:5 μL。
2.2 质谱条件离子源为电喷雾离子源,负离子模式监测,毛细管温度:350 ℃;干燥气流速:9 L/min;雾化器压力:30 psi;碎裂电压:175 V;碰撞能量:8 V,35 V。
2.3 对照品溶液的制备分别精密称取羟基红花黄色素A、原儿茶醛、原儿茶酸、迷迭香酸、咖啡酸、没食子酸、阿魏酸、绿原酸、丹参素、芍药苷、芍药内酯苷、氧化芍药苷、苯甲酰芍药苷、鸟苷、尿苷、金丝桃苷、没食子酰芍药苷、洋穿芎内酯I、丹酚酸A、丹酚酸C对照品各1 mg,用甲醇溶解,配制为1 mg/mL的对照品储备溶液。4 ℃冰箱冷藏备用。
2.4 供试品溶液的制备血必净注射液用超纯水稀释10倍,经0.22 μm微孔滤膜过,即得。
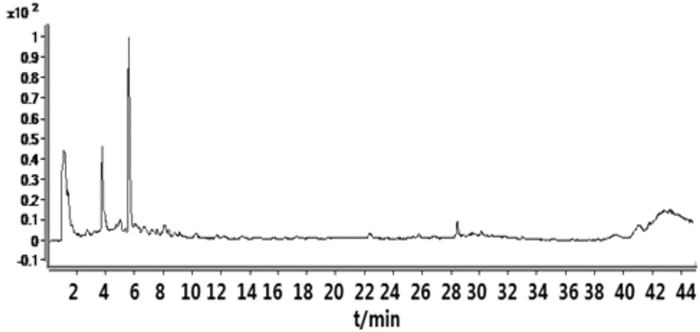
3 结果与分析采集负离子模式下的总离子流图,见图 1。利用Agilent Masshunter Qualitative Analysis分析软件,对负离子模式下采集的血必净注射液总离子流图进行提取,根据准离子分子峰,确定化合物的分子量和分子式,结合二级质谱碎片,并对比对照品进行鉴定。结果见表 1。
|
| 图 1 血必净负离子模式下总离子流图 |
| 编号 | 保留时间tR(min) | 监测离子 | MS(m/z) | MS2碎片(m/z) | 分子式 | 化合物 |
| 1 | 1.409 | [M-H]- | 243.062 8 | 200.060 4、185.994 1 | C9H12N2O6 | 尿苷 |
| 2 | 1.579 | [M-H]- | 283.079 2 | 150.040 0 | C10H13N5O5 | 鸟苷 |
| 3 | 1.974 | [M-H]- | 169.001 3 | 125.010 9 | C7H6O5 | 没食子酸 |
| 4 | 2.777 | [M-H]- | 197.044 5 | 179.031 7 | C9H10O5 | 丹参素 |
| 5 | 3.158 | [M-H]- | 153.0186 | 109.030 7 | C7H6O4 | 原儿茶酸 |
| 6 | 3.810 | [M-H]- | 495.149 6 | 137.023 5 | C23H28O12 | 氧化芍药苷 |
| 7 | 3.931 | [M-H]- | 137.025 7 | 108.028 7 | C7H6O3 | 原儿茶醛 |
| 8 | 4.072 | [M-H]- | 353.088 9 | 191.056 2 | C16H18O9 | 绿原酸 |
| 9 | 4.589 | [M-H]- | 179.033 5 | 135.044 0 | C9H8O4 | 咖啡酸 |
| 10 | 4.927 | [M-H]- | 611.1699 | 491.120 0 | C27H32O16 | 羟基红花黄色素A |
| 11 | 5.173 | [M+HCOO]- | 525.1611 | 479.154 8, 283.080 2, 121.029 7 | C23H28O11 | 芍药内酯苷 |
| 12 | 5.951 | [M+HCOO]- | 525.1614 | 479.154 4、449.144 2、327.107 5、165.055 4、121.028 4 | C23H28O11 | 芍药苷 |
| 13 | 6.882 | [M-H]- | 193.049 8 | 149.059 9、134.036 7 | C10H10O4 | 阿魏酸 |
| 14 | 7.086 | [M-H]- | 631.1683 | 613.157 6、509.135 9、491.119 7、399.095 1、313.057 2 | C30H32O15 | 没食子酰芍药苷 |
| 15 | 7.143 | [M-H]- | 463.088 6 | 302.033 2, 301.033 2, 300.020 9 | C21H20O12 | 金丝桃苷 |
| 16 | 10.686 | [M-H]- | 359.076 3 | 197.045 5, 179.035 9^161.023 1 | C18H16O8 | 迷迭香酸 |
| 17 | 12.185 | [M-H]- | 223.096 8 | 205.086 4、187.063 3、179.090 0、161.095 4、112.986 3 | C12H16O4 | 洋川芎内酯I |
| 18 | 22.740 | [M-H]- | 493.1119 | 295.219 0 | C26H22O10 | 丹酚酸A |
| 19 | 28.665 | [M-H]- | 583.1768 | 553.168 4、535.181 0、431.129 2、121.029 4 | C30H32O12 | 苯甲酰芍药苷 |
| 20 | 29.173 | [M-H]- | 491.286 2 | 311.047 5、293.0502 | C26H20O10 | 丹酚酸C |
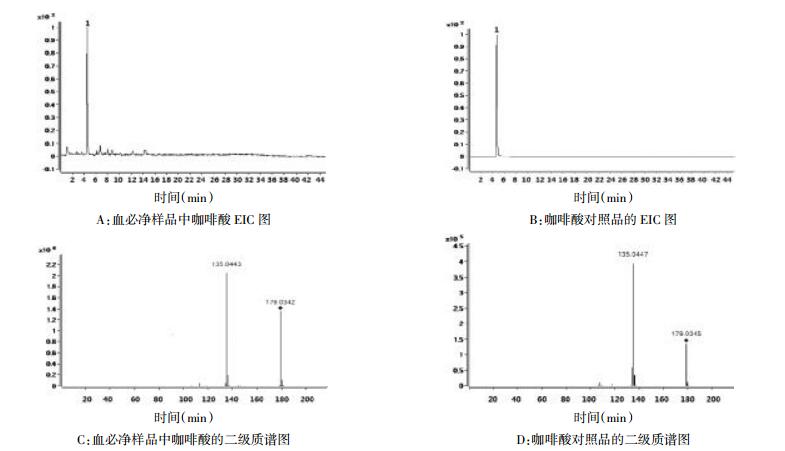
以咖啡酸为例,咖啡酸的EIC图及二级质谱图见图 2。
|
| 图 2 咖啡酸的EIC图及二级质谱图 |
化合物1:tR=1.409 min,一级产生[M-H]-峰,m/z=243.062 8,二级裂解产生m/z=200.060 4、185.994 1。对照品tR=1.411 min,裂解规律为m/z=243.062 8 [M-H]-,二级扫描裂解产生200.055 0[M-H-CONH]-。分子式为C9H12N2O6,相对分子质量为244.069 5,对比对照品鉴定化合物1为尿苷。
化合物2:tR=1.579 min,一级产生[M-H]-峰,m/z=282.079 2,二级裂解产生m/z=150.040 0。对照品tR=1.612 min,裂解规律为m/z=282.079 2[M-H]-,二级扫描裂解产生150.041 7[M-H-C5H8O4]-。分子式为C10H13N5O5,相对分子质量为283.091 7,对比对照品鉴定化合物2为鸟苷。
化合物3:tR=1.974 min,一级产生[M-H]-峰,m/z=169.001 3,二级裂解产生m/z=125.010 9。对照品tR=1.967 min,裂解规律为m/z=169.001 7[M-H]-,二级扫描裂解产生125.024 0[M-H-CO2]-。分子式为C7H6O5,相对分子质量为170.011 5,对比对照品鉴定化合物3为没食子酸。
化合物4:tR=2.777 min,一级产生[M-H]-峰,m/z=197.044 5,二级裂解产生m/z=179.031 7。对照品tR=2.812 min,裂解规律为m/z=197.044 6[M-H]-,二级扫描裂解产生179.034 2[M-H-H2O]-。分子式为C9H10O5,相对分子质量为198.052 8,对比对照品鉴定化合物4为丹参素。
化合物5:tR=3.158 min,一级产生[M-H]-峰,m/z=153.018 6,二级裂解产生m/z=109.030 7,对照品tR=3.177 min,裂解规律为m/z=153.018 5[M-H]-,二级扫描裂解产生109.029 1[M-H-CO2]-。分子式为C7H6O4,相对分子质量为154.026 6,对比对照品鉴定化合物5为原儿茶酸。
化合物6:tR=3.810 min,一级产生[M-H]-峰,m/z=495.149 6,二级裂解产生m/z=137.023 5,对照品tR=3.813 min,裂解规律为m/z=495.149 7[M-H]-,二级扫描裂解产生137.023 7[M-H-C16H22O9]-。分子式为C23H28O12,相对分子质量为496.158 1,对比对照品鉴定化合物6为氧化芍药苷。
化合物7:tR=3.931 min,一级产生[M-H]-峰,m/z=137.025 7,二级裂解产生m/z=108.028 7,对照品tR=3.927 min,裂解规律为m/z=137.025 9[M-H]-,二级扫描裂解产生108.021 2[M-H-HCO]-,分子式为C7H6O3,相对分子质量为138.031 7,对比对照品鉴定化合物6为原儿茶醛。
化合物8:tR=4.072 min,一级产生[M-H]-峰,m/z=353.088 9,二级裂解产生m/z=191.056 2,对照品tR=4.099 min,裂解规律为m/z=353.087 8[M-H]-,二级扫描裂解产生191.055 8[M-H-CH2O]-,分子式为C16H18O9,相对分子质量为354.095 1,对比对照品鉴定化合物8为绿原酸。
化合物9:tR=4.589 min,一级产生[M-H]-峰,m/z=179.034 2,二级裂解产生m/z=135.044 3,对照品tR=4.581 min,裂解规律为m/z=179.034 5[M-H]-,二级扫描裂解产生135.044 7[M-H-CO2]-,分子式为C9H8O4,相对分子质量为180.042 3,对比对照品鉴定化合物9为咖啡酸。
化合物10:tR=4.927 min,一级产生[M-H]-峰,m/z=611.169 9,二级裂解产生m/z=491.120 0,对照品tR=4.881 min,裂解规律为m/z=611.168 7[M-H]-,二级扫描裂解产生491.118 7[M-H-C8H8O]-,分子式为C27H32O16,相对分子质量为612.169 0,对比对照品鉴定化合物9为羟基红花黄色素A。
化合物11:tR=5.173 min,一级产生[M+HCOO]-峰,m/z=525.161 1,二级裂解产生m/z=479.154 8、283.080 2、121.029 7。对照品tR=5.159 min,裂解规律为m/z=525.161 2[M+HCOO]-,二级扫描裂解产生479.155 4[M-H]-、121.029 1[C8H9O]-。分子式为C23H28O11,相对分子质量为480.163 2,对比对照品鉴定化合物11为芍药内酯苷。
化合物12:tR=5.951 min,一级产生[M+HCOO]-峰,m/z=525.160 4,二级裂解产生m/z=479.154 4、449.144 2、327.107 5、165.055 4、121.028 4。对照品tR=5.957 min,裂解规律为m/z=525.160 5[M+HCOO]-,二级扫描裂解产生479.155 7[M-H]-、449.145 4 [M-H-COH2]-、327.108 3[M-H-COH2-C7H6O2]-、165.054 9、121.029 2[C8H9O]-,分子式为C23H28O11,相对分子质量为480.163 2,对比对照品鉴定化合物12为芍药苷。
化合物13:tR=6.882 min,一级产生[M-H]-峰,m/z=193.049 8,二级裂解产生m/z=149.059 9、134.036 7。对照品tR=6.878 min,裂解规律为m/z=193.050 3[M-H]-,二级扫描裂解产生149.060 4 [M-H-CO2]-、134.036 9[M-H-CO2-CH3]-,分子式为C10H10O4,相对分子质量为194.057 9,对比对照品鉴定化合物13为阿魏酸。
化合物14:tR=7.086 min,一级产生[M-H]-峰,m/z=631.168 3,二级裂解产生m/z=613.157 6、509.135 9、491.119 7、399.095 1、313.057 2。对照品tR=7.100 min,裂解规律为m/z=631.168 3[M-H]-,二级扫描裂解产生613.168 3[M-H-H2O]-、491.118 8[M-H-H2O-C7H6O2]-、313.056 7[M-H-H2O-C7H6O2-C10H9O3]-,分子式为C30H32O15,相对分子质量为632.174 1,对比对照品鉴定化合物12为没食子酰芍药苷。
化合物15:tR=7.143 min,一级产生[M-H]-峰,m/z=463.088 6,二级裂解产生m/z=302.033 2[M-H-C6H9O5]-、301.033 2、300.020 9。对照品tR=7.145 min,裂解规律为m/z=463.088 2[M-H]-,二级扫描裂解产生302.038 0[C6H11O5]-、301.034 3、300.027 2,分子式为C21H20O12,相对分子质量为464.095 5,对比对照品鉴定化合物15为金丝桃苷。
化合物16:tR=10.686 min,一级产生[M-H]-峰,m/z=359.076 3,二级裂解产生m/z=197.045 5、179.035 9、161.023 1。对照品tR=10.692 min,裂解规律为m/z=359.076 9[M-H]-,二级扫描裂解产生197.044 5[M-H-C9H6O3]-、179.033 8[M-H-C9H6O3-H2O]-、161.023 6[M-H-C9H6O3-H2O-H2O]-,分子式为C18H16O8,相对分子质量为360.084 5,对比对照品鉴定化合物16为迷迭香酸。
化合物17:tR=12.185 min,一级产生[M-H]-峰,m/z=223.096 8,二级裂解产生m/z=205.086 4、187.063 3、179.090 0、161.095 4、112.986 3。对照品tR=12.212 min,裂解规律为m/z=223.096 4[M-H]-,二级扫描裂解产生205.085 1[M-H-H2O]-、187.082 6[M-H-H2O-H2O]-,分子式为C12H16O4,相对分子质量为224.104 9,对比对照品鉴定化合物17为洋川芎内酯I。
化合物18:tR=22.740 min,一级产生[M-H]-峰,m/z=493.111 9,二级裂解产生m/z=295.219 0。对照品tR=22.738 min,裂解规律为m/z=493.111 9[M-H]-,二级扫描裂解产生295.217 9[M-H-C9H10O5]-。分子式为C26H22O10,相对分子质量为494.121 3,对比对照品鉴定化合物18为丹酚酸A。
化合物19:tR=28.665 min,一级产生[M-H]-峰,m/z=583.176 8,二级裂解产生m/z=553.168 4、535.181 0、431.129 2、121.029 4。对照品tR=28.738 min,裂解规律为m/z=583.176 9[M-H]-,二级扫描裂解产生m/z=121.029 4[C8H9O]-。分子式为C30H32O12,相对分子质量为584.189 4,对比对照品鉴定化合物19为苯甲酰芍药苷。
化合物20:tR=29.173 min,一级产生[M-H]-峰,m/z=491.186 2,二级裂解产生m/z=311.047 5、293.050 2。对照品tR=29.179 min,裂解规律为m/z=491.186 1[M-H]-,二级扫描裂解产生293.045 0[M-H-C9H10O5]-。分子式为C26H20O10,相对分子质量为492.105 6,对比对照品鉴定化合物20为丹酚酸C。
3 讨论实验分别考察了乙腈-水、乙腈-水(0.1%甲酸)作为流动相,结果表明当乙腈-水(0.1%甲酸)作为流动相时,电离效果更好。电喷雾质谱法(ESI-MS)定性分析时,分别采用正、负离子全扫描以获得更多的离子信息,结果表明负离子监测模式下目标物质的响应值明显,而正离子检测信息量少,故选择负离子模式进行分析。
对血必净注射液中的化学成分进行定性分析,根据相对分子质量信息和二级质谱碎片的裂解规律并与对照品进行对比,共鉴定出包括羟基红花黄色素A、芍药苷、芍药内酯苷、氧化芍药苷、苯甲酰芍药苷、阿魏酸、没食子酸、丹参素、绿原酸、丹酚酸A、丹酚酸C、金丝桃苷、迷迭香酸、咖啡酸、原儿茶酸、原儿茶醛、鸟苷、尿苷和洋川芎内酯I在内的20个化合物。该方法与传统液相方法相比更为简单,准确,并充分体现出了UPLC-Q-TOF-MS/MS技术在复杂体系中对未知化合物进行快速鉴定的优势。本实验进一步为血必净药效成分的筛选、定量分析及质量控制提供参考依据,对揭示其药效物质基础具有现实意义。
| [1] | 张继翱, 李家瑞, 乔佑杰, 等. 血必净注射液治疗脓毒症急性肾损伤的临床疗效及对炎症因子的影响[J].天津中医药, 2016, 33(1): 13–16. DOI:10.11656/j.issn.1672-1519.2016.01.04 |
| [2] | 冀兰鑫, 黄浩, 姜民, 等. HPLC测定血必净注射液内11种主要成分[J].中国中药杂志, 2010, 35(18): 2395. |
| [3] | 武子霞, 李银平, 乔佑杰, 等. 血必净注射液对脓毒症大鼠器官功能及死亡率的影响[J].天津中医药大学学报, 2007, 26(2): 68–70. DOI:10.11656/j.issn.1673-9043.2007.02.06 |
| [4] | 王永明, 乔佑杰, 李家瑞, 等. 血必净对脓毒症大鼠巨噬细胞移动抑制因子和急性肾损伤的干预效果[J].天津中医药, 2015, 42(10): 988–991. |
| [5] | 杨锡燕. 血必净注射液治疗脓毒症30例临床观察[J].天津中医药, 2006, 23(2): 92. DOI:10.11656/j.issn.1673-9043.2006.02.15 |
| [6] | 李娜, 蒋林伟, 俞璐, 等. 血必净注射液治疗脓毒症的系统评价[J].中国现代药物应用, 2013, 7(22): 8. |
| [7] | 梁显泉, 李志军, 刘红栓, 等. 血必净注射液治疗脓毒症42例[J].中国中西医结合急救杂志, 2005, 12(4): 251. |
| [8] | 付素珍. 血必净注射液对复苏后的多器官功能障碍患者脏器保护作用的研究[J].天津中医药, 2014, 31(8): 469–471. DOI:10.11656/j.issn.1672-1519.2014.08.08 |
| [9] | 曹书华, 王今达. 血必净对感染性多器官功能障碍综合征大鼠组织及内皮损伤保护作用的研究[J].中国危重病急救医学, 2002, 4(8): 489. |
| [10] | 张畔, 曹书华, 崔克亮, 等. 血必净对多脏器功能障碍综合征单核细胞HLA-DR表达影响的研究[J].中国中西医结合急救杂志, 2002, 9(1): 21. |
| [11] | 张雅军. 血必净联合抗生素治疗重症肺炎疗效评价[J].中国实用医药, 2014, 9(28): 126. |
 2017, Vol. 36
2017, Vol. 36




